基于影像组学临床病理列线图预测低级别星形细胞瘤的总生存期
刘中一 阎静 张振宇 周金桥
郑州大学第一附属医院神经外科 郑州 450052
低级别星形细胞瘤(low-grade astrocytoma)是中枢神经系统最常见的肿瘤之一,占原发性脑肿瘤的15%[1]。生长相对缓慢,具有非常异质临床行为,部分患者手术后有较长生存期,但仍可复发甚至向高级别星形细胞瘤转化[2]。因此对患者的总生存期预测有助于改善疾病管理和指导个体化治疗。影像组学是通过提取医学图像中的定量指标,然后单独或与其他预后因素结合,用于评估治疗反应和生存率的预测[3-5]。研究表明,胶质母细胞瘤影像组学特征的纳入比单独临床病理危险因素展现出更好的预后价值[6]。本研究旨在建立预测低级别星形细胞瘤总生存期的影像组学联合临床因素的预后模型。
1 资料与方法
1.1一般资料回顾性分析2004-01—2020-12我院神经外科收治并确诊的223例低级别星形细胞瘤患者的临床资料。纳入标准:(1)均为首次手术,病理结果为低级别星形细胞瘤,WHO分级Ⅱ级或Ⅲ级。(2)生存资料完整。(3)术前多参数MRI (T1WI、T1c、T2WI、FLAIR和ADC轴位)图的可用性。(4)神经外科和神经放射科医生均依据MRI图像无明显伪影确认可用性。患者的临床信息包括年龄、性别、术前Karnofsky评分(KPS)、切除程度(全切或次全切)、总生存期(overall survival,OS)、病理分级、术后放疗和术后化疗。所有的临床信息均来自病历系统。总生存期是手术日期至死亡日期,或至末次随访日期间的时间。
1.2方法
1.2.1 仪器方法 所有MR图像均于临床检查期间在3.0T扫描仪(西门子Magnetom Skyra;GE DiscoveryMR750或飞利浦Ingenia)获取。包括以下序列:轴位和矢状位T1WI,轴位T2WI,轴位FLAIR。扩散加权成像(diffsion-weighted imaging, DWI)和相应的表观弥散系数(apparent diffusion coefficient,ADC)图。静脉注射0.1 mmol/kg剂量的钆喷酸葡胺盐造影剂后获得的轴向、矢状位和冠状位T1c图像。
1.2.2 图像分析 对图像进行预处理,实现图像的标准化。预处理从基于N4ITK的偏置场失真校正开始,使用三线性插值将所有体素各向同性地重新采样为1 mm3×1 mm3×1 mm3。使用3D Slicer软件对每个多参数MRI图像进行刚性配准,以轴向重采样的T1c为模板,结合信息相似性度量,生成配准图像T1WI、T1c、T2WI、FLAIR和ADC。一名有15年经验的神经放射科医师使用开源软件(ITK-SNAP,版本3.8.0)在横断面上逐节手动绘制肿瘤轮廓。放射科医生对临床和组织病理学数据不详。肿瘤的描绘主要基于FLAIR图像,其中T2WI和T1c用于交叉检查肿瘤延伸并微调肿瘤轮廓。将感兴趣区 (region of interest,ROI)划分为肿瘤区域,包括增强、非增强和肿瘤坏死区域。一周后,由同一神经放射科医师和另一名神经外科医师在25名随机选择的患者中重复ROI描绘,获得可重复性测试数据集。
1.2.3 提取及筛选特征 使用开源的Python软件包PyRadiomics(3.1版本)提取影像特征[7],从5个磁共振序列中提取了5 985个特征。对提取到的特征进行标准化后筛选,首先删除组内相关系数(inter-class correlation coefficient,ICC)较低的特征(ICC<0.85)。使用单变量选择法筛选剩余特征,保留与预后相关的特征,并去除不相关特征。将患者按7∶3的比例随机分为影像组学训练集(155例)和影像组学验证集(68例)。在训练集中,利用最小绝对收缩和选择算子算法选择最优特征[8],用最小准则的10次交叉验证对模型进行优化,最终获得的非零特征计算影像组学评分(Radscore)。根据Radscore,用R包“cutoff”计算训练集的最佳临界值(cutoff值),将训练集中的患者分为高风险组和低风险组。验证集使用相同的cutoff值。在验证队列中,通过Kaplan-Meier生存分析评估影像组学的预后意义。
1.2.4 统计学方法及模型构建 训练集与验证集的临床变量间使用卡方检验或t检验进行分析。对所有变量进行单因素分析,对单因素分析有统计学意义的因素,进行多因素Cox回归分析,以确定低级别星形细胞瘤独立的预后因素。使用R包“survival”构建预后模型,一致性指数(concordance index,C-Index)用于评估模型的预测能力[9]。所有的统计学分析均使用R软件(版本4.1.2)进行。P<0.05表示有统计学意义。
2 结果
2.1临床资料本研究共纳入223例患者,训练集和验证集的临床特征见表1。2集患者的临床资料差异均无统计学意义(P>0.05)。见表1。
2.2影像特征及独立危险因素的筛选经过特征的筛选,最终获得10个非零特征,包含有5个强度特征和5个纹理特征,见图1。对临床危险因素及Radscore进行单因素分析,对单因素分析有统计学意义的危险因素,进行多因素Cox回归分析,最终得到切除程度、术后放疗、病理分级和Radscore为独立的预后危险因素(P均<0.05)。
2.3影像组学评分的预后意义在训练集中根据Radscore计算的cutoff值为-0.12。根据cutoff值将患者分为高风险组(Radscore>0.05)与低风险组(Radscore<0.05)。为了证明放射组学与OS的相关性,我们使用R包“survival”进行分析,得到在训练数据集上放射学特征与OS具有显著相关性(P<0.001)。将相同的cutoff值用于验证集验证,证明放射学特征与OS之间的显著相关性(P=0.0032),如图2。
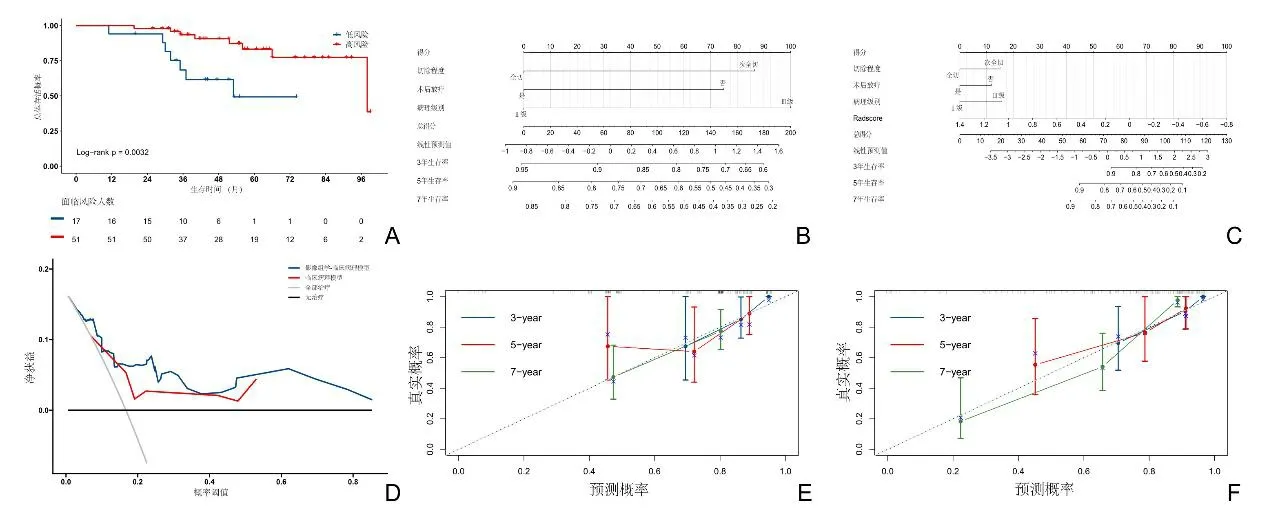
图2 A.验证集中Radscore的KM生存曲线 B.验证集临床病理列线图 C.验证集Radscore-临床病理列线图 D.验证集DCA曲线 E. 验证集临床病理列线图校正曲线 F.验证集Radscore-临床病理列线图校正曲线
2.4模型的建立与效能评估首先基于独立的临床危险因素建立了多因素Cox回归模型的临床病理列线图。然后将Radscore与独立的临床危险因素结合建立了Radscore-临床病理列线图。在训练集与验证集中对OS进行预测,影像组学模型的C-Index分别为0.746和0.701,临床病理列线图的C-Index分别为0.691和0.707。将Radscore与独立临床因素结合后,Radscore-临床病理列线图在训练集与验证集的C-Index提升至0.817与0.778。且在所有的预测模型中,Radscore-临床病理模型的赤池信息准则(akaike information criterion,AIC)最低,见表2。为了对模型进行评估和验证其性能,建立了术后3 a-5 a-7 a生存概率的临床病理列线图的校正曲线,并使用决策曲线分析法对模型进行评估。验证集的校正曲线与决策曲线结果显示了模型的临床实用性,见表2。
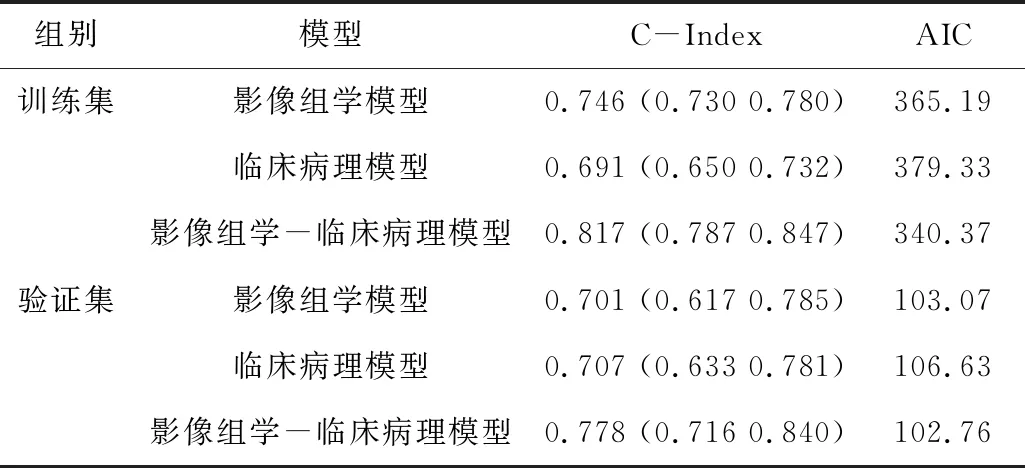
表2 训练集与验证集对OS预测的C-Index
3 讨论
低级别星形细胞瘤是一种生长较为缓慢、广泛发生于中枢神经系统的恶性肿瘤,部分患者术后复发且可向高级别恶性胶质瘤转变,总体预后欠佳。因此,对患者的预后进行分级与预测,可为治疗提供指导与帮助,影像组学已经被证明是影像学与个体化之间的桥梁[10]。基于此,本研究开发并验证了一个依托于影像组学特征联合临床病理因素的低级别星形细胞瘤预后模型。
本研究筛选出的用来构建模型的10个影像特征中,有5个强度特征,5个纹理特征。纹理特征包含1个灰度共生矩阵,3个灰度游程矩阵和1个灰度区域大小矩阵。在先前的研究中,纹理特征已被证明可用来构建模型并预测颅内肿瘤的分级及预后[11-13],本研究的发现与之相符。本研究根据获得的影像组学评分,可将患者分为高风险组及低风险组,2组患者的总生存期有明显差异,这可能对指导患者的个体化治疗具有一定帮助。
本研究的预测模型是基于独立的临床预后因素及最优影像组学特征建立的[14]。在训练集及验证集中,Radscore-临床病理模型均具有更高的C-Index。表明加入影像组学评分后,模型的预测能力得到了提高,联合模型具有最小的AIC值,表明其具有相对较好的抗过拟合性[15]。通过校正曲线可看出,生存期与预测生存期间的一致性在影像组学-临床病理模型上有更好的表现[16],表明其具有更好的预测准度。决策曲线表明了Radscore-临床病理模型具有更好的可用性及效益。亦表明联合影像组学后构建的预后模型对低级别星形细胞瘤患者总生存期的预测准确性得到了进一步提升。
本研究是回顾性研究,样本数量较少,故具有一定局限性。尚需继续进行前瞻性多中心的大样本研究,进一步证实本文所构建的影像组学模型预测的准确性。
综上所述,基于影像组学联合临床因素建立的Radscore-临床病理列线图,可较准确预测低级别星形细胞瘤患者的总生存期,且基于影像学评分对患者进行风险分级后,指导后续的治疗方案。

