胆囊静脉是如何回流的?
——临床解剖学研究
丁冉,郑雪峰,丁自海,吴涛
1.南方医科大学基础医学院,广州 510515;2.暨南大学基础医学与公共卫生学院,广州 510632
笔者前期曾经通过显微解剖和超声解剖方法,观察了胆囊的动、静脉分布和走行[1]。但没能清晰地观察到胆囊静脉确切的属支、分支模式和注入部位。在肝外胆道系统中,胆囊颈、胆囊管、肝管、肝总管和胆总管的静脉回流已比较清楚,但胆囊体和底部的静脉是如何组成和分支的,是以什么方式注入肝门静脉的什么部位,各家没有描述或描述不一[2~12]。胆囊静脉是胆囊癌血管转移的主要途径之一[13~19],了解注入部位,有利于手术切除范围的确定;腹腔镜胆囊切除术只解剖游离、夹闭和切断胆囊动脉,静脉则不做游离,直接电凝切断,但明确主要胆囊静脉的位置,会使电凝切断更加安全。因此,本研究通过改良的管道铸型充填剂和灌注技术进行胆囊静脉铸型[20],希望能阐明胆囊静脉的回流模式和注入部位。
1 材料和方法
1.1 材料
新鲜成人肝脏和胆囊标本32 例(郑州国希望医教集团提供),制成肝门静脉、胆囊静脉和动脉铸型标本。
1.2 方法
血管灌注方法:在肝门处,所有标本分别通过肝门静脉、肝固有动脉灌注黄色和红色改良ABS 充填剂,直至血管充盈,此后每间隔3 h 补充1 次,共3 次。待ABS 固化后,自然腐蚀,显示铸型血管[20]。显露所需血管后,直视或手术显微镜下观察胆囊静脉的属支和分支,回流路径,胆囊动、静脉的伴行关系,胆囊静脉注入肝门静脉分支的部位。数码相机(Sony RXlO)照相。镜内标尺测量胆囊静脉及其分、属支的直径和长度(注:测量的是ABS 充填剂的直径,即代表血管管腔的直径)。
1.3 统计学分析
血管直径≥1.0 mm 以上的属支和分支纳入统计分析。采用SPSS17.0 统计软件包处理数据。
2 结果
2.1 胆囊门静脉
胆囊静脉的组成和分支类似肝门静脉模式,故本研究称胆囊门静脉(cholecystic portal vein)模式(图1)。胆囊静脉有2~4 支,长1.6 cm (1.1~2.1 cm),中部直径3.1 mm(2.4~4.1 mm)。胆囊静脉属支有3 支(2~5 支),末端直径1.6 mm(0.8~2.8 mm)。胆囊静脉分支有4 支(3~5 支),起始处直径1.5 mm(0.8~2.2 mm)。共观察到胆囊静脉95 支,其中左、右侧各1 支的有10例;左、右侧各2 支的有8 例;左侧1 支、右侧2 支的有6 例;左侧2 支、右侧1 支的有7 例;左侧3 支、右侧1 支的有1 例。
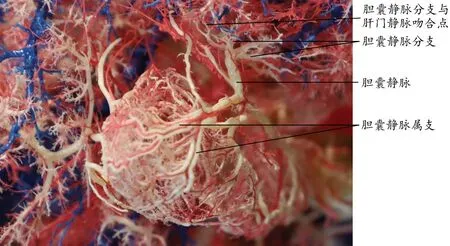
图1 胆囊门静脉(铸型,上面观)Fig.1 Cholecystic portal vein(cast,superior view)
2.2 胆囊静脉的组成和分支
在胆囊体和底部起始的细小胆囊静脉属支与胆囊动脉分支伴行,呈树枝状向胆囊两侧走行,经2~3级汇合,近胆囊床边缘处2~5 支属支汇合为胆囊静脉。而后胆囊静脉走行1~2 cm,呈爪样分出3~5 个分支,走行5~8 mm 后与肝门静脉右支的第4~5 级分支吻合(图2,3)。在胆囊床底部,有3~5 支微细胆囊静脉直接进入肝实质内,与肝门静脉右支的分支吻合。胆囊颈部和胆囊管的静脉与胆总管或肝总管静脉吻合,上行注入肝门静脉左支或右支(图4)。
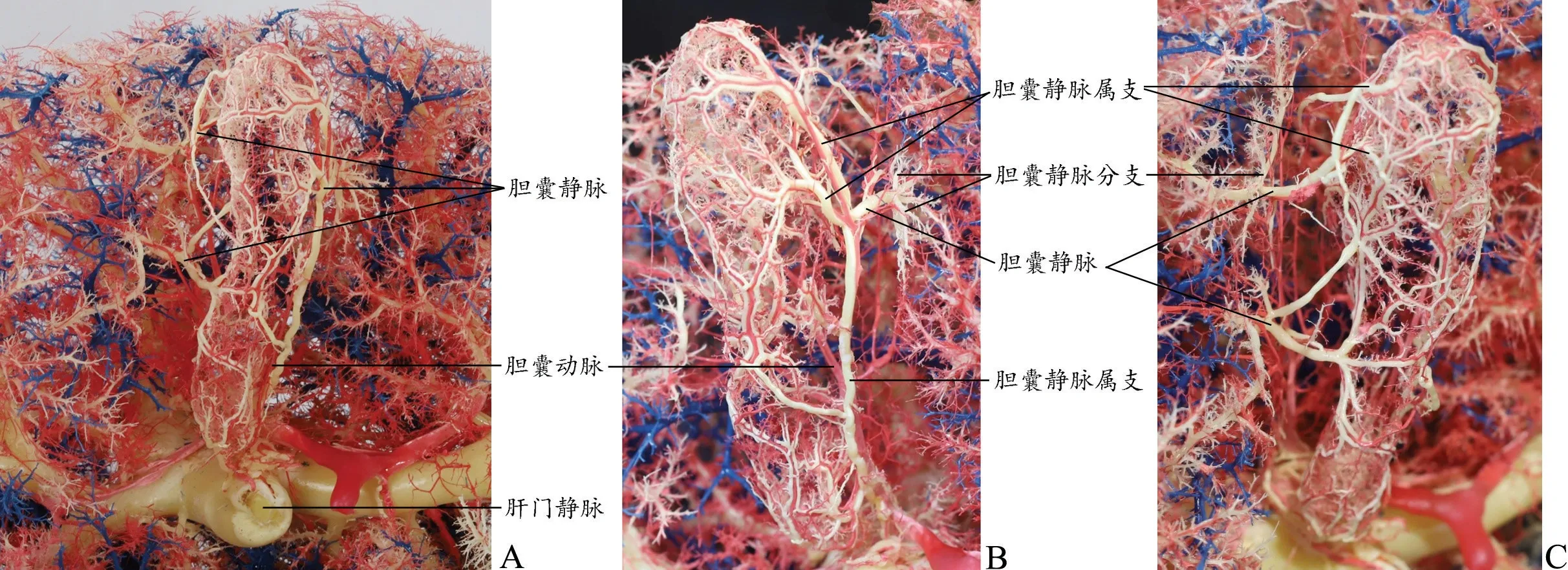
图2 胆囊静脉(铸型)A: 下面观B:左侧面观C: 右侧面观Fig.2 Cholecystic vein (cast)A:inferior view;B: left lateral view;C: right lateral view
有的胆囊静脉分支末端未见与肝门静脉分支吻合,呈细微盲端结束,是标本制作技术问题,还是进入了肝血窦,尚不清楚,目前血管铸型技术尚无法显示肝血窦。胆囊静脉终末支是否汇入肝血窦需进一步观测证实。
3 讨论
通过管道铸型技术研究胆囊静脉,可显示胆囊静脉的组成及微细属支、分支的走行和毗邻关系,对其最终走向能清晰辨认。常规显微解剖技术难以解剖出胆囊静脉微细属支和分支。目前的各种影像技术还无法显示胆囊静脉与其他管道的层次关系,胆囊静脉的分支与肝门静脉分支的吻合部位也不能显示,故既往的研究都无法提供胆囊静脉两端这一奇特的属支、分支现象[2,4,6,7]。
毫无疑义,胆囊静脉是通过肝门静脉回流的。因为本研究在制作铸型标本时,充填剂只注入到肝门静脉内,并没有专门注入到胆囊静脉内,胆囊静脉出现充填剂而铸型是由于肝门静脉内的充填剂逆流进入胆囊静脉内所致。通过直视或镜下可清晰看到胆囊静脉分支与肝门静脉分支的吻合处(图1)。
Kai[2]采用吲哚青绿(ICG)荧光血管造影评价胆囊静脉的回流(图5,6),发现胆囊静脉血流通过两种不同的途径进入肝脏,一种是直接流入邻近胆囊的肝实质,另一种是与胆囊交界的部位。荧光模式分为两种类型,在1 型模式中,胆囊期后立即对邻近胆囊的肝实质进行染色,染色与胆囊静脉流入的部位一致。在2 型模式中,胆囊期后不久,与胆囊毗邻的肝段表面被染色。荧光最常出现在S4,其他区域为S1~3 等处。但这种技术只能观察肝表浅的血流,因为位于肝脏深处的荧光无法被近红外摄像系统检测到。因此,胆囊静脉与肝门静脉分支之间的连接是什么情况则无法显示(注:S:肝段)。
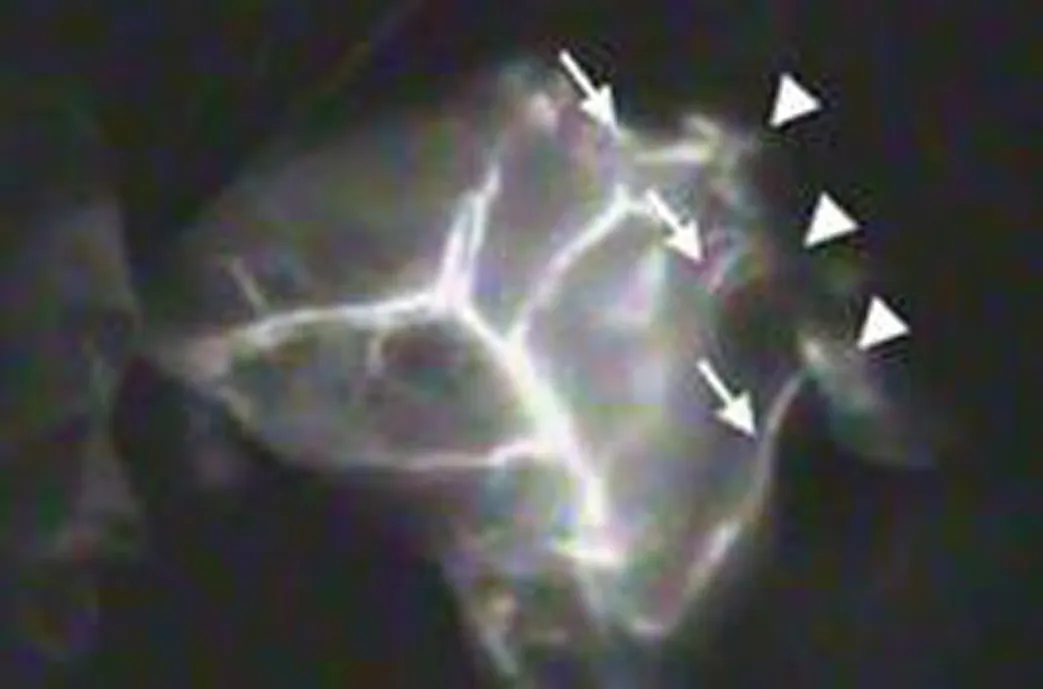
图5 胆囊静脉荧光图像,粗箭头示肝实质,箭头示胆囊静脉流入肝实质内Fig.5 Fluorescence image of the cholecystic veins (thick arrows) and hepatic parenchyma (arrowheads).The cholecystic veins flowed directly into the hepatic parenchyma adjacent to the gallbladder
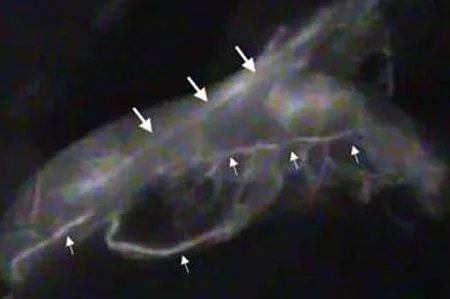
图6 胆囊静脉荧光图像,细箭头示胆囊动脉,粗箭头示胆囊静脉Fig.6 Fluorescence image of the cholecystic artery (thin arrows),and vein (thick arrows) was visualized
Sugita[4]采用血管-CT 扫描的分析技术观察胆囊静脉肝内流入区。胆囊静脉回流是胆囊癌转移至肝的主要路径。他们共显示72 支胆囊静脉,均流入肝门静脉分支或肝窦。胆囊静脉回流的途径有两组,一组是从胆囊颈发出胆囊静脉经过肝门进入肝内,另一组自胆囊体和底部经肝床流入肝内(没说明流入肝内什么部位)。前者17 例,共有静脉21 支,后者23 例,共有静脉51 支,约43%胆囊静脉经肝门流入1 级或2级肝门静脉分支。大多数经胆囊床的胆囊静脉流入肝S4、5 的肝门静脉分支。本研究的观察结果,没有流入肝门静脉1 级或2 级分支的。从解剖结构上看,胆囊静脉细小的3~5 级分支是不可能流入肝门静脉1级或2 级分支的。
Satoh[6]在52 例标本中观察胆囊静脉的回流。所有的静脉进入邻近的肝组织参与肝门静脉循环,只有1 例胆囊静脉直接进入主肝门静脉。胆囊静脉分为侧边组和周边组。侧边组进入方叶、S4 或S5 肝门静脉分支。周边组横过Calot 三角内的动脉,终于肝门静脉。
Yoshimitsu[7]在胆囊动脉超选择性插管后进行血管CT,报告了胆囊静脉引流的最常见部位是胆囊周围的S4 和S5,确定了通过胆囊床流入肝门静脉分支或肝血窦的胆囊静脉。
陈亚进[13]指出,浸润转移途径的胆囊癌是胆道系统恶性肿瘤中生存期最短、预后最差的一种恶性疾病,其原因之一是与胆囊静脉回流的解剖关系密切。胆囊静脉直接汇入肝门静脉。胆囊附着于肝S4b、5交界的胆囊床内,有数支小静脉经胆囊床直接汇入肝实质,或汇合成1~2 支后再进入肝实质,最后汇入肝门静脉末梢,这些静脉可以灌注肝S4~6 的胆囊周围肝实质,胆囊癌可以通过血行转移至上述肝段内。但作者也没有说明胆囊静脉与肝门静脉是以什么方式汇合的。
可以看出,上述通过影像技术都无法显示胆囊静脉的组成、分支及与肝门静脉分支的汇合。在本研究观察的标本中,确切的描述了胆囊静脉回流的胆囊门静脉模式,为人体中描述肝门静脉、垂体门静脉之后发现的胆囊静脉回流的又一奇特现象。为什么出现胆囊门静脉引流模式尚无法解释。有的胆囊静脉分支末端未见与肝门静脉分支吻合,而是以一细长终端结束。这是标本制作的技术问题,还是进入了肝血窦,尚不清楚,因血管铸型技术尚无法显示肝血窦。如是进入了肝血窦,据推测,胆囊静脉微分支进入靠近胆囊床附近的门管区内,与小叶间动脉、小叶间静脉的血液一道进入肝血窦,进而注入中央静脉[4,7]。
胆囊体和底部的静脉以胆囊门静脉的形式汇入肝门静脉右支的第4~5 级分支。与肝门静脉回流的形式相似,即首先以毛细血管静脉端汇合为小静脉,进而在胆囊床左、右缘附近汇合为数支胆囊静脉,走行1~2 cm 后分出数支分支,与肝门静脉右支的分支吻合。在胆囊床底部,有3~5 支微细胆囊静脉直接进入肝实质内,与肝门静脉右支的分支吻合。胆囊颈部和胆囊管的静脉与胆总管或肝总管静脉吻合,上行注入肝门静脉左支或右支。