结肠腺瘤性息肉病患者接受遗传咨询及基因检测的意愿调查*
赵子夜,蒋宇亮,汪昭明,高显华,徐晓东,邢俊杰,王颢,张卫,于恩达△
1 上海长海医院肛肠外科/遗传性结直肠癌筛查防治中心 上海 200433
2 北京世纪坛医院消化内科 北京 100038
结肠腺瘤性息肉病(colonic adenomatous polyp⁃osis,CAP)是最常见的遗传性息肉病型结直肠癌综合征,APC相关息肉病【通常称为家族性腺瘤性息肉病(familial adenomatous polyposis,FAP)】是其中的代表[1]。此类疾病多为单基因遗传病(即孟德尔遗传病)[2],其结肠息肉的数量可为数十枚至上千枚不等,且可伴有多种结肠外表现。结直肠癌发病风险增加是此类疾病患者的首要关切。
CAP 患者多有结肠息肉病或结肠癌家族史,但由于临床工作中的多种局限性问题,开展家系调查的成效并不十分理想。欧美国家的成功经验表明,息肉病注册中心的建立对于结肠息肉病的防控成效可观。芬兰的国家息肉病注册中心数据表明在FAP家系开展调查可以将风险亲属的结直肠癌发病风险降低(先证者风险为65.5%,潜在发病风险人员相应为6.6%)[3];丹麦的全国研究数据表明开展家系调查及防范工作后FAP患者的预期寿命得到了显著的延长[4]。
近年来,基因检测技术快速发展,但总体上来说,其在临床实践中的应用是既不充分也不恰当的,包括患者受检态度在内的导致这一问题的影响因素很少被关注和研究[5-6]。本研究旨在通过问卷调查来探索CAP患者接受遗传咨询与基因检测的意愿及其影响因素。
1 病例与方法
1.1 研究支持
上海长海医院结肠腺瘤性息肉病注册中心成立于2005年8月,主要进行CAP 患者的家系调查和遗传咨询。在此基础上,全新的上海长海医院遗传性结直肠癌筛查防治中心在2019年1月成立。研究者借助不断发展的信息技术和基因检测技术,得以更好地开展患者家系调查和基因检测工作。本项研究所涉及内容均获得上海长海医院伦理委员会批准。
1.2 病例管理
此项横断面调查在2020年2月—3月开展,研究对象为临床诊断为CAP/FAP 的患者,未能很好理解及配合研究工作的患者予以剔除。受访者的疾病诊断均通过上海长海医院遗传性结直肠癌筛查防治中心的登记信息进行确认。
对于已经明确APC致病胚系突变的CAP 患者,在获取受访者及其一级亲属同意的前提下,研究者向其免费提供一级亲属的家系致病突变预测性检测[7]。预测性检测的受检者必须为CAP/FAP 患者的无症状一级亲属,研究者所关注的相关症状包括慢性腹泻,便血及结肠外表现(胃—十二指肠息肉、甲状腺癌、骨瘤、纤维瘤、肝母细胞瘤等)。这些受检者未接受过结肠镜检查,因此未明确其是否罹患CAP。
1.3 研究流程
研究者通过微信手机应用(weixin.qq.com,深圳腾讯科技有限公司)向潜在的受访者发出邀请,同意受访则在开始填写问卷的同时完成电子版知情同意书。对于年龄不足18 岁的受访者,知情同意书和问卷的填写均需由其父母(或其他监护人)完成。
研究者使用问卷星软件(www.wjx.cn,长沙冉星信息科技有限公司)设计电子问卷,通过微信手机应用发送并回收。
1.4 调查内容
问卷设计为结构式设计,包含20 个问题。由于设有跳题逻辑,故每位受访者所需回答的问题均少于20 个。调查问卷共包含三部分内容:(1)一般信息,包括年龄、性别、民族、出生地、居住地、婚育状态、父母生存状态;(2)临床信息,包括明确CAP 诊断的时间和方法,家族史,受检原因,结肠外表现,检查及治疗方法;(3)接受遗传咨询和基因检测的意愿,包括受访者接受遗传咨询的主要目的,受访者是否计划接受基因检测及其影响因素,子女是否罹患CAP,受访者是否计划让子女接受基因检测及其影响因素,受访者的生育计划,受访者对基因检测的总体态度。
1.5 统计学分析
使用SPSS 25.0进行数据统计分析。计量资料采用M(QL,QU)表述,计数资料采用例数及百分比表述。
2 结果
2.1 一般信息及临床信息
发放并回收问卷101 份,经确认符合要求的共89 份,受访者来自全国多地,但未有来自新疆维吾尔自治区,西藏自治区,青海省,宁夏回族自治区,吉林省,福建省,香港特别行政区,澳门特别行政区及台湾地区的受访者。其中,长江三角洲地区(上海市、江苏省、浙江省、安徽省)来源的问卷较多(35/89,39.3%)。受访者完成问卷的平均时间不足4 min。
受访者特征见表1:中位年龄为34 岁,男性较多(56.2%),汉族占大部分比例(96.6%),67.4%的受访者有家族史,55.1%的受访者其父母已故或其父母一方已故。受检原因(寻求临床诊疗的指征)包括筛查、腹泻、便频、血便、黏液便、腹痛、腹胀及其他原因。接受过结肠镜检查的占比为98.9%,未接受结肠镜检查的唯一患者的初始表现为项部硬纤维瘤且无消化系统症状。分别有74.2%、70.8%的受访者接受过上消化道内镜检查、结肠手术。在结肠外表现方面,软组织囊肿/肿瘤最为常见(24.7%),其余依次为牙齿异常(13.5%)、先天性视网膜色素上皮肥大(5.6%)、骨瘤(4.5%)。需要指出的是,很多受访者并没有接受过相应的专科检查,因此未能明确其是否存在结肠外表现;所有受访者均未提及曾罹患肝母细胞瘤。
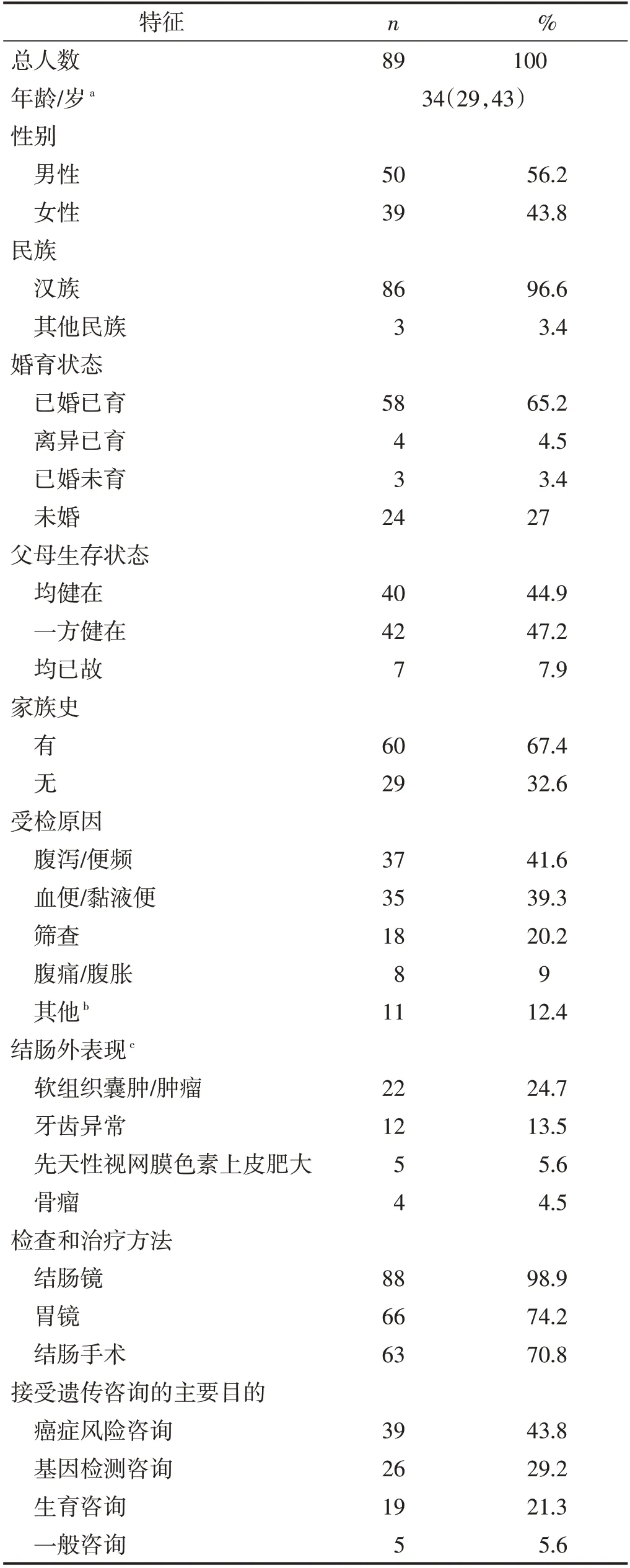
表1 受访者特征
2.2 接受遗传咨询及基因检测的意愿
受访者接受遗传咨询的主要目的包括四个方面:癌症风险咨询占比最高(43.8%),其后是基因检测咨询(29.2%)、生育咨询(21.3%)、一般咨询(5.6%)。见表1。
65.2%的受访者已婚已育,4.5%的受访者离异并育有子女,因此共有69.7%的受访者(62 名)育有子女,受访者的子女是风险亲属家系致病突变预测性检测的主要目标人群。27 名受访者尚未育有子女,他们对未来的生育计划存在疑虑,因此他们是进行辅助生殖技术干预的主要目标人群。
多达66.3%(59/89)的受访者尚未确认选择何种生育方式(图1)。72 名受访者(80.9%)已经接受或计划接受针对FAP 的基因检测,主要目的是寻找致病基因(诊断,47.2%)。在62名育有子女的受访者中,38名(61.3%)已经让子女接受或计划让子女接受针对FAP 的基因检测,主要目的是预测子女是否会发病(预测性检测,71.1%),导致受访者拒绝让其子女接受基因检测的因素较多,对检测结果恐惧是最主要原因(33.3%),见图1、表2。
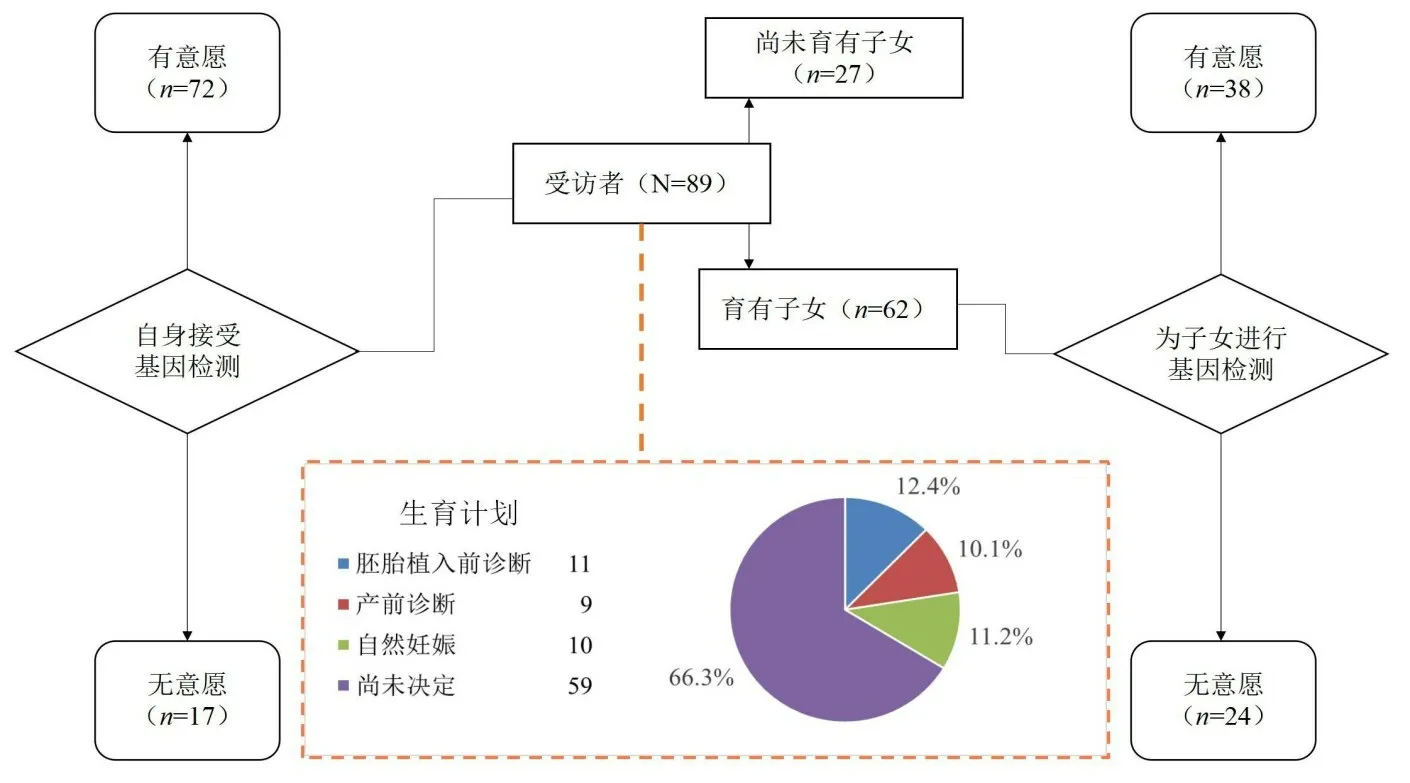
图1 受访者的生育计划及接受基因检测的意愿调查结果
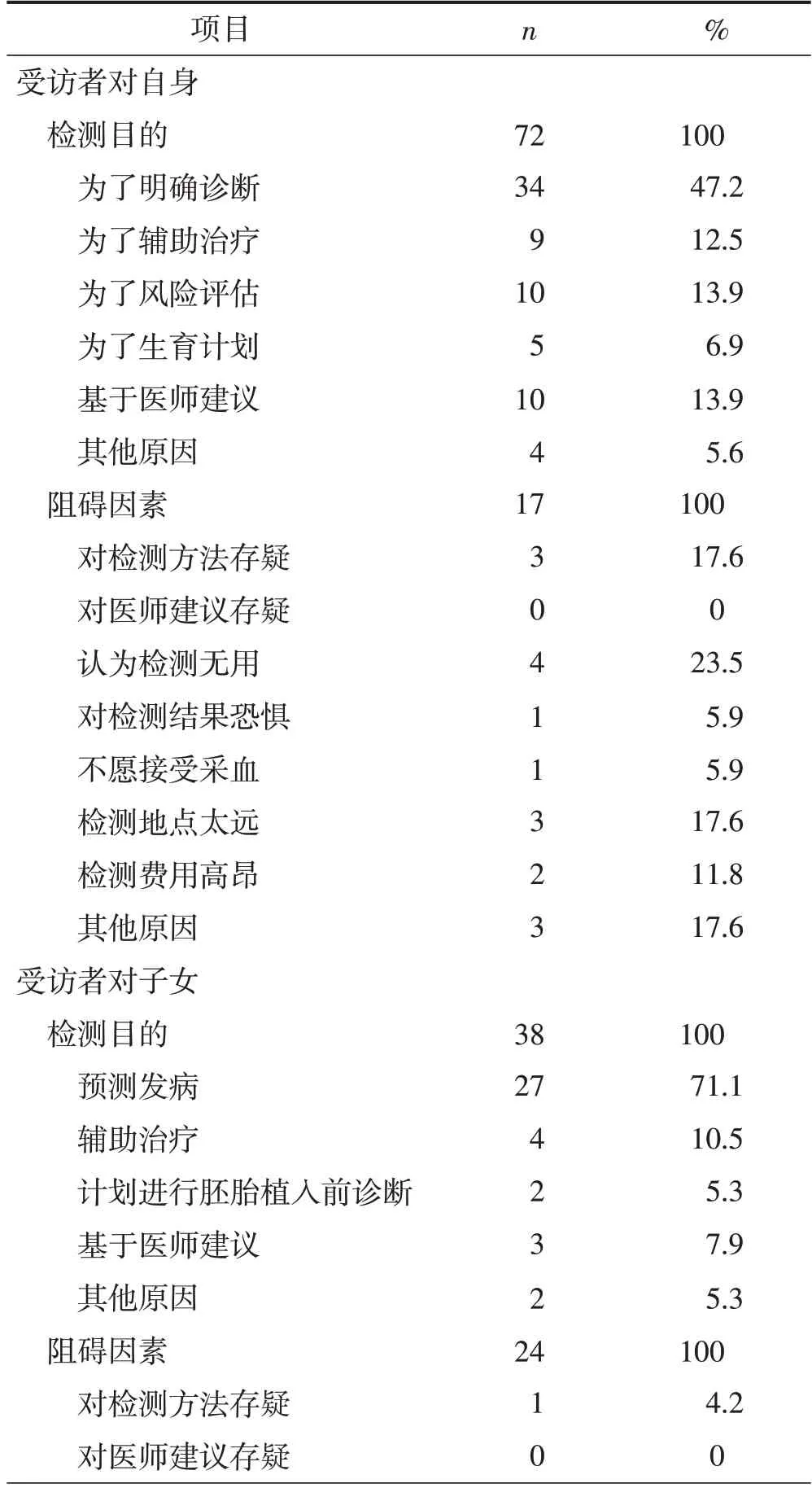
表2 受访者对自身及其子女接受基因检测的意愿分析结果

表2(续)
在问卷的最后,设置了3个问题用以探索受访者拒绝接受基因检测的相关因素(表3)。在理论层面上,对基因检测方法可信度的担忧(37.1%)和检测结果对诊疗的影响(33.7%)是两大主要影响因素。在操作层面上,87 名受访者提供了有效答案,其中标本获取困难(44.8%)和检测费用昂贵(36.8%)是主要影响因素。在心理层面上,出于对子女基因突变状态的担忧(58.4%)是主要影响因素。
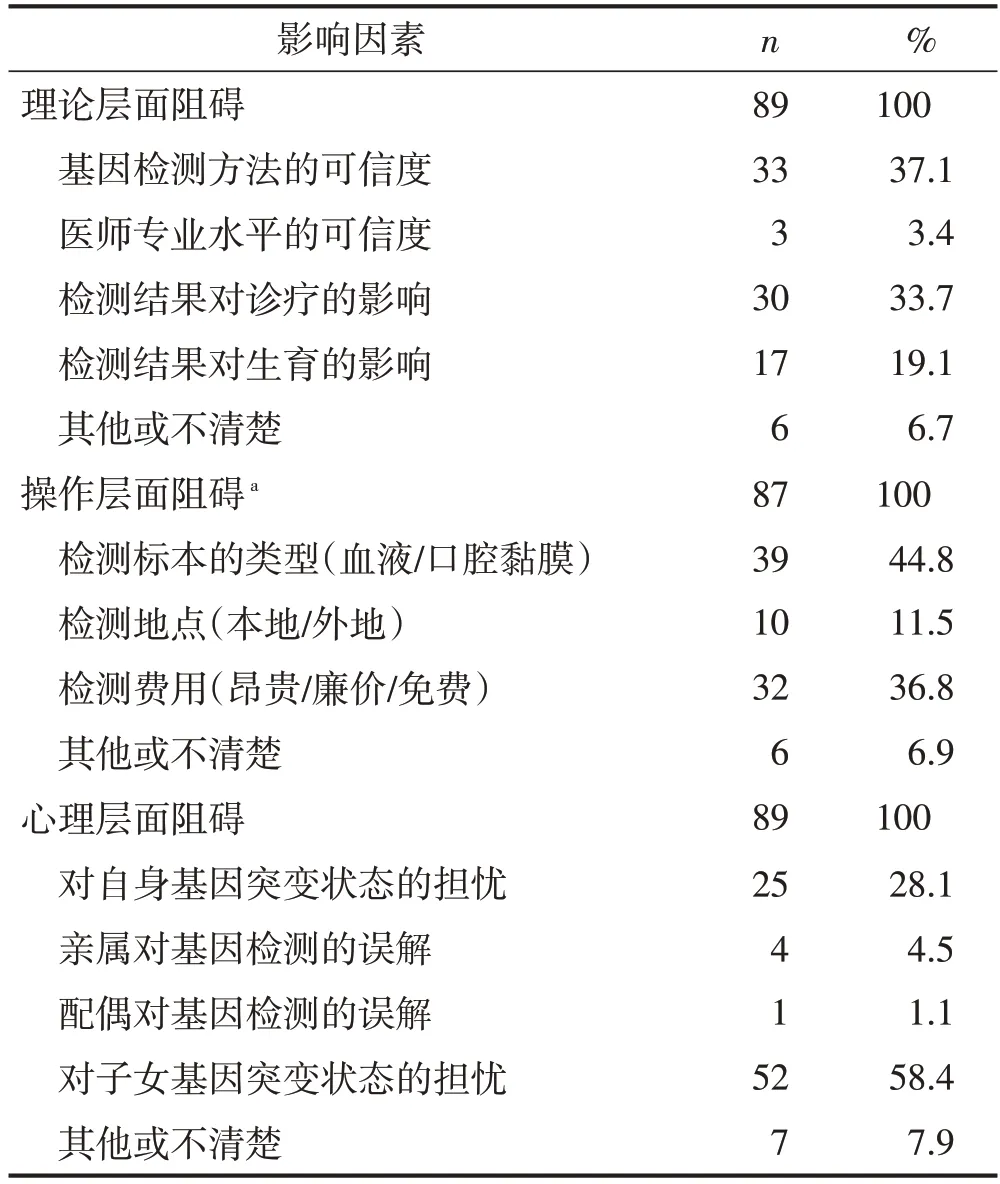
表3 受访者拒绝接受基因检测的影响因素分析结果
3 讨论
FAP(OMIM175100)是一种常染色体显性肿瘤综合征,由肿瘤抑制基因APC的杂合致病性突变引起,临床特点包括CAP、结肠外表现和癌易感性[1]。FAP 的人群发病率预计为(2~3)/10 万[8-10]。Gardner综合征是FAP 的一种变体,此类患者除结肠腺瘤外,兼具硬纤维瘤、骨瘤或其他肿瘤,并以首次报道美国犹他州FAP 家系的医师的名字命名[11]。Gard⁃ner 综合征及其他的FAP 变体综合征(包括Turcot 综合征[12])的疾病名称均已废用,并统一命名为APC相关息肉病,因为上述综合征均已被证明是APC胚系突变所致,属于同一种疾病。
世界上最早的结肠息肉病注册中心于1924年由Dr.Cuthbert Dukes 在英国圣马克医院(St Mark’s Hospital)建立。自此之后,以家系调查为基础的系统性信息收集便开始应用于结肠息肉病的临床诊疗,有关这一疾病的规律也开始逐渐被认识,家系防控的策略也随之逐渐成熟起来。早在20世纪90年代,APC基因突变检测已经开始服务于FAP 的诊断和治疗[13]。然而,这一基因检测技术的开展有赖于临床医师承担起为先证者及其家庭成员解读检测结果的临床含义(指导意义)的重要任务。基因检测是遗传咨询的组成部分,所以其必须建立在系统的遗传咨询和家系调查的基础上,国际上的成功经验便是建立专门的结肠息肉病注册中心。在圣马克结肠息肉病注册中心之后,北欧国家和美国的注册中心也陆续建立起来并运行至今。我国的专业化注册中心起步较晚,故在家系调查和疾病防控方面落后于欧美国家。据了解,我国目前已有的遗传咨询专业学会包括中国遗传学会遗传咨询分会(成立于2015年2月)[14]和中国抗癌协会家族遗传性肿瘤专业委员会(成立于2018年8月)[15]。近十年来,随着技术的进步,我国在家系调查方面也实现了快速发展。基于移动通讯和互联网应用的便捷与价廉特点,我国大部分患者都能够借助网络技术与医师实现跨区域的联系,家系调查的信息支持手段高效且易得。与此同时,基因检测技术快速升级,传统技术诸如Sanger 测序和多重连锁探针扩增(multiplex ligationdependent probe amplification,MLPA)变得更为普及或者被新的技术取代[7],新检测技术的检测费用也有降低的趋势,从而使得临床医师可以将这些技术应用于临床实践。基因检测结果可助力疾病评估、辅助生殖,提升遗传咨询的价值。辅助生殖技术也在快速发展,产前诊断[16-17]、无创产前诊断、胚胎植入前诊断等技术共同助力单基因遗传病的遗传阻断,给患者家庭带来福音。
结肠息肉病注册中心的建立和遗传咨询的开展在我国正迎来一个黄金时期。作为一个人口超十亿的大国,我国预计有数万至数十万FAP 患者。自1985年以来,上海长海医院已接诊500 名以上的结肠息肉病患者,这使上海长海医院成为国内主要的结肠息肉病诊疗中心之一。基于上海长海医院消化内镜中心和肛肠外科的技术条件[18],我们已经成功地开展了FAP 的诊治和监测工作,并在FAP 的遗传咨询方面积累了一定的经验[19-20]。建立跨区域的结肠息肉病注册中心将有助于改善结肠息肉病患者的预后并提升其生活质量。“既不充分也不恰当”的观点基于基因检测技术的应用现状得出,主要原因在于临床医师和患者均对其缺乏充分的了解。为改善这一现状,临床医师需要在以下四个场景考虑应用或推荐应用基因检测技术:(1)拟诊FAP时;(2)FAP患者近期有生育计划时;(3)FAP患者子女拟进行疾病发病风险预测时[21];(4)家族风险成员进行筛查时[22]。
在此次调查中,我们尝试探索影响CAP 患者对基因检测的认知和意愿的因素,这些内容在既往研究中鲜有涉及。参与此次调查的受访者其父亲和(或)母亲多健在(44.9%的受访者的父母均健在,47.2%的受访者的父母一方健在),受访者较年轻(中位年龄为34 岁),但是有家族史者占比高(67.4%)。理论上,年轻患者有更大的父母健在的可能性,而家族史则多与父亲和(或)母亲已故相关,所以,此次调查研究的结果数据似乎存在一些矛盾之处。
受访者接受遗传咨询的主要目的是癌症风险评估,这也符合医疗现状,即患者就诊的最主要诉求是关注自身的健康。紧随其后的咨询目的包括基因检测咨询和生育咨询,这些是患者更高层次的需求,也是我们努力的方向。在欧美国家的高度专业化医疗体系中,医学遗传科在医院中独立运作,遗传咨询师专注于为患者解决遗传学相关问题。但我国的情况并非如此,一方面,医学遗传科的建设尚未完善,另一方面,大部分患者更信任直接负责其诊疗工作的医师,而不是遗传咨询师,这并不是他们就诊的最初目的。由此,我们发现外科医师是目前最适合向其提供遗传咨询的医务人员,而进行遗传咨询最合适的时机是在患者术后病情平稳时,恰当选择工作切入的时机有助于实现患者获益最大化。
Levine 等[23]曾对28 名身为父母的FAP 患者开展了针对患者为其子女进行基因检测意愿的调查,他们发现常见的促进因素包括遗传咨询师主动提供建议和个性化的诊疗内容,而常见的阻碍因素包括缺少遗传咨询师的专业建议和基因检测费用昂贵。在此次调查中,我们发现了此前研究报道未提及的因素,即对子女患病状态的担忧,可能的原因在于本次受访者的子女低龄比例较高,且尚未出现相关症状。对检测结果恐惧是阻碍受访者为其子女进行基因检测的最主要原因,也是我们最需要关注的问题。将人文关怀渗透到医疗过程中,是重点,亦是难点,在遗传咨询工作中尤为如此。有时候,临床医师对疾病诊治予以绝对的关注,对患者的个人因素及其家庭背景考虑较少。患者的种族、宗教、职业、生活(风俗)习惯、经济状况、家庭关系等因素都可能影响到其对遗传咨询的态度,这些都是遗传咨询师必须理解和考虑的。我们认为,作为遗传咨询师,了解上述信息将会对其工作的开展大有裨益;作为研究者,更全面了解患者意愿及其影响因素并寻求改进方法将是未来的努力方向。此次调查的结果在一定程度上体现了我国FAP 患者接受遗传咨询意愿的现状,当然,这是片面化的数据结果。目前我们正尝试调查针对FAP 患者的预测性检测在国内的开展情况。
由于样本量所限和研究样本选择偏倚,本研究存在一些局限性,包括但不限于以下方面。首先,超过4/5的受访者已经接受基因检测或计划进行基因检测,这会对他们的反馈结果产生多方面的积极影响。造成受访者是否(计划)接受基因检测这一比例悬殊的根本原因在于临床诊疗依从性,即此类调查结果的获得始终依赖于受访者较好的临床诊疗依从性。其次,没有受访者报告“对医师建议存疑”作为其接受基因检测的阻碍因素(表2),同时仅有3名受访者选择“医师专业水平的可信度”作为理论层面的阻碍因素(表3)。实际上,本次调查的所有受访者均已和研究者建立良好的信任,所得研究结果呈现的情况是存在选择偏倚的,这也导致调查结果难以反映当前真实情况(临床中普遍存在的诊疗依从性欠缺)。最后,有36.8%的受访者对检测价格表示担忧(表3),但选择“检测费用高昂”具体选项的受访者却非常少(表2)。我们在长海注册中心提供了部分免费的APC基因检测,因此部分受访者已经接受了免费的基因检测。然而,基因检测的高价格毫无疑问仍然是开展此项技术的一个主要制约因素。
总的来说,CAP 的遗传咨询和基因检测的开展在我国正迎来一个黄金时期,但临床医师和患者对其了解有限。遗传咨询和基因检测的开展与完善将使得CAP 患者在疾病评估、疾病预测和制定生育计划方面得到更多帮助。
利益冲突声明全体作者均声明不存在与本文相关的利益冲突。