VR/AR康复训练对早期脑梗死患者上肢运动功能的影响及其弥散张量成像研究
吴龙强,黄倩倩,金韵,苏婷婷,陈晓勇,蒋松鹤
1.温州医科大学附属第二医院育英儿童医院 康复医学中心,浙江 温州 325027;2.厦门市第五医院康复医学科,福建 厦门 361000;3.温州医科大学 国际针灸康复研究所智能康复研究中心,浙江 温州 325027
据统计,在全世界范围内,脑卒中位列老年人死亡原因的第二位,同时高居18~60 岁人群死亡的第五位原因[1]。脑卒中可引起肌力下降、关节活动受限、疼痛、认知下降等功能障碍,中国每年新发的数百万脑卒中患者中,功能障碍率达70%~80%[2],给人们的生产生活带来极大影响。上肢功能在人体的平衡、运动、姿势调节等方面起着非常重要的作用,上肢功能障碍将极大限制脑卒中患者的日常生活能力。当前有越来越丰富的常规康复方法用于改善脑梗死患者的功能障碍,然而,功能障碍的恢复是个漫长的过程,常规康复方法枯燥无味、相对困难且数量较多,长期下去易降低患者的主动性及康复训练效果[3]。
虚拟现实(virtual reality, VR)技术、增强现实(augmented reality, AR)技术目前已广泛应用于商业、娱乐、测绘、医学、军事、远程教育等领域[4],作为一种新式的治疗手段,在促进脑梗死患者功能障碍恢复方面也得到了越来越多的应用[5]。观察脑组织微观结构的变化需要借助磁共振弥散张量成像(diffusion tensor imaging, DTI)技术,而弥散张量纤维束成像(diffusion tensor tracking,DTT)是DTI的进一步延伸,通过对皮质脊髓束(corticospinal tract, CST)的三维重建,可以无创性地评估脑梗死功能障碍患者的预后[6]。本研究采取沉浸式VR康复训练结合AR环境,融入脑梗死患者的上肢功能康复训练中,研究此康复治疗方案对脑梗死患者上肢运动功能的影响,并比较脑梗死患者病灶周围CST与运动功能恢复情况的重组修复关系。
1 对象和方法
1.1 对象 经本院伦理委员会授权同意,伦理审批编号:2016科研课题第73号,选取2016年11月至2018年9月在温州医科大学附属第二医院育英儿童医院康复医学中心住院治疗的早期脑梗死偏瘫患者20例,均符合中国急性缺血性脑卒中诊治指南[7]。
1.2 纳入及排除标准 纳入标准:①病情平稳,体温、血压、脉搏等生命体征平稳;②病程小于3个月;③首次发病,年龄30~70岁;④患侧上肢、手Brunnstrom分期评定≥II期,且患侧上肢各关键肌群肌张力评定≤2级(改良Ashworth肌张力量表);⑤简易精神状态检查[8]评分>23 分;⑥双眼视力或矫正视力≥1.0;⑦入组者或其监护人签署知情同意书。排除标准:①严重认知功能障碍或精神疾病无法配合;②多种原因导致上肢关节疼痛、活动受限;③合并严重内科系统疾病,如不稳定型心绞痛、肝功能损伤、尿毒症等;④具有半侧空间忽略或视听觉障碍;⑤生命体征不稳定;⑥具有幽闭恐惧症,或体内有金属内固定、心脏起搏器等,无法完成DTI扫描者。按随机数字表法将患者均分为对照组和实验组,2组各10例,2组性别构成均为男6例,女4例,对照组年龄(62.7±4.5)岁,实验组年龄(67.3±15.5)岁,对照组病程(18.1±4.2)d,实验组病程(18.1±6.9)d,2组偏瘫侧均为左右侧各5例。2组患者在年龄、性别、偏瘫侧别、病程等方面组间差异均无统计学意义(P>0.05)。
1.3 康复训练方法 2组患者均给予常规的基础药物治疗及常规康复训练方法。常规药物治疗主要包括抗血小板聚集药物、改善循环、调脂稳定斑块及个体基础疾病的治疗,如高血压病、糖尿病等慢性疾病。对照组:常规康复训练方法包括借助滚筒、篮球进行关节活动度训练,磨砂板训练,拧螺丝或毛巾,中低频脉冲电治疗,被动牵伸,bobath握手、抗痉挛模式治疗、Rood技术、PNF等神经肌肉疗法,纠正异常模式,增强上肢运动控制训练,肌力训练等综合康复训练,训练时间为每次60 min,每天1次,每周训练5 d,共治疗3周。实验组:在常规康复训练的基础上加用AR环境下的VR康复训练。本次实验所应用的设备为沉浸式VR康复训练设备,主要由沉浸式头盔、两侧操作手柄、定位器、操作系统等部件组成,借助本实验室自主设计及开发的增强环境显示系统,将两者结合,进一步增强沉浸性及趣味性,提高患者的主动参与的积极性。VR/AR康复训练具体任务包括日常生活能力(activities of daily living, ADL)厨房训练(肩关节、肘关节、手指等各大关节综合性配合动作)、触碰球训练(肩关节及肘关节屈伸)、拳击训练(肘关节屈伸)、射击训练(手指按压肌力、上肢内收外展及转移)、敲打训练(肩关节、肘关节、腕关节协同完成)等5个项目,用于增强脑梗死患者偏瘫上肢大关节、手眼协调、上肢控制及手指抓握能力;若患者上肢主动运动功能较差,无法独立完成,可在治疗师的指导和帮助下辅助患侧上肢训练。VR/AR康复训练每次30 min,每天1次,每周训练5 d,共治疗3周。
1.4 评价方法 治疗前后由一名不参与治疗的康复医师对所有入组的患者进行功能评定,2组患者分别于治疗前和治疗3周后进行日常生活活动能力和上肢运动功能评定。评估量表主要包括上肢和手Brunnstrom运动恢复分期评分(Brunnstrom评分)、上肢部分Fugl-Meyer量表(Fugl-Meyer assessment for upper extremity, FMA-UE)和改良Barthel指数(modified Barthel index, MBI)[9]。
1.4.1 Brunnstrom评分:用于评估患侧上肢的运动功能,包括上肢及手的运动能力,评定标准分I-VI期。为了便于统计分析,不同的阶段分期将以对应的阿拉伯数字来表示,如Brunnstrom IV期计为4分,以此类推。所得阶段分期越高,代表肢体运动功能越好。
1.4.2 FMA-UE:用于患者上肢运动功能的评估,评定内容包括上肢腱反射、屈肌伸肌共同运动、分离运动、腕稳定性、手协调性等9项,共33个项目,合计66分。得分越高,肢体功能越好。
1.4.3 MBI:包括进食、穿衣、修饰、洗澡、控制小便、控制大便、用厕、转移、行走、上下楼梯十个部分,总分100分,ADL能力缺陷程度:0~20分为极严重功能缺陷;25~45分为严重功能缺陷;50~70分为中度功能缺陷;75~95分为轻度功能缺陷;100分为ADL能自理。
1.5 MRI检查及图像后处理与分析 实验组和对照组患者在治疗前后均进行颅脑MRI检查,采集患者颅脑磁共振弥散张量数据,采用GE-Discovery MR750 3.0T MR扫描。扫描过程中,患者保持制动,双耳佩戴耳塞预防耳鸣、头晕等不适,平卧为扫描台上。扫描患者颅脑MRI平扫成像序列,在此基础上施加对弥散敏感的脉冲,采用多次激发平面图像技术扫描内囊、胼胝体、外囊等大脑结构,将收集到的所有入组患者功能磁共振的影像通过弥散张量纤维素成像专业软件进行处理并计算得到相应CST的具体数值(单位为束),见图1。
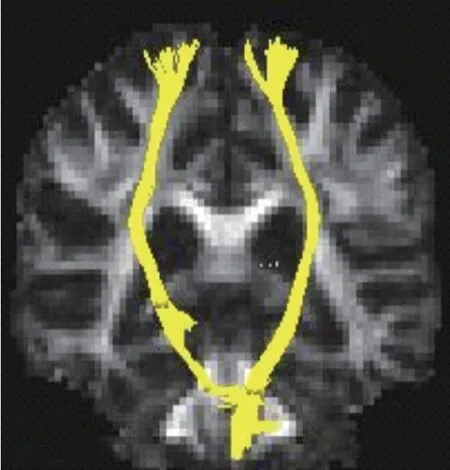
图1 颅脑MRI图像示CST重建图像
1.6 突发情况及意外的措施应对及预防 在实验过程中发生的意外突发情况主要为肢体疼痛、视力模糊、跌倒、胸闷、胸痛、心悸等不良反应。应对措施为在训练及检查前,充分告知患者的治疗、检查过程及可能出现的意外情况,消除患者的恐惧感。患者在住院期间应具有良好的精神状况和身体反应能力,控制好基础疾病,保持主动、耐心参与训练的良好积极性。此外,为了在意外等突发情况发生时使患者可得到迅速有效的治疗,每位参与评估和治疗的医务人员均进行规范培训,具备突发情况发生时的正确应对能力,并及时向上级医师汇报。
1.7 统计学处理方法 采用SPSS22.0统计软件进行数据分析。正态分布计量资料以±s表示,2组间均值比较采用两独立样本t检验,自身前后对照均值比较采用配对t检验。2 组数据相关分析采用Pearson相关分析。P<0.05为差异有统计学意义。
2 结果
2.1 治疗前后2 组患者上肢及手Brunnstrom评分、FMA-UE评分、MBI评分 治疗前,2组患者上肢Brunnstrom运动恢复分期(Brunnstrom assessment for upper limb extremity, BRU)评分、手Brunnstrom运动恢复分期(Brunnstrom assessment for hand extremity, BRH)评分、FMA-UE评分、MBI评分比较差异均无统计学意义(P>0.05)。经过3周的训练,2组患者相应评分均较治疗前明显改善,差异均有统计学意义(P<0.05)。实验组患者FMAUE评分、上肢和手Brunnstrom分期评分高于对照组,差异有统计学意义(P<0.05);2组患者MBI评分组间比较,差异无统计学意义(P>0.05)。治疗后2组患者MBI评分和FMA-UE评分差值比较差异有统计学意义(P<0.05)。见表1。
表1 治疗前后2组患者上肢及手Brunnstrom评分、FMA-UE评分、MBI评分比较(每组n=10,±s )

表1 治疗前后2组患者上肢及手Brunnstrom评分、FMA-UE评分、MBI评分比较(每组n=10,±s )
与本组治疗前比:aP<0.05:与对照组差值比:bP<0.05
组别 BRU评分 BRH评分 FMA-UE评分 MBI评分对照组 治疗前 2.50±1.35 1.70±1.16 15.50± 4.33 53.50± 7.92治疗后 3.10±1.37a 2.40±1.65a 25.80± 5.75a 75.00± 7.49a差值 0.75±0.75 0.75±1.06 9.33±10.07 20.42±16.44实验组 治疗前 2.70±0.82 2.10±1.37 18.90± 3.62 50.00± 6.41治疗后 4.30±1.06a 4.00±1.16a 42.20± 4.70a 84.00± 4.58a差值 1.25±0.97 1.75±1.38 19.67±12.54b 32.92± 8.91b
2.2 2组患者治疗前后患侧CST神经纤维数量比较
所有患者在治疗前后均进行磁共振扫描,最后共有19例患者同意并顺利完成颅脑磁共振扫描。治疗前,2组患者患侧CST神经纤维数量差异无统计学意义(P>0.05)。治疗3周后,2组患者患侧CST神经纤维数量均较前明显增多(P<0.05);实验组和对照组治疗后患侧CST神经纤维数量比较差异无统计学意义(P>0.05),见表2。
表4 2组患者治疗前后患侧CST神经纤维数量比较(±s )
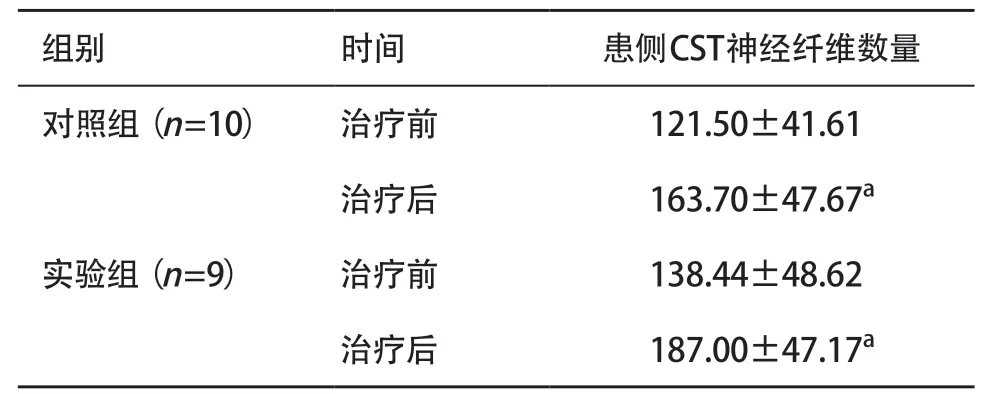
表4 2组患者治疗前后患侧CST神经纤维数量比较(±s )
与本组治疗前比:aP <0.05
组别 时间 患侧CST神经纤维数量对照组(n=10) 治疗前 121.50±41.61治疗后 163.70±47.67a实验组(n=9) 治疗前 138.44±48.62治疗后 187.00±47.17a
2.3 患侧CST神经纤维数量与治疗前后患侧上肢FMA-UE评分的Pearson相关性分析 治疗前,患侧上肢部分FMA-UE评分与患侧CST神经纤维数量呈正相关(r=0.733,P<0.001);康复治疗3周后,患侧上肢部分FMA-UE评分与患侧CST神经纤维数量呈正相关(r=0.615,P=0.005),即患者患侧CST神经纤维数量越多,其上肢运动功能越好。
3 讨论
研究显示,不断重复的康复训练能够改善中枢神经系统的可塑性,在早期康复介入的同时,进行大量针对性、重复性、高强度的康复训练与功能障碍的恢复高度相关,VR康复训练具备此治疗要求的相关要素条件[10]。本研究将VR康复训练与AR环境相结合,希望通过各自不同的训练特点,在丰富的不同视听触反馈下为患者提供个体化的康复治疗,弥补常规康复训练的不足。此VR/AR康复训练系统适应范围较广,可针对患者上肢不同部位的功能障碍提供相应的训练模式,包括肩肘腕关节各个关节活动方向、手指的抓握和伸展等灵活性的训练。
VR技术具有人机交互性、充分的想象性、完全深入的沉浸性的特点。在过去的几年中,被越来越广泛地运用于脑卒中患者肢体运动功能的康复训练中。近些年来,国内外已有多项相关临床研究证实,VR发挥着不可替代的作用,不仅提高了患者主动参与的积极性,而且提高了治疗效果,且患者的满意度高。HUNG等[11]运用自身开发的VR系统,对17例脑卒中偏瘫患者上肢行采摘植物和互相击打等训练,经治疗后,实验组患者的上肢wolf康复评分较治疗前明显提高。CARREGOSA等[12]对脑卒中偏瘫患者运动VR游戏参与系统,在游戏过程中训练患者上肢,通过偏瘫上肢各关节肌群的协调性、持久性、方向性调动,极大拓展了相应的方向运动及运动控制能力,结果显示,实验组患者患侧FMA-UE评分较前提高。AR技术与VR技术具有相似性,又具有自身的优势特征,它广泛应用了多媒体、多模块、实时跟踪和注册、智能交互、传感等多项技术,不仅也具有沉浸性、参与性、趣味性的特点,关键在于它能将训练画面与现实环境相结合,使得训练场景更贴近实际生活,从而实现对真实环境进行增强。HOSSAIN等[13]为脑卒中患者设计了一款无线振动设备,为患者提供触觉感应反馈,患者可利用此装备感知在融入现实环境中的物品,如拿取杯子、球类运动比赛、射击炮战互动游戏等,且治疗师可以根据不同脑卒中患者的功能障碍情况,选择不同训练强度的康复治疗方案,大大提高了患者参与的趣味性,且积极性大大提高。经过系统的训练后,结合康复评定结果,患者的运动功能较训练前有了明显改善。
本研究结果显示,2组患者经治疗后,上肢功能评分及ADL评分均较治疗前有所改善,提示常规康复疗法与VR/AR康复训练均有助于增强早期脑梗死患者的上肢运动功能及ADL。在治疗后实验组患者的评分高于对照组,提示在改善程度的表现上要优于对照组,表明基于AR环境下的VR康复训练系统结合常规康复训练相比单纯康复治疗更有优势。本研究应用的VR/AR康复训练系统,为患者的治疗创建了更贴近生活环境的状态,患者通过完成真实的操作来训练其偏瘫上肢的功能,在训练中学得的技能可更好的应用于日常生活中,进而提高其生活自理能力。
CST主要控制骨骼肌的随意运动,DTI和DTT技术可以无创性地显示人体中脑纤维束的走形和形态,通过选择性地对大脑中CST进行三维重建,直观地显示其形态、完整性、方向性,通过对病灶及周围的正常组织弥散对比,判断其与运动功能连接的完整性。本研究综合利用了DTI和DTT技术,并在匹配软件的加持下,研究CST的纤维数量与对应肢体运动功能恢复方面的关系,使我们更直观地了解皮质激活兴奋与皮质下结构完整性的关系。结果显示,2组患者在康复治疗3周后,患侧CST神经纤维数量均较前增多,提示治疗后可能存在神经重组或代偿。康复训练3周后2组患者患侧CST神经纤维数量对比差异无统计学意义,造成此结果的可能因素有:①脑梗死造成中枢神经系统损伤,其生长恢复的速度较为缓慢;②脑梗死造成的神经损伤恢复可能由健侧或周围皮质代偿,并且其恢复速度与损伤的程度相关[14-15]。研究结果显示,患侧FMA-UE评分与患侧CST的神经纤维数量成正相关,提示早期脑梗死患者CST神经纤维数量与上肢运动功能恢复情况具有相关性,即患者CST神经纤维数量越多,该患者上肢运动功能分级越高,预后越好,FMA-UE评分可较好地评估早期脑梗死患者上肢运动功能恢复情况。
本研究应用VR技术,配合AR环境的融入,增强了患者训练的主动性和针对性,结合常规康复疗法,更能增强脑梗死患者上肢运动能力。此外,经治疗后,实验组患者患侧CST神经纤维数量均较前有所增多,与脑梗死患者运动功能量表评估呈正相关,可通过DTI技术分析早期脑梗死患者运动能力变化情况。由于本研究康复治疗具有特殊性,样本量较少,混杂因素较多,可能会对实验结果造成一定程度的误差,在今后的研究中,还将进一步追加样本的数量,不断改进VR/AR康复训练系统,使其更具人性化及贴合试验设计,提高试验的准确性。

