基于12 个产地的白及冻干片质量标准
徐雨生,滕晓梅,辛文锋,高明菊,田迎秋,余正勇
(1.湖南农业大学农学院,长沙 410128;2.湖南杂交水稻研究中心杂交水稻国家重点实验室,长沙 410125;3.文山学院三七医药学院,云南 文山 663000)
白及(Bletilla striata)是兰科白及属多年生草本植物,色彩丰富、花型端庄典雅、叶态美观,具有很高的观赏价值、药用价值和经济价值,主要分布在云南省、贵州省、安徽省、陕西省和甘肃省[1-3]。研究表明,茎中白及胶具有增稠、延缓衰老、悬浮、保湿、抗菌和抗肿瘤作用[4]。近年来,白及因其独特的药用和保健价值而得到广泛应用。
中药饮片的干燥方式有多种,按其发展过程可分为传统干燥和现代干燥。传统干燥方法受环境和技术的限制,主要是晒干和阴干,操作简单,无需特殊设备,经济实惠。随着科学技术的不断发展,干燥方法日益多元化、现代化。目前常用的干燥方法包括热风干燥、红外线干燥、喷雾干燥、真空冷冻干燥等。热风干燥通过吹热风来蒸发水分[5],具有传热面积大、热效率高、处理量大、结构简单、生产能力大、操作方便、投资成本低、工艺简单、易于控制等优点,但需要消耗大量的电能;红外线干燥利用波长为0.75~40 μm 的红外线辐射来干燥物料[6],具有热损失小、易于控制、传热效率高、损失小等优点,但设备操作复杂且需要消耗大量能量;喷雾干燥具有时间短、得粉率高等优点,但对含糖量高的药物有风险[7];真空冻干中药材可以避免目标成分的氧化变质和分解,产品不会出现干缩、变形及褐变现象。因此,真空冷冻干燥技术可以较好地保存样品,改善中药材自身的色、香、味及营养成分,在食品、中草药和中药饮片加工中得到深入研究和广泛应用[8,9]。但是从中药材的饮片处理来看,真空冷冻干燥技术处于一个空白状态。本研究通过对12个地区的白及冻干片进行研究,测定其中的有效成分含量,建立白及新的处理工艺,以期能更清楚地了解冻干处理白及的质量,为建立白及冻干片质量标准提供试验依据。
1 材料与方法
1.1 材料与试剂
1)材料。取12 个地区的白及药材,经冻干处理后切片待用,如表1 所示。
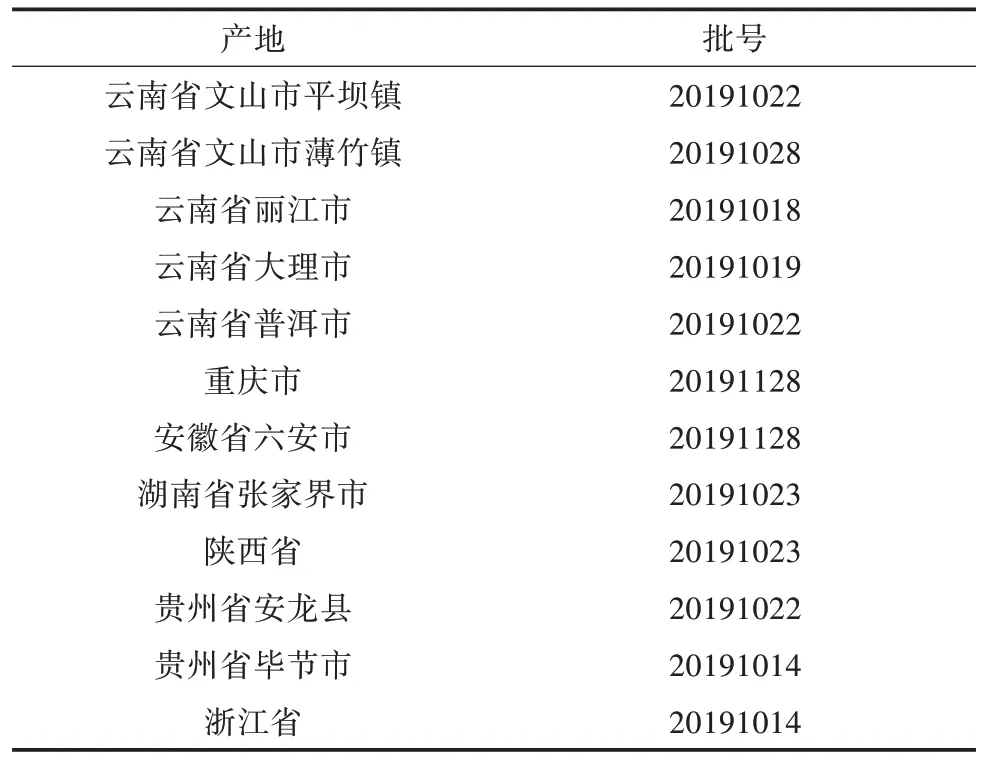
表1 白及产地与批号
2)试剂。无水葡萄糖、乙醇、乙醚、双[4-(β-D-吡喃葡萄糖氧)苄基]-2-异丁基苹果酸酯(Militarine)、酚酞、乙腈等均购于国药集团化学试剂有限公司。
1.2 仪器和设备
UV-800S 型紫外-可见分光光度计,上海越众仪器设备有限公司;BP211D 型电子天平,上海梅颖浦仪器仪表制造有限公司;DZKW-S-C 型恒温水浴锅,上海华玺科学仪器有限公司;LC-2030 型岛津高效液相色谱仪,岛津(上海)实验器材有限公司;十八烷基硅烷键合硅胶柱(4.6 mm×250 mm,5 μm),宁波鸿普仪器科技有限公司;FA1004 型分析天平,上海光学仪器厂;KQ3200 型超声波清洗器,青岛精诚仪器仪表有限公司;MB25 型水分测定仪,上海方瑞仪器有限公司;GY-605D 型体视显微镜,深圳市光亿光学仪器有限公司;MHY-2000 型薄层色谱系统,北京美华仪科技有限公司;TCXC-1400 型箱式电阻炉,上海仝科电炉设备有限公司;VYJG-9420 型电热鼓风干燥箱,杭州亿捷科技有限公司。
1.3 方法
1.3.1 白及的一般理化鉴别
1)性状。通过眼观、手摸、口试等方法,观察冻干白及片的形状、大小、表面、颜色、质地、断面、气味。
2)显微鉴别。参照白及药材的纤维特征进行试验,采用粉末制片法,取少量白及冻干片粉末置于载玻片上,滴加水合氯醛数滴,用酒精灯透化。(尽量用镊子夹着载玻片)透化多次,慢慢将水合氯醛溶液蒸至近干。再滴加稀甘油,将盖玻片沿液体边缘慢慢盖上,尽量减少气泡的产生。先用10 倍镜观察,再用50 倍镜观察,从一角开始慢慢寻找白及粉末中的显微特征。
3)薄层鉴别。取白及冻干片粉末2 g,放入锥形瓶中,加入20 mL 70%甲醇,在超声波清洗机中处理30 min,过滤,然后将滤液放入水浴锅中蒸发,加入10 mL 去离子水溶解残渣,用乙醚摇匀提取2次,每次20 mL,合并乙醚液,在水浴锅中挥发至1 mL,作为供试品溶液。取白及对照药材粉末1 g,用同样方法制备对照药材溶液。根据薄层色谱法通则(0502),分别吸取5 μL 供试品溶液和对照药材溶液,置于同一硅胶G 薄层板上,以环己烷-乙酸乙酯-甲醇(6∶2.5∶1)作为展开剂展开,取出,干燥,用10%硫酸乙醇溶液喷洒。在105 ℃下加热3~5 min,静置30~60 min,在紫外光灯(365 nm)下检视。
1.3.2 基本成分测定
1)水分测定。根据《中华人民共和国药典:四部》[10](简称《中国药典》)水分检测方法(通则0832,第二法)测定。取白及冻干片粉末2 g,放入称量瓶,厚度不超过5 mm,放入干燥箱,105 ℃干燥5 h,冷却30 min后,105 ℃干燥1 h,冷却后称量2次,相差不超过5 mg。
2)总灰分含量测定。根据《中国药典》[10]总灰分含量测定法(通则2302,第二法)测定。取白及冻干片粉末2 g,放入恒重的小坩埚(通常恒重2 次)。用小电炉慢慢升温后再灼烧,至完全炭化时,取出放凉,放入烘干机,干燥15 min。当马弗炉温度逐渐升至600 ℃时,将坩埚放入马弗炉中,燃烧2 h,然后取出冷却,称重。当马弗炉温度降低至300 ℃时,放入马弗炉内燃烧30 min,使其完全炭化。称重至恒重。根据残渣重量计算白及的总灰分含量。
3)二氧化硫残留量测定。根据《中国药典》[10]二氧化硫残留量的测定方法(通则2331,第一法)测定。取白及冻干片粉末10 g,放入双颈圆底烧瓶,加去离子水350 mL。打开回流冷凝器的开关,将连接到冷凝器上端口的橡胶空气导管放在100 mL 锥形瓶底部。向锥形瓶中加入50 mL 3%过氧化氢溶液,作为吸收溶液。使用时,向吸收液中加入3 滴甲基红乙醇液指示剂,用0.1 mol/L 氢氧化钠溶液滴定至黄色。打开分液漏斗的活塞,取10 mL 盐酸溶液缓慢流入蒸馏瓶,立即将溶液加入双颈烧瓶,加热至沸腾,沸腾90 min 后停止。吸收液冷却后,在磁力搅拌器上连续搅拌,用氢氧化钠溶液滴定至溶液呈黄色,保持20 s,用空白试验修正滴定结果[11]。
4)浸出物测定。根据《中国药典》[10]醇溶性浸出物测定方法(通则2201,热浸法)测定。取白及冻干片粉末2 g,放入250 mL 锥形瓶,加入50 mL 50%乙醇,称重,静置1 h,然后接回流冷凝器,加热至沸腾,保持微沸1 h。冷却后称重,用50%乙醇补足损失的重量,取滤液25 mL,放入蒸发皿,105 ℃干燥3 h,冷却,快速称重,计算浸出物含量。
1.3.3 总多糖测定
1)对照品溶液制备。称取10.45 mg 无水葡萄糖,置于10 mL 容量瓶,加去离子水溶解并定容至刻度线,摇匀。
2)供试品溶液制备。取白及冻干片粉末0.200 0 g,放入具塞试管,加入6 mol/L 10 mL 盐酸、15 mL 去离子水,摇匀,沸水浴加热30 min,取1~2滴,放在白瓷板上,滴1 滴I-KI 溶液,检查水解是否完全。如果水解完成,则不会出现蓝色。完全水解,冷却至室温,加入1 滴酚酞指示剂,用10%氢氧化钠溶液滴定至中性,过滤至100 mL 容量瓶,备用。
3)线性关系。分别取0.2、0.4、0.6、0.8、1.0 mL葡萄糖溶液(对照品溶液),放入5 个25 mL 具塞比色管中,加入去离子水至2.5 mL 刻度线,摇匀,沸水浴30 min,取1~2 滴置于白瓷板上,加入1 滴I-KI 溶液,检查水解是否完全。水解完全后,冷却至室温后加入1 滴酚酞指示剂,用10%氢氧化钠溶液滴定至中性,过滤至100 mL 容量瓶,定容摇匀备用。以0.3 mL 去离子水为空白对照,在495 nm 波长下测定吸光度。
4)精密度试验。取0.3 mL 文山市平坝镇白及冻干片的供试品溶液,用紫外分光光度仪在495 nm波长下,同一个样品测定5次,计算平均值。
5)重复性试验。取6 份0.500 0 g 文山市平坝镇白及冻干片粉末,制备供试品溶液,分别吸取0.3 mL供试品溶液至25 mL 容量瓶,加去离子水至2.5 mL,以0.3 mL 去离子水为空白对照,在495 nm 波长下测定每份吸光度,计算总多糖的含量。
6)稳定性试验。取0.3 mL 文山市平坝镇白及冻干片供试品溶液,在495 nm 波长下,1 h 内每10 min 测定1次,测定吸光度。
7)回收试验。取6 份0.500 0 g 文山市平坝镇白及冻干片粉末,制备供试品溶液,分别取0.15 mL 供试品溶液于25 mL 容量瓶,加入0.15 mL 葡萄糖溶液,加去离子水至2.5 mL,以0.5 mL 去离子水为空白对照,在495 nm 波长下测定吸光度,计算总多糖的回收率。
8)样品含量测定。取12 个产地的白及冻干片粉末各0.500 0 g,制备供试品溶液,分别取0.3 mL 供试品溶液于25 mL 容量瓶,加去离子水至2.5 mL,以0.3 mL 去离子水为空白对照,在495 nm 波长下测定吸光度,每个样品平行操作3份,计算各产地白及冻干片的总多糖含量。
1.3.4 Militarine 含量测定
1)对照品溶液制备。取4.10 mg Militarine(批号CSF201803)于20 mL 容量瓶,用50%乙醇溶解并定容至刻度线,用0.45 μm 微膜过滤,取滤液备用。
2)供试品溶液制备。取0.200 0 g 白及冻干片粉末,放入150 mL 具塞锥形瓶,加入50% 25 mL 乙醇,超声波处理30 min,取出,放冷,用50%乙醇补足失重,过滤,取续滤液,0.45 μm 微膜过滤,取滤液备用。
3)色谱条件与系统适用性试验。色谱柱为Sepax Gp-C18(4.6 mm×250 mm,5 μm),检测波长为223 nm,柱温为25 ℃,进样量为10 μL,流速为1 mL/min,用流动相A(乙腈)和流动相B(0.1%磷酸-去离子水)进行梯度洗脱(表2)。

表2 样品洗脱条件
4)线性关系考察。分别取0.41、0.82、1.23、1.64、2.05、3.08、4.10、5.13、6.15、7.18 mL Militarine的标准储备溶液至10 mL 的容量瓶,加50%乙醇定容,制成浓 度为0.041、0.082、0.123、0.164、0.205、0.308、0.410、0.513、0.615、0.718 μg/μL 的溶液,分别取10 μL 上述溶液,记录色谱图,以Militarine 的峰高为纵坐标,Militarine 实际进样量为横坐标,绘制标准曲线。
5)样品含量测定。称取12 个产地的白及冻干片粉末各0.200 0 g,制备供试品溶液,按上述色谱条件进样分析,绘制标准曲线并计算Militarine 的含量。
2 结果与分析
2.1 性状鉴别
根据图1 的3 批样品发现白及的断面呈白色、角质坚硬、不易破碎;气微,味苦,嚼起来有黏性。经冷冻干燥技术处理的白及性质为表面呈白色或淡黄色的中空泡沫状薄片;气微、味苦微甜、有黏性、易碎;断面类白色、角质样。

图1 3 批白及样品
2.2 显微镜鉴别
白及冻干片粉末为黄白色。由图2 可知,在10 nm×10 nm 的电子显微镜下观察发现,草酸钙针晶团存在于大的圆形黏液细胞中,或散在各处,针状晶体长18~88 μm。含硅质块的细胞很小,位于纤维周围,垂直排列。纤维束直径为11~30 μm,木质壁,人字形或椭圆形孔纹;梯纹导管、具缘纹孔导管及螺纹导管直径为10~32 μm,糊化淀粉颗粒无色。

图2 白及冻干片显微结构
2.3 薄层色谱测定
与对照药材比较(图3)发现,12 个产地的白及冻干片均出现相同颜色的棕红色斑点,效果良好。

图3 白及冻干片薄层色谱
2.4 白及冻干片含水量测定
对12 个产地的白及冻干片粉末含水量进行测定。由表3 可知,白及冻干片粉末含水量为1.87%~6.37%,平均含水量为4.48%。
2.5 总灰分含量测定
对12 个产地的白及冻干片总灰分含量进行测定,由表4 可知,白及冻干片的总灰分含量为1.70%~4.50%。
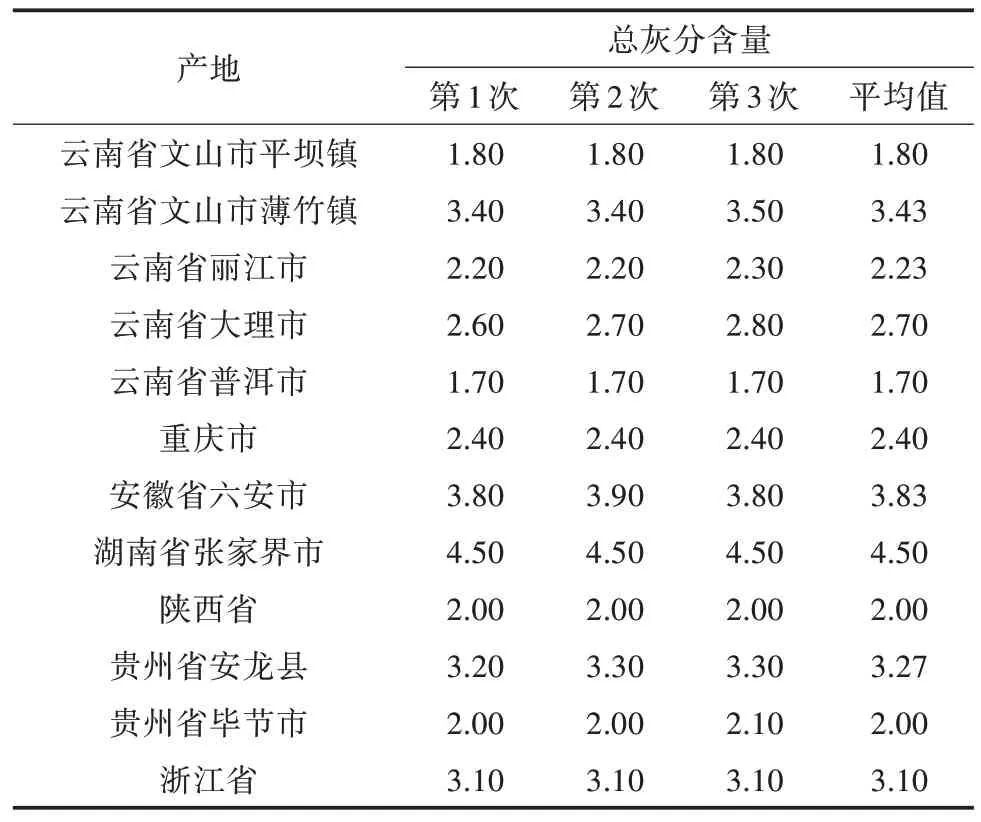
表4 白及冻干片总灰分含量测定 (单位:%)
2.6 二氧化硫残留量测定
根据中药材冻干片标准要求,白及冻干片中的二氧化硫残留量不得超过400 mg/kg。由表5 可知,12 个产地白及冻干片的二氧化硫残留量均未超过400 mg/kg。由于白及产地丰富,生长环境不同,白及冻干片中二氧化硫残留量也不相同。

表5 白及冻干片二氧化硫残留量测定(单位:mg/kg)
2.7 浸出含量物测定
由表6 可知,12 个产地白及冻干片的乙醇浸出物含量均高于30%,部分地区白及冻干后乙醇浸出物含量高于40%,故本研究中白及冻干片中的乙醇浸出物含量规定不低于30%。
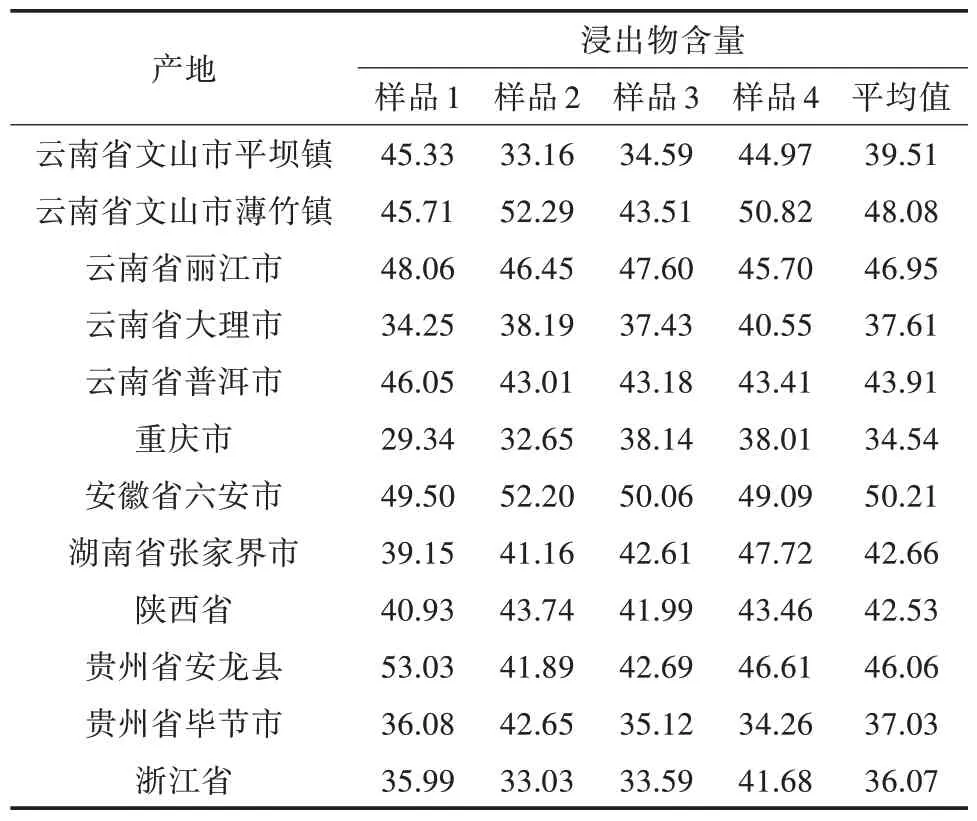
表6 白及冻干片浸出物含量测定(单位:%)
2.8 总多糖测定
2.8.1 线性关系考察 由图4 可知,以葡萄糖(对照品)溶液浓度为横坐标,吸光度(A)为纵坐标绘制标准曲线。标准回归方程为y=0.979 3x-0.062 5,R2=0.998 1,对照品溶液的线性关系好,对照品溶液浓度在0.209~1.045 mg/mL 时线性关系较好。
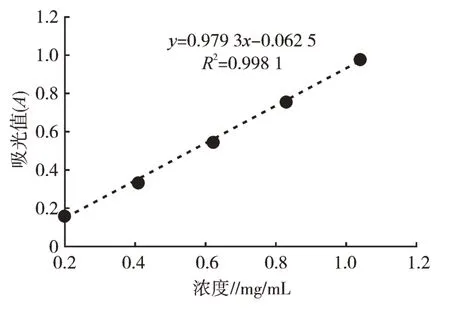
图4 葡萄糖(对照品)溶液的标准曲线
2.8.2 精密度试验 由表7 可知,5 个文山市平坝镇白及冻干片样品的测定结果相差较小,样品的RSD为3.21%,表明仪器精密度良好。

表7 精密度试验结果
2.8.3 重复性试验 由表8 可知,文山市平坝镇白及冻干片样品总多糖含量的RSD为6.68 %,表明该方法重复性良好。
2.8.4 稳定性试验 取文山市平坝镇白及冻干片样品,在不同的时间测定样品的吸光度。由表9 可知,在40 min 内吸光度波动较小,表明该检测方法在40 min 内稳定。

表9 稳定性试验结果
2.8.5 回收率试验 由表10 可知,取6 份文山市平坝镇白及冻干片样品,平均回收率为101.1%,RSD为7.23%,表明该方法稳定可靠。

表10 回收率试验结果
2.8.6 总多糖测定 由表11 可知,12 个产地的白及冻干片总多糖含量相差不大,含量较稳定,总多糖含量的平均值为38.48%。
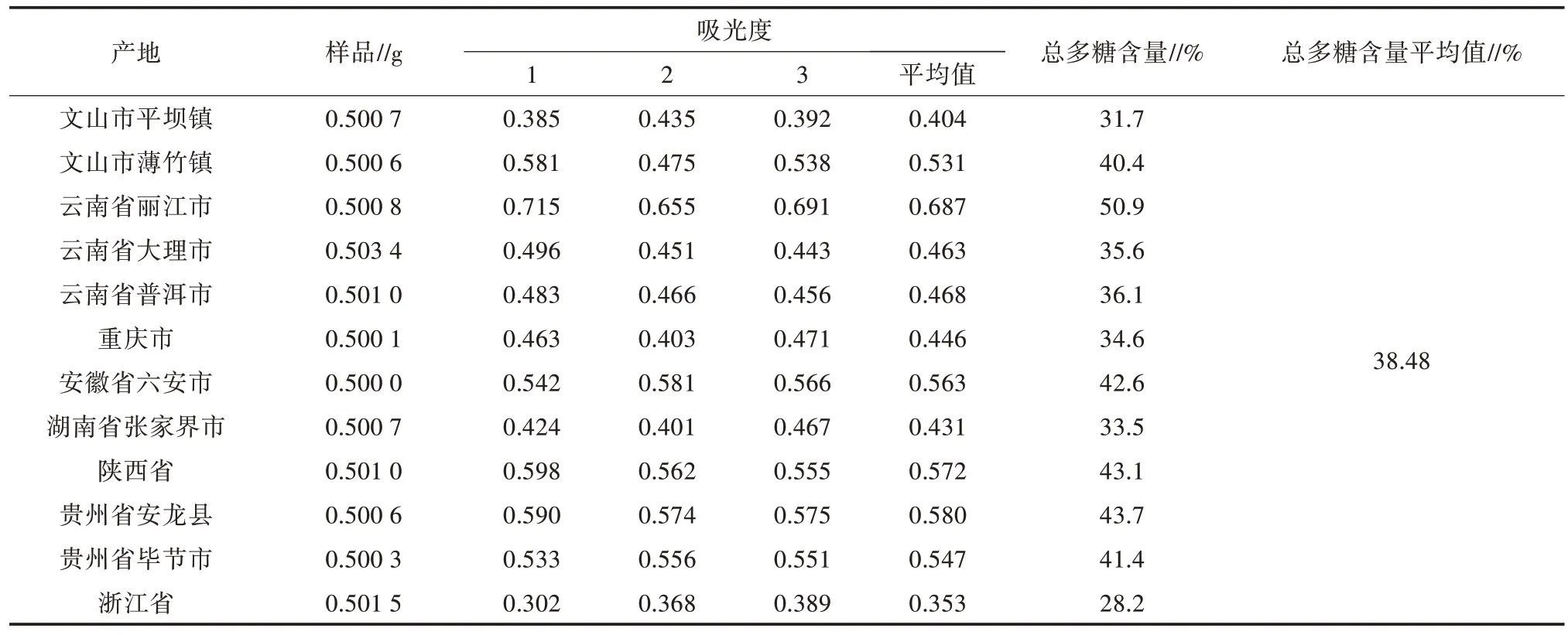
表11 白及冻干片总多糖含量测定
2.9 Militarine 含量测定
2.9.1 对照品、供试品溶液色谱测定 由图5 可知,对照品在整个系列中只显示Militarine 的单峰,不存在其他的杂峰,表明试验过程中无其他影响,即仪器、试剂、样品等都符合试验要求。由图6 可见,白及冻干片供试品溶液的HPLC 色谱图有Militarine 对应锋出现,且峰值较好。

图5 Militarine(对照品)溶液HPLC 色谱
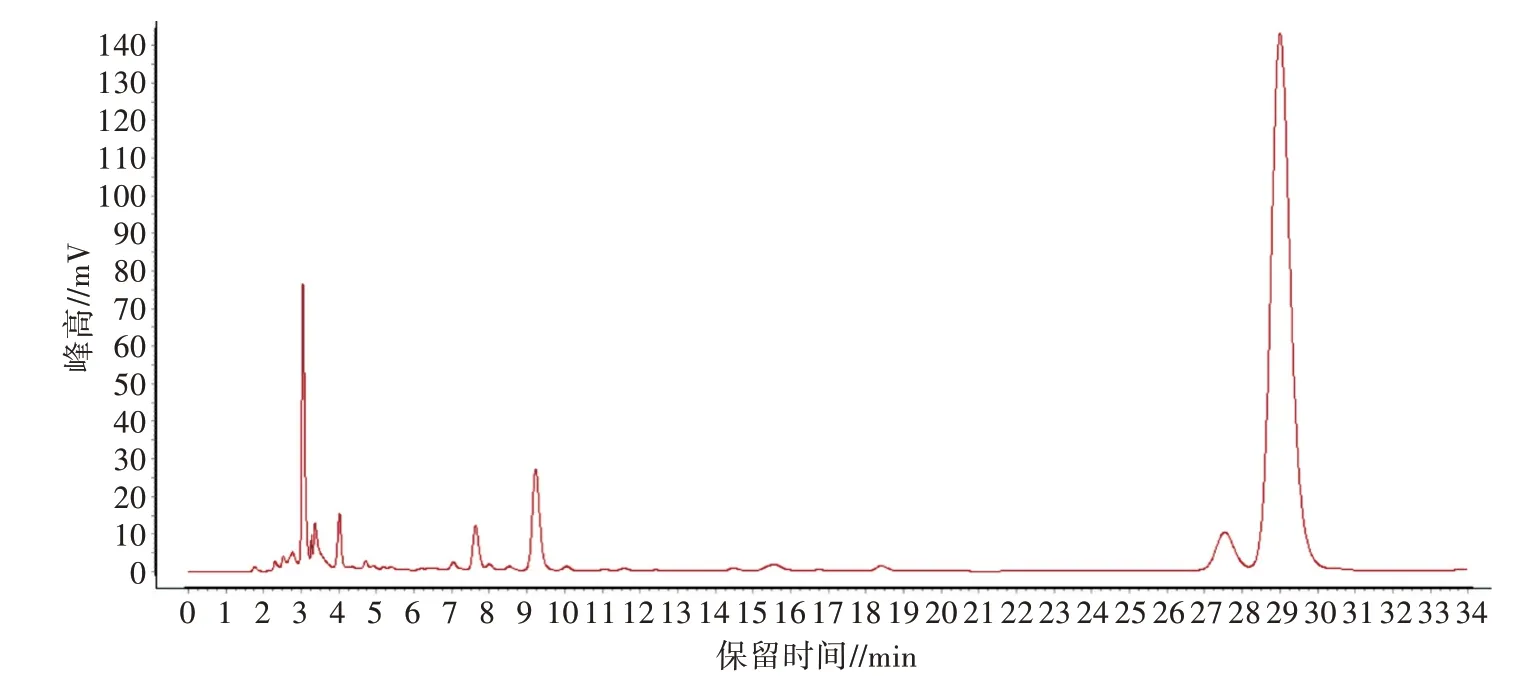
图6 白及冻干片溶液HPLC 色谱
2.9.2 线性关系考察 由图7 可知,回归方程为y=1000 000x-3 783.9,R2=0.999 9,表明对照品溶液在0.041~0.718 mg/mL 时线性关系良好。
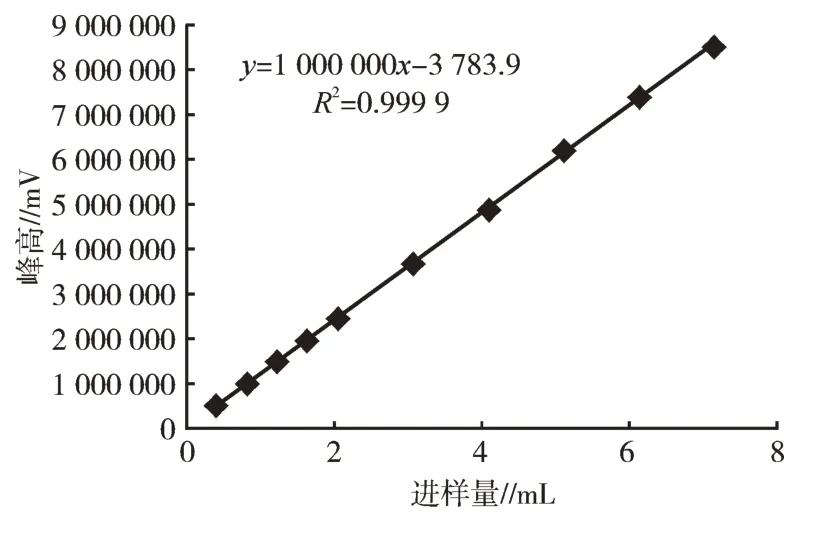
图7 Militarine 对照品的标准曲线
2.9.3 样品含量测定 由表12 可知,12 个产地的白及冻干片Militarine 含量为5.32%~10.73%,其中,云南省普洱市、重庆市、陕西省的白及冻干片Militarine 含量均低于6.00%,湖南省张家界市的白及冻干片Militarine 含量高于9.00%,其余8 个产地的白及冻干片Militarine 含量均在6.00%~9.00%,表明不同产地的白及冻干片Militarine 含量存在一定差异。
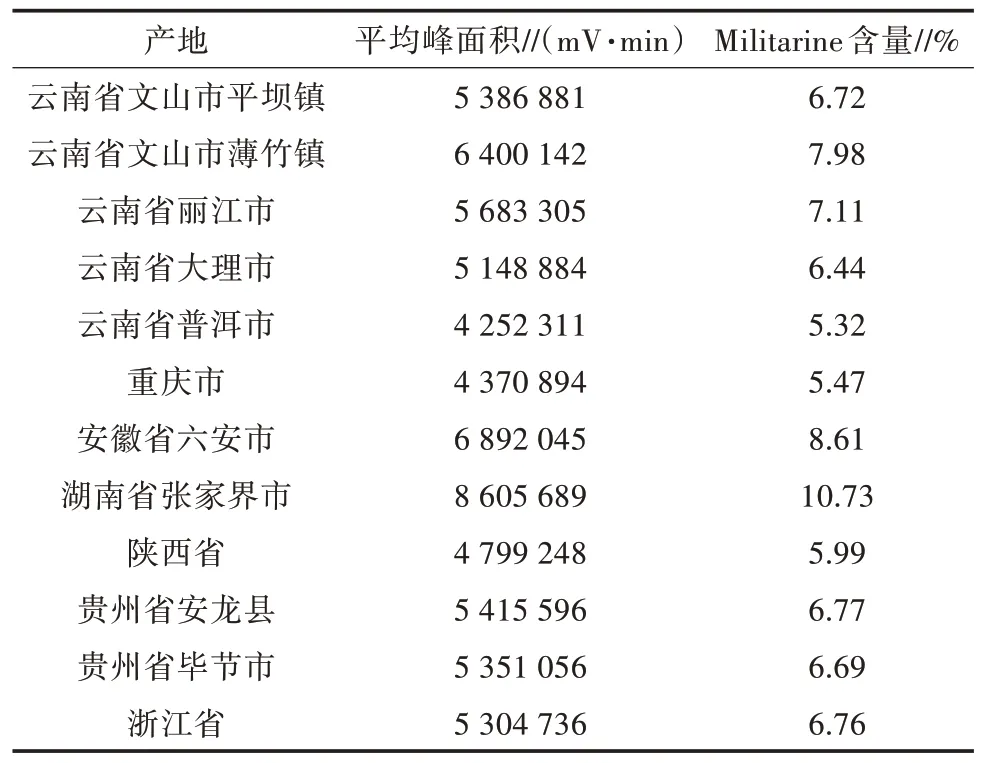
表12 白及冻干片Militarine 含量测定
3 小结与讨论
随着冷冻干燥技术的发展,越来越多的人选择冷冻干燥产品,这种产品可以保持食品的原有形状,更好地保护产品中一些热敏性和不稳定的活性成分。本研究以12 个产地的白及冻干片为原料,对白及冻干片的质量进行研究,发现不同产地白及冻干片的总多糖与Militarine 含量丰富,新加工工艺能更好地保留有效成分,质量符合规定。
白及冻干片粉末显微特征明显,草酸钙针状结晶、纤维束及硅质块细胞、导管、糊化淀粉块清晰可见,与白及显微特征一致,鉴定结果符合《中国药典》[10]相关规定。本研究发现12 个产地的白及冻干片含水量均不超过7.00%,与《中国药典》[10]规定的白及粉末的含水量不同,这可能与白及的生长环境、种植方式等有关;白及冻干片的总灰分含量符合《中国药典》[10]规定的限量;白及多糖的含量一直备受关注,白及多糖的药效作用也不断得到证实,本研究结果表明,12 个产地白及冻干片总多糖含量差异较小但也存在一定的差异,可能与白及的产地和种植方式有关,为药材冻干处理方法的研究提供了一定的理论依据;测定12 个产地的Militarine 含量,并对白及冻干片的质量进行评价,结果表明,湖南省张家界市的Militarine 含量最高(10.73%),云南省普洱市的Militarine 含量最低(5.32%),不同产地的白及冻干片Militarine 含量差异较大,说明地域、生长环境、采收时间等因素影响其内在质量[12]。

