阿伐曲泊帕治疗肝硬化和原发性肝癌患者血小板减少症疗效分析*
钟 欢,叶 伟
血小板(platelet,PLT)减少(<100×109/L)是肝硬化和原发性肝癌(primary liver cancer,PLC)患者常见的血液学异常表现之一。在肝硬化患者,PLT减少发生率高达64%~84%,是预后不良的独立预测因子[1]。中重度PLT减少可能导致出血风险增加,影响侵入性检查和治疗的进行[2]。阿伐曲泊帕,一种新型口服促PLT生成素受体激动剂(thrombopoietin receptor agonists,TPO-RA),ADAPT-1和ADAPT-2 Ⅱ期临床研究显示该药对肝硬化和PLC患者PLT减少有显著的疗效[3],并于2020年7月在中国获批上市。目前,我国关于阿伐曲泊帕治疗慢性肝病导致的PLT减少的真实世界研究还较少。本研究回顾性分析了我院应用阿伐曲泊帕治疗肝硬化和PLC患者PLT减少症的疗效,现将结果报道如下。
1 资料与方法
1.1 病例来源 2021年1月~2022年8月南京市第二医院诊治的肝硬化和PLC并发PLT减少症患者40例,脱落4例(无PLT随访记录),纳入36例,男性26例,女性10例;平均年龄为55.92±10.03岁。在20例肝硬化患者中,HBV感染 11例,HCV 感染2例,原发性胆汁性肝硬化 4例,酒精性肝病 1例,不明原因 2例;在16例PLC患者中,HBV感染12例,HCV感染1例,不明原因肝硬化3例。肝硬化的诊断依据《肝硬化诊治指南(2019年)》的标准[4],PLC的诊断依据《原发性肝癌诊疗指南(2022年版)》的标准[5]。临床上,分别将PLT为50~100 × 109/L、20~50 × 109/L和<20 × 109/L定义为轻、中、重度PLT减少症[2]。在本组36例患者中,轻、中、重度PLT减少症患者分别为3例、26例和7例。
1.2 治疗方法 对于PLT <40× 109/L患者,给予马来酸阿伐曲泊帕(苏可欣,Kawashima PLant,Eisai co.,Ltd)60 mg口服,1次/d,共5 d;对于PLT为 40~50× 109/L患者,给予40 mg口服,治疗5 d;对于PLT低于20× 109/L患者,给予苏可欣60 mg口服,联合应用重组人PLT生成素(recombinant human thrombopoietin, rhTPO,特比澳,沈阳三生制药有限责任公司)300 U.kg-1.d-1皮下注射,在7例患者,给予重组人白介素-11(interleukin-11,IL-11)(巨和粒,齐鲁制药有限公司)25~50μg.kg-1皮下注射,1次/d。在10例患者,因在有创操作前PLT仍未达到50×109/L患者,给予单采PLT 1个治疗量输注。
1.3 检测与检查 使用美国贝克曼公司生产的COULTER LH 750 / LH 755 全自动血液分析仪及其配套试剂检测外周血PLT计数;使用日立7600全自动生化分析仪及其配套试剂检测血生化指标;使用希森美康CS-5100全自动凝血分析仪检测凝血功能指标,包括国际标准化比值(INR);使用飞利浦 Brilliance 64排螺旋CT行腹部检查,测量脾脏长径。
2 结果
2.1 治疗前后PLT变化情况 治疗后,外周血PLT 计数显著升高,差异有统计学意义(P<0.001,图1),提示阿伐曲泊帕可有效升高肝硬化和PLC患者PLT水平。阿伐曲泊帕治疗后PLT升高的高峰出现在(10.5±3.7)d。本组另有4例(11.1%)出现治疗后PLT计数较基线下降,3例(9.7%)PLT计数升高<10×109/L。

图1 阿伐曲泊帕治疗前后PLT计数变化
2.2 治疗后PLT≥50×109/L的独立因素分析 33例中重度PLT减少患者治疗后PLT≥50×109/L者21例(63.6%),被定义为应答组,PLT<50×109/L者12例(36.4%),被定义为未应答组,两组间各指标差异见表1。进一步将两组年龄、性别、肝硬化合并肝癌、病毒性肝炎、Meld评分、脾脏上下径、应用rhTPO/IL-11和输注PLT等相关因素进行单因素和多因素分析,结果显示Meld评分是影响应答的独立危险因素(P=0.041),Meld评分越低的患者治疗后PLT≥50×109/L的可能性越大(表2)。当Meld评分为16时,其预测的敏感度为81.0%,特异度为66.7%(图2)。

表1 两组有关指标[%,(x2)]比较
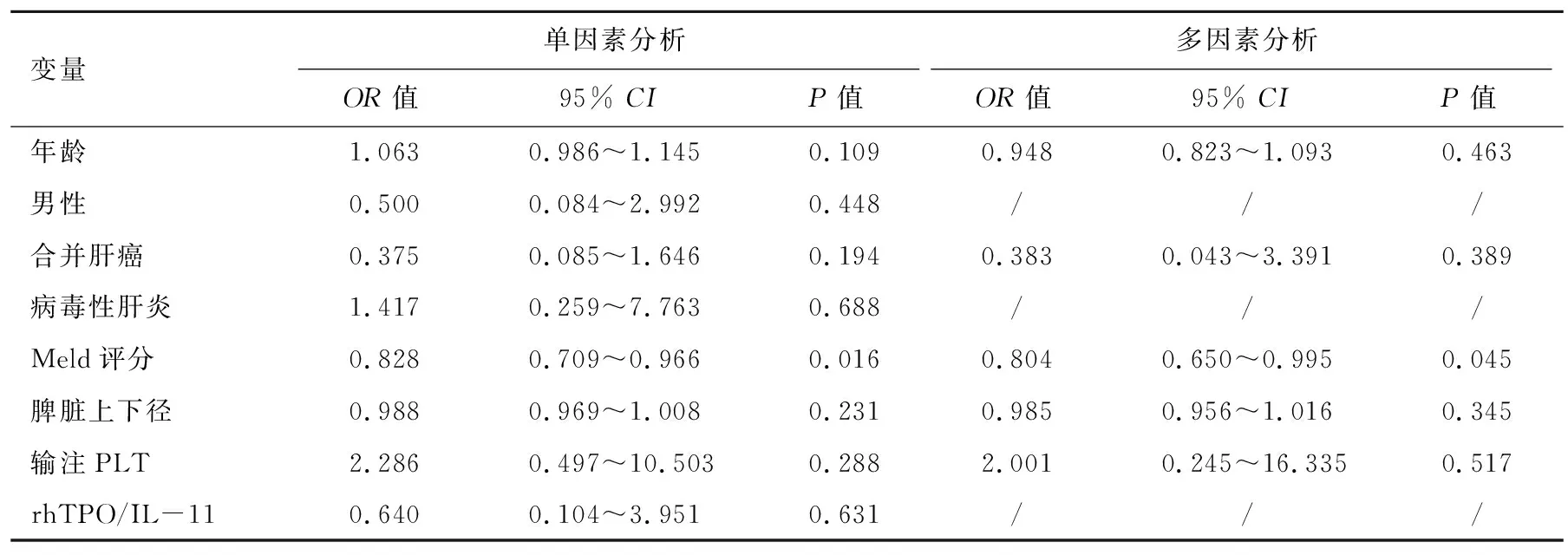
表2 影响阿伐曲泊帕治疗应答的单因素和多因素Logistics回归分析

图2 Meld评分预测阿伐曲泊帕治疗应答的ROC曲线
3 讨论
处理肝硬化和PLC导致的PLT减少症的方法包括输注单采PLT、脾动脉栓塞、脾切除和经颈静脉肝内门腔静脉分流术等[6]。与缓解PLT破坏相比,刺激PLT再生是一个新方法。阿伐曲泊帕是第二代 TPO-RA,可用于择期行诊断性操作或手术的成人慢性肝病导致的PLT减少症的治疗。在亚洲人群,例如中国和日本的研究均显示其安全有效[7-9]。在本研究,治疗后63.6%(21/33)中重度PLT减少症患者PLT≥50 × 109/L,PLT的高峰出现在10 d,这些结果均与ADAPT-1和ADAPT-2研究结果相类似。
肝硬化和PLC导致PLT减少的病理生理学机制主要与脾功能亢进、促PLT生成素分泌减少有关[1]。有研究显示肝硬化患者血循环内高达90%PLT可能被隔离在肿大的脾脏内,脾脏大小在一定程度上与PLT计数呈负相关[10],但也有研究显示终末期肝病患者脾脏体积与PLT关系并不密切[11]。TPO主要在肝脏产生。TPO生成减少与肝脏疾病的严重程度有关[12]。本研究结果显示Meld评分是预测治疗应答的独立因素,表明肝脏功能可能是决定阿伐曲泊帕治疗效果的关键因素之一。有研究显示慢性丙型肝炎患者PLT减少的发病率要高于慢性乙型肝炎患者[13]。本组仅有3例丙型肝炎患者,无法进行比较。
目前,国内外有多部指南和共识均推荐慢性肝病导致的PLT减少症(PLT<50×109/L)患者在侵入性操作和围手术期前应用阿伐曲泊帕以升高PLT计数[14,15]。本组29例患者在治疗过程中行侵入性操作,包括经血管介入手术、肝穿刺活检、胸腹腔穿刺术、内镜下操作等。对于重度血小板减少症患者联合应用rhTPO/IL-11和输注PLT等治疗,仍有8例患者在操作前PLT仍然<50×109/L,但均未见术中或术后出血并发症发生。本组应用阿伐曲泊帕联合rhTPO/IL-11与单用阿伐曲泊帕治疗对PLT计数的影响无显著差别,此前也有类似的报道[16]。目前,普遍认为对于PLT<50×109/L、需行有创手术的慢性肝病患者,预防性输注PLT从而降低出血风险。但反复多次输注PLT,可产生同种免疫反应,导致PLT输注无效或发热反应等[17]。对于阿伐曲泊帕治疗效果不应答的患者,输注PLT的有效性也值得进一步研究。

