替吉奥联合吉西他滨治疗晚期胰腺癌的疗效及对卡氏评分的影响
周园,叶振君
胰腺癌作为临床中常见的消化系统恶性肿瘤,具有较高的病死率。根据相关资料统计数据发现,大部分患者确诊时已发生远处转移,且一定数量患者已发展为晚期,无法进行根治性切除手术。对于此类型患者,临床中多应用化疗措施,延长患者生存期。需注意的是,胰腺癌多发于高龄群体,因为机体功能降低,耐受不理想等因素的影响下,常规化疗药物对机体的损伤较大,伴有严重程度不同的不良反应,大大降低患者的生活质量[1]。故选择何种药物实施化疗可保证效果的同时,降低不良反应是当下研究的重点。吉西他滨作为临床基础性化疗药物,长时间使用的效果理想,但经由研究证明,尤其是胰腺癌患者术后应用吉西他滨会对消化道和免疫功能造成严重影响,限制了预后,因此单纯使用吉西他滨对晚期胰腺癌患者尽管存在一定效果,但整体疗效偏低。替吉奥作为一种氟尿嘧啶类药物,也是近年来推广应用的新型抗肿瘤药物,在药物使用后可抑制氟尿嘧啶活化物降解、抑制5-氟尿嘧啶磷酸化的方式发挥抗肿瘤作用,吉西他滨、替吉奥均是目前用于治疗胰腺癌的一线药物[2]。本文观察替吉奥联合吉西他滨治疗晚期胰腺癌的疗效及对卡氏评分的影响,总结其应用价值,现报道如下。
1 资料与方法
1.1 临床资料 选择2017年11月—2020年11月广东省惠州市第六人民医院收治的晚期胰腺癌患者60例,其中囊腺癌21例,腺癌30例,未分化癌9例;Ⅲ期18例,Ⅳ期42例。根据随机数字表法分为观察组和对照组各30例。观察组患者男16例,女14例,年龄60~88(72.33±0.38)岁。对照组患者男13例,女17例,年龄59~86(72.35±0.35)岁。2组临床资料比较差异无统计学意义(P>0.05),存在可比性。
1.2 选择标准 纳入标准:(1)所有患者均经B超、CT、逆行胰胆管造影、细胞学检查等方式确诊为晚期胰腺癌;(2)未进行抗肿瘤治疗。排除标准:(1)对本研究药物无法耐受者;(2)交流障碍者;(3)急性期和生命体征不稳定者。
1.3 治疗方法 对照组单纯应用注射用盐酸吉西他滨(江苏豪森药业集团有限公司生产)1 000 mg/m2静脉滴注,第1天、第8天,28 d为1个周期,最少治疗2个周期。观察组在对照组基础上联用替吉奥片(福州海王福药制药有限公司生产)40~60 mg口服,每天2次,体表面积1.25 m2口服40 mg/次;体表面积1.25~1.50 m2口服50 mg/次;体表面积>1.50 m2口服60 mg/次,持续口服2周后,停药1周,为1个周期,最少治疗2个周期。
1.4 观察指标与方法 比较2组治疗效果,治疗前后卡氏评分、癌胚抗原、糖类抗原199(CA199)水平、生活质量评分及不良反应。(1)卡氏评分:>80分为非依赖,50~80分为半依赖,<50分为依赖,得分与生活自理功能呈正比;(2)癌胚抗原和CA199水平:应用酶联免疫吸附法测定(ELISA)法检测癌胚抗原和CA199水平;(3)生活质量评分:使用QLQC-30生活质量核心调查评分量表,包括认知水平、情绪状态、角色功能、身体功能、社会功能评分及总分;(4)不良反应。
1.5 疗效评定标准 显效:临床症状消失,病灶消除;有效:肿瘤体积有所缩小,幅度>50%,症状有所缓解;无效:治疗后肿瘤大小、临床症状无改善或加重。总有效率=(显效+有效)/总例数×100%。

2 结 果
2.1 治疗效果比较 观察组临床治疗总有效率为93.33%,高于对照组的56.67%(χ2=10.755,P=0.001),见表1。

表1 对照组与观察组治疗效果比较 [例(%)]
2.2 治疗前后卡氏评分比较 治疗前,2组卡氏评分比较差异无统计学意义(P>0.05);治疗后,2组卡氏评分均高于治疗前,且观察组高于对照组(P<0.01或P<0.05),见表2。
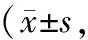
表2 对照组与观察组治疗前后卡氏评分比较分)
2.3 治疗前后癌胚抗原及CA199水平比较 治疗前,2组癌胚抗原及CA199水平比较差异无统计学意义(P>0.05);治疗后,2组癌胚抗原水平低于治疗前,且观察组低于对照组(P<0.01或P<0.05);治疗后,2组CA199水平均无显著变化(P>0.05),见表3。
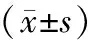
表3 对照组与观察组治疗前后癌胚抗原及CA199水平比较
2.4 治疗前后生活质量评分比较 治疗前,2组生活质量评分比较差异无统计学意义(P>0.05);治疗后,2组认知水平、情绪状态、角色功能、身体功能、社会功能评分及总分均高于治疗前,且观察组高于对照组(P<0.01或P<0.05),见表4。
2.5 不良反应比较 观察组消化道反应、肝功能异常、肾功能异常不良反应总发生率为13.33%,低于对照组的36.67%(χ2=4.355,P=0.036),见表5。

表5 对照组与观察组不良反应比较 [例(%)]
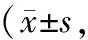
表4 对照组与观察组治疗前后生活质量评分比较分)
3 讨 论
胰腺癌起病隐匿,具有较高的病死率,患者在诊断的过程中多数已发展为晚期,失去手术根治的机会,因此需要化疗保守治疗[3]。对高龄患者来说,因为老年患者机体功能降低,对药物耐受性下降,合并各种慢性疾病,影响化疗的实施。结合实际情况分析,晚期胰腺癌的治疗较为困难,故目前研究重点已放在缓解疼痛和控制病情方面[4]。
吉西他滨作为一种胞嘧啶核苷产物,在胰腺癌的治疗中发挥显著效果,但根据相关资料显示,应用该药物治疗后,患者将会存在各种不良反应,影响其预后,该药物是一种嘧啶类抗代谢物,在细胞内经核苷激酶的作用,被代谢为具有活性的二磷酸、三磷酸核苷。其可抑制DNA合成,发挥吉西他滨的细胞毒作用,并抑制肿瘤细胞DNA的合成[5]。尽管吉西他滨是晚期胰腺癌的一线方案,但在相关治疗中记载,应用吉西他滨的患者生存期并不理想,且随着胰腺癌的发病率上升,其治疗困难的问题逐渐严重。替吉奥是由替加氟、吉美嘧啶、奥替拉西钾组成的复方制剂,口服给药后替加氟在机体内转化为5-FU发挥抗肿瘤效果[6]。吉美嘧啶主要在肝脏分布,对5-FU分解代谢酶DPD具有选择性拮抗作用,提高替加氟转化为5-FU的浓度,促使肿瘤内5-FU的磷酸化代谢产物5-FUMP以高浓度持续存在,提高抗肿瘤效果[7]。该药口服后,主要对消化道内分布的乳清酸磷酸核糖基转移酶有选择性拮抗作用,抑制5-FU转化为5-FUMP[8]。在胰腺癌中,氟尿嘧啶是广泛应用的药物,研究显示,替吉奥单药或联合治疗可提高胰腺癌的临床治疗效果,并延长患者的生存期[9]。因为替吉奥的血药浓度更高、给药便捷、具有较高安全性等优势,在高龄胰腺癌晚期患者的化疗中,适用性更高,结合吉西他滨的优势和缺点分析,尽管可缓解病情,但生存期较短,使联合化疗的方案更为关键,吉西他滨通过竞争性抑制肿瘤细胞遗传物质的形成,替吉奥则预防成分降解,避免消化道不良反应,前者可提高氟尿嘧啶的活性,提高替吉奥的抗肿瘤活性,两种药物联合使用,效果明显。本研究结果显示,观察组癌胚抗原水平及卡氏评分均优于对照组,主要原因在于,替吉奥联合吉西他滨治疗可显著改善患者的免疫功能,并增强抗肿瘤效果。CA199在胰腺癌的诊断中具有高度敏感性和特异性,但差异并不明显,主要原因可能与疾病恶性程度、肿瘤负荷具有密切联系。观察组认知水平、情绪状态、角色功能、身体功能、社会功能评分及总分等各项生活质量明显改善,其幅度较对照组差异明显,主要因素在于化疗药物的使用、肿瘤负荷的上升均会导致患者的不良反应,化疗药物在杀伤肿瘤细胞的同时,也会对机体的正常细胞造成影响,发生多种不良反应,联合用药可减少药物毒性,提高精神状态,从而提高生活质量,同时也减少消化道反应、肝功能异常、肾功能异常等不良反应。尤其是消化道不良反应方面,替吉奥可预防有效成分的降解,并减轻消化道不良反应。相关研究显示,替吉奥联合吉西他滨可降低骨髓抑制发生率,总体来说,替吉奥联合吉西他滨较之单药治疗效果更明显,可显著降低不良反应,改善免疫功能,加强抗肿瘤效果,改善生活质量。
综上所述,替吉奥联合吉西他滨治疗晚期胰腺癌患者的整体治疗效果更优,可降低癌胚抗原水平,改善患者的生活自理能力,综合提高生活质量,其值得临床研究和借鉴。
利益冲突:所有作者声明无利益冲突。

