虚拟手术规划在肺结节微弹簧圈定位胸腔镜切除术中的应用
崔翔宇 鲁瑞珍 由玉梅 韩文洁 张志学 赵景岚

[摘要] 目的
探讨基于医学影像控制系统虚拟围手术期规划在肺结节有创定位解剖性亚肺叶胸腔镜切除术中的应用价值。
方法 收集2019年4月—2020年7月于青岛市中心医院胸外科行胸腔镜亚肺叶切除术的病人75例。根据对病人肺结节采取的定位方法分为三维重建、微弹簧圈及三维重建+微弹簧圈3组,比较3组并发症、定位时间、手术时间、确定结节位置时间、使用闭合器钉仓数量、结节一次性切除情况及住院总费用的差异。
结果
3组定位方法定位时间的差异有统计学意义(F=265.37,P<0.05),三维重建+微弹簧圈组较三维重建组和微弹簧圈组的定位时间长,三维重建组较微弹簧圈组的定位时间长(P<0.05)。3组确定病变结节位置时间差异有统计学意义(F=2.98,P<0.05),三维重建+微弹簧圈组长于三维重建组和微弹簧圈组(P<0.05)。3组使用闭合器钉仓数量差异有统计学意义(F=2.51,P<0.05),三维重建+微弹簧圈组使用数量少于三维重建组(P<0.05)。3组的手术时间、住院总费用和结节一次切除率差异无显著意義(P>0.05)。
结论 肺结节穿刺定位后行三维重建虚拟手术规划并联合微弹簧圈标记定位,在解剖性亚肺叶胸腔镜切除术中可确保安全切缘距离,同时能迅速确定离体组织病变结节位置,有精准、安全、有效的特点,具有很好的临床应用价值。
[关键词] 成像,三维;胸外科手术,电视辅助;定位;多发性肺结节
[中图分类号] R445;R561
[文献标志码] A
[文章编号] 2096-5532(2023)06-0921-05
doi:10.11712/jms.2096-5532.2023.59.193
[网络出版] https://link.cnki.net/urlid/37.1517.R.20231229.1009.001;2023-12-29 12:08:08
APPLICATION OF VIRTUAL SURGICAL PLANNING IN THORACOSCOPIC RESECTION WITH MICROCOIL LOCALIZATION FOR PULMONARY NODULES
CUI Xiangyu, LU Ruizhen, YOU Yumei, HAN Wenjie, ZHANG Zhixue, ZHAO Jinglan
(Department of Thoracic Surgery, The Affiliated Central Hospital of Qingdao University, Qingdao 266042, China)
; [ABSTRACT]ObjectiveTo evaluate the value of perioperative virtual planning based on the medical image control system for thoracoscopic anatomical sublobectomy with invasive localization for pulmonary nodules.
MethodsWe included a total of 75 patients who underwent thoracoscopic sublobectomy in the Department of Thoracic Surgery of Qingdao Central Hospital from April 2019 to July 2020. According to the lung nodule localization methods, they were divided into three groups: three-dimensional (3D) reconstruction group, microcoil group, and 3D reconstruction + microcoil group. The three groups were compared in terms of complications, localization time, surgical time, nodule localization time, the number of closure staples used, first-attempt success rate for nodule resection, and total hospitalization cost.
ResultsThe localization time differed significantly between the three groups (F=265.37,P<0.05); the 3D reconstruction + microcoil group had a significantly longer localization time than the 3D reconstruction group and the microcoil group, and the 3D reconstruction group had a significantly longer localization time than the microcoil group (P<0.05). The nodule localization time was significantly different between the three groups (F=2.98,P<0.05), which was significantly longer in the 3D reconstruction + microcoil group than in the 3D reconstruction group and the micro coil group (P<0.05). There was a significant difference in the number of staples used between the three groups (F=2.51,P<0.05); the 3D reconstruction + microcoil group used significantly fewer staples than the 3D reconstruction group (P<0.05). No significant differences were found between the three groups in surgical time, total hospitalization cost, and first-attempt success rate for nodule resection (P>0.05).
Conclusion3D reconstruction-based virtual surgical planning combined with microcoil localization after puncture localization of pulmonary nodules can ensure a safe distance to the margin and quickly determine the location of no-
dules during thoracoscopic anatomical sublobectomy. It is accurate, safe, effective, and of great value for clinical application.
[KEY WORDS]imaging, three-dimensional; thoracic surgery, video-assisted; positioning; multiple pulmonary nodules
肺段切除是早期发现的肺结节的有效诊疗手段。但肺段解剖结构复杂、变异较多,肺段精准切除较为困难。特别对于位置较深、体积较小、亚实性的结节,术中难以找到[1-2]。精准有效地切除肺段、提高手术的成功率是胸外科研究的热点。目前尚未发现三维重建技术与微弹簧圈穿刺定位技术在肺结节定位胸腔镜切除手术中应用的对比研究文献。我院术前将三维重建和微弹簧圈定位肺结节联合应用,充分发挥两者的优势,弥补三维重建的不足,缩短术中发现肺结节的时间,提高解剖性肺段精准切除的安全性、有效性,以期为临床肺小结节外科手术治疗提供参考。现将结果报告如下。
1 资料与方法
1.1 研究对象
选取2019年4月—2020年7月于青岛市中心医院胸外科行胸腔镜亚肺叶切除手术的病人75例,其中女性45例,男性30例,年龄36~77岁。按术前对病人采取的定位方法不同分为单纯三维重建肺结节定位组(三维重建组,A组)、单纯肺结节微弹簧圈标记定位(微弹簧圈组,B组)及三维重建+微弹簧圈肺结节定位组(三维重建+微弹簧圈组,C组),每组25例。本研究经本院伦理委员会批准,所有入组病人均签署知情同意书。
1.2 纳入及排除标准
纳入标准:①临床CT随访1年以上高度怀疑为恶性病变的病人;②术前已获病理学支持为原位腺癌、微浸润性腺癌或者浸润性腺癌且无肺外转移且影像学检查证实肿瘤倍增时间≥400 d的病人;③在肺高分辨率CT下肺内周围型非侵袭性病变(肺实质外侧1/3)、病变直径在0.5~2.0 cm且纯磨玻璃结节或实性成分≤50%的非纯磨玻璃结节病人;④同意参加本研究并且签署知情同意书和临床手术及CT引导下肺穿刺知情同意书的病人。排除标准:①直径<0.5 cm的纯磨玻璃影结节病人;②凝血障碍和严重心、肺功能不全无法耐受手术的病人;③合并其他病变情况需先行处理的病人。
1.3 设備与材料
采用美国GE Lightspeed 16排螺旋CT,扫描方法:扫描时嘱病人平静呼吸,根据结节所在位置确定扫描层面,扫描层厚2.5 mm,重建层厚2.5 mm,螺距1.375∶1。采用美国COOK公司的微弹簧圈(国械注进20173776536,规格9、15 cm)和日本八光公司的穿刺针(国械注进20173156872,规格22G)。肺结节数字三维重建采用Mimics Medical 21.0虚拟三维重建软件(MIMICS)。
1.4 肺结节定位方法
1.4.1 三维重建定位方法 将胸部CT图像导入MIMICS软件,对肺结节、动静脉血管及支气管进行重建,明确肺结节所在靶肺段、肺叶解剖关系,规划手术方案。MIMICS虚拟三维重建由经过专业培训并能熟练操作的主治医师完成。
1.4.2 微弹簧圈定位法 ①选取适宜穿刺路径摆放体位(穿刺路径一般取结节至胸膜最短径),体位摆放要求稳定。②低剂量CT扫描,体表标记定位,消毒、铺洞巾、局部浸润麻醉。③非血管介入穿刺针沿穿刺路径穿刺至胸膜,行胸膜麻醉;行低剂量CT扫描(脏、壁层胸膜间最好形成液平便于留尾)。④非血管介入穿刺针入肺,针尖至结节旁(<1 cm)行低剂量CT扫描。⑤将弹簧圈头端沿非血管介入穿刺针推至结节边缘,退针(非血管介入穿刺针退至脏层胸膜外),低剂量CT扫描。⑥将弹簧圈尾端完全推出至脏层胸膜表面(留尾),嘱病人屏气后拔针,局部包扎。行低剂量CT扫描,检查有无出血、气胸等并发症,观察弹簧圈位置。嘱病人静卧休息,观察10 min,如病人无明显不适即可返回病房待手术。穿刺定位由从事放射介入工作>10年的副主任医师完成。
1.4.3 三维重建+微弹簧圈定位 将三维重建定位和微弹簧圈定位联合应用。
1.5 手术方法
①采用双腔气管插管全麻,单肺通气,选取腋中线第7肋间约1 cm切口作为观察孔,腋前线第4或第5肋间约3~4 cm切口作为主操作切口;②置入切口保护套及腔镜器械,离断靶肺段动脉、支气管、静脉,注意保留段间静脉避免损伤,利用肺膨胀萎陷原理确定段间平面,直线切割吻合器切除靶肺段送快速病理检查,淋巴结采样,严格止血,放置20号引流管1根。手术由从事胸外科工作>30年的同一主任医师完成。
1.6 观察指标
收集病人的性别、年龄、结节位置、结节大小、结节深度、结节影像学表现等信息。比较3组定位成功率和并发症发生率;比较3组病人的手术时间、术中出血量、结节切缘距离、切除病变组织后寻找病灶时间、使用闭合器钉仓数量、结节一次性切除情况及住院总费用。
1.7 统计学分析
采用SPSS 26.0统计学软件进行统计学分析。
符合正态分布的计量资料以±s表示,多组均数的比较采用单因素方差分析,两两比较采用LSD法。计数资料以例数和百分数表示,组间比较采用卡方检验和Fisher确切概率法。P<0.05为差异有统计学意义。
2 结 果
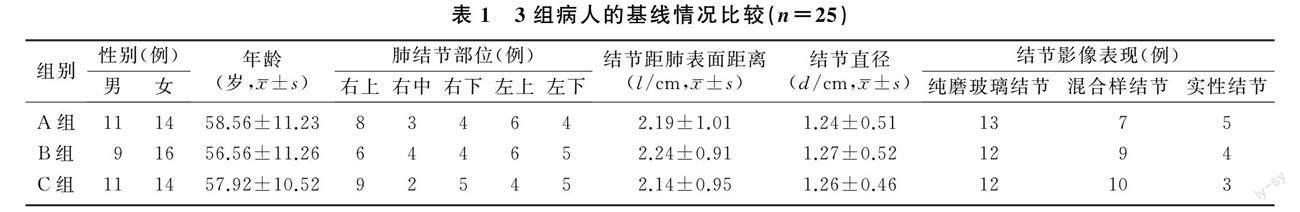
2.1 3组病人基线情况比较
本研究75例病人中,右肺上、中、下叶结节病人分别有23、6、14例,左肺上、下叶结节病人分别有17、15例。所有病人的病变直径为 0.5~2.0 cm,病变距离最近处胸膜0.4 cm。3组病人的性别、年龄、结节距肺表面距离、结节直径、肺结节部位和结节影像表现等基线资料比较差异均无统计学意义(P>0.05)。见表1。
2.2 3组并发症发生率比较
本文3组并发症发生率比较差异无统计学意义(P>0.05)。见表2。
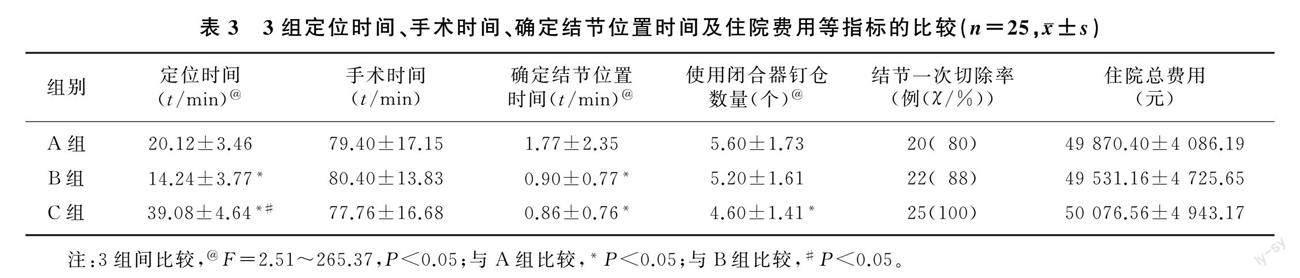
2.3 3组定位时间、手术时间、确定结节位置时间及住院费用比较
本文3组定位时间差异具有统计学意义(F=265.37,P<0.05),三维重建+微弹簧圈组较三维重建组和微弹簧圈组的定位时间长(P<0.05),三维重建组较微弹簧圈组的定位时间长(P<0.05)。3组确定病变结节位置时间差异有统计学意义(F=2.98,P<0.05),三维重建组的时间长于微弹簧圈组和三维重建+微弹簧圈组(P<0.05)。3组使用闭合器钉仓数量差异具有统计学意义(F=2.51,P<0.05),三维重建+微弹簧圈组使用数量少于三维重建组(P<0.05)。3组手术时间、住院总费用和结节一次切除率差异无显著意义(P>0.05)。见表3。
3 讨 论
电视辅助胸腔镜(VATS)手术在肺小结节治疗中的安全性、有效性及微创性已获得广泛共识[3-5]。然而,由于很难在VATS手术中进行非浅表肺结节的准确定位,往往造成术后切缘距离不足,甚至残留结节的发生[6]。准确、有效的肺小结节定位及充分的术前手术路径规划成为手术成功的关键因素之一。磨玻璃结节术中快速定位常用方法有Hookwire定位针、微弹簧圈、亚甲蓝等术前CT引导下的有创穿刺定位[7-9]。有創穿刺定位常会导致气胸、疼痛、出血、胸膜反应等并发症的发生[10]。定位针脱靶、染色剂弥散导致定位失败也时有发生[11],造成术中无法快速定位结节位置,甚至出现离体标本无法找到靶病灶而不得不扩大切除的事件发生。
近年来,基于肺部增强CT图像的术前三维重建技术广泛应用于临床[12]。影像医师将胸部肺小结节CT图像数据进行三维重建处理,使得二维CT图像转变为三维立体影像,可准确判断靶病灶的肺叶、肺段归属,进行合理术前手术规划,避免误切未受累的肺叶、肺段,最大化保留正常肺组织功能;同时准确判断病灶与血管关系,避免误断段间静脉,防止术后咯血等并发症;此外还可以发现解剖变异,有
效提高肺段切除的整体安全精确率[13-15]。HAGI-WARA等[16]证明了术前三维成像技术在评估血管分支模式方面的有效性,大约97.8%的肺动脉分支能够被准确地识别出来,并且该技术明显降低了术后并发症的发生率。在KATO等[17]的研究中,有19%的病人根据模拟结果改变了原来的手术方案。该技术实现虚拟三维结构与现实解剖结构一一对应,通过建立虚拟三维解剖结构,进行术前合理手术路径规划,避免了手术的盲目性,极大增强了外科医生对肺段、联合亚段等复杂手术实施的信心[18-19]。但是三维重建技术是在肺组织处于膨胀状态下完成的,术中肺处于萎陷状态,不容易分辨肺表面解剖标志线,并且靶病灶位置改变,当在没有更好的参照物情况下,仍然有切缘距离不足,甚至残留结节的可能发生。
目前,任何一种单一定位方法都有其局限性。刘庆文等[20]通过应用CT三维重建构建肺部的解剖结构,预先模拟手术,并联合应用Hookwire定位针技术定位肺结节,获得良好效果。但当病灶距离脏层胸膜太近时,Hookwire钩易松脱,且在牵拉钩子的过程中,甚至病人剧烈咳嗽时均会加重对肺组织的损伤,出现出血、剧烈胸痛等并发症[21]。微弹簧圈主体构造为螺旋不锈钢丝,表面缠绕人造纤维毛,置入肺内后有摩擦力且不会因呼吸运动或器械钳夹等因素的影响而移动位置,降低了脱钩率[22];其促血栓形成能力和内皮化能力使定位严重出血风险降低[23]。我们前期研究亦证实,微弹簧圈相较于亚甲蓝及Hookwire定位针定位具有精准度高、并发症少的特点[24]。本研究术前使用MIMICS虚拟三维重建软件对胸部肺小结节CT图像进行三维重建处理。相比于传统的CT成像方式,三维重建技术在许多方面都展现出了巨大的优势。通过对二维图像的三维化,可以判断靶病灶肺段、肺亚段归属,全方位、多角度观察结节与重建血管、支气管的关系。并可与软件处理工具相配合,使医生通过旋转、平移、结节分析等操作对病灶的性质和三维结构关系获得精确判断,合理规划手术路径。本研究结果提示,虽然在结节术前定位时间上三维重建+微弹簧圈组较其他两组时间显著延长,但是在离体组织结节的寻找时间以及闭合器组件的使用数量上三维重建+微弹簧圈组明显减少,减轻了病人的经济负担;由于联合了微弹簧圈定位方法,能更快定位靶病灶位置,提高切除效率,同时尽量少地切除健康肺组织,最大程度地保护了病人的肺功能。本研究结果还显示,在并发症发生率上,3组之间差异无统计学意义,但微弹簧圈定位作为有创操作,个别病例还是会有发生气胸、出血、疼痛的风险。随着术前微弹簧圈定位及对重建软件操作越来越熟练,并发症发生率会有所降低,术前定位的总时间将会逐步缩短,三维重建+微弹簧圈的联合优势将更加突出。但由于仍需术前CT引导定位,对于位置特殊病变需反复CT扫描辅助定位,不可避免地使病人过多暴露于射线环境,对病人身体健康会造成损害。
综上所述,胸腔镜亚肺叶切除手术术前进行肺三维重建虚拟手术规划结合术前微弹簧圈定位,能够直观、准确评估病变情况,合理规划手术路径,避免多切、误切肺叶和肺段,尽可能保留病人更多的正常肺功能,实现快速、有效、精准切除靶病灶的目的,而且不会增加术中出血、术后并发症等情况,可以进一步推广和应用于临床。
[參考文献]
[1]喻傲,焦子宸,周勇,等. CT引导下弹簧圈定位在肺小结节(直径≤15 mm)单操作孔胸腔镜手术中应用的回顾性队列研究[J]. 中国胸心血管外科临床杂志, 2022,29(1):68-73.
[2]GRUBER-ROUH T, NAGUIB N N N, BEERES M, et al. CT-guided hook-wire localisation prior to video-assisted thoracoscopic surgery of pulmonary lesions[J]. Clinical Radiology, 2017,72(10):898.e7-898.e11.
[3]SIHOE A D L. Video-assisted thoracoscopic surgery as the gold standard for lung cancer surgery[J]. Respirology, 2020,25(Suppl 2):49-60.
[4]NAKAZAWA S, SHIMIZU K, MOGI A, et al. VATS segmentectomy: past, present, and future[J]. General Thoracic and Cardiovascular Surgery, 2018,66(2):81-90.
[5]JEON Y J, CHOI Y S, CHO J H, et al. Thoracoscopic vs open surgery following neoadjuvant chemoradiation for clinical N2 lung cancer[J]. Seminars in Thoracic and Cardiovascular Surgery, 2022,34(1):300-308.
[6]LV K, MENG Y S, ZHANG T, et al. Preliminary application of body surface theodolitic puncture localization method in thoracoscopic surgery of pulmonary ground-glass nodules[J]. Chinese Journal of Lung Cancer, 2020,23(8):662-666.
[7]FAN L W, MA W Y, MA J, et al. The improved success rate and reduced complications of a novel localization device vs. hookwire for thoracoscopic resection of small pulmonary no-
dules: a single-center, open-label, randomized clinical trial[J]. Translational Lung Cancer Research, 2022,11(8):1702-1712.
[8]XU Q S, WANG T, CAO W, et al. Coil localization assisted wedge resection for pulmonary nodules in patients with malignant history[J]. Medicine, 2021,100(47):e28025.
[9]FENG Z, LIAO Q X, XIE J B, et al. Utility of methylene
blue mixed with autologous blood in preoperative localization of pulmonary nodules and masses[J]. Open Life Sciences, 2023,18(1):20220645.
[10]YANG Y L, LI Z Z, HUANG W C, et al. Electromagnetic navigation bronchoscopic localization versus percutaneous CT-guided localization for thoracoscopic resection of small pulmonary nodules[J]. Thoracic Cancer, 2021,12(4):468-474.
[11]KLIJIAN A S. Agar blue localization of small pulmonary no-
dules and ground glass opacifications for thoracoscopic resection[J]. Journal of Thoracic Disease, 2016,8(Suppl 9):S677-S680.
[12]HU C G, YANG X T, ZHAO M, et al. Three-dimensional computed tomography bronchography and angiography-guided thoracoscopic segmentectomy for pulmonary nodules[J]. Surgical Innovation, 2022,29(3):343-352.
[13]MOAL J L, PEILLON C, DACHER J N, et al. Three-dimensional computed tomography reconstruction for operative planning in robotic segmentectomy: a pilot study[J]. Journal of Thoracic Disease, 2018,10(1):196-201.
[14]LIMMER S, DICKEN V, KUJATH P, et al. Three-dimensional reconstruction of central lung tumors based on CT data[J]. Der Chirurg; Zeitschrift Fur Alle Gebiete Der Operativen Medizen, 2010,81(9):833-840.
[15]吴卫兵,唐立钧,朱全,等. 3D-CTA重建肺血管、支气管在胸腔镜复杂肺段切除中应用[J]. 中华胸心血管外科杂志, 2015,31(11):649-652.
[16]HAGIWARA M, SHIMADA Y, KATO Y, et al. High-quality 3-dimensional image simulation for pulmonary lobectomy and segmentectomy: Results of preoperative assessment of pulmonary vessels and short-term surgical outcomes in conse-
cutive patients undergoing video-assisted thoracic surgery[J]. European Journal of Cardio-Thoracic Surgery: Official Journal of the European Association for Cardio-Thoracic Surgery, 2014,46(6):e120-e126.
[17]KATO H, OIZUMI H, SUZUKI J, et al. Thoracoscopic anatomical lung segmentectomy using 3D computed tomography simulation without tumour markings for non-palpable and non-visualized small lung nodules[J]. Interactive Cardiovascular and Thoracic Surgery, 2017,25(3):434-441.
[18]WU W B, XU X F, WEN W, et al. Three-dimensional computed tomography bronchography and angiography in the preoperative evaluation of thoracoscopic segmentectomy and subsegmentectomy[J]. Journal of Thoracic Disease, 2016,8(Suppl 9):S710-S715.
[19]WU Z, HUANG Z F, QIN Y, et al. Progress in three-dimensional computed tomography reconstruction in anatomic pulmonary segmentectomy[J]. Thoracic Cancer, 2022,13(13):1881-1887.
[20]刘庆文,殷志敏,王霄霖,等. 三维重建联合Hookwire定位肺小结节在胸腔镜肺段切除术中的应用[J]. 中国胸心血管外科临床杂志, 2020,27(7):802-806.
[21]KLEEDEHN M, KIM D H, LEE F T, et al. Preoperative pulmonary nodule localization: a comparison of methylene blue and hookwire techniques[J]. AJR American Journal of Roentgenology, 2016,207(6):1334-1339.
[22]DONAHOE L L, NGUYEN E T, CHUNG T B, et al. CT-guided microcoil VATS resection of lung nodules: a single-centre experience and review of the literature[J]. Journal of Thoracic Disease, 2016,8(8):1986-1994.
[23]GUGLIELMI G, VIUELA F, DION J, et al. Electrothrombosis of saccular aneurysms via endovascular approach. Part 2: preliminary clinical experience[J]. Journal of Neurosurgery,1991,75(1):8-14.
[24]崔翔宇,徐平,戴錦朝,等. CT引导下经皮肺穿刺定位在亚肺叶切除术中应用[J]. 青岛大学学报(医学版), 2023,59(2):287-291.
(本文编辑 周晓彬)
青岛大学学报(医学版)2023年6期
