达格列净对T2DM伴HFPEF患者胰岛素抵抗、心室重构及MHR、NT-proBNP水平的影响
刘姗姗 商素亮 苏华 刘翠青★
射血分数保留的心力衰竭(Heart failure with preserved ejection fraction,HFpEF)是一种病理生理异质性较高的临床综合征,约占心力衰竭(Heart failure,HF)患病人群的40%~71%,是指患者存在心衰症状及体征,但左心室射血分数(Left ventricular ejection fraction,LVEF)大致正常[1]。有研究认为2型糖尿病(Type 2 diabetes mellitus,T2DM)与HFpEF 发生密切相关,可能与T2DM 引起的内皮细胞功能紊乱、胰岛素抵抗等导致的心脏收舒功能失调、微血管顺应性降低等因素相关[2]。达格列净是一种具有高效率、可逆性及高选择性的钠-葡萄糖协同转运蛋白(Sodium-glucose cotransporter 2,SGLT-2)抑制剂,不仅能抑制肾脏葡萄糖重吸收,还具有良好的心脏及肾脏保护作用,被认为是一种新型的口服降糖药及抗心衰药物[3]。但关于SGLT-2 在T2DM 伴HFpEF 中是否也具有心血管保护作用还需进一步研究证实。本研究主要探讨达格列净在此类患者中的治疗效果,报道如下:
1 资料与方法
1.1 一般资料
选取2021年4月至2022年4月河北省第八人民医院收治的87 例T2DM伴HFPEF患者。纳入标准:①均符合T2DM 及心衰诊断[4-5];②LVEF≥50%;③心功能分级Ⅰ~Ⅲ级[6]。排除标准:①合并急性冠脉综合征、高度房室阻滞、扩张性心肌病、肺源性心脏病等;②对研究药物过敏或不耐受患者;③存在自身免疫性疾病或肝肾功能异常;④恶性肿瘤患者;⑤拒绝签署知情同意书。将患者按照随机数字表法分为对照组43 例和观察组44 例,两组一般资料比较差异无统计学意义(P>0.05),见表1。本研究经院医学伦理委员会批准通过,受试者或家属已签署知情同意书。
表1 两组一般资料对比[(±s),n(%)]Table 1 Comparison of general data between the two groups[(±s),n(%)]
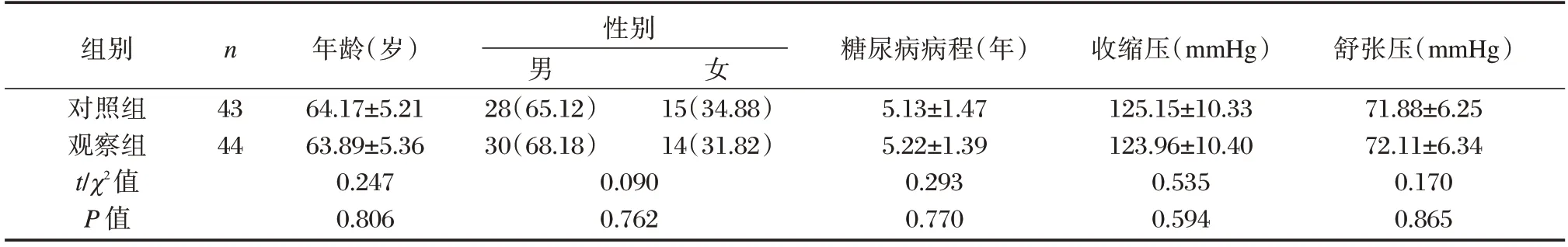
表1 两组一般资料对比[(±s),n(%)]Table 1 Comparison of general data between the two groups[(±s),n(%)]
组别对照组观察组t/χ2值P 值n 43 44年龄(岁)64.17±5.21 63.89±5.36 0.247 0.806性别男28(65.12)30(68.18)0.090 0.762女15(34.88)14(31.82)糖尿病病程(年)5.13±1.47 5.22±1.39 0.293 0.770收缩压(mmHg)125.15±10.33 123.96±10.40 0.535 0.594舒张压(mmHg)71.88±6.25 72.11±6.34 0.170 0.865
1.2 治疗方法
对照组予常规控制血糖及抗心力衰竭药物治疗,常规予血管紧张素转换酶抑制药、β 受体阻滞药、利尿剂等行抗心衰治疗,包括美托洛尔(阿斯利康,国药准字:H32025390)6.25 mg/次,3 次/日;呋塞米(上海朝晖药业,国药准字:H31021074)20 mg/次,1 次/日;阿司匹林(Bayer Healtncare Manufacturing S.r.l,国药准字:HJ20120237)100 mg/d;贝那普利(北京诺华制药,国药准字:H20000292)2.5 mg,1 次/d,无缓解可调整为5 mg/次。并予二甲双胍(正大天晴药业,国药准字:H20031104)500 mg/d或胰岛素控制血糖。
观察组在对照组基础上予达格列净(AstraZeneca Pharmaceuticals LP,国药准字:HJ20170118)10 mg/d 口服,两组均连续治疗6 个月。
1.3 观察指标
1.3.1 糖代谢及胰岛素抵抗指数
于治疗前及治疗6 个月后取患者肘静脉血液样本5 mL,3 000 r/min 离心5 min(离心半径10 cm)后分离血清,以罗氏全自动血糖仪检测患者空腹血糖(Fasting plasma glucose,FPG)、餐后2 h 血糖(2 hours postprandial blood glucose,2 hPG)、糖化血红蛋白(glycosylated hemoglobin,HbAlc)水平,并计算胰岛素抵抗指数(homeostasis model assessment-insulin resistance index,HOMA-IR)。
1.3.2 心室重构参数及血清生化指标
于治疗前及治疗6 个月后以JH-970 多普勒超声诊断仪(江苏佳华电子设备)对患者进行检测,计算两组患者左心室舒张末期容积指数(Left ventricular end-diastolic volume index,LVEDVI)、左心室收缩末期容积指数(Left ventricular end-systolic volume index,LVESVI)及左心室质量指数(Left ventricular mass index,LVMI)、左心室重构指数(Left ventricular remodeling index,LVRI)。同时收集患者空腹静脉血3 mL,3 000 r/min 离心5 min(离心半径10 cm)后分离血清,以酶联免疫吸附法完成血清基质金属蛋白酶-9(Matrix metalloproteinase-9,MMP-9)、血清胱抑素C(Cystatin C,CysC)水平检测,试剂盒购自赛默飞世尔科技有限公司。
1.3.3 单核细胞/高密度脂蛋白胆固醇比值(monocyte/HDL-C ratio,MHR)及氨基末端脑利钠肽前体(N-terminal prosoma of B-type natriuretic peptide,NT-proBNP)水平
取患者坐位肘静脉血3 mL,采集时间同上,3 000 r/min 离心5 min(离心半径10 cm)后分离血清,使用HA-360 全自动血细胞分析仪(艾康生物技术)完成单核细胞数目检测,以BS-280 全自动生化仪(迈瑞医疗)完成高密度脂蛋白胆固醇(High density lipoprotein -cholesterol,HDL-C)检测,计算MHR。并使用快速免疫分析仪检测血清NT-proBNP 水平,试剂盒购自南京基蛋生物。
1.3.4 不良反应
观察两组患者用药期间有无肝肾功能异常、低血压、低血糖等不良反应发生。
1.4 统计学方法
以SPSS 23.0 软件处理数据,计量资料以()表示,行t检验,计数资料以n(%)表示,行χ2检验,以P<0.05 为差异具统计学意义。
2 结果
2.1 两组糖代谢指标及胰岛素抵抗指数对比
观察组治疗后FPG、2 hPG、HbAlc 及HOMA-IR均低于对照组,差异有统计学意义(P<0.05)。见表2。
表2 两组糖代谢指标及胰岛素抵抗指数对比(±s)Table 2 Comparison of glucose metabolism indicators and insulin resistance index between the two groups(±s)
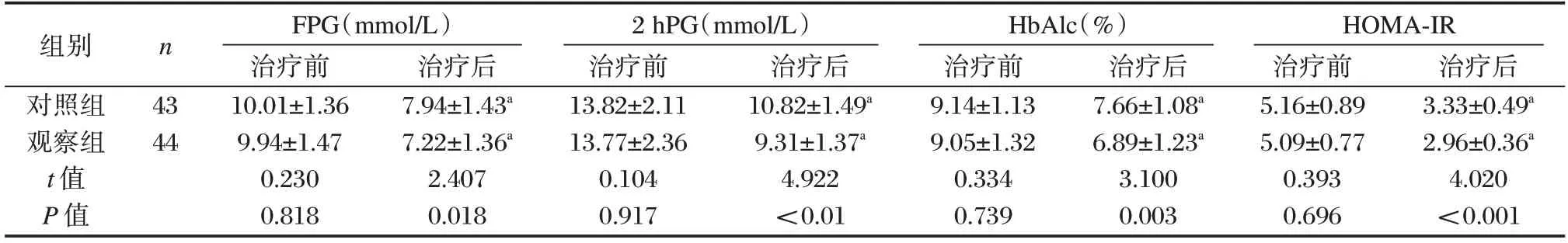
表2 两组糖代谢指标及胰岛素抵抗指数对比(±s)Table 2 Comparison of glucose metabolism indicators and insulin resistance index between the two groups(±s)
注:与本组治疗前相比,aP<0.05。
组别对照组观察组t 值P 值n 43 44 FPG(mmol/L)治疗前10.01±1.36 9.94±1.47 0.230 0.818治疗后7.94±1.43a 7.22±1.36a 2.407 0.018 2 hPG(mmol/L)治疗前13.82±2.11 13.77±2.36 0.104 0.917治疗后10.82±1.49a 9.31±1.37a 4.922<0.01 HbAlc(%)治疗前9.14±1.13 9.05±1.32 0.334 0.739治疗后7.66±1.08a 6.89±1.23a 3.100 0.003 HOMA-IR治疗前5.16±0.89 5.09±0.77 0.393 0.696治疗后3.33±0.49a 2.96±0.36a 4.020<0.001
2.2 两组心室重构参数对比
观察组治疗后LVEDVI、LVESVI、LVMI、LVRI 均低于对照组,差异有统计学意义(P<0.05)。见表3。
表3 两组心室重构参数对比(±s)Table 3 Comparison of ventricular remodeling parameters between two groups(±s)
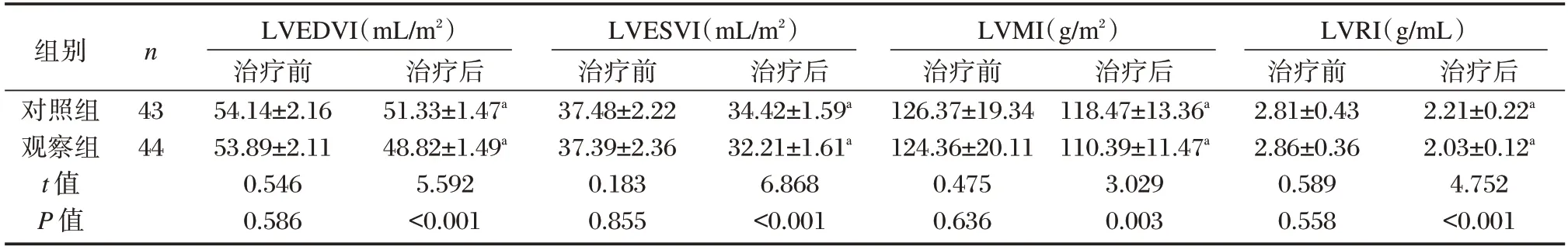
表3 两组心室重构参数对比(±s)Table 3 Comparison of ventricular remodeling parameters between two groups(±s)
注:与本组治疗前相比,aP<0.05。
组别对照组观察组t 值P 值n 43 44 LVEDVI(mL/m2)治疗前54.14±2.16 53.89±2.11 0.546 0.586治疗后51.33±1.47a 48.82±1.49a 5.592<0.001 LVESVI(mL/m2)治疗前37.48±2.22 37.39±2.36 0.183 0.855治疗后34.42±1.59a 32.21±1.61a 6.868<0.001 LVMI(g/m2)治疗前126.37±19.34 124.36±20.11 0.475 0.636治疗后118.47±13.36a 110.39±11.47a 3.029 0.003 LVRI(g/mL)治疗前2.81±0.43 2.86±0.36 0.589 0.558治疗后2.21±0.22a 2.03±0.12a 4.752<0.001
2.3 两组心室重构血清指标对比
观察组治疗后MMP-9、CysC 均低于对照组,差异有统计学意义(P<0.05)。见表4。
表4 两组心室重构血清指标对比(±s)Table 4 Comparison of serum ventricular remodeling indicators between the two groups(±s)
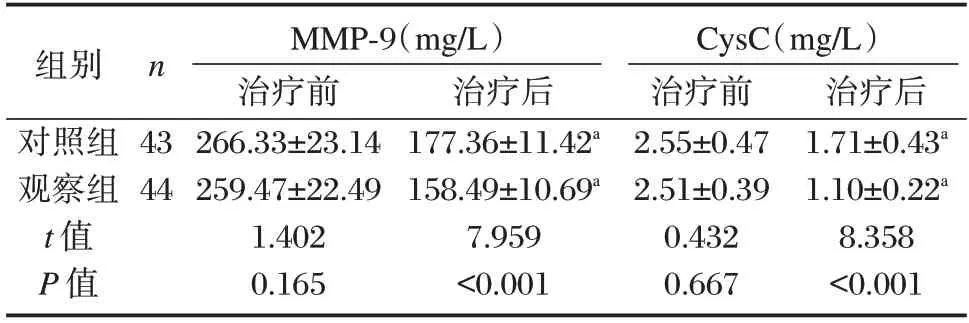
表4 两组心室重构血清指标对比(±s)Table 4 Comparison of serum ventricular remodeling indicators between the two groups(±s)
注:与本组治疗前相比,aP<0.05。
组别对照组观察组t 值P 值n 43 44 MMP-9(mg/L)治疗前266.33±23.14 259.47±22.49 1.402 0.165治疗后177.36±11.42a 158.49±10.69a 7.959<0.001 CysC(mg/L)治疗前2.55±0.47 2.51±0.39 0.432 0.667治疗后1.71±0.43a 1.10±0.22a 8.358<0.001
2.4 两组NT-proBNP 及MHR 水平对比
观察组治疗后NT-proBNP 及MHR 水平均低于对照组,差异有统计学意义(P<0.05)。见表5。
表5 两组NT-proBNP 及MHR 水平对比(±s)Table 5 Comparison of levels of NT-proBNP and MHR between the two groups(±s)
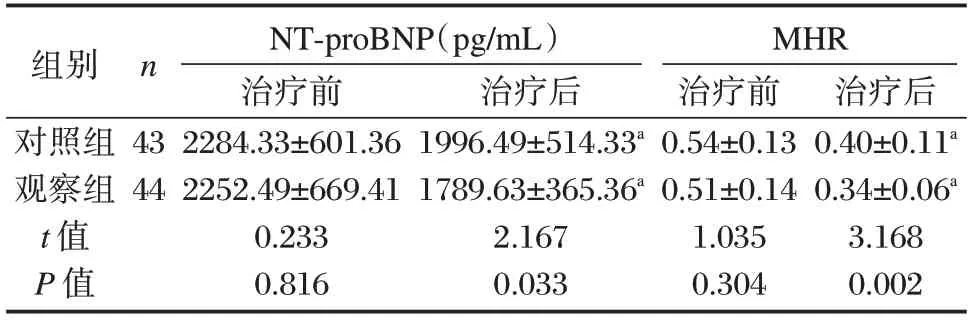
表5 两组NT-proBNP 及MHR 水平对比(±s)Table 5 Comparison of levels of NT-proBNP and MHR between the two groups(±s)
注:与本组治疗前相比,aP<0.05。
组别对照组观察组t 值P 值n 43 44 NT-proBNP(pg/mL)治疗前2284.33±601.36 2252.49±669.41 0.233 0.816治疗后1996.49±514.33a 1789.63±365.36a 2.167 0.033 MHR治疗前0.54±0.13 0.51±0.14 1.035 0.304治疗后0.40±0.11a 0.34±0.06a 3.168 0.002
2.5 两组不良反应发生情况对比
观察组出现2 例肝功能不全,另有3 例出现肾功能异常,不良反应发生率为11.36%(5/44);对照组出现低血糖1 例,肾功能异常2 例,不良反应发生率为6.98%(3/43),两组不良反应发生率对比,差异无统计学意义(χ2=0.501,P>0.05)。
3 讨论
研究认为[7],T2DM 是导致心功能异常而引发HF 的重要因素之一,其可增加心室负荷,加重心肌缺血缺氧损害。而HFpEF 常与T2DM 合并存在,与未合并T2DM 患者相比,此类患者肾功能不全及心血管不良事件发病率更高,常出现不良预后。常规治疗尽管能有效控制患者疾病进展,但诸多研究认为其远期疗效欠佳,患者再住院率仍处于较高水平,仍需探讨更趋于完备的治疗方案[8]。
达格列净为SGLT-2 抑制剂,可有效减轻肾脏水钠重吸收,并降低肾葡萄糖阈值,使葡萄糖通过尿液排出体外,以达到降低血糖的作用。江耀辉等[9]指出,在不增加胰岛素浓度的情况下,达格列净可以通过促使葡萄糖分泌进入尿液来降低机体血糖水平。本研究结果与上述研究相似。Son等[10]研究指出,胰岛素抵抗可能参与HFpEF 的病理过程,其机制与其导致的交感神经活性增加、肾素-血管紧张素-醛固酮系统活化等因素加重心脏负荷及介导心肌重构、促进心肌细胞凋亡等因素相关,积极地改善胰岛素抵抗作用对治疗HFpEF有一定的积极意义。
心肌重构是HFpEF 发生的重要病理过程,心肌细胞凋亡、胶原代谢紊乱等因素均可造成心室重构,影响患者心功能。本研究结果提示达格列净可有效逆转心室重构,改善心功能。考虑其原因除达格列净能够有效降低心脏负荷外,还与其可抑制心肌钠氢交换,降低胞质钠钙含量,减少心肌纤维细胞浸润,调节心室舒张功能,进而调节心肌能量代谢,降低不良心室重塑发生风险有关[11]。此外,研究认为NT-proBNP 水平与心脏功能关系密切,可用于反映心室壁张力降低,与心衰远期预后密切相关[12]。本研究中,观察组治疗后NT-proBNP 水平明显低于对照组,证实达格列净一定程度上可改善患者预后,考虑与其改善心肌纤维化、抑制心室重构及心脏保护作用的发挥具有一定的相关性,能够有效延缓心衰进展。
临床研究指出[13],HFpEF 患者心脏功能储备较差与患者微血管功能障碍有关,而血管炎症是其功能障碍的诱发因素之一。MHR 为单核细胞及HDL-C 比值,其中,单核细胞主要介导机体炎性反应,并参与血栓形成,与心肌细胞受损也有一定的相关性,而HDL-c水平升高可抑制单核细胞相关炎性反应。故MHR 水平升高则代表机体抗炎及抗氧化能力下降。本研究结果,提示达格列净还能参与调节机体炎性反应。既往研究已证实[14],达格列净可直接下调促炎因子释放。Daniele 等[15]指出,SGLT-2 抑制剂可以将心肌代谢的能量需求来源转化为酮体代谢,而作为抗氧化剂及抗炎因子,酮体又可以减轻炎症反应及氧化应激。故达格列净可能具有下调促炎介质表达、参与调节机体氧化应激作用,但具体机制仍需进一步探讨。而两组不良反应发生率均处于较低水平,且发生率接近,说明达格列净临床应用具有一定的安全性。
综上所述,达格列净可有效控制T2DM伴HFPEF患者血糖水平,对改善胰岛素抵抗有一定的积极作用,还能逆转心室重构,改善心功能,下调NT-proBNP 及MHR 水平,且安全性较高。

