替雷利珠单抗治疗腹直肌转移性膀胱尿路上皮癌1例
王 莹,张明晖
(1.内蒙古医科大学赤峰临床医学院,内蒙古 赤峰 024000;2.赤峰市医院肿瘤内三科,内蒙古 赤峰 024000)
1 临床资料
患者男,年龄60 岁,曾主因“发现膀胱占位3月余”就诊于西安交通大学附属医院。2020 年6 月6日行机器人辅助腹腔镜下根治性膀胱全切+ 回肠膀胱术。术后病理示:膀胱浸润性高级别尿路上皮癌伴鳞状分化(约10%),伴多数脉管内癌栓,侵犯膀胱全层至其外侧纤维脂肪组织,左盆腔淋巴结9 枚、右盆腔淋巴结8 枚,无癌转移。前列腺尿道部切缘及另送输尿管残端未见癌组织,pT3N0。患者围手术期共行6 周期的吉西他滨+ 顺铂方案化疗(术前2 周期、术后4 周期)。2021 年2 月初因“发现腹壁肿物伴疼痛”就诊于赤峰市医院,入院后评估ECOG PS 评分1 分,NRS 评分6 分,计算体表面积1.72cm2(身高178cm,体重60kg),查体左下腹可扪及包块,压痛阳性。行腹部肿块穿刺明确病理,完善腹部CT 示左侧腹直肌占位性病变,腹腔内强化结节,考虑转移瘤(图1)。由于该患者在较短时间内就出现转移征象,肿瘤明显增大,恶性程度高,预后差,建议应用替雷利单抗联合白蛋白紫杉醇化疗,因外送腹部肿物穿刺病理结果未回及替雷利珠单抗报销问题,先行给予白蛋白紫杉醇(200mg)单药化疗2 周期。后腹壁肿物穿刺活检病理回报:(腹壁活检)转移性中分化鳞癌,免疫组化:AE1/AE3(+),CK5/6(+),P40(-),CK7(+),Vimentin(-),Uroplinkin(-),CK20(-),pd-L1(约10%)。2021 年2 月4 日开始行白蛋白紫杉醇(200mg)化疗3 周期,2021 年3 月17 日(第3 周期)开始联合替雷利珠单抗(200mg)治疗。治疗后患者腹部症状明显减轻,给药后出现轻度恶心、呕吐及Ⅰ~Ⅱ度骨髓抑制等症状,对症处理后好转。2021 年4 月8 日复查腹部CT 显示腹部肿物明显缩小(图2)。2021 年4 月9 日至2021 年6 月10 日继续给予第4、第5、第6 周期的白蛋白紫杉醇联合替雷利珠单抗治疗。2021年6 月10 日再次复查CT,肿物继续缩小,相邻腹腔内强化结节较前显示不清(图3),余病情稳定。病情持续好转,继续行原免疫联合化疗方案治疗1 周期后于2021 年7 月2 日起改为替雷利珠单抗(200mg)单药免疫治疗。2021 年8 月12 日行CT 检查评估肿物已缩小至1cm 以下。2021 年8 月13 日至2021 年9 月29日继续行免疫单药治疗3 周期,治疗期间病情稳定。

图1 治疗前影像
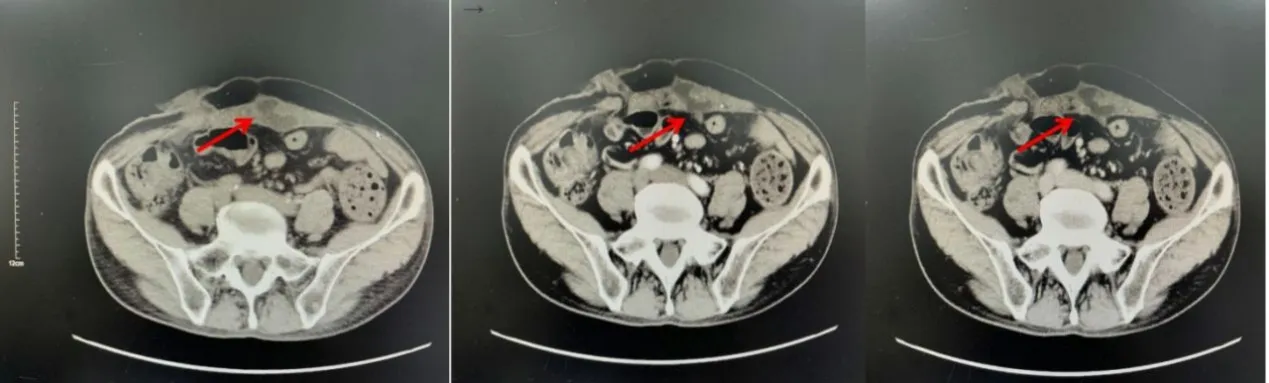
图2 1 周期免疫治疗后

图3-1 4 周期免疫治疗后

图3-2 7 周期免疫治疗后
2 讨论
据统计,尿路上皮癌(urothelial carcinoma, UC)是导致癌症相关死亡的第九大原因,UC 是发生远处转移后致死率极高的一种恶性肿瘤[1]。以铂类为基础的化疗是转移性UC 的一线综合治疗方案;治疗后患者的中位总生存期(overall survival, OS)约为12 ~15 个月[2]。一项相关的Ⅱ期临床试验[3]表明,吉西他滨+ 顺铂(GC)方案的有效率数据较为可观,约21% 的可评估患者为完全缓解(completeresponse,CR)(6/28),37%(10/28)达 部 分 缓 解(partial response, PR),总缓解率(overall response rate, ORR)为57%(16/28),OS 达13.2 个 月。然 而,大 多 数进展期或转移性UC 患者会在接受铂基础一线治疗后病情复发,大量数据已经证明了靶向治疗在UC 的二线治疗中的无效性。近些年,许多免疫治疗药物在UC 的二线治疗中显现出良好的效果[4],这为晚期UC 患者提供了更多的治疗选择。正常情况下,当肿瘤相关抗原被识别成外来物质时,免疫系统会启动T 细胞介导的抗肿瘤效应,对肿瘤细胞造成破坏。T细胞是肿瘤免疫最关键的介质之一。然而,肿瘤细胞可逃脱免疫系统的识别,不断进行自我复制,导致患者病情进展,直至死亡[5]。免疫检查点抑制剂(immune checkpoint inhibitors, ICIs)由此应运而生。ICIs 锚定于细胞程序性死亡蛋白1(programmed cell death protein 1, PD-1)、细胞程序性死亡蛋白配体1(programmed cell death 1 ligand 1, PD-L1)及 细 胞毒T 淋巴细胞关联蛋白4(cytotoxic T-lymphocyteassociated protein 4, CTLA-4),可负性减少肿瘤细胞与其表面的结合,增强T 细胞的抗肿瘤效应[6]。替雷利珠单抗正是众多PD-1 抑制剂中的一员。2020 年4 月10 日,替雷利珠单抗在中国获批用于PD-L1 高表达局部晚期或转移性UC 的治疗。它是第一个在中国被批准用于治疗尿道癌的PD-1 单克隆抗体。多项Ⅰ/ Ⅱ期临床研究表明,替雷利珠单抗在所有肿瘤的治疗中都显示出良好的安全性和耐受性[7-9]。其中一项单臂Ⅱ期试验(NCT04004221)[9]评估了替雷利珠单抗在PD-L1 阳性亚洲晚期或转移性UC 患者治疗中的安全性、耐受性和有效性。在104 例可评估患者中,其相关客观反应率为24%,包括10 例CR 和15 例PR。相关疾病控制率(disease control rate, DOR)达38%,中位无进展存活期(progressive-free survival,PFS)和OS 分别为2.1 个月和9.8 个月,PFS 率及OS率同样出色(6 个月和12 个月PFS 率:32%、20%;6 个月和12 个月OS 率:67%、43%);最常见的副反应为贫血(27%)和发热(19%),这与其他几种免疫治疗药物(阿替利珠单抗、纳武利尤单抗等)的临床数据几乎相当(ORR:21% ~46%;中位OS:10.3 ~16 个 月;中 位PFS:12 周~5.5 个 月)[10]。我国的一项真实世界数据分析[11]显示,对于接受一线含铂化疗或病情复发的晚期UC 患者,替雷利珠单抗能够更好地改善其生活质量(health-related QoL,HRQoL)。随着治疗时间的延长,在使用替雷利珠单抗的持续治疗组中,患者的生活质量随着症状的减少日趋改善;而在单纯化疗组中,患者的生活质量则随着症状的增加而降低。一项回顾性临床研究[12]分析了几种ICIs(替雷利珠单抗、特瑞普利单抗、卡瑞利珠单抗、信迪利单抗)对晚期UC 产生的免疫性副作用(immune-related adverse events,irAEs),其中95%的患者出现了以贫血最为常见的AE,88% 的患者发生了1 ~2 级AE,51% 的患者发生了3 ~4 级AE;然而,没有出现与治疗有关的死亡。需要注意的是,ICIs 治疗期间相关irAEs 的发生可能与对基础疾病的治疗有关[13-14]。据统计,晚期或进展期UC 的5 年OS 率仅为6%[15]。尽管铂类化疗在UC 治疗中的有效率很高,但大多数患者最终还是会出现疾病进展。相关免疫疗法已显示出良好的临床疗效以及可控的安全性,但仍迫切需要更多有效的治疗方案,包括单药或联合方案,以期进一步为患者带来临床获益。

