血液病住院患者感染肠道致病菌的临床特点及危险因素*
胡 波,齐 凌,卢 玮,李 菲△
1.南昌大学第一附属医院血液科,江西南昌 330006;2.江西省血液病临床医学研究中心,江西南昌330006
肠道是许多微生物的重要宿主,肠道微生物组成与越来越多的健康状况有关,尽管理想健康肠道的微生物组成尚未明确,但微生物多样性提供了微生物组内不同功能基因库的潜力,可对宿主产生有益影响,对健康或免疫功能低下的个体均可提供至关重要的保护[1-3]。而致病性微生物群的存在会破坏正常肠道微生物群,病原体的过度生长会导致腹痛、出血性腹泻、伪膜性结肠炎、毒素介导的溶血性尿毒症综合征等,严重的可引起死亡[2]。在住院患者中,腹泻随后又会导致致病性病原体传播到医疗环境中。更重要的是,当肠道黏膜屏障受损时,肠道微生物可能会转移到肠道以外,导致深层组织和血液感染[4]。
血液病包括白血病、淋巴瘤、多发性骨髓瘤、贫血等多种疾病,由于患血液病的人群免疫力低下、化学药物损伤、广谱抗生素使用,导致这类疾病患者感染肠道致病菌的风险大幅度增加,也增加了肠道致病菌感染转为血流感染的可能,进而加重患者病情[5-7]。国内关于血液病患者肠道致病菌的研究非常少见,因此本研究回顾性分析血液病住院患者感染肠道致病菌的临床特点及相关危险因素,为肠道致病菌感染的早期识别提供参考。
1 资料与方法
1.1一般资料 对2019年2-11月在南昌大学第一附属医院住院并进行粪便肠道微生物检测的血液病患者进行回顾性调查,选择粪便细菌培养分离出肠道致病菌的血液病住院患者50例作为观察组,并以同期66例无肠道致病菌的血液病患者作为对照组。
1.2方法 通过设计的调查表收集所有患者的临床资料,主要包括以下方面:患者人口学特征 (性别和年龄)、血液病类型、肠道致病菌类型、疾病状态(初治、复发、缓解)、总住院时间、消化道症状、肛周感染、侵入性操作、反复住院史、药物治疗史(化疗史、1个月内使用糖皮质激素、2个月内使用质子泵抑制剂)以及3个月内抗菌药物暴露史。

2 结 果
2.1两组患者临床资料比较 两组患者年龄、性别以及血液病分布差异无统计学意义(P>0.05)。观察组具体致病菌类型中肠球菌占比最高(40.0%),其次为真菌(8.0%)、铜绿假单胞菌(6.0%)、嗜麦芽窄食单胞菌(2.0%),其他不明确菌类占44.0%。感染肠道致病菌的血液病住院患者继发血流感染2例,感染的肠道致病菌均为肠球菌。观察组血液疾病分布中急性髓系白血病是最常见的,占56.0%,其次为淋巴瘤(12.0%)、急性淋巴细胞白血病(8.0%)。见表1。
观察组患者的初治人群比例明显低于对照组(P<0.05),而有反复住院史、化疗史及3个月内青霉素类抗菌药物、替加环素、碳青霉烯类抗菌药物暴露史的比例明显高于对照组(P<0.05)。在复发或缓解疾病状态、中性粒细胞缺乏、住院时间、消化道症状、肛周感染、侵入性操作、1个月内使用糖皮质激素、2个月内使用质子泵抑制剂及3个月内头孢菌素、喹诺酮类抗菌药物、氨基糖苷类抗菌药物、替考拉宁、利奈唑胺暴露史方面,两组比较差异均无统计学意义(P>0.05)。见表1。

表1 两组患者临床资料比较或 n(%)或M(P25,P75)]

续表1 两组患者临床资料比较或 n(%)或M(P25,P75)]
2.2血液病住院患者感染肠道致病菌的风险因素 以是否感染肠道致病菌为因变量,初治、反复住院史、化疗史及3个月内青霉素类抗菌药物、替加环素、碳青霉烯类抗菌药物暴露为自变量进行多因素Logistic回归分析。结果显示,3个月内青霉素类及碳青霉烯类抗菌药物暴露是血液病住院患者感染肠道致病菌的独立危险因素(P<0.05),见表2。
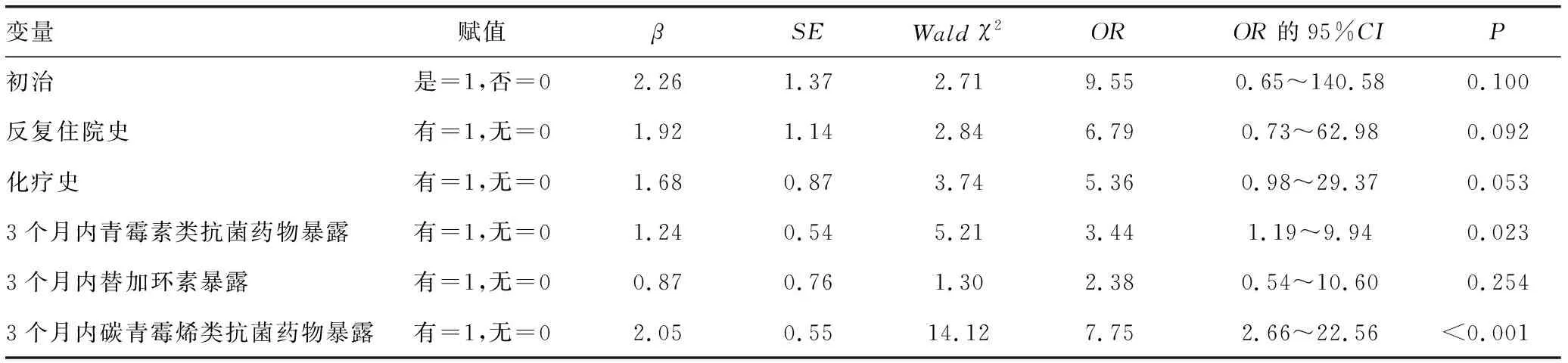
表2 血液病住院患者感染肠道致病菌的危险因素分析
3 讨 论
肠道微生态是人体内复杂和重要的有机组成部分,人体中肠道菌群数量达400~500种[8]。研究发现肠道微生物多样性具有帮助免疫系统成熟、产生短链脂肪酸、合成维生素,以及对潜在病原体定植产生屏障等多种作用,有助于抵抗外源微生物的定植(即定植抗性)[9-10]。血液病患者化疗药物相关的肠道炎症或抗菌药物处理可增加结肠上皮的氧化作用,从而破坏厌氧环境、驱动兼性厌氧菌的扩张,而导致肠道致病菌存在,进而成为优势群体,减少有益微生物的数量[2]。尤其对于免疫力低下的血液病患者,肠道致病菌定植亦是发生血流感染的早期步骤[11-13]。因此对于血液病患者肠道致病菌感染的早期识别及预防极其重要。
本研究结果显示肠道致病菌继发血流感染概率达4.0%,这与黄细莲等[14]研究耐碳青霉烯类肠道定植菌继发血流感染率类似。在肠道致病菌具体类型中,肠球菌占比最高(40.0%),其次是真菌、铜绿假单胞菌、嗜麦芽窄食单胞菌。研究发现广谱抗菌药物的广泛使用和侵入性设备的应用是导致肠球菌成为医院感染重要病原体的主要因素[15],血液病患者是感染肠球菌的高危人群。菌血症是由肠球菌引起的最常见和最重要的感染之一[15-17],本研究也体现了这一点,发生血流感染的微生物均为肠球菌。众所周知,在免疫力低下的血液病患者中真菌感染率显著增加[18],真菌一直是血液科医生防范粒细胞缺乏期白血病患者感染的重点菌属。铜绿假单胞菌及嗜麦芽窄食单胞菌是血液病患者感染耐碳青霉烯类肠杆菌的重点菌属,与病死率相关[19-21]。
本研究对存在肠道致病菌感染的血液病住院患者进行分析,发现急性髓系白血病患者发生肠道致病菌感染的风险最高,这与既往研究结果一致[22-23]。其次是淋巴瘤、急性淋巴细胞白血病。急性髓系白血病是成年人中最常见的急性白血病[24]。而此类患者由于疾病特征,需要反复住院、化疗及强力抗菌药物治疗,从而会诱发肠道微生物生态失调、总体微生物多样性减少,导致有宿主防御作用的有益细菌的破坏,而致病菌的优势增加[25]。这也提示临床医生对于上述血液病患者要注意肠道致病菌的预防。
本研究多因素Logistic回归分析提示3个月内青霉素类和碳青霉烯类抗菌药物暴露是血液病住院患者出现肠道致病菌感染的危险因素,这与既往研究结果相似[26]。通过单因素分析,本研究也注意到化疗史、反复住院史和3个月内替加环素暴露史对肠道致病菌的影响。以上结果可能与血液病患者反复医院暴露、使用全身性免疫抑制剂导致免疫防御功能受损及损伤肠黏膜、大量抗菌药物暴露导致肠道微生态失衡引起肠道定植抗性丧失有关[3]。因此对于血液科医师而言,尽管由于血液病的治疗避免不了化疗药物的使用,也要致力于在临床中如何减少患者的住院次数,并且须严格把握血液病患者青霉素类、碳青霉烯类抗菌药物以及替加环素药物的使用指征,尤其是前两者。本研究单因素分析结果还显示无肠道致病菌感染的血液病患者中初治占比高于感染肠道致病菌的患者,这也是可以理解的,因为初治的血液病患者相对于有血液病史的患者其化疗、反复入院以及广泛抗菌药物暴露史显著减少。
综上所述,本研究得出以下结论:首先,3个月内青霉素类和碳青霉烯类抗菌药物暴露是血液病患者感染肠道致病菌的独立危险因素,这有助于识别早期肠道致病菌感染以及可能感染源;其次,急性白血病及淋巴瘤住院患者是感染肠道致病菌的高危人群;最后,肠球菌是血液病住院患者院内感染肠道致病菌的常见细菌。此外研究发现不同抗菌药物类型暴露对肠道微生物群会产生不同影响[3],因此今后本研究团队可以进一步研究血液病住院患者抗菌药物治疗前后的肠道微生态变化,探讨某些抗菌药物对肠道微生物群的影响,为患者制订个性化和优化的治疗方案。

