营养不良老年人非药物干预临床实践指南
中国老年护理联盟,中南大学湘雅护理学院(中南大学湘雅泛海健康管理研究院),中南大学湘雅医院(国家老年疾病临床医学研究中心),北京医院(国家老年医学中心、国家老年疾病临床医学研究中心)
营养不良又称营养不足,是指由于摄入不足或利用障碍引起能量或营养素缺乏的状态[1]。老龄化与营养不良密切相关,老年人由于消化系统功能减退、口腔问题增多、服药等原因使营养不良的发生风险升高[2]。一项基于240项研究的系统评价结果显示,社区老年人营养不良患病率为3.10%,老年住院患者的患病率为22.00%[3]。我国老年人营养不良的发生情况更为严峻,中国健康与养老追踪调查(China Health and Retirement Longitudinal Study,CHARLS)结果表明,我国社区老年人营养不良的发生率为12.60%[4]。老年人营养不良与衰弱、肌少症、抑郁等密切相关,增加了老年人的住院天数、医疗保健相关费用与死亡率,严重影响其身体健康和生活质量,给家庭和社会造成了沉重负担[5-7]。因此,采取有效措施改善老年人的营养不良至关重要。
非药物干预是改善营养状态的重要措施[8],其中膳食指导、口服营养补充、运动干预和联合干预是最为常见的非药物干预方法[9-10],需制订相关规范指导其在营养不良老年人中的应用实施。目前,国外一些机构已经发布了针对一般人群营养不良的相关指南和共识[11-14],考虑到人群、文化、医疗环境的不同,这些指南对于我国人群的适用性值得深入探讨,且国内尚无针对老年人营养不良的非药物干预指南。因此,由中国老年护理联盟牵头发起,组织国内专家按照临床循证实践指南制订的方法和步骤,基于研究证据,并结合我国临床实际,聚焦于可经口进食的营养不良老年人,制订《营养不良老年人非药物干预临床实践指南》,为在营养不良老年人中实施膳食指导、口服营养补充、运动干预和联合干预提供参考,从而改善老年人营养不良状况,提高其生活质量,减轻家庭和社会负担。
1 指南制订方法
1.1 指南的总目标和具体目标 本指南的总目标是为医护人员提供营养不良老年人非药物干预的实施指导。具体为:(1)为膳食指导在营养不良老年人中的应用提供指导;(2)为口服营养补充在营养不良老年人中的应用提供指导;(3)为运动干预在营养不良老年人中的应用提供指导;(4)为联合干预在营养不良老年人中的应用提供指导。
1.2 指南制订发起机构、组织及注册 本临床实践指南于2021年6月由中国老年护理联盟发起,参与单位包括中南大学、北京医院(国家老年医学中心、国家老年疾病临床医学研究中心)、中南大学湘雅医院(国家老年疾病临床医学研究中心)、中南大学湘雅三医院等。本指南已在国际实践指南注册与透明化平台(Practice Guideline Registration for Transparency,PREPARE)进行注册(注册号:PREPARE-2022CN751)。
1.3 指南使用者与目标人群 本指南使用者为对营养不良老年人实施非药物干预的医护人员。目标人群为医院、社区和养老机构等场所中年龄≥60岁的营养不良老年人。
1.4 指南范围与优先临床问题的确定 秘书组首先按照人群(population,P)、干预(intervention,I)、对照(control,C)和结局(outcome,O)的原则拟临床问题和结局指标,之后遵照推荐分级的评估、制订与评价(Grading of Recommendations Assessment,Development,and Evaluations,GRADE)中关于构建临床问题和确定重要结局的方法[15],通过专家函询的方式,邀请营养学、老年医学、老年护理学和全科医学的临床实践专家对拟定的临床问题的重要性进行判断、对表述的准确性进行讨论,并补充其他可能遗漏的重要问题,同时对问题的结局指标的重要性进行排序[16],7~9分表示结局对决策关键,4~6分表示重要,1~3分则表示不重要,纳入评分≥4分者,最终确立指南的临床问题和相应的结局指标,详见表1。

表1 指南的临床问题及结局指标Table 1 Clinical issues and outcome indicators for the guidelines
1.5 文献检索与证据整合
1.5.1 文献检索 根据优选的临床问题确定检索策略,由秘书组对临床实践指南、最佳实践、专家共识、系统评价及随机对照试验(randomized controlled trial,RCT)进行检索,侧重于对来源于系统评价和RCT证据的检索,其余类别文献证据作为补充与参考。检索的PICO为:(1)人群(population,P):可经口进食且存在营养风险或营养不良的老年人。营养风险或营养不良诊断标准应符合国际通用标准,如:使用微型营养评估简化版(MNA-SF)进行评估等。(2)干预(intervention,I):各类非药物干预方法,包括但不限于口服营养补充、膳食指导及运动干预,或以上几类干预的联合干预等。(3)对照(comparison,C):与干预组采取不同的措施,包括空白对照或日常饮食等。(4)结局(outcome,O):任何类型能够反映干预方式对营养不良影响的结局指标,如能量摄入、体质量变化及生活质量等。检索时间为建库至2022-12-01,具体检索策略见表2。

表2 文献检索策略Table 2 Literature search strategy
1.5.2 证据整合 秘书组成员采用Excel设计标准化文献提取表格,由2名经循证护理培训的成员进行文献提取、翻译与整合。提取内容包括:文献类型、作者、年份、样本量、研究对象、营养状况评估方法、干预措施、对照组、干预效果、结局指标等。不同来源的证据进行整合时,针对同一内容,如果各文献的推荐意见或研究结论一致,则进行合并;针对同一主题内容互补的推荐意见,根据语言逻辑关系,将其合并;如果不一致,则追溯其证据来源,找出其做出不同推荐建议的原因,以证据质量高、年代新的文献为准;推荐意见中涉及多个策略时,则进行拆分。整合过程中如遇分歧,由2人讨论或由第3位成员决定。
1.6 证据质量分级及推荐意见形成 秘书组采用GRADE[15]对纳入的营养不良老年人非药物干预相关证据体进行质量分级。在证据分级过程中,考虑5个降级因素(偏倚风险、不精确性、不一致性、间接性以及发表偏倚)和3个升级因素〔效应量大、剂量-效应关系以及可能的混杂因素(负偏倚)〕。完成证据分级后,通过证据总结表呈现证据。
专家共识组采用GRADE决定推荐意见方向和强度。秘书组制作推荐意见决策表。推荐意见方向和强度通过专家共识会确定,专家阅读证据总结表,并填写推荐意见决策表,包括:强推荐、弱推荐、不清楚、弱不推荐、强不推荐,见表3。一个推荐意见被列为强推荐或强不推荐,至少需要得到70%的参与者认可;对于持续存在分歧的部分,推荐或反对某一干预措施至少需要50%的参与者认可,少于20%选择替代措施,未满足此项标准将不产生推荐意见。秘书组统计最终推荐结果。
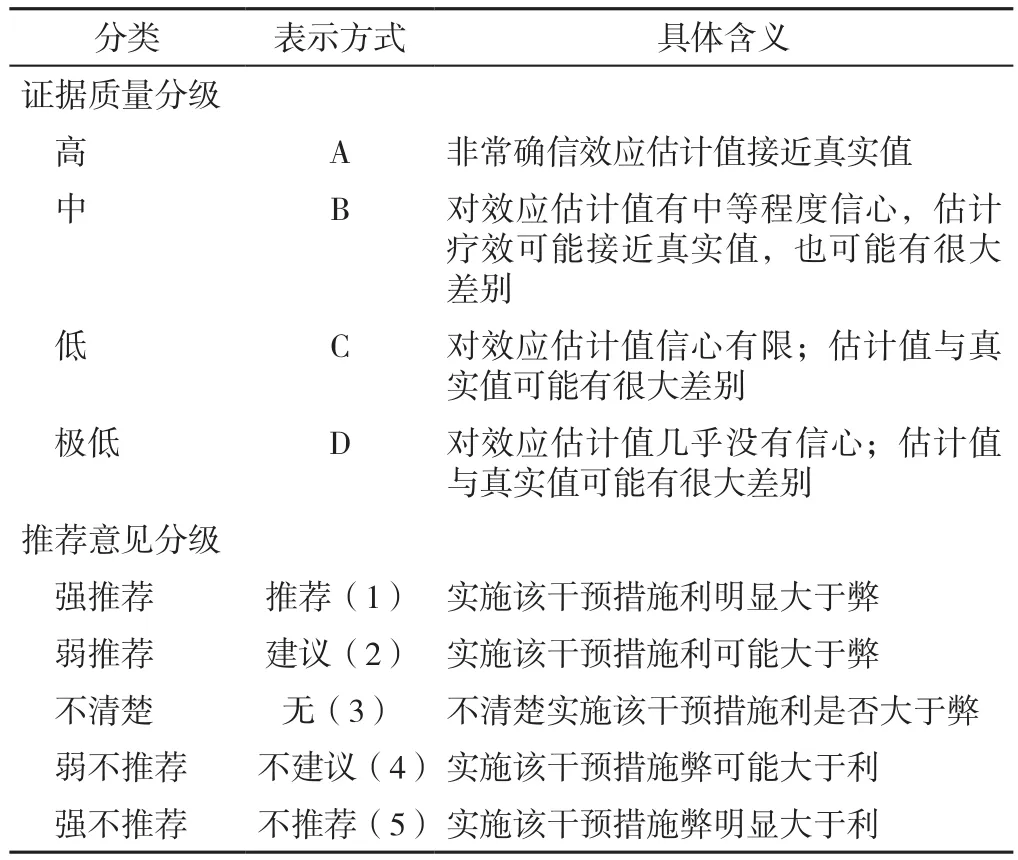
表3 证据质量等级及推荐意见的表达Table 3 Quality of evidence grades and expression of recommendations
最终,经过德尔菲法投票及一轮终审会后达成共识(共识度>75%)。秘书组对专家意见进行讨论、修改、完善,最终形成营养不良老年人非药物干预推荐意见概要表,见表4。

表4 推荐意见概要表Table 4 Summary table of recommendations
2 推荐意见及证据说明
2.1 膳食指导
2.1.1 推荐意见:膳食指导是建立在“知- 信 -行”理论基础上的营养干预手段。对存在营养风险或营养不良的老年人而言,膳食指导可作为营养干预的优先手段。(1B)
操作要点:当营养风险筛查2002(Nutritional Risk Screening 2002,NRS-2002)总分≥ 3 分[17],或MNA-SF总分≤11分时[18],考虑存在营养风险,有进一步制订营养支持计划或进行营养评定的指征。营养不良问题全球领导倡议(Global Leadership Initiative on Malnutrition,GLIM)标准指出,在营养风险筛查阳性基础上,需至少符合表型指标〔非自主性体质量降低、低体质指数(BMI)、肌肉量丢失〕之一和病因指标(食物摄入减少或消化功能障碍、炎症或疾病负担)之一,可评定为营养不良[12]。如下(1)至(3)为表型指标,(4)和(5)为病因指标。
(1)无自主意愿体质量减轻,即非主动减肥基础上:6个月内体质量下降>5%,或6个月后体质量下降>10%;(2)欧美人群:70岁以下 BMI<20 kg/m2,70 岁以上 BMI<22 kg/m2;亚洲人群:70 岁以下 BMI<18.5 kg/m2,70 岁以上 BMI<20 kg/m2;(3)通过有效人体成分检测技术确定的肌肉量降低〔去脂体重(FFMI)、握力等〕;(4)摄入量≤50%的能量需求(>1周),或能量摄入降低(>2周),或存在任何影响消化吸收的慢性胃肠状况;(5)存在急性疾病、损伤,或者慢性疾病相关的炎症。
推荐说明:我国老年人群的营养知识水平及营养素养现状并不乐观,《国民营养行动计划2017—2030》明确指出应“建立满足不同老年人群需求的营养改善措施”“依托基层医疗卫生机构,为居家老年人群提供膳食指导和咨询”[19]。膳食指导也称营养指导或营养教育,是指营养专科人员对老年人进行营养评估后,针对老年人的营养现状,结合其日常饮食与生活习惯,提供合适的、有针对性的营养知识和日常饮食建议[20]。老年人的认知功能和接受能力相对较差,膳食指导的效果常难以得到保证,照护者参与式膳食指导(即鼓励老年人照护者积极参与膳食指导干预)有利于老年人更好地理解和接受膳食指导的内容,提升膳食指导的有效性。
证据总结:(1)一项纳入8项RCT的系统评价显示,基于“知-信-行”理论基础,通过膳食指导的方式改变老年人日常饮食,可帮助其建立良好的饮食习惯以及改善营养状态[21]。(2)另一项纳入8项RCT的系统评价指出,与其他营养干预方式相比,膳食指导的可操作性强,且干预效果好[22],即使在没有额外使用营养补充剂的情况下,单一的膳食指导也可改善老年人的营养状况,对存在营养风险或营养不良的老年人而言,膳食指导可作为营养干预的优先手段。
2.1.2 推荐意见:膳食指导由营养专科医务人员主导的膳食指导和自我管理的膳食指导干预组成,各方法内容基本一致,可因地制宜进行选择。(2B)
频率:30~60 min·次-1·周-1。(1B)
周期:通常6周为一个干预周期。(1B)
方式:面对面或线上、线下结合开展。(1B)
类型:由营养专科医务人员主导的膳食指导干预和自我管理的膳食指导干预。(2C)
推荐说明:由营养专科医务人员组建的多学科团队所主导的膳食指导的内容通常围绕老年人营养需求、各营养素功能、健康饮食组成和老年人常见的营养不良问题等展开,以丰富老年人营养知识,提高老年人营养意识,进而改善老年人饮食习惯和生活方式[20-23]。膳食指导通常包含个体开展和团体开展两种形式,个体开展的膳食指导较为具体,可为老年人提供个性化的膳食指导;而团体开展的膳食指导则可一次为多名老年人提供服务,更具有普及性。因此,需因地制宜选择适合的膳食指导方式。
自我管理的膳食指导是指营养师或经过营养师培训的医务人员与老年人一起制订营养计划,为其配备营养指导手册和用以设定目标、自我监测及自我评估的记录手册等,由老年人自我记录、自我管理每日的食物摄入量[24]。本方法适用于社区居住的老年人,通常需要营养师或经过营养师培训的医务人员进行定期监测,并对老年人营养状况进行定期评估[23]。随着独居老人、空巢老人数量的增加,膳食自我管理可成为老年人营养干预的一种重要措施。
证据总结:(1)一项RCT结果显示,在实施膳食自我管理计划前,应先帮助老年人提高其自我效能感,让老年人认识到自我管理的重要性,提升其膳食自我管理的技能,给予老年人自我管理改善营养状况的机会,同时应注意膳食自我管理干预各个阶段的实施均应由营养专科医务人员参与并指导[25]。(2)一项纳入4项RCT的系统评价评估了线上或线下膳食指导对存在营养风险的老年人的影响,结果显示,老年人在能量摄入〔均数差(mean difference,MD)=1.10 kcal,95% 置信区间(confidence interval,CI)(0.66,1.54)〕、蛋白质摄入〔MD=10.13 g,95%CI(5.14,15.13)〕、 体 质 量〔MD=1.01 kg,95%CI(0.08,1.95)〕等方面均有所增加[20]。(3)一项纳入32项RCT和一项纳入8项RCT的系统评价指出,膳食指导的干预要分阶段进行,通常6周为一个干预周期,根据每个阶段的干预效果调整和完善干预方案,以使干预方案更加科学有效[26-27]。不论是由营养专科医务人员主导的膳食指导还是自我管理的膳食指导干预,均需要营养专科医务人员及老年人的共同参与,共同讨论形成指导方案。随着网络技术的不断发展,膳食指导也可通过线上的方式开展,使干预的过程更加简单高效。(4)一项纳入4项RCT和一项纳入8项RCT的系统评价发现[20,22],老年人对膳食指导的接受率较高,尤其是患病老年人,更愿意接受医务人员的膳食指导与饮食建议,进而改变不良饮食习惯,改善其营养状况。(5)一项纳入8项研究的系统评价评估了膳食指导对营养不良老年人的影响,结果显示,老年人营养知识水平得到显著提升〔MD=3.95,95%CI(1.64,5.06)〕,同时,与常规护理相比,膳食指导能够显著降低老年人30 d再入院的风险〔风险比(hazard ratio,HR)=0.40,95%CI(0.20,0.90)〕和90 d再入院的风险〔HR=0.40,95%CI(0.20,0.80)〕[21]。(6)一项纳入 18项研究的范围综述[28]和一项纳入8个研究的综述[26]调查了膳食指导对老年人的影响,结果均显示膳食指导能够有效改善老年人的营养知识素养并改善营养状况。
2.2 口服营养补充
2.2.1 推荐意见:当存在营养风险或营养不良的老年人需进行营养支持时,口服营养补充(ONS)为首选方法。(1A)
推荐说明:ONS是指在正常饮食之外,增加一类或多类营养成分以补充膳食不足的情况或特别需要的制品[29-30](亦称膳食补充剂),既可在饮食中代替部分食物,也可作为加餐,给予额外的补充[31]。
证据总结:(1)3项RCT结果证实,ONS可增加老年人能量及蛋白质摄入量、纠正老年人体质量下降的情况、改善老年人营养及功能状态,并减少患病老年人并发症、降低病死率,是预防及治疗老年人营养不良的重要措施[32-34]。当老年人存在营养风险或营养不良状况,且在尝试饮食调整及优化后,老年人的日常饮食摄入量仍无法满足其机体目标需要量的60%时,应开始给予ONS。(2)一项RCT结果显示,老年人能量摄入应达到 20~30 kcal·kg-1·d-1,而存在营养风险或营养不良、低体质量或处于应激状态的老年人的能量摄入则应提高至30~40 kcal·kg-1·d-1[30]。
2.2.2 推荐意见:推荐存在营养风险或营养不良的老年人进行标准整蛋白配方的全营养制剂ONS补充,当标准整蛋白配方的全营养制剂ONS补足能量后仍有蛋白质或者必需氨基酸摄入不足时,建议口服补充蛋白质类或者必需氨基酸类,补充方法通常为小口啜饮。(11AA)
频率:2~3次/d。(1B)
剂量/周期:标准整蛋白配方的全营养制剂ONS用量应达到400~600 kcal/d或补足老年人的蛋白质摄入量达到 1.00~1.20 g·kg-1·d-1,经过 30~900 d 的补充周期,通常可改善老年人营养状态和临床结局。(1B)
类 型: 蛋白质类(protein)、 能量类(energy)和必需氨基酸补充(essential amino aacciidd supplements),如肌酸补充(creatine supplemeennttss)和亮氨酸补充(leucine supplements)等多种类型。(1B)
推荐说明:ONS通常为粉剂、半固体或液体形式,有多种口味、类型及能量密度等供选择。同时,根据ONS的配方,成分也多种多样,如整蛋白型、短肽型、平衡型及疾病特异型等,而标准整蛋白配方的全营养ONS制剂适合大多数老年患者。当标准整蛋白配方的全营养制剂ONS补足能量后,仍有蛋白质摄入的缺口,可以进行蛋白类口服营养补充。
证据总结:(1)一项RCT结果显示,标准整蛋白配方的全营养制剂ONS用量应达到400~600 kcal/d[30]。随着年龄增长,老年人因生理性原因(如口腔问题、食欲下降、消化功能减退等),会出现能量摄入减少的情况,导致饮食中的蛋白质摄入量下降[35-36]。研究显示,当饮食中能量摄入量不足以维持机体能量消耗,机体内肌肉蛋白基础合成率会降低20%,甚至导致肌少症的发生[37]。在关于健康老年人对蛋白质的相对最佳摄入量的研究中,当老年人蛋白质摄入量≤0.80 g·kg-1·d-1时,机体就很难保持原有的肌肉质量;在安全和耐受情况下,1.00~1.20 g·kg-1·d-1的蛋白质摄入则为老年人最佳蛋白质摄入量[38];而高蛋白质摄入量(≥ 1.20 g·kg-1·d-1)和中蛋白质摄入量(≥1.00 g·kg-1·d-1)可以很好地维持全身的氮平衡,减少老年机体蛋白质的消耗,对老年人的下肢肌肉功能也有一定改善作用[31]。(2)一项纳入62项研究的系统评价评估了在15 d~6个月不等的干预时间里,每天对存在营养风险或营养不良老年人进行2~3次蛋白质补充的影响,结果显示,营养不良老年人的病死率〔危险度比(risk ratio,RR)=0.79,95%CI(0.64,0.97)〕及并发症风险〔RR=0.86,95%CI(0.75,0.99)〕有所降低[39]。一项纳入了36项RCT的系统评价评估了通过10 d~9个月不等的高蛋白质补充对老年人的影响,结果显示,高蛋白质补充有利于降低营养不良老年人的疾病并发症风险〔优势比(odds ratio,OR)=0.68,95%CI(0.55,0.83)〕及住院率〔OR=0.59,95%CI(0.41,0.84)〕,增 加 握 力〔MD=1.76 kg,95%CI(0.36,3.17)〕,提高能量〔MD=314 kcal,95%CI(146,482)〕与蛋白 质 摄 入〔MD=22 g,95%CI(10,34)〕, 以及增加老年人体质量〔MD=1.74 kg,95%CI(0.79,2.70)〕[40]。此外,一项纳入17项RCT的系统评价评估了4周~9个月时间内2~3次/d的高蛋白质补充对老年人的影响,结果显示,高蛋白质补充能显著提升老年人的生活质量〔标准化均数差(standardized mean difference,SMD)=2.58,95%CI(2.05,3.10)〕[41]。(3)蛋白类口服营养补充的方式主要包括进餐时补充和两餐间加餐补充两种形式,可根据老年人的健康状况及偏好选择补充[29-30,42-43]。如两项以豆基为载体添加多种微量营养素补充剂的RCT结果显示,该干预可有效改善老年人机体血红蛋白及多种微量营养素水平,而乳清蛋白口服营养补充,除能够有效改善老年人营养状况外,还可有效提升老年人的握力〔MD=1.29 kg,95%CI(0.45,2.14)〕[44]。多项研究采用餐间分次口服的方式为老年人提供ONS,通常采用小口啜饮(即:少量多次饮用)的方式,该方法既有利于老年人的营养吸收,不容易噎食或呛食,同时,即使老年人并不喜欢某种ONS的口感,也能分次饮用,完成补充任务[39]。在老年人营养素的补充过程中,单纯的蛋白质补充有时候并不能够达到期望的效果,还应适量补充氨基酸以直接辅助机体蛋白质的合成[45-46]。(4)必需氨基酸能够起到刺激信号作用,富含亮氨酸的必需氨基酸有助于老年人机体的蛋白合成。研究表明,老年人对摄入的食物蛋白质合成反应较为迟钝,而摄入亮氨酸则能够逆转老年患者肌肉蛋白合成对氨基酸或蛋白质摄入的迟钝反应[47]。此外,亮氨酸具有抗蛋白质分解作用,因此可以通过抑制蛋白质的分解来增加蛋白质的合成代谢,长期摄入富含亮氨酸的食物结合运动干预具有协同作用,可有效增加骨骼肌质量[45]。一项纳入39项RCT的系统评价总结了经过1~24个月的1~3次/d的必需氨基酸补充对老年人的影响,结果显示,必需氨基酸能够有效改善老年人的肌肉质量〔SMD=0.21,95%CI(0.07,0.35)〕、肌力〔SMD=0.27,95%CI(0.10,0.44)〕和躯体功能〔SMD=0.24,95%CI(0.13,0.36)〕,尤其对营养不良的老年人有效[43]。外源肌酸的补充除了满足老年人所需的营养成分外,还能够有效增加老年人肌肉质量和力量,同时,肌肉收缩会促进肌酸进入骨骼肌,从而使肌肉内肌酸储备增加[48]。对于大多数老年人来说,根据肌肉总量和身体活动水平,需要摄入1.00~3.00 g/d外源性肌酸[49-50]。(5)尽管高蛋白饮食方式可为老年人补充营养,并维持其肌肉质量和功能,但摄入过量蛋白质可能会对老年人的肾功能产生潜在的负面影响,尤其是肾小球的滤过率[39,51]。研究结果显示,在肾功能正常的人群中,高蛋白摄入量(>1.50 g·kg-1·d-1)对肾小球滤过率的影响微乎其微[19];但在肾功能障碍的老年人中却必须考虑其影响。因此,关于蛋白质和氨基酸的补充应充分考虑老年人的身体状况,对有肾脏等器官基础疾病的老年人的补充量应做特殊要求。同时,研究结果表明,单独补充蛋白质或某类氨基酸并不能显著改善老年人的肌肉力量或功能[52],但目前半数以上的研究周期较短,多在6个月以内,并不足以观察长期变化[53]。故蛋白质补充对治疗老年人营养风险或早期营养不良的效果更佳,如果营养不良较为严重如已经出现肌少症或衰弱等情况,则可能短期效果不够显著。
2.2.3 推荐意见:当老年人存在某种特异性营养风险或营养不良情况时,应进行追加补充;推荐该类老年人根据营养需求选取含不同组分(或类型)的微量元素类作为补充,以满足身体对不同营养元素的需求;此外,还应定期监测以防止补充过量。(1B)
频率:1~2次/d。(1B)
周期:通常30 d为一个补充周期。(1B)
类型:维生素和矿物质补充(vitamin and mineerraall supplements)、免疫营养素补充(immunonutriieenntt supplements)等。(1C)
推荐说明:当摄入某种营养成分不足时,老年人会出现某种特异性成分的营养风险或营养不良情况,此时就应根据具体不足情况进行针对性补充。微量元素类口服营养补充更加注重高密度某类单一营养元素的补充,效果也较为显著。通过总结现有研究,发现该类补充通常包括维生素和矿物质类的补充,免疫营养素的补充和中链甘油三酯(medium chain triglycerides,MCTs)等。同时,由于老年人随着年龄增长会出现生理性食欲下降的问题,会导致单次补充营养成分过少,因而通常需进行多次补充,其中夜间进行补充尤为重要且易被忽视,本指南对夜间补充的证据也进行说明。
证据总结:(1)两项分别纳入26项RCT和7项队列研究的系统评价都指出,通过每日服用维生素和矿物质的组合进行配方营养补充,以达到每日推荐摄入量的维生素和矿物质,可降低老年人出现衰弱的风险,并有效提升老年人的机体免疫力与躯体功能[54-55]。(2)一项纳入36项RCT的系统评价评估了1~2次/d维生素D补充对老年人的影响,结果显示,使用维生素D作为营养补充可提高老年人在起立行走测试中的表现〔MD=-0.75 s,95%CI(-1.44,-0.07)〕,且当维生素 D用量在400~1 000 U 时,这种提高更加明显[56]。通常30 d为一个维生素D补充周期,应注意长期过量的服用维生素D会引起中毒的风险,有必要定期监测以防止补充过量。(3)免疫营养素配方是免疫营养的重要组成部分,除了能够改善老年人的免疫功能外,还能一定程度上减少白三烯和前列腺素的形成,进而减少炎症反应[57]。免疫营养素配方通常包含多种能够提高免疫功能的营养素,如ω-3多不饱和脂肪酸(ω-3 polyunsaturated fatty acid,ω-3 PUFA)、精氨酸(arginine)、核酸(nucleic acid)、谷氨酰胺(glutamine)和抗氧化剂(antioxidant)等[30,57]。其中,ω-3 PUFA 包括α-亚麻酸(α-linolenic acid,ALA)、二十碳五烯酸(eicosapentaenoic acid,EPA)和二十二碳六烯酸(docosahexaenoic acid)等。精氨酸能在一定程度上增强老年人机体内T淋巴细胞的活性,同时增强体内中性粒细胞的吞噬能力与多形核细胞的黏附力,减少损伤部位白介素(IL)-1β等炎症递质的产生,从一定程度上提高老年人的免疫功能。谷氨酰胺则能够刺激老年人体内肠道的固有黏膜免疫能力,被称为“肠道黏膜的特殊能源”,不仅能够维护肠道的正常生理结构,还能够维护肠道吸收和屏障功能、防止细菌和毒素移位,对维护老年人肠道功能具有重要意义[58]。(4)一项纳入31项RCT的系统评价总结了经过26 d~6个月的干预效果,结果显示,使用ω-3 PUFA进行干预的老年人虽然在体质量和生活质量上与对照组老年人没有差异,但却能够有效降低老年人周围性神经炎的发生风险〔OR=0.20,95%CI(0.10,0.40)〕[59]。当前关于MCTs对营养不良的治疗管理的研究较少。一项RCT发现体弱的老年人能良好地耐受6 g剂量的MCTs,MCTs能够激活胃饥饿素的释放,从而刺激老年人的食欲,并增加肌肉质量[47]。但是,目前仍需要更多客观的研究加以证实MCTs的效果。(5)一项纳入9项RCT的系统评价指出,夜间补充对存在营养风险或营养不良的老年人来说尤为关键。夜间补充能够解决老年人夜间饥饿的问题,并为老年人提供所需营养素[60]。夜间补充通常应注意不能使老年人的血糖等指标上升过快,以防发生意外或影响睡眠。一项纳入8项研究的系统评价和一项干预研究评估了夜间补充对老年人的影响,结果显示,夜间补充能够显著提升老年人生活质量[61-62]。夜间补充时,可选用密集营养零食、能量丰富的粗粮、易消化的水果类、饱腹感强的坚果等[32]。同时,可根据地域、季节的不同,为老年人提供当季并符合其饮食习惯的食物[63]。
2.3 运动干预
2.3.1 推荐意见:推荐存在营养风险或营养不良的老年人在身体状况允许的情况下进行运动干预,有效促进老年人营养吸收,进而增加其营养摄入和改善营养状况。(1B)
推荐说明:运动干预指的是通过适量的身体活动,刺激体内营养物质的消耗,以达到通过营养消耗带动营养摄取的目的,同时,运动后增加的蛋白质合成速率可抑制机体肌肉细胞分解,还可达到抑制老年人体内肌肉减少的目的[64]。关于其机制,一种说法是机体的衰老与肌肉组织中蛋白质和脂质等的氧化损伤积累有关,而这种损伤可能会损害细胞中线粒体的正常功能,导致机体能量产生不足,而运动可以减少此类有害过程的发生,同时促进营养物质的摄取,进而产生积极效应间的互相促进作用[65]。适量的运动可对老年人的神经系统、免疫系统、内分泌系统等均产生积极的生理影响。
证据总结:三项分别纳入7项、26项和13项RCT的系统评价结果显示[52,66-67],运动对存在营养风险或营养不良的老年人均有效,运动不仅能够在一定程度上增强老年人的食欲,促进能量摄入,改善营养不良症状,还能够改善躯体功能。老年人运动干预开展的前提是要确保总体运动量不超过老年人所能耐受的心肺负荷,因此,运动方式和强度的选择应基于对其基础疾病和心肺功能的评估结果[68]。此外,运动计划的制订也应与相关专科医务人员和老年人本人进行讨论[69],且必须在运动训练的过程中进行监测。
2.3.2 推荐意见:运动干预包括多种类型,可结合我国传统运动开展,应根据老年人的营养状况及躯体功能等情况确定运动类型及频率。(1C)
频率:15~30 min/次,1 次 /d,1~3 d/周。(1C)
周期:通常6周为一个干预周期。(1C)
方式:面对面或线上、线下结合开展。(1C)
类型:抗阻力训练、传统中医运动干预和耐力训练等。(2D)
推荐说明:运动干预的具体类型需基于老年人的身体状况进行选择,因此,运动干预之前需评估老年人的身体状况并与专业人员制订详细、合理的计划,同时,要密切关注老年人运动过程中的情况,以防运动量过大、跌倒、心血管意外等不良事件发生[70]。
运动干预的具体类型包括抗阻力训练、传统中医运动干预和耐力训练等类型。抗阻力运动,又称阻力运动或力量运动,主要包括负重抗阻运动、对抗性运动、克服弹性物体运动和利用力量训练器械等[71]。老年人有必要在医生或物理治疗师的指导下,有计划地针对日常生活活动(如起床站立、行走、如厕等)所使用的核心肌肉群进行渐进性锻炼[72],从而改善其肌肉质量、肌肉力量和肌肉功能。传统中医运动干预以阴阳学说、整体观念为主要理论指导,通过调动人体自身潜能,达到祛病强身、防病治病的目的,常见的中医运动干预包括太极拳、五禽戏、八段锦、易筋经等。
证据总结:(1)一项范围综述指出,在社区营养不良的老年人中应用传统中医运动干预有助于强壮筋骨,改善老年人平衡能力、肌肉力量以及减轻慢性疼痛[73]。耐力训练通常以低负荷长时间的运动为主,且已有研究显示耐力训练可增加老年人骨骼肌线粒体合成以及氧化能力,保持低负荷长时间运动的老年个体的平均线粒体体积密度大于同龄久坐不动的人[74]。因此,耐力训练可以作为改善老年人线粒体功能的重要干预措施,耐力训练的常见方式包括功率自行车、跑步机、慢跑等。老年人可每周进行3~5次,每次不少于15 min的耐力训练来增加能量消耗,进而提高营养摄入。(2)一项纳入20项RCT的系统评价[75]中的5项研究[76-80]和多项临床研究[79,81-90]调查了耐力训练和其他运动方式对营养不良老年人的影响,结果显示,每周1~3次,持续6至32周不等的耐力训练能够有效提升老年人的躯体功能状况〔SMD=0.32,95%CI(0.11,0.45)〕。
2.4 联合干预
2.4.1 推荐意见:联合干预通过多学科团队协同合作,针对老年人的营养问题提出全方位的解决策略,以改善老年人的营养不良状况。(1B)
推荐说明:联合干预是通过整合多学科资源,分析导致老年人营养不良的原因,结合使用多种干预措施,用以延缓或逆转老年人的营养不良状况[33]。本指南将联合干预定义为在开展营养干预项目时,使用了两种或两种以上干预的混合干预方式。联合干预团队由营养专科医务人员、全科医务人员、运动康复治疗师、社会工作者和志愿者等组成。通过此类多学科团队的协同合作,为老年人制订专属的“营养日历”,有利于促进干预项目顺利实施和开展[91]。
证据总结:(1)一项RCT结果表明,联合干预比单一的营养干预措施内容更加丰富,对于改善营养状况的针对性更强,能够从多方面解决营养状况不佳的问题[45]。(2)联合干预项目通常包括以下几个方面:①使用合适的工具评估老年人的营养状况、饮食摄入情况、身体健康状况及活动能力等。②了解老年人的营养状况后,营养专科人员和老年人共同讨论制订营养计划。③指导老年人或其照护者通过平衡膳食餐盘等工具记录营养摄入情况并设定阶段性营养目标。④为老年人提供具体的膳食指导,必要时提供营养补充剂支持。⑤对于心理状况不佳或存在社交孤独的老年人,在帮助其改善营养状况的同时,对其进行心理疏导,如鼓励其参加社交活动、参加营养知识活动小组等。⑥对于存在衰弱、肌少症等情况的老年人,在保证其营养状况有所提升的基础上,指导其进行居家运动。为了保证老年人运动的依从性,医务人员可以对老年人的运动自我效能、动机准备和目标达成程度等进行评估,并基于评估结果为每位老年人形成一套有针对性、目标明确的居家运动项目。⑦有条件时,可以通过远程网络辅助进行干预。⑧对存在慢性病、疼痛和其他老年综合征的老年人,在进行营养状况管理的基础上,还需对相关疾病进行管理。⑨对服药的老年人,鼓励其遵医嘱用药[33]。联合干预将多种非药物干预的方法进行整合,可使不同干预方法间相互促进和补充,取得更好的健康结局[75]。但由于本类干预方法通常需要多团队合作,需较多的人力物力配合,具体实施存在较大难度。
2.4.2 推荐意见:联合干预比单一的营养干预措施内容更加丰富,应考虑到各种干预内容间的互相促进作用,使干预效果达到最大化。(1B)
周期:通常12周为一个干预周期。(1B)
方式:面对面或线上、线下结合开展。(1B)
团队:营养专科医务人员、全科医务人员、运动康复治疗师、社会工作者及志愿者等。(1C)
类型:口服营养补充结合运动干预,口服营养补充结合膳食指导,口服营养补充结合膳食指导与运动干预等。(1B)
推荐说明:联合干预的形式通常是将两种或多种干预方式结合开展,如:(1)个性化膳食指导与营养补充联合的干预方式[92];(2)个性化膳食指导与运动干预联合的干预方式[52];(3)运动干预与营养补充联合的干预方式。通常,存在营养风险或营养不良的老年人的运动功能也会出现不同程度的下降,单纯进行营养补充可能无法充分改善老年人的衰弱、肌少症等问题,而营养补充联合运动干预可使老年人整体健康状况得到更好的改善,可在有效提高老年人的整体营养状况的同时,提升老年人的肌肉力量和步速等。
证据总结:(1)一项纳入9项RCT的系统评价评估了口服营养补充联合运动干预对存在营养风险的老年人的影响,结果显示,经过12周的线上、线下联合干预,能够显著提升老年人的能量摄入〔OR=2.28,95%CI(1.90,2.73)〕和体质量〔OR=2.48,95%CI(1.92,3.31)〕[33]。(2)联合其他干预方式共同进行的营养补充应考虑老年人的身体评估结果,如包含运动干预的联合干预项目,除进行每日基础营养补充外,还应适量补充维生素D和脂肪酸,如在一定干预时间内,每4个月共口服100 000 U的维生素D3等[93-94]。研究显示,维生素D可作用于骨骼肌,直接影响肌肉力量和功能,提高老年人的平衡能力,减少跌倒和骨折的发生,同时提高肌肉功能和运动能力;而脂肪酸可帮助提升老年人肌肉蛋白的合成能力[93]。(3)一项纳入26项RCT的系统评价评估了ONS联合膳食指导对营养不良老年人的影响,结果显示,经过10 d~12个月不等的联合干预能够有效提升老年人的体质量〔MD=1.70 kg,95%CI(0.86,2.55)〕[95]。(4)一项纳入11项RCT的系统评价评估了2周到9个月不等的ONS和运动干预对营养不良老年人的影响,结果显示,ONS联合运动干预能够显著提升营养不良老年人的肢体力量〔SMD=0.33,95%CI(0.13,0.53)〕和步速〔SMD=0.38,95%CI(0.19,0.56)〕[52]。另一项纳入 16篇 RCT的系统评价研究了营养补充与运动干预对存在营养风险的老年人的影响,结果显示,经过6周~36个月不等的联合干预能够显著提升下肢力量〔SMD=0.54,95%CI(0.33,0.75)〕和起立行走能力〔MD=0.29 s,95%CI(0.23,0.35)〕[96]。(5)联合干预项目由于干预内容复杂多样,应加强对老年人运动及营养相关的健康指导,充分了解老年人的需求和偏好,及时反馈老年人的疑问,以使联合干预项目顺利开展。此外,因联合干预项目通常需协调多方面人员,且干预周期较长,在实施过程中存在一定的挑战。因此,可使用远程网络帮助参与干预的各方面人员进行周期性讨论或开展干预,以辅助干预内容的顺利实施。
3 讨论
本指南是国内第一部专门针对营养不良老年人的非药物干预临床实践指南。老年人是发生营养不良的高危人群,非药物干预是改善老年人营养状况的重要措施。其中,膳食指导、口服营养补充、运动干预和联合干预是较为常见的非药物干预方法,医务人员应结合老年人的不同营养状况和身体情况,制订适宜的营养干预措施。此外,营养干预对老年人和医务人员而言,均是一个长期、循序渐进的过程。除口服营养补充方式外,大多干预方法的短期效果并不显著,需通过长期随访来验证其干预效果,最终达到通过营养干预来减少老年人的医疗支出,改善老年人的营养状况,提高老年人生活质量的目的。
本文无利益冲突。
《营养不良老年人非药物干预临床实践指南》专家组成员名单
指南牵头人:冯辉(中南大学湘雅护理学院 中南大学湘雅泛海健康管理研究院)、孙超(北京医院护理部 国家老年医学中心 中国医学科学院老年医学研究院)、陈琼(中南大学湘雅医院老年病科)、吴心音(中南大学湘雅公共卫生学院)
执笔者:李孟琦、宁红婷、伍丽娜
指南指导委员会:奚桓(北京医院 国家老年医学中心 中国医学科学院老年医学研究院)、唐四元(中南大学湘雅护理学院)、刘敏(中南大学湘雅三医院营养科)、苑鹏(中国食品发酵工业研究院食品工程研发部)、于普林(北京医院期刊编辑部 国家老年医学中心 中国医学科学院老年医学研究院)
指南秘书组(按姓氏拼音首字母排序):胡慧秀、李孟琦、宁红婷、伍丽娜、曾宪梅
指南专家组(按姓氏拼音首字母排序):陈琼(中南大学湘雅医院老年病科)、段盛林(中国食品发酵工业研究院食品部)、冯辉(中南大学湘雅护理学院)、侯茜(中南大学湘雅医院营养科)、黄苇萍(中南大学湘雅医院 国家老年疾病临床医学研究中心)、廖晓阳(四川大学华西医院心血管内科)、刘晓红(北京协和医院老年医学科)、马冠生(北京大学公共卫生学院)、马永慧(厦门大学医学院)、牛璐(中南大学湘雅公共卫生学院)、孙超(北京医院护理部 国家老年医学中心 中国医学科学院老年医学研究院)、王芳(中南大学湘雅三医院内分泌科)、吴心音(中南大学湘雅公共卫生学院)、许静涌(北京医院肝胆外科 国家老年医学中心 中国医学科学院老年医学研究院)、杨剑(重庆医科大学附属第三医院临床营养科)、杨莘(首都医科大学宣武医院护理部)、张秋香(中南大学湘雅三医院护理部)、朱旭萍(中南大学湘雅二医院营养科)
指南外审组(按姓氏拼音首字母排序):范自力(中南大学湘雅三医院全科医学科)、郭雅伟(中山大学公共卫生学院)、李琳(长沙市一医院内分泌代谢科)、林秀芳(四川大学华西医院老年医学中心/干部医疗科)、刘红(中南大学湘雅三医院营养科)、陆煜(南华大学附属第一医院全科医学科)、罗米杨(中南大学湘雅公共卫生学院)、石海燕(解放军总医院第二医学中心消化内科)、涂秋云(中山大学附属第五医院老年病科)、肖红菊(解放军总医院第一医学中心护理部)

