灵芝酸A分子印迹聚合物电化学传感器的制备及应用
黄桂珍 汪庆祥 陈金美 詹峰萍 魏 岚 郑婉榕
(1.闽西职业技术学院,福建 龙岩 364021;2.闽南师范大学化学化工与环境学院,福建 漳州 363000)
灵芝是一种具有抗肿瘤、调节免疫、防艾滋病病毒、抗氧化、延缓衰老等多种作用的药用真菌[1-3],其药理作用主要归因于灵芝中含有的多种三萜类化学成分和多糖等。灵芝酸A(GAA)作为灵芝的主要活性成分之一,表现出显著的抗肿瘤、护肝及抗癌作用[4],GAA含量直接影响灵芝的药用价值,因此建立一种简单、快速的GAA分析方法对评价灵芝品质具有重要意义。
目前,GAA的检测方法有分光光度法[5-7]、离子色谱法[8-9]、高效液相色谱法[10-12]等。但上述方法存在操作繁琐、成本高昂及分析时间长等问题。相比之下,分子印迹聚合物(MIP)基传感技术具有选择性强、化学性质稳定、对环境的耐受性好和制备简单、造价低廉等优点。与电化学技术相结合得到分子印迹电化学传感器不仅操作简单、成本低廉、选择性较好,而且能获得高的灵敏度[13-15]。MIP基电化学传感器目前已被广泛用于药物分子[16]、环境污染物[17]、生物分子[18]的检测。然而,截至目前,关于GAA的分子印迹电化学传感器的研究尚未见报道。邻苯二胺(OPD)易发生聚合反应,适用于一步电合成聚邻苯二胺超薄膜,并且在不添加交联剂和致孔剂的情况下即可与模板分子产生作用,是电化学传感器中实现非共价分子印迹最常用的单体之一,且具有选择性高和响应时间短的特点[19-21]。
研究拟以OPD作为功能单体,采用一步电化学聚合法在玻碳电极表面制备一层能特异性识别GAA的MIP膜,用于GAA的快速、灵敏检测,为灵芝粉浸出液中GAA检测及灵芝粉品质评价提供新的技术支持。
1 材料与方法
1.1 材料与试剂
OPD和GAA:分析纯,上海源叶生物科技有限公司;
木犀草素:分析纯,上海麦克林生化科技有限公司;
绿原酸、盐酸多巴胺、冰醋酸和醋酸钠:分析纯,上海阿拉丁生化科技有限公司;
试验用水均为去离子水。
1.2 仪器与设备
扫描电子显微镜(SEM):S-4800型,日本Hitachi公司;
电化学工作站:CHI-650D型,上海辰华仪器有限公司;
超声波清洗器:KQ52200E型,上海超声仪器有限公司;
电子天平:AL224CN型,奥豪斯仪器有限公司;
恒温培养摇床:20140639型,上海苏坤实业有限公司;
傅里叶变换红外光谱仪(FTIR):NICOLETiS10型,美国赛默飞世尔科技公司;
三电极系统:玻碳电极(GCE,直径3 mm)为工作电极,Ag/AgCl为参比电极,铂柱电极为对电极,上海辰华仪器有限公司。
1.3 试验方法
1.3.1 前驱溶液的制备 称取1.0 mg(0.2 mmol)GAA和1.3 mg(1.2 mmol)OPD,加入到2 mL HAc-NaAc(pH 5.2)缓冲液中,配制成含有0.1 mmol/L GAA和0.6 mmol/L OPD的混合溶液。搅拌2 min后得到均匀溶液后,将混合溶液超声反应1 h,随后通入氮气10 min以除去溶液中的氧气,得到MIP电聚合制备前驱液,密封备用。上述过程中不加入GAA模板分子,得到非印迹聚合物(NIP)制备前驱液,用于对照试验。
1.3.2 MIP/GCE的电化学制备 首先,将玻碳电极(GCE)依次在0.05 μm和0.3 μm Al2O3粉浆中打磨,再用去离子水冲洗电极表面吸附的Al2O3颗粒,随后置于超纯水中超声5 min除去电极表面杂质,通氮气吹干,得到干净的基底GCE。将GCE置于MIP前驱液中,采用循环伏安法(CV)在0~0.8 V电位范围内扫描30圈。随后,将其转移到0.1 mol/L NaOH中,在-1~1 V电位窗口条件下扫描50圈,将电极上的模板分子、未聚合的物质以及其他杂质洗脱出来,最后用超纯水冲去MIP电极表面的NaOH以及剩余杂质,即制得MIP/GCE,烘干备用。相似地,将不含GAA的NIP前驱液替换MIP前驱液,采用相同电聚合和洗涤步骤制备NIP修饰电极(NIP/GCE)。
1.3.3 GAA在MIP/GCE的吸附和电化学测试 将MIP/GCE浸入不同浓度的GAA溶液中,在77 r/min转速下吸附50 min,随后用去离子水淋洗,去除电极表面非特异性吸附的GAA分子,从而得到GAA吸附电极(GAA/MIP/GCE)。将GAA/MIP/GCE置于0.1 mmol/L 的[Fe(CN)6]3-/4-溶液中进行循环伏安扫描(CV)和电化学阻抗法(EIS)表征。CV扫描范围-0.2~0.6 V,扫描速率100 mV/s。EIS频率范围0.1 Hz~100 kHz,振幅5 mV。同样以[Fe(CN)6]3-/4-为指示探针,采用微分脉冲伏安法(DPV)进行定量分析,DPV参数:电位区间-0.1~0.5 V、脉冲幅度0.05 V、脉冲宽度0.05 V。采用同样方法考察NIP/GCE对GAA的识别性能。基于OPD聚合膜的GAA分子印迹电化学传感器构建如图1所示的示意图。
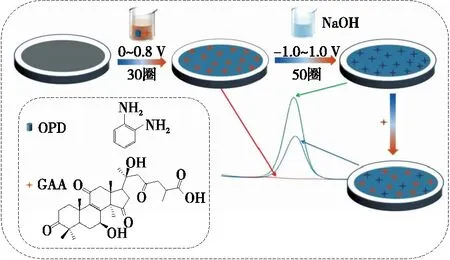
图1 GAA分子印迹电化学传感器构建示意图
1.3.4 试验条件优化 为达到传感器对GAA最佳的分析性能,从OPD电化学聚合扫描圈数、模板分子GAA洗脱圈数和GAA吸附时间进行试验条件优化。具体方法:将GCE置于OPD和GAA混合溶液中进行电化学聚合,直至所得的CV曲线趋于稳定,考察OPD在GCE表面聚合是否达到饱和;将聚合后的电极在0.1 mol/L NaOH空白液中进行不同圈数CV扫描用于GAA洗脱,在[Fe(CN)6]3-/4-溶液中进行电化学检测,当[Fe(CN)6]3-/4-峰电流达到最大稳定值,验证GAA已洗脱完全;进一步将洗脱后的电极在GAA溶液中吸附不同时间,考察其在[Fe(CN)6]3-/4-溶液中的电化学响应,当信号降到最低,验证GAA与MIP吸附达到平衡。
2 结果与分析
2.1 电聚合过程
图2(a)为GCE在含NIP前驱液中连续电聚合30圈的CV图。聚合第一圈时,0.48 V处出现一个不可逆的氧化峰,对应于OPD上的氨基被氧化成带正电荷的自由基的不可逆过程[22-23]。随着扫描圈数的增加,该氧化峰强度逐渐下降,说明有不导电产物吸附在GCE表面,抑制了后续聚合吸附过程。当聚合至30圈时,该氧化峰趋于消失,表明GCE表面已完全被OPD聚合膜覆盖。而当电解液为MIP前驱液时[图2(b)],同样观察到0.48 V附近有一不可逆氧化峰,证实了该峰来自于OPD的氧化。随着扫描圈数的增加,该峰逐渐降低,说明不导电聚合产物吸附在电极表面。该结果也表明GAA的存在不会影响OPD的电化学聚合过程。值得注意的是,在相同的电聚合扫描圈数下,NIP前驱液的峰信号强度均低于MIP的峰信号强度。这可能是因为在电聚合成膜的过程中,由于MIP前驱液中的GAA与OPD通过氢键作用掺入聚合膜中,降低了OPD聚合膜的致密度,从而有利于后续的OPD在电极表面的扩散和氧化。

图2 GCE在NIP和MIP前驱液中连续扫描的CV曲线
2.2 MIP物化表征
2.2.1 SEM表征 由图3可知,经电化学聚合的NIP和MIP在电极表面均呈无规则颗粒状材料,且覆盖了整个电极表面。NIP表面光滑,而MIP材料表面具有大量孔洞。该差异表明,印迹模板分子GAA可有效从MIP中洗脱出来,并在MIP膜上留下与GAA分子匹配的“孔穴”。

图3 NIP和MIP的SEM图
2.2.2 FT-IR表征 采用FT-IR对NIP和MIP的化学结构进行表征,结果(如图4所示)显示NIP和MIP的特征吸收带完全一致,表明二者的化学结构相同。在3 430 cm-1附近的宽吸收带和1 650 cm-1处的吸收峰归属于N—H收缩振动和弯曲振动[24]。2 947 cm-1和2 882 cm-1归属于饱和的C—H振动吸收峰[25]。1 430 cm-1的吸收峰归因于苯环上C═C骨架的伸缩振动[26]。1 043 cm-1处的吸收峰对应于聚合物中的C—N收缩振动。851 cm-1处的吸收峰表明存在吩嗪结构。上述结果证实电化学合成的MIP为在吩嗪的主链上具有苯环和喹环结构头尾相连的聚合物。

图4 NIP和MIP的FT-IR图
2.3 不同修饰电极的电化学表征
使用CV法和EIS法,在0.1 mmol/L的[Fe(CN)6]3-/4-溶液中对不同修饰电极进行电化学表征,结果如图5所示。由图5(a)可以看出,[Fe(CN)6]3-/4-在裸GCE上有一对可逆的氧化还原峰(曲线a),表明[Fe(CN)6]3-/4-在裸GCE表面发生很好的电子转移过程。而[Fe(CN)6]3-/4-在电聚合后的GAA/MIP复合修饰电极上的氧化还原峰完全消失(曲线b),是因为电极上覆盖了一层致密且不导电的绝缘聚合膜,阻碍了[Fe(CN)6]3-/4-与基底电极的接触。当去除GAA模板分子后,[Fe(CN)6]3-/4-在电极上又重新出现一对明显的氧化还原峰(曲线c),表明GAA分子可以有效地从MIP膜中洗脱,并留下空腔,成为[Fe(CN)6]3-/4-扩散到GCE表面的通道。对OPD-MIP重新吸附GAA的电极,发现[Fe(CN)6]3-/4-的氧化还原信号相比吸附前有明显减弱(曲线d)。该试验表明,GAA洗脱后的空腔构象与GAA功能基团相匹配,可用于GAA的吸附识别,重新占据MIP膜上空腔位点,导致[Fe(CN)6]3-/4-的CV信号减弱。
由图5(b)可知,裸GCE上只有很小的电荷转电阻(Rct)(曲线a),表明GCE具有很好的导电能力。聚合后的GAA/MIP修饰电极Rct值最大(曲线b),电极表面覆盖了一层致密不导电的聚合物。在洗脱后的MIP/GCE上Rct值降低(曲线c),是因为GAA模板分子被去除形成空腔,导电性增强。当在GAA溶液中重新结合后,形成复合物,阻碍了[Fe(CN)6]3-/4-靠近电极表面,所对应的Rct值有所升高(曲线d),说明MIP电极对GAA具有识别能力。

a.裸GCE b.GAA/MIP/GCE c.MIP/GCE d.冲洗吸附后的GAA/MIP/GCE
2.4 模板洗脱圈数和GAA吸附时间优化
2.4.1 洗脱扫描圈数优化 在0.1 mol/L NaOH中进行GAA洗脱的CV扫描圈数直接影响传感器MIP膜的空腔数量,洗脱圈数太少会导致大量GAA模板分子残留在膜内,降低传感器对GAA检测的识别能力。由图6可知,洗脱圈数为10~50圈时,峰电流值随洗脱圈数的增加而增加,说明印迹孔穴逐渐增多。当洗脱圈数达到50圈后,峰电流值达到最大值,之后峰电流值不再有明显的变化,说明GAA模板分子已从MIP膜中洗脱干净。因此,选择50圈为最优的CV洗脱圈数。

图6 峰电流与CV扫描洗脱圈数关系曲线图
2.4.2 GAA吸附时间优化 将GAA洗脱完全的传感器浸入0.1 μmol/L GAA溶液不同时间,然后取出,在[Fe(CN)6]3-/4-溶液中进行扫描,考察不同吸附时间对传感器峰电流的影响。由图7可知,峰电流值随吸附时间的增加而减小,当吸附时间增加到50 min时电流峰值基本趋于稳定,说明GAA在MIP膜上的吸附达到平衡,因此50 min为传感器吸附GAA的最佳时间。

图7 峰电流与GAA吸附时间的关系曲线
2.5 分析性能
在最佳条件下,将MIP/GCE浸入不同浓度(1.0 pmol/L~1.0 μmol/L)的GAA溶液中吸附50 min,再在[Fe(CN)6]3-/4-溶液中进行DPV扫描,考察分子印迹传感器对GAA的分析性能。由图8(a)可知,随着GAA浓度的增加,使所测的峰电流值逐渐降低,表明越来越多的GAA目标分子占据了MIP/GCE上空腔位点。峰电流值(Ip)与GAA浓度负对数(-lgC)在1.0 pmol/L~1.0 μmol/L范围内呈良好的线性关系[图8(b)],其线性回归方程为:Ip=18.2-0.710lgC,相关系数R2=0.995 1,检出限为0.21 pmol/L。
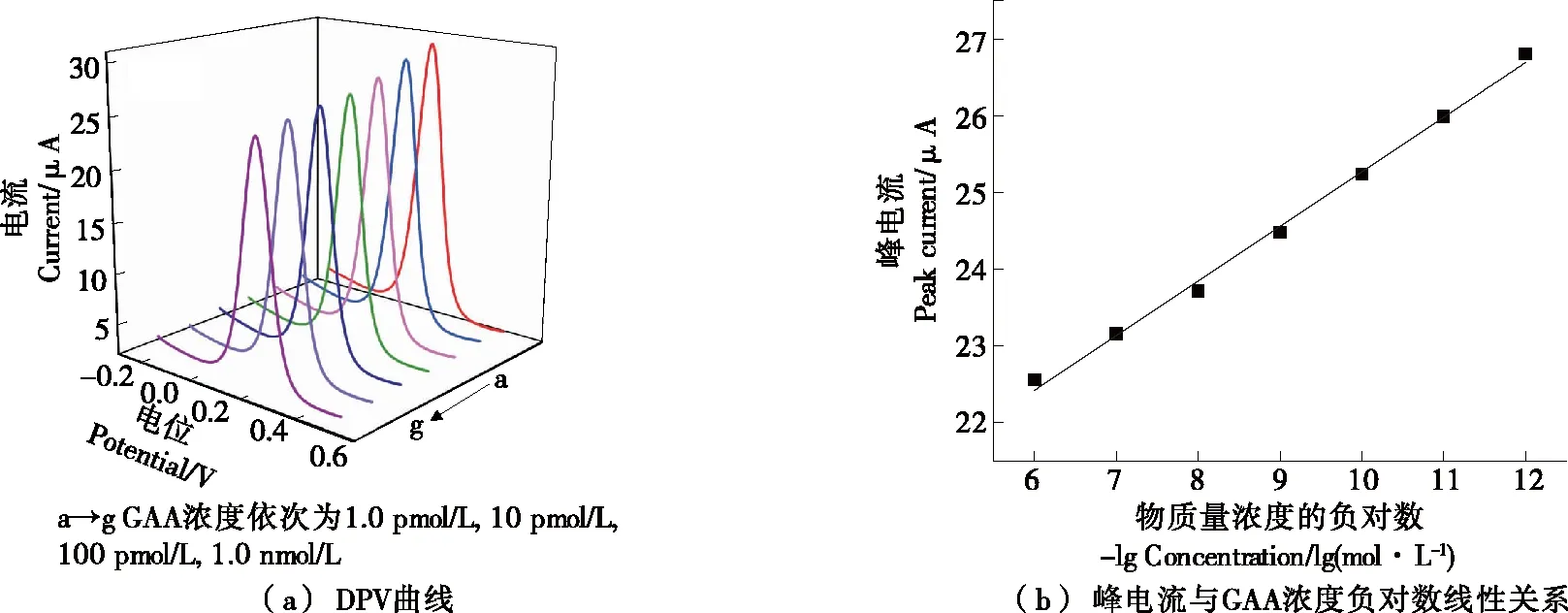
图8 MIP/GCE与不同浓度GAA吸附后的DPV曲线及其峰电流与GAA浓度负对数线性关系
2.6 重现性、稳定性和选择性
平行制备5支MIP/GCE,在相同条件下对1.0 μmol/L GAA目标分子进行检测,结果如图9(a)所示。根据信号变化,求得相对标准偏差(RSD)为3.3%,表明所制备的传感器具有良好的重现性。

图9 MIP电化学传感器的重复性和稳定性
将制备的MIP/GCE置于4 ℃冰箱中保存,每隔24 h使用DPV法对其进行连续检测,并在第7天考察其对1.0 μmol/L GAA溶液的分析性能。结果如图9(b)所示,MIP/GCE连续6 d的DPV峰电流变化很小;且第7天仍能用于GAA检测,说明MIP/GCE具有良好的稳定性。
图10为分子印迹传感器在不同溶液(浓度均为1.0 μmol/L)中浸泡50 min后,在[Fe(CN)6]3-/4-中的DPV曲线。由图10可知,MIP/GCE在空白液中的信号(曲线a)与其在绿原酸(曲线b)、木犀草素(曲线c)、多巴胺(曲线d)溶液中浸泡后的信号接近,表明传感器对上述溶液不产生响应。而在GAA溶液中浸泡后,信号降低,且与在混合溶液中浸泡后的DPV峰电流值无明显差异,表明该电化学传感器对GAA有良好的选择识别性。

a.空白液 b.绿原酸 c.木犀草素 d.多巴胺 e.GAA溶液 f.GAA、绿原酸、木犀草素和多巴胺混合溶液
2.7 实际样品的检测
将市场购买的灵芝粉实际样品用水或乙醇作为溶剂分别配制10 mg/mL的灵芝液,静置24 h。离心,取100 μL 灵芝液,用MIP/GCE进行浸泡吸附,后在[Fe(CN)6]3-/4-中进行检测,根据峰电流值代入线性回归方程计算分析得到相应的GAA的浓度。随后在浸出灵芝液中分别加入不同浓度的标准GAA溶液进行回收率测定,结果如表1所示。结果显示以乙醇为溶剂的浸出浓度为1.15 nmol/L,而以水为溶剂的浸出浓度仅为3.00 pmol/L,表明乙醇能更有效地使GAA从实际样品中溶解出来。在两种溶剂浸出液中进行标准加入法,得到的回收率分别为99%~102%和98%~101%,说明该方法所制备的分子印迹电化学传感器对GAA的检测具有较高的准确度,可用于灵芝粉等实际样品的检测。建立灵芝活性成分的快速检测方法,有助于灵芝药材的质量控制与现代剂型的开发。
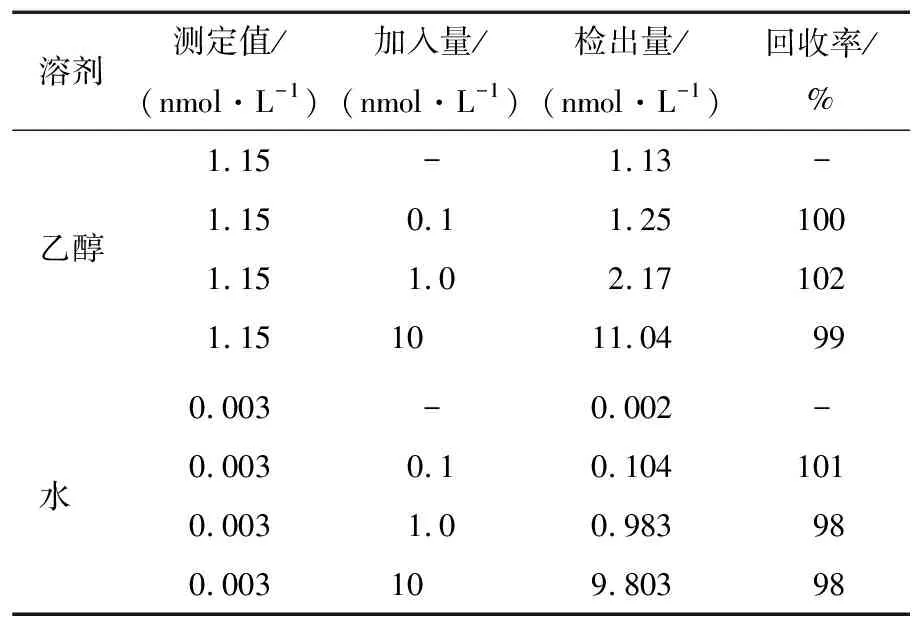
表1 用乙醇或水配制的灵芝液实际样品中GAA测定结果
3 结论
将分子印迹技术和电化学传感器结合,采用电聚合的方法,以邻苯二胺为功能单体,灵芝酸A为模板分子,在无需交联剂条件下合成分子印迹聚合物,并利用IR和SEM对其进行结构和形貌表征。在最佳的试验条件下,以灵芝酸A为模板分子,以邻苯二胺为功能单体合成的分子印迹电化学传感器具有良好的重现性、稳定性和选择性,在1.0 pmol/L~1.0 μmol/L 范围内,灵芝酸A的浓度(mol/L)和峰电流(μA)有良好的线性关系,拟合线性方程为Ip=18.2-0.710lgC,相关系数R2=0.995 1,检出限为0.21 pmol/L,在灵芝实际样品检测中其回收率为98%~102%,具有良好的检测性能。

