贝伐珠单抗一线治疗驱动基因阴性晚期肺腺癌的效果与安全性
丁若瀛,胡伟,刘奎元,刘金耿,程铭震
(郑州大学第一附属医院 胸外二科,河南 郑州 450000)
肺癌是我国最常见的恶性肿瘤类型,是导致癌症相关死亡的主要因素,非小细胞肺癌 (non small cell lung cancer,NSCLC)是其主要亚型[1]。一部分患者在确诊时存在局部晚期或广泛转移,所以预后较差。但近年来,得益于针对各个敏感突变靶点的新型靶向药物不断问世[2],NSCLC特别是肺腺癌死亡率下降明显。而对于驱动基因阴性无法进行靶向治疗的肺腺癌患者,免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)和含铂双药化疗联合,用于一线治疗晚期转移性肺腺癌,取得了良好疗效[3]。卡瑞利珠单抗是一种人源化单克隆抗体,可与细胞程序性死亡受体-1靶向结合发挥良好的抗肿瘤效果[4]。培美曲塞联合顺铂是晚期肺腺癌一线化疗方案,该方案副作用较小,患者耐受性良好[5]。近年来的研究显示,联合抗血管生成药物和ICIs可能会增加免疫治疗的有效性,并降低治疗相关不良反应的风险[6]。那么加用抗血管生成药物能否获得更好的临床疗效及较好的安全性,需要进一步探讨。
贝伐珠单抗是一种抗血管生成药物,通过阻断血管内皮生长因子(vascular endothlial growth factor,VEGF)抑制肿瘤血管生成[7]。本研究收集相关临床数据,通过对贝伐珠单抗、卡瑞利珠单抗、培美曲塞联合顺铂的疗效进行分析,进而明确应用贝伐珠单抗的疗效及安全性。
1 对象与方法
1.1 研究对象回顾性分析2020年12月至2022年6月在郑州大学第一附属医院接受治疗的初治驱动基因阴性的晚期转移性肺腺癌患者的临床资料。所有病例都有明确的组织病理学诊断,提示肺腺癌,二代测序技术检测肿瘤组织标本中的TMB水平及各个敏感突变靶点基因的变异。通过免疫组化技术进行细胞程序性死亡-配体1(programmed cell death-ligand 1,PD-L1)水平的检测。本研究获得郑州大学第一附属医院医学伦理委员会审批通过,所有患者信息及数据均符合相关数据保护和隐私规定。
1.2 纳入及排除标准
1.2.1纳入标准 (1)病理及影像学证明分期为不适合手术的Ⅲb、Ⅲc及Ⅳ期初治肺腺癌患者(以第8版TNM分期[8]为标准)。(2)符合实体瘤临床疗效评价标准(response evaluation criteria in solid tumors,RECIST),至少有1个可测量病灶。(3)基因检测无敏感突变。(4)年龄50~70岁。(5)东部肿瘤协作组(eastern cooperative oncology group,ECOG)评分为0~1分[9]。(6)无其他严重疾病史及肿瘤病史。
1.2.2排除标准 (1)敏感突变阳性或仍有合适靶点可行靶向治疗的患者。(2)既往接受过细胞毒性药物或免疫检查点抑制剂治疗的患者。(3)有症状的中枢神经系统转移患者。(4)有自身免疫性疾病个人史的患者或有长期糖皮质激素及免疫抑制剂应用的患者。(5)治疗周期内有放疗的患者。(6)治疗前肝、肾功能异常者。(7)继发性肺肿瘤者。
1.3 治疗方案治疗期间患者未接受其他抗肿瘤治疗方案,只接受相应镇痛及营养支持等治疗。(1)对照组患者接受注射用卡瑞利珠单抗(苏州盛迪亚生物医药有限公司,国药准字S20190027)治疗,将200 mg注射用卡瑞利珠单抗经5 mL灭菌注射用水复溶后加入100 mL生理盐水中,使用精密过滤输液器静脉滴注,每3周重复。将注射用培美曲塞二钠(齐鲁制药有限公司,国药准字H20060672)以 500 mg·m-2的剂量加入100 mL生理盐水中,第1天静脉滴注,每3周重复。注射用顺铂(齐鲁制药有限公司,国药准字H37021356)80 mg·m-2加入500 mL生理盐水中,第1~3天静脉滴注,每3周重复,直至病情出现进展。(2)观察组患者在对照组的基础上加用贝伐珠单抗注射液(Roche Pharma Ltd,注册证号SJ20170035,),以15 mg·kg-1的剂量加入100 mL生理盐水中静脉滴注,每3周重复,直至病情出现进展。
1.4 资料采集内容包括患者的年龄、性别、初诊分期、自治疗开始至疾病出现进展的时间、吸烟史、PD-L1表达状态、TMB水平、ECOG评分、是否有脑转移、是否有肝转移、接受治疗2周期后外周血中中性粒细胞与淋巴细胞的比值(neutrophil-to-lymphocyte ratio,NLR)和乳酸脱氢酶(lactate ehydrogenase,LDH)水平。
1.5 观察指标根据RECIST对入组患者临床疗效进行评价。2个治疗周期后根据患者影像学复查资料进行疗效评估。具体评估标准如下。完全缓解(complete response,CR):所有靶病灶消失,无新病灶出现。部分缓解(partial response,PR):靶病灶最大径减小≥30% 。疾病进展(progressive disease,PD):病灶增加≥20%或出现新的病灶。疾病稳定(stable disease,SD):靶病灶最大直径缩小未达PR且增大未达PD。客观缓解率(objective response rate,ORR):肿瘤体积缩小达到预先规定值并能维持最低时限要求的患者占比。疾病控制率(disease control rate,DCR):经治疗后获得缓解和病变稳定的病例数占可评价例数的百分比。无进展生存期(progression-free survival,PFS):从疾病开始治疗至PD或随访时间截止或因各种原因死亡的时间。本研究主要观察指标为PFS,次要观察指标为ORR及治疗安全性。采用常见不良时间评价标准(common terminology criteria for adverse events, CTCAE)用以评估不良事件。
1.6 统计学方法采用SPSS 26.0以及Graphpad Prism 7.0软件进行数据分析和图片绘制。以χ2检验或Fisher精确检验比较两组间人口一般特征以及客观疗效及安全性差异。生存分析采用Kaplan-Meier法,通过log-rank检验进行比较。用森林图描述亚组分析的结果。P<0.05为差异有统计学意义。
2 结果
2.1 一般资料两组患者的一般资料比较,差异无统计学意义。见表1。

表1 入组患者临床特征[n(%)]
2.2 生存分析观察组患者mPFS为9.7个月,95%置信区间为8.6~10.8个月。对照组患者mPFS为6.5个月,95%置信区间为4.3~8.7个月。两组间mPFS对比,差异有统计学意义(P=0.031)。见图1。
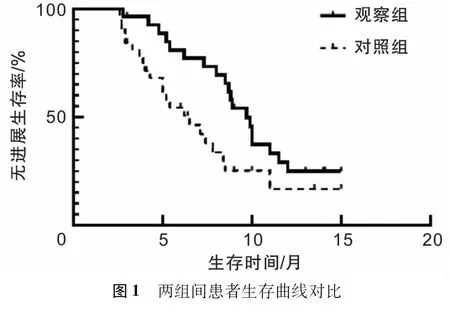
2.3 亚组分析观察组在总体人群及各个亚组人群中PFS均长于对照组(P<0.05)。见图2。在肝转移人群中,观察组mPFS长于对照组(P=0.019)。见图3。在高TMB人群中,观察组mPFS长于对照组(P=0.034)。见图4。

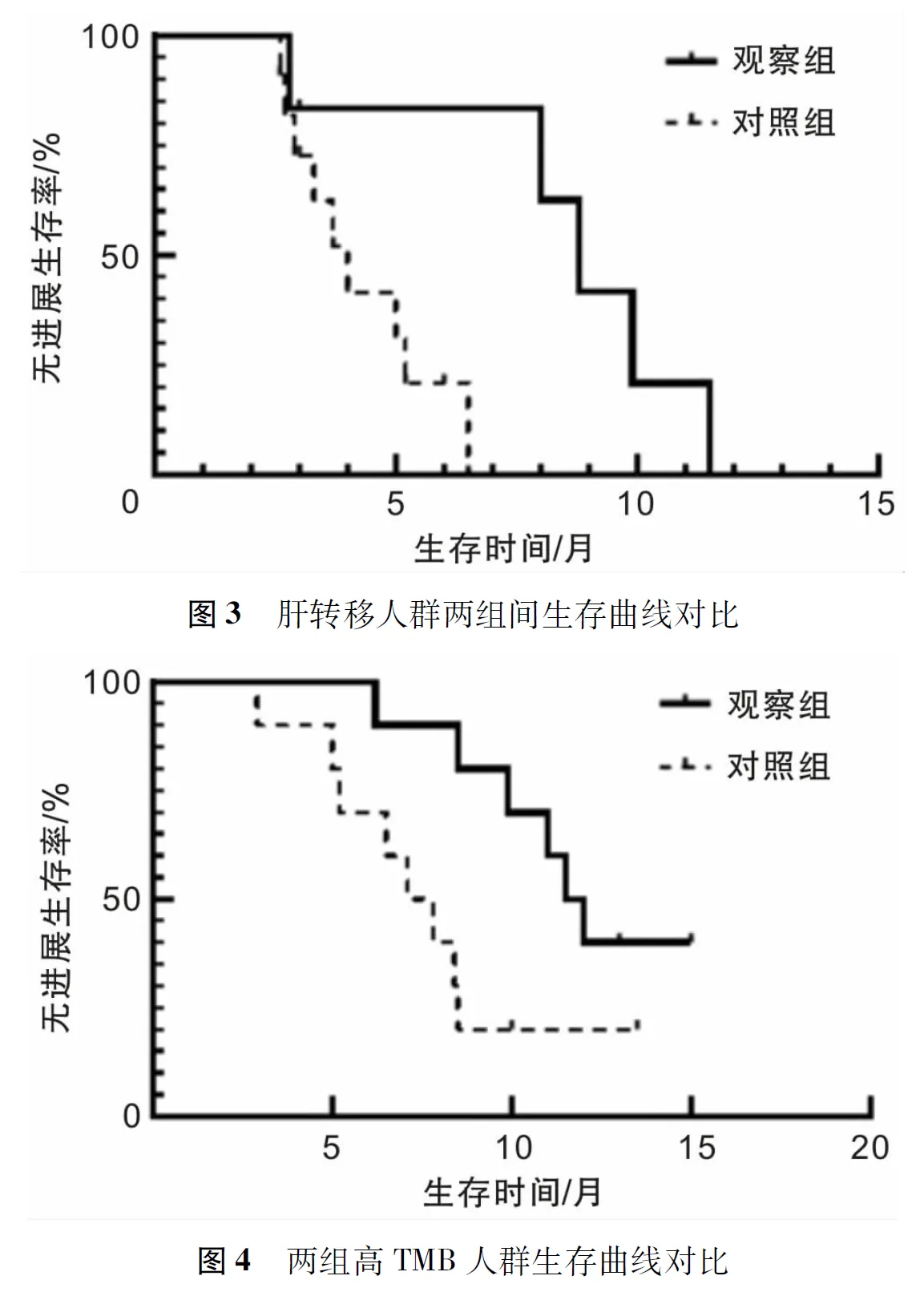
2.4 短期疗效评价及安全性评估入组患者短期疗效评价显示,治疗2个周期后,观察组ORR为53.6%,高于对照组(28.1%),差异有统计学意义(P=0.045)。两组DCR比较,差异无统计学意义。见表2。

表2 两组患者的短期疗效评价(n,%)
2.5 不良反应2级不良事件中,观察组肝功能损伤、高血压例数高于对照组,差异具有统计学意义(P<0.05)。两组3级不良事件发生情况比较,差异无统计学意义(P>0.05)。见表3。两组均未出现4级及以上不良反应及与不良反应相关的停药事件。

表3 两组患者不良反应发啥情况比较[n(%)]
3 讨论
在全世界范围内,肺癌仍是发病率以及死亡率最高的癌种,近85%为NSCLC,虽然随着CT检查的普及,早期肺癌检查率得到提高,但仍有部分患者在初诊时即出现局部淋巴浸润及远处转移,这些患者预后不佳,通常5 a生存率极低[5]。近10年来,随着各类靶向药物的研发与出现,以EGFR-TKI为代表的针对各个敏感突变靶点的靶向药物将晚期肺癌患者的总生存期(overall survival,OS)提高到3 a以上[10]。但一些存在不敏感突变的人群无法接受靶向药物治疗。对于这些人群,相较于传统的铂类药物为基础的双药化疗方案,ICIs联合化疗在多项三期临床试验中展示出了良好的疗效[11-12]。有研究显示卡瑞利珠单抗联合铂类及培美曲塞治疗驱动基因阴性晚期肺腺癌改善了PFS及OS,且安全可控,且患者耐受性好[13]。
而近年来研究表明,联合抗血管生成药物和免疫治疗可能会增加免疫治疗的有效性,并降低细胞毒性药物造成的相关不良反应的风险[14]。前期理论研究表明,血管异常是肿瘤重要的免疫逃避机制,相比于正常的结构,肿瘤血管在结构和功能上都是异常的,这种异常通过损害灌注促进肿瘤进展,在肿瘤微环境(tumor microenvironment,TME)中,血管的异常导致其内部缺氧,pH值降低,血管通透性增加,渗漏过多,同时淋巴引流功能紊乱导致间质液体压力增高,肿瘤细胞相比正常细胞更加适应这种TME的改变,缺氧和酸中毒还会导致免疫抑制,同时异常的血管和低灌注也可以限制细胞毒药物及ICIs治疗肿瘤的效果。VEGF是导致血管异常的关键介质。VEGF由TME中肿瘤细胞、免疫细胞、内皮细胞、间质细胞产生,直接或间接参与和介导免疫抑制,导致肿瘤细胞的免疫逃逸[15-16]。
此外,大量的临床试验也对抗血管生成联合免疫治疗的效果及安全性提供了证据。IMpower150的Ⅲ期临床研究证实免疫治疗联合抗血管生成治疗和化疗模式一线治疗转移性NSCLC后,患者PFS及OS均获益[17]。JVDF临床试验(NCT02443324)是雷莫芦单抗联合帕博利珠单抗治疗晚期实体瘤的多队列研究,结果显示,与标准疗法相比,该治疗方案下的患者OS延长明显,安全性及患者耐受性良好[18]。
基于这些基础理论与临床证据,本研究通过对收集的临床数据进行回顾性分析和组间比较,希望对驱动基因阴性的晚期肺腺癌的一线治疗提供新的参考。研究结果显示,在卡瑞利珠单抗及含铂两药化疗的治疗方案中加入贝伐珠单抗,可以延长患者PFS,且总体短期客观疗效较好,安全性良好,两组3~4级不良事件发生率比较,差异无统计学意义。在肝转移人群中,加用贝伐珠单抗可改善患者PFS;在高TMB人群中,加用贝伐珠单抗也可改善患者PFS。但本研究也具有自身局限性,单中心回顾性研究样本量较小,多种偏倚无法完全排除。另外,随访时间较短,OS数据未能得出。未来还需多中心、大样本、前瞻性研究所佐证。

