在线固相萃取/二维液相色谱法同时测定婴幼儿配方奶粉中多种脂溶性维生素
毛燕妮,许晴,李宏铨,聂懿,朱静璇,柳慧冰,康翠欣*
1(武汉食品化妆品检验所,湖北 武汉,430040)2(国家市场监管重点实验室(食用油质量与安全),湖北 武汉,430040)
维生素是为维持人体正常代谢和生理功能而必须从食物中获得的一类非常重要的有机化合物,分为脂溶性维生素和水溶性维生素两大类[1-2]。其中脂溶性维生素主要包括维生素A、D、E、K1,是婴幼儿生长发育的必需营养素,但其添加量必须控制在一定范围,如果缺乏或摄入过量都会引起代谢失衡,造成健康问题[1-2]。由于婴幼儿食物来源单一,乳粉中维生素的含量直接影响婴幼儿的健康。因此,快速、准确检测婴幼儿配方奶粉中脂溶性维生素的含量极其重要。
目前,脂溶性维生素A、D、E、K1通常采用高效液相色谱法进行检测,由于婴幼儿配方奶粉中维生素A、E、K1、D的含量存在从纳克级到毫克级不同含量水平,并且基质复杂,使得其无法共同提取和分析。现行国家标准方法GB 5009.82—2016《食品安全国家标准 食品中维生素A、D、E的测定》和文献报道测定维生素A、D、E方法多采用长时间碱性皂化破壁、多次液液萃取净化、浓缩的前处理方式[3-8],且维生素D需要正相高效液相色谱半制备分离浓缩后由反相高效液相色谱仪检测,操作繁琐、费时,重复性差。现行国家标准方法GB 5009.158—2016《食品安全国家标准 食品中维生素K1的测定》和文献报道测定维生素K1方法多采用酶解、液液萃取、浓缩的前处理方式,柱后锌粉还原-高效液相色谱-荧光检测法进行检测分析[9-15]。由于婴幼儿配方奶粉基质复杂、维生素含量差别大且测定灵敏度低等原因,同时测定脂溶性维生素A、D、E、K1的检测方法鲜有报道。
在线固相萃取/二维液相色谱法是将分离机制不同的2根色谱柱串联起来构成的分离系统,通过浓缩、捕集和切割后,在一维中不能完全分离的组分则可以在第二维中得到更好的分离,从而实现样品的在线净化,可以提高分析灵敏度[16-19]。已有文献报道,利用在线固相萃取/二维液相色谱法同时测定脂溶性维生素的方法,仅测定维生素A、维生素D、α-维生素E、γ-维生素E、δ-维生素E,未测定β-维生素E、维生素K1。本文中样品经皂化后,利用在线固相萃取技术与二维液相色谱技术的联用,同时测定婴幼儿配方奶粉中维生素A、维生素D2、维生素D3、α-维生素E、β-维生素E、γ-维生素E、δ-维生素E和维生素K1,直接进样分析,大大提高了检测效率。该方法回收率高、灵敏度高、重现性好。
1 材料与方法
1.1 材料与试剂
维生素A(99.4%),SIGMA公司;维生素D2(99.6%)、维生素D3(99.6%)、维生素K1(99.29%),英国LGC;α-维生素E(98%)、β-维生素E(98%)、δ-维生素E(98%)、γ-维生素E(98%),美国TLC公司;甲醇、乙腈、甲基叔丁基醚、无水乙醇(色谱纯),德国默克公司;氢氧化钾、抗坏血酸(分析纯),国药集团化学试剂有限公司。
1.2 仪器与设备
1260二维液相色谱仪:配有2个四元泵、1个二元泵、3个六通阀、1个紫外检测器(VWD)、1个二极管阵列检测器(DAD HS)、1个柱温箱、1个自动进样器,美国安捷伦公司;ME204天平,美国梅特勒-特利多仪器有限公司;Milli-Q超纯水仪,美国密理博公司;水浴恒温振荡器,中国常州国华电器有限公司;X-15冷冻离心机,美国贝克曼库尔特公司;UV-1800紫外可见分光光度计,日本岛津公司;Poroshell 120 PFP色谱柱(4.6 mm×100 mm, 4 μm)、Eclipse PAH色谱柱(2.1 mm×100 mm, 3.5 μm)、Poroshell 120 EC-C18色谱柱(4.6 mm×5 mm, 4 μm)、ONLINE PLRP-S固相萃取柱(4.6 mm×12.5 mm, 15 μm~20 μm),美国安捷伦公司。
1.3 实验方法
1.3.1 标准溶液配制
分别取维生素A、维生素D2、维生素D3、α-维生素E、β-维生素E、δ-维生素E、γ-维生素E和维生素K1各10 mg于10 mL棕色容量瓶中,无水乙醇溶解并定容,再分别用无水乙醇稀释,紫外可见分光光度计对其进行浓度校正。用V(乙醇)∶V(水)=1∶1稀释并定容至刻度配制混合标准曲线,各种维生素的浓度梯度见表1。

表1 维生素A、维生素D2、维生素D3、α-维生素E、β-维生素E、δ-维生素E、γ-维生素E和维生素K1曲线浓度
1.3.2 试剂配制
氢氧化钾溶液:称取氢氧化钾50 g,加入40 mL水溶解,混匀。
1.3.3 样品前处理
称取5 g样品,加入20 mL 40~60 ℃温水,混匀;再加入1.0 g抗坏血酸,混匀。分别加入30 mL无水乙醇和15 mL氢氧化钾溶液,边加边振摇,充分混匀后于80 ℃恒温水浴震荡皂化15 min。皂化后立即用冷水冷却至室温,用V(乙醇)∶V(水)=1∶1溶液转移并定容至100 mL棕色容量瓶中,混匀。取适量上述溶液,10 000 r/min离心5 min,上清液过0.22 μm有机系滤膜,待测。
1.4 仪器分析条件
色谱柱:Poroshell 120 PFP柱为一维分析柱,Eclipse PAH柱为二维分析柱,Poroshell 120 EC-C18柱为捕获柱,ONLINE PLRP-S固相萃取柱为皂化液净化柱。进样量:100 μL。柱温:30 ℃。检测波长:VWD(一维):0~14 min:325 nm、14~17 min:264 nm、17~28 min:294 nm;DAD(二维):0~24 min:264 nm、24~28 min:248 nm。流速:SPE泵:1.0 mL/min;一维泵:0~6.5 min:0.5 mL/min、6.5~22 min:1.0 mL/min、22~28 min:0.5 mL/min;二维泵:0.4 mL/min。流动相:SPE泵:A:水;B:乙腈;C:甲醇;D:甲基叔丁基醚;一维泵:A:水;B:甲醇;二维泵:A:乙腈;B:甲醇,洗脱程序见表2。流路连接示意图见图1,阀A切换时间:0~4.5 min(位置1-6),4.5~5.9 min(位置1-2),5.9~28 min(位置1-6),阀B切换时间:0~15.7 min(位置1-6),15.7~16.5 min(位置1-2),16.5~19.7 min(位置1-6),19.7~20.7 min(位置1-2),20.7~28 min(位置1-6)。
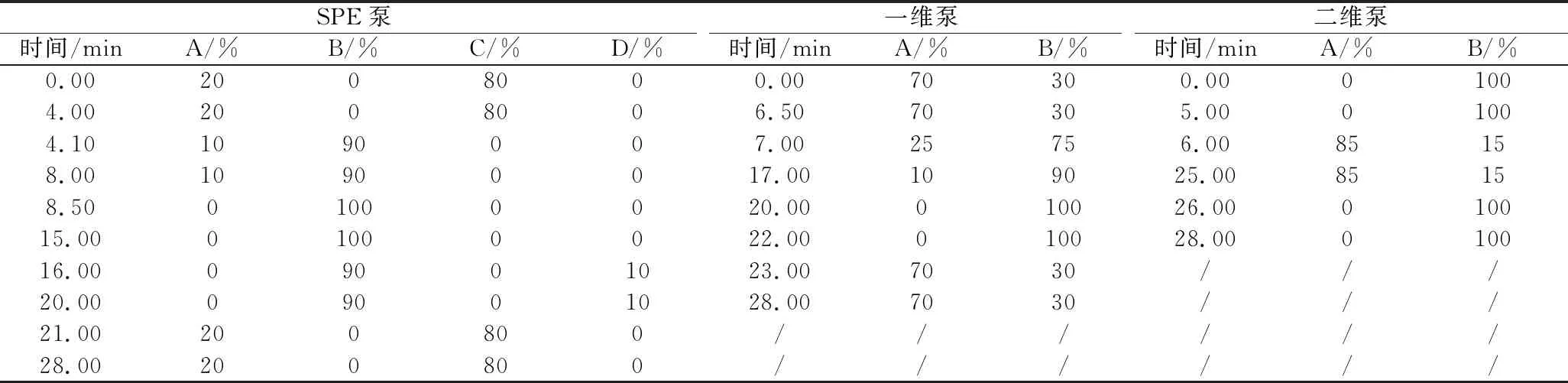
表2 流动相洗脱程序

图1 流路连接示意图
2 结果与分析
2.1 仪器方法的建立
2.1.1 色谱柱的选择
为了使4种维生素E的异构体能够得到有效的分离,一维色谱柱分别比较了Poroshell 120 PFP柱、EC-C8柱和Poroshell 120 EC-C18柱。其中Poroshell 120 PFP柱能较好分离4种维生素E,其他色谱柱不能将β-维生素E、γ-维生素E有效分离。而为了使维生素D2和维生素D3能够有效分离,二维色谱柱又比较了Eclipse PAH柱和Poroshell 120 EC-C18柱,Eclipse PAH柱能够有效分离维生素D2和维生素D3。因此选择Poroshell 120 PFP柱和Eclipse PAH柱分别作为一维和二维色谱柱。
2.1.2 色谱条件的优化
构建在线固相萃取/二维液相色谱法,关键的色谱条件体现在以下3点:
(1)利用在线固相萃取装置去除皂化液中的强碱、较强极性和强极性物质。通过阀A在位置1-6及SPE泵的初始流动相[V(甲醇)∶V(水)=8∶2]将目标物保留在SPE柱上,除掉大部分强碱和极性强的物质,当阀A切换为位置1-2,实现一维泵初始流动相[V(甲醇)∶V(水)=3∶7]对SPE柱的反冲,将目标物洗脱至一维色谱系统,再将阀A切换回位置1-6,再生SPE柱。
(2)由于婴幼儿配方奶粉中维生素A和维生素E含量较高,维生素D和维生素K1含量较低,故需要在一维上将维生素A和4种维生素E进行分离,并且将维生素D和维生素K1通过阀B切换到捕获柱上,通过灵敏度更高的检测器即二维进行分析。采用先将浓度较高的维生素A、α-维生素E、β-维生素E、δ-维生素E、γ-维生素E在一维色谱系统上进行分离,同时确定维生素D2、维生素D3和维生素K1在一维检测器的保留时间,再将阀B在维生素D2、维生素D3和维生素K1出峰的时间段从位置1-6切换至1-2,使目标物保留在捕集柱上,最后通过二维液相色谱的流动相将目标物洗脱,在二维检测器上进行测定。
(3)二维色谱系统上需要将维生素D2和维生素D3进行有效分离,并且选择合适的流动相条件测定维生素K1。一维和二维色谱图见图2。

a-一维液相色谱图;b-二维液相色谱图
2.2 前处理条件的选择
样品前处理的过程参照GB 5009.82—2016中的皂化过程,为防止维生素变性,在充分讨论了抗坏血酸添加量的基础上,沿用上述食品安全国家标准中1.0 g抗坏血酸的加入量,但不再加入2,6-二叔丁基对甲酚。通过持续一周对样品溶液中各维生素的含量进行测定,结果发现样品溶液保存在-18 ℃条件下,维生素含量基本保持稳定。此外对于氢氧化钾溶液的加入量,发现加入10~20 mL时各维生素的含量无明显变化。为了保证皂化反应完全以及在线固相萃取柱除碱效率最大化,选择加入15 mL氢氧化钾溶液。另外考察了温度对皂化效率以及维生素分解的影响,发现80 ℃水浴15 min能使样品皂化完全且维生素A、维生素D2、维生素D3、α-维生素E、β-维生素E、δ-维生素E、γ-维生素E和维生素K1均未发生变性、分解的情况。此外,还比较了定容溶剂,发现纯乙醇定容时仪器响应高,但峰面积、保留时间不稳定,而用V(乙醇)∶V(水)=1∶1定容时所测定的各种脂溶性维生素能维持较好的稳定性,所以最后采用V(乙醇)∶V(水)=1∶1对皂化液进行定容。
2.3 方法学验证
2.3.1 线性范围
按照1.3.1配制标准储备溶液及标准曲线,进样量100 μL,对各浓度梯度下维生素A、维生素D2、维生素D3、α-维生素E、β-维生素E、δ-维生素E、γ-维生素E、维生素K1进行测定。维生素A在2~500 ng/mL相关系数0.999 9,维生素D2在0.5~125 ng/mL相关系数0.998 9,维生素D3在0.5~125 ng/mL相关系数0.999 1,α-维生素E在20~5 000 ng/mL相关系数0.999 4,β-维生素E在20~5 000 ng/mL相关系数0.999 3,δ-维生素E在20~5 000 ng/mL相关系数0.999 0,γ-维生素E在20~5 000 ng/mL相关系数0.998 5,维生素K1在2~500 ng/mL相关系数0.998 4,表明各目标物在一定的浓度范围内线性关系良好。
2.3.2 方法检出限及方法定量限
分别根据S/N=3和S/N=10确定各种脂溶性维生素的检出限和定量限,维生素A、维生素D2、维生素D3、α-维生素E、β-维生素E、δ-维生素E、γ-维生素E和维生素K1检出限分别为4.0、1.0、1.0、40.0、40.0、40.0、40.0、4.0 μg/100 g;定量限分别为10.0、2.5、2.5、100.0、100.0、100.0、100.0、10.0 μg/100 g,均能满足婴幼儿配方奶粉的检测要求,与GB 5009.82—2016第一法和第四法、GB 5009.158—2016第一法中的检出限和定量限相近。
2.3.3 准确度和精密度
对空白样(乳清蛋白粉)进行加标回收实验,按定量限、2倍定量限和10倍定量限3种浓度水平制备加标回收样品,按照上述实验操作进行6平行实验,得到维生素A、维生素D2、维生素D3、α-维生素E、β-维生素E、δ-维生素E、γ-维生素E和维生素K1加标回收率在91.23%~107.2%,相对标准偏差在0.67%~8.06%。该方法的准确度和精密度较好,可以满足实验需求。
2.3.4 Fapas能力验证结果及与食品安全国家标准方法结果的比较
参加了2021年度婴幼儿配方奶粉中维生素A、维生素D3、α-维生素E和维生素K1的Fapas能力验证,采用在线固相萃取/二维液相色谱法对维生素A、维生素D3、α-维生素E和维生素K1进行测定,结果均满意,z值分别为0.4、0.3、0.2和1.1,均在允许误差范围内。将本方法与GB 5009.82—2016第一法、第四法和GB 5009.158—2016第一法检测结果分别进行比较,实验结果表明,本方法测定结果更接近指示值,详见表3,且前处理步骤简单,一方面省去了食品安全国家标准中液液萃取等繁琐步骤,耗时短、消耗溶剂少、准确度和稳定性高;另一方面降低了检测和人工成本,并且可实现批量同时检测婴幼儿配方奶粉中维生素A、维生素D2、维生素D3、α-维生素E、β-维生素E、δ-维生素E、γ-维生素E和维生素K1。

表3 Fapas样品中维生素A、维生素D3、α-维生素E 和维生素K1的测定结果
2.3.5 实际样品检测
随机选取11批次市售婴幼儿配方奶粉,按照1.3进行检测,结果见表4。测定结果均符合食品安全国家标准相关限量规定。
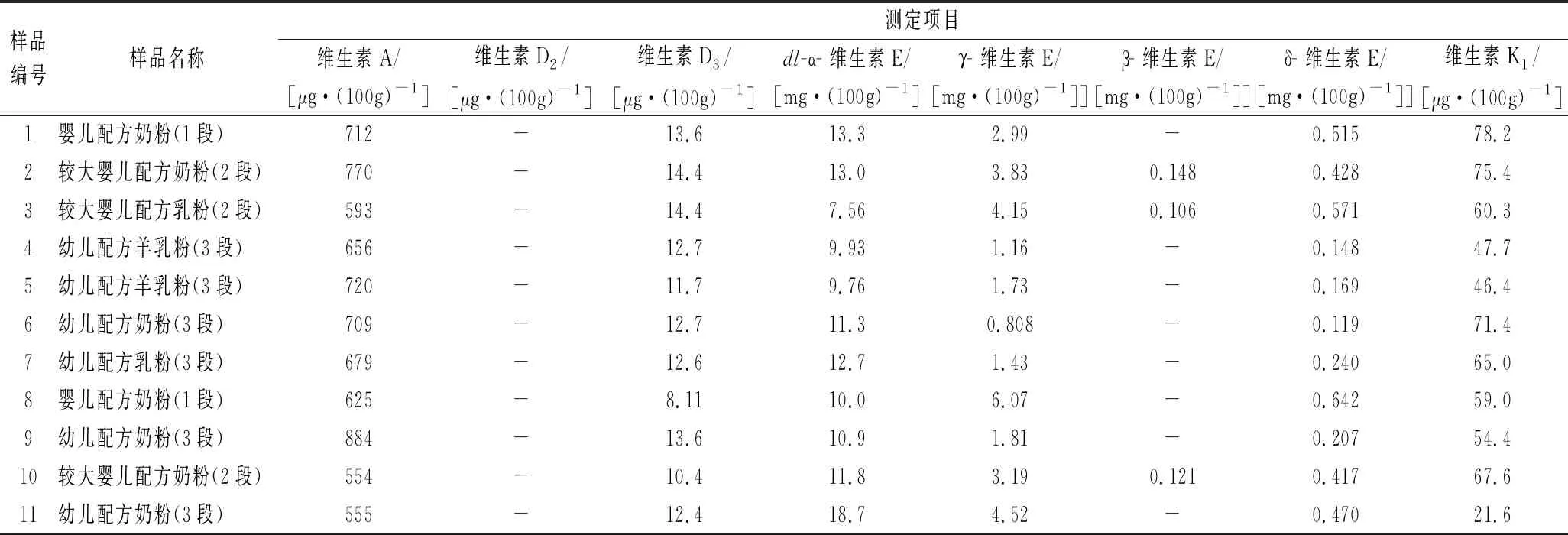
表4 实际样品中维生素A、维生素D3、α-维生素E和维生素K1测定结果
3 结论
本方法建立了在线固相萃取/二维液相色谱的方法,用于同时测定婴幼儿配方奶粉中多种脂溶性维生素,大大提高了检测效率,方法学验证结果较好。该方法能同时满足食品安全国家标准3个方法的检测要求,为婴幼儿配方奶粉中脂溶性维生素的检测方法提供了新的思路。

