干旱和高温胁迫下紫花苜蓿PEPC酶活性变化及其基因序列分析
侯燕红, 生小燕, 韩 博, 姜 华, 何承刚
(云南农业大学动物科学技术学院, 云南 昆明 650201)
紫花苜蓿(MedicagosativaL.)是一种适口性好,蛋白质含量高,营养价值全面,利用年限长,分布极其广泛的多年生优质豆科牧草。随着全球气候变暖并伴随着降水量减少的形势不断加剧,高温和干旱已经成为制约紫花苜蓿生产的一个难题。在中国南方,紫花苜蓿生长主要受高温的限制,因此,突破高温限制是实现其在该地区的开发与利用的关键[1]。同时,干旱也严重影响着苜蓿的产量和品质,研究表明干旱和高温在自然环境中通常会伴随出现,两者同时出现对植物生长和产量的危害比单独出现更大[2]。光合作用是植物生长发育过程中极其重要的生理过程[3],磷酸烯醇式丙酮酸羧化酶(Phosphoenolpyruvate carboxylase,PEPC)是C4植物光合作用的重要关键酶之一,其功能是催化磷酸烯醇式丙酮酸(Phosphoenolpymvate,PEP)和碳酸氢根离子的反应,生成草酰乙酸(Oxaloacetate,OAA)和无机磷酸(Inorganic phosphate,Pi),这是C4植物和景天酸代谢植物同化与固定CO2的重要步骤,是植物光合作用必不可少的一步[4]。PEPC在高等植物、藻类、细菌中广泛存在[5],目前,PEPC基因相继在拟南芥(Arabidopsisthaliana(L.) Heynh.)、大豆(Glycinemax(Linn.) Merr.)、水稻(OryzasativaL.)、玉米(ZeamaysL.)、甘蔗(Saccharumofficinarum)等植物中得到鉴定[6~9]。研究表明,PEPC参与了植物逆境胁迫的应答[10],关于这方面的研究近年来也有很多。丁在松等[11]研究转PEPC基因水稻在不同程度干旱胁迫下的光合特性,发现PEPC增强了干旱胁迫下水稻抵御强光胁迫的能力。Jeanneau等[12]研究发现,玉米在适度干旱条件下,PEPC基因过表达能使其水分利用率和干物质积累量增加。方立锋等[13]研究转PEPC基因水稻苗期抗旱性,发现其抗氧化能力和渗透调节能力均高于对照。赵晋峰等[14]从谷子基因中筛选出6个PEPC基因,得出SiPEPC基因广泛参与了谷子苗期非生物逆境胁迫应答。张庆琛等[15]研究了强光胁迫下玉米PEPC基因等对拟南芥光合特性的影响,发现强光处理下PEPC转基因拟南芥的光合速率显著高于正常处理,进而获得较高的生物量。另外也有研究表明,植物在面对干旱、冷害、强光、盐和低磷等非生物逆境胁迫时[16-20],PEPC基因均能够被强烈诱导并表达,说明植物在面对非生物逆境胁迫时PEPC在其中发挥着一定作用。
当前,对于各种植物在逆境胁迫下的研究比较广泛,有关于紫花苜蓿在干热胁迫下Rubisco羧化酶和活化酶活性变化及其基因表达的研究[21],也有紫花苜蓿的耐盐基因[22]、抗逆基因[23]等的研究,但是对于紫花苜蓿在干旱和高温胁迫下PEPC基因的研究比较缺乏。因此,本研究以抗逆性均较强的‘阿尔冈金’紫花苜蓿和云南省德钦县野生紫花苜蓿为材料,测定两者在高温胁迫和干旱胁迫下的PEPC酶活性,并扩增了PEPC基因,对PEPC蛋白进行了生物信息学分析和系统发育分析,为提高高温和干旱条件下紫花苜蓿的生物产量提供理论依据。
1 材料与方法
1.1 供试材料
供试的2个材料为采集于云南省迪庆州德钦县奔子栏乡干热河谷区的野生紫花苜蓿和引自加拿大的‘阿尔冈金’紫花苜蓿,前者在云南干热河谷地区干热条件下能够繁衍后代,能较好适应类似云南迪庆的生态条件,具有较强的抗旱性,后者抗逆性强,适应性广。
1.2 试验设计
试验采用盆栽方式,每盆种植20~30粒均匀饱满的紫花苜蓿种子,放置于云南农业大学草业科学实习基地温室内,选取3~4片叶期的幼嫩叶片存放于-80℃冰箱中用于DNA的提取及PEPC基因的扩增。每个品种随机选取生长150 d并且长势一致的6盆材料,每盆10株。其中3盆进行干旱胁迫处理,将其置于室内并在常温(温度23℃,湿度40%)下处理,开始处理后不再浇水;另外3盆进行干热胁迫处理,将其放入人工气候箱,空气湿度设定为30%,白天温度为32℃保持14 h,夜间温度为28℃保持10 h。分别于胁迫处理前(对照)以及胁迫处理后第4 h,8 h,12 h,16 h,24 h,4 d,8 d,12 d以及复水(恢复为处理前的湿度和温度,并浇水至花盆底部有水溢出为止)后2 d(在图表中用r表示),取相同部位叶片经液氮处理后置于-80℃冰箱中,用于PEPC酶活性的测定(试验做了3个技术重复,3个生物学重复)。
1.3 试验内容与方法
1.3.1PEPC酶活性测定 酶液提取和活性测定参照BERVEILLER等的方法[22]。(1)提取液制备:0.01%(v/v)Triton X-100;1 mmol·L-1EDTA;50 mmol·L-1Tris-HCl,pH 7.8;10 mmol·L-1MgCl2;10 mmol·L-1dtt;(2)酶液提取:在预冷研钵中放入称好的0.25 g新鲜叶片后加入液氮迅速研磨,随后加4 ml预冷提取液,在冰浴中研磨至匀浆,4℃、15 000 g离心15 min,取上清液保存于-20℃条件下备用;(3)酶活性测定:反应体系为1 mL 100 mmol·L-1Tris-HCl缓冲液(pH7.4),0.1 mL酶提取液,1 mL 10 mmol·L-1MgCl2,1 mL 10 mmol·L-1NaHCO3,0.2 mL 40 mmol·L-1PEP,0.3 mL 1 mg·mol·mL-1NADH(pH 8.9),0.3 mL 12 U·mL-1苹果酸脱氢酶。反应液混匀,28℃水浴10 min,用200 μL PEPC提取液启动反应,测定波长在340 nm处的吸光度。酶活性计算公式如下:
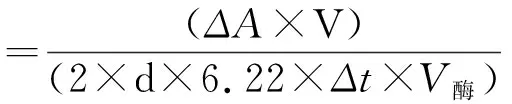
其中ΔA为反应前后的差值,V为反应体系总体积,d(cm)为比色光程,6.22为每微摩尔NADH在340 nm处的吸光度,2表示每固定1 mol CO2有2 mol NADH被氧化,Δt为测定时间,V酶为酶液体积。计算结果单位为μmol·g-1·min-1。
1.3.2DNA提取 取叶期的紫花苜蓿3~4幼嫩叶,采用上海生工生物工程股份有限公司的Ezup柱式植物基因组DNA抽提试剂盒提取紫花苜蓿的DNA。
1.3.3PCR扩增 在National Center for Biotechnology Information(NCBI)上搜索已知紫花苜蓿的PEPC基因序列,利用网站(sg.idtdna.com)进行引物设计:F(GACCTACCCATCTTGCTATCTTG),R(CTCCAAAGCCCAACCATACT),引物由上海生工生物工程股份有限公司合成。PCR反应总体积为25 μL,包括上下游引物各1 μL,Taq PCR Mix预混液12.5 μL,模板DNA0.5 μL,ddH2O 10 μL。扩增程序为95℃预变性3 min;94℃变性30 s,56℃复性30 s,72℃延伸90 s,33个循环,72℃延伸7 min。
1.3.4产物回收及测序 将经1%琼脂糖凝胶电泳检测合格后的PCR扩增产物进行回收纯化并测序。
1.4 数据处理
数据统计和折线图采用Excel 2010软件进行。采用单因素方差分析法对同一材料不同条件下的差异显著性(P<0.05)进行分析,对不同材料同一处理条件之间显著性差异(P<0.05和P<0.01)作独立样本T检验,单因素方差分析和独立样本T检验均采用SPSS 23.0软件进行。采用DNAMAN 8.0软件将本试验的紫花苜蓿PEPC基因核酸序列翻译成蛋白质并作多序列比对,利用Protparam软件分析并预测紫花苜蓿PEPC蛋白的理化性质。在NCBI网站上将测序结果进行比对后,用DNAMAN 8.0软件对本研究的两个材料以及NCBI网站上下载的鹰嘴豆(Cicerarietinum,XM_004488973.2)、紫花苜蓿(Medicagosativa,M83086.1)、蒺藜苜蓿(Medicagotruncatula,XM_003596337.4)和菜豆(Phaseolusvulgaris,XM_007133140.1)6个PEPC蛋白序列间同源关系进行比较,构建系统发育树。
2 结果与分析
2.1 高温胁迫下紫花苜蓿PEPC酶活性变化
两种紫花苜蓿PEPC酶活性变化随胁迫时间的延长都呈现出先上升后下降、再上升再下降、复水后上升的趋势(图1),在胁迫第12 h达到峰值,且显著高于其他处理(P<0.05),此时野生紫花苜蓿的PEPC酶活性是胁迫前的14.3倍,‘阿尔冈金’紫花苜蓿是胁迫前的9.2倍;两种紫花苜蓿PEPC酶活性在复水后均显著高于胁迫结束时(P<0.05)。野生紫花苜蓿PEPC酶活性在胁迫第16 h、4 d和复水后极显著高于相同条件下的‘阿尔冈金’紫花苜蓿(P<0.01),在胁迫第12 h和24 h显著高于‘阿尔冈金’紫花苜蓿(P<0.05),其他条件下两种紫花苜蓿PEPC酶活性之间均无显著差异。
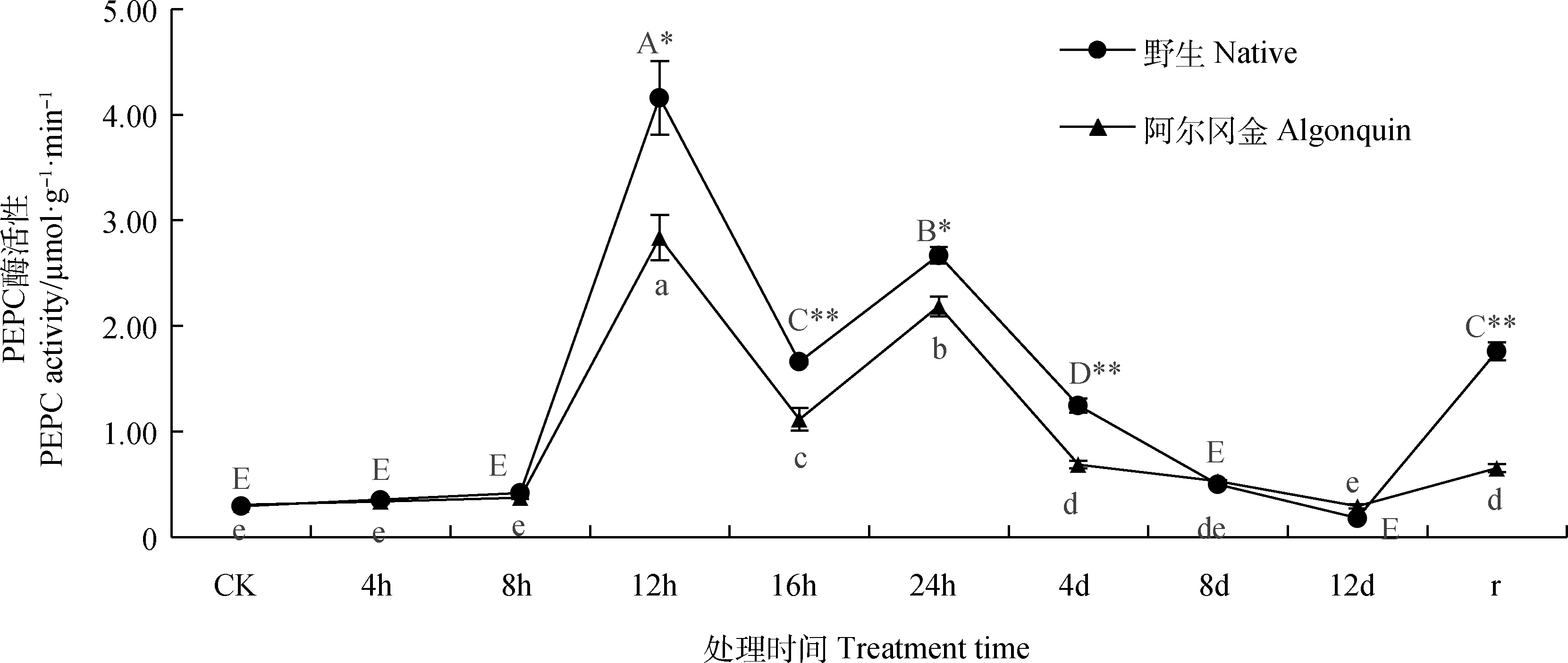
图1 高温胁迫下紫花苜蓿PEPC酶活性变化Fig.1 Changes of PEPC activity in Alfalfa under high temperature stress注:大写字母表示野生紫花苜蓿各项处理间的差异显著性(P<0.05),小写字母表示‘阿尔冈金’紫花苜蓿各项处理间的差异显著性(P<0.05);*和**分别表示在相同条件下不同材料之间在0.05和0.01水平存在显著性差异,下同Note:Lowercase letters indicated the significant difference between the treatments of Medicago stativa ‘Algonquin’ and wild alfalfa (P<0.05),uppercase letters indicated the significant difference between the treatments of Medicago stativa ‘Algonquin’ alfalfa(P<0.05). * and ** indicate significant differences between tested materials under same treatment time at the 0.05 and 0.01 level,respectively,the same as below
2.2 干旱胁迫下紫花苜蓿PEPC酶活性变化
野生紫花苜蓿PEPC酶活性变化随胁迫时间的延长呈现先上升、后下降、复水后上升的趋势,而‘阿尔冈金’紫花苜蓿呈现先上升后下降、再上升再下降、复水后上升的趋势(图2);两种紫花苜蓿均在在胁迫第12 h达到峰值,且显著高于其他处理(P<0.05),此时野生紫花苜蓿的PEPC酶活性是胁迫前的14.8倍,‘阿尔冈金’紫花苜蓿是胁迫前的12.7倍;两种紫花苜蓿PEPC酶活性在复水后均显著高于胁迫结束时(P<0.05)。野生紫花苜蓿PEPC酶活性在胁迫第16 h,8 d,12 d和复水后极显著高于相同条件下的‘阿尔冈金’紫花苜蓿(P<0.01),在胁迫第8 h和12 h显著高于‘阿尔冈金’紫花苜蓿(P<0.05),其他条件下两种紫花苜蓿PEPC酶活性之间均无显著差异。
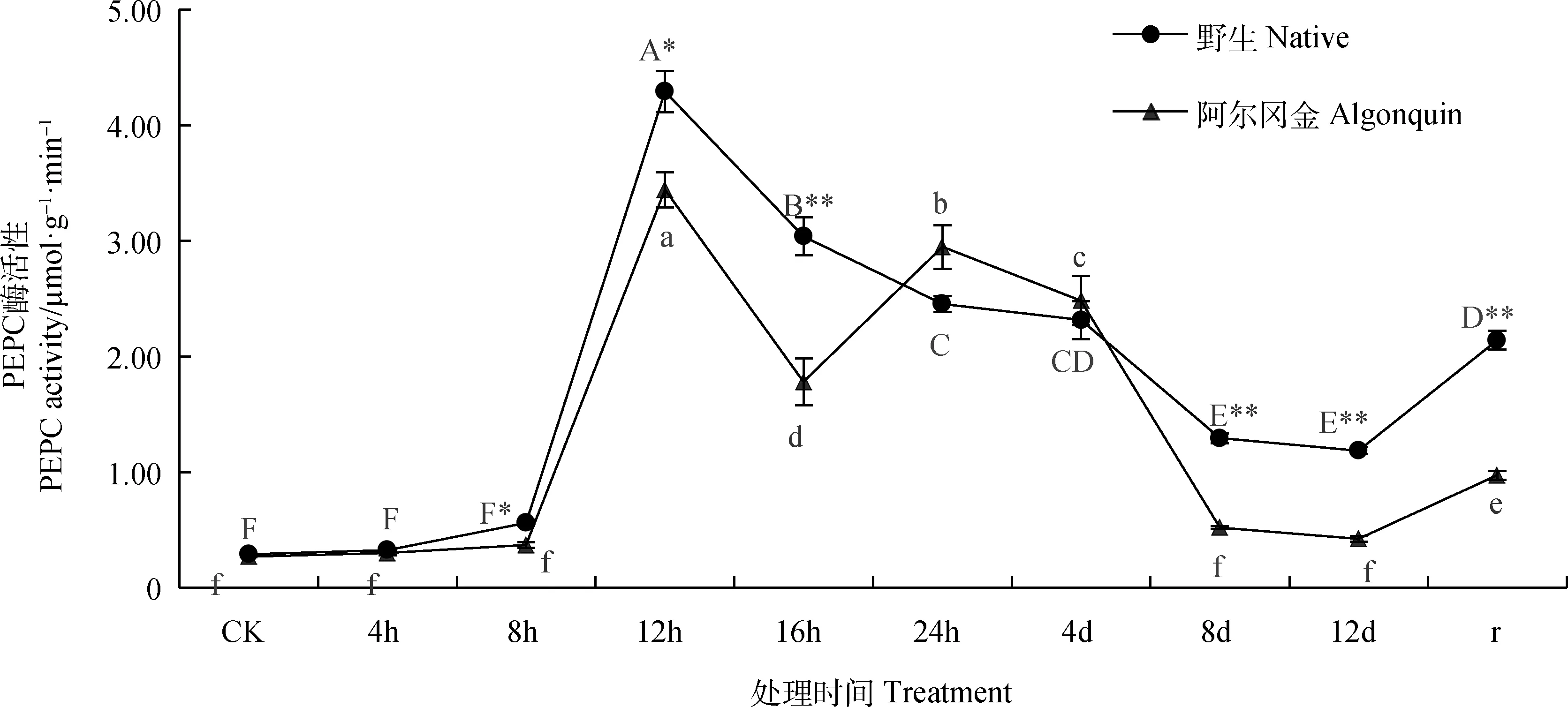
图2 干旱胁迫下紫花苜蓿PEPC酶活性变化Fig.2 Changes of PEPC activity in Alfalfa under drought stress
2.3 紫花苜蓿PEPC基因PCR扩增结果
两种紫花苜蓿PEPC基因PCR扩增产物电泳检测(图3)均得到一条清晰明亮的条带。野生紫花苜蓿和‘阿尔冈金’紫花苜蓿扩增序列长度分别为739 bp和750 bp,且两份材料的序列均与Genbank中紫花苜蓿PEPC基因序列(M83086.1)相似率为100%,与蒺藜苜蓿PEPC基因序列(XM_003596337.4)相似率为99%。结果表明,获得的两份紫花苜蓿材料的目的片段均属于PEPC基因家族。
2.4 紫花苜蓿PEPC蛋白理化性质
表1可以看出,野生紫花苜蓿和‘阿尔冈金’紫花苜蓿的分子量分别为25.886和26.501 KDa,氨基酸总数分别为228和233 aa;理论等电点均大于7,为带正电荷蛋白;蛋白质不稳定指数均大于4,均属于不稳定蛋白;亲水性平均系数均为负数,预测均为亲水性蛋白。
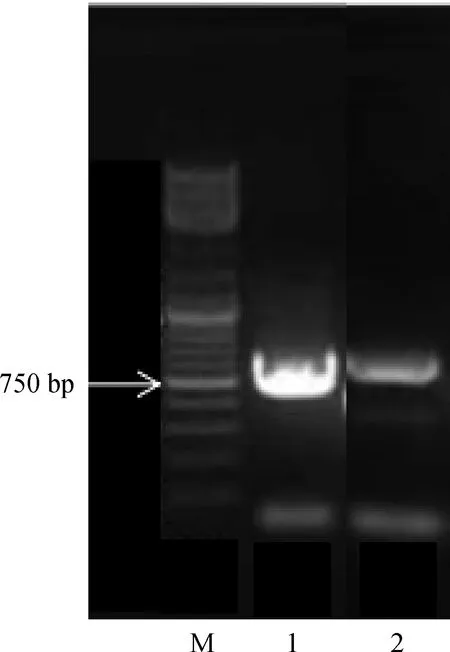
图3 两种紫花苜蓿PEPC基因PCR电泳图Fig.3 PCR electrophoresis of PEPC gene in two alfalfa species注:1,‘阿尔冈金’紫花苜蓿;2,野生紫花苜蓿Note:1, Medicqgo stativa‘ Algonquin’;2,Native Medicago stativa
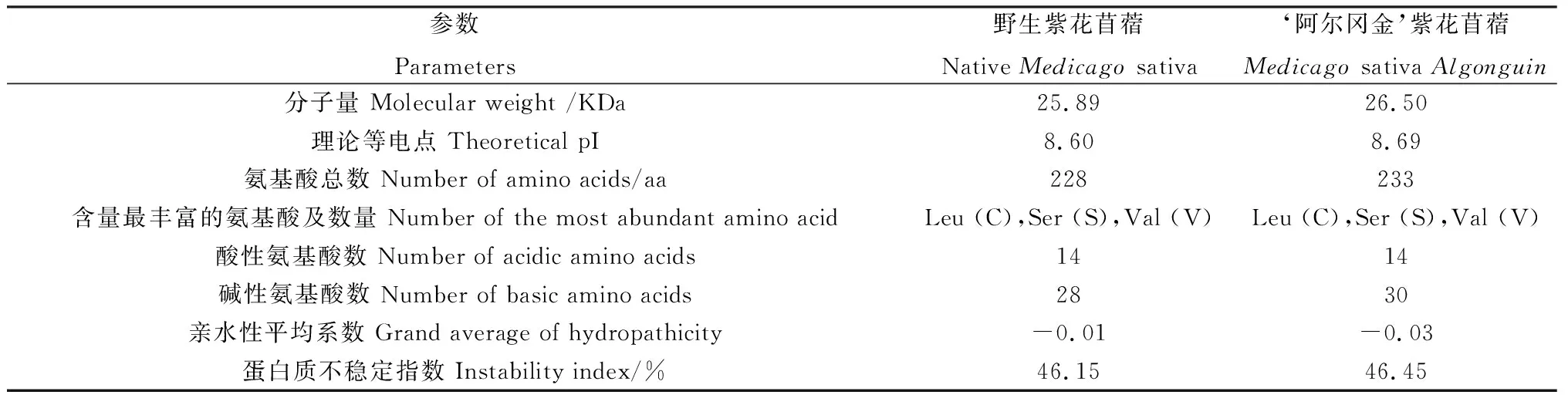
表1 两种紫花苜蓿PEPC蛋白理化性质Tab 1 Physicochemical properties of PEPC proteins in two alfalfa species
2.5 紫花苜蓿PEPC基因遗传距离分析
紫花苜蓿PEPC蛋白同源性分析结果显示(表2),野生紫花苜蓿和蒺藜苜蓿与紫花苜蓿之间,以及紫花苜蓿和蒺藜苜蓿之间同源性较高,均为1;‘阿尔冈金’紫花苜蓿与野生紫花苜蓿、紫花苜蓿和蒺藜苜蓿之间一致性均大于0.9;菜豆与其他5个近缘种间相似性较低,均小于0.5。
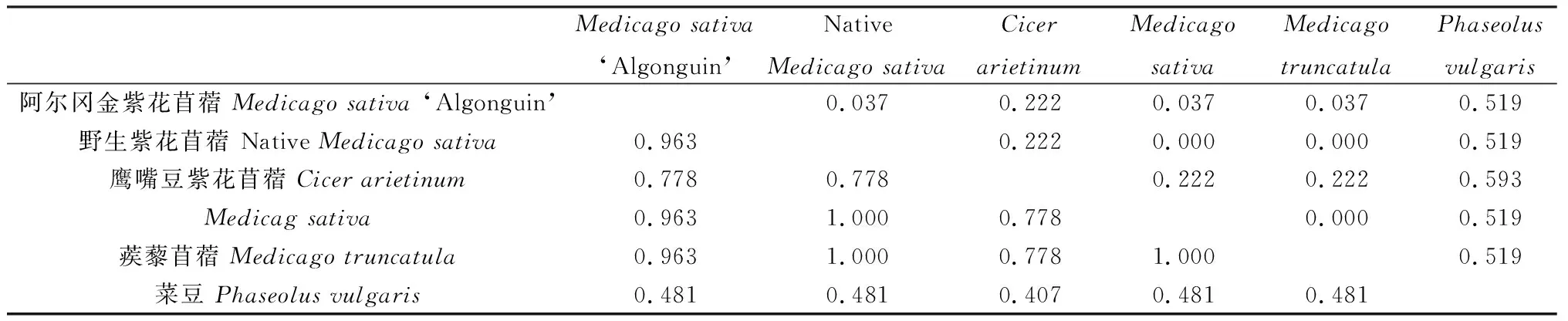
表2 紫花苜蓿6个近缘种间PEPC蛋白同源性分析Tab 2 Homology of PEPC proteins sequences among 6 related species of alfalfa
2.6 紫花苜蓿PEPC基因系统发育分析
对野生紫花苜蓿、‘阿尔冈金’紫花苜蓿及4个PEPC基因近缘种间转录蛋白同源关系进行比较,结果显示(图4):野生紫花苜蓿、紫花苜蓿和蒺藜苜蓿以100%的支持率聚为一组,这一组与‘阿尔冈金’紫花苜蓿聚为一支,支持率为96%;四种苜蓿与鹰嘴豆的同源关系为78%,而与菜豆同源关系最远,其关系距离为47%。
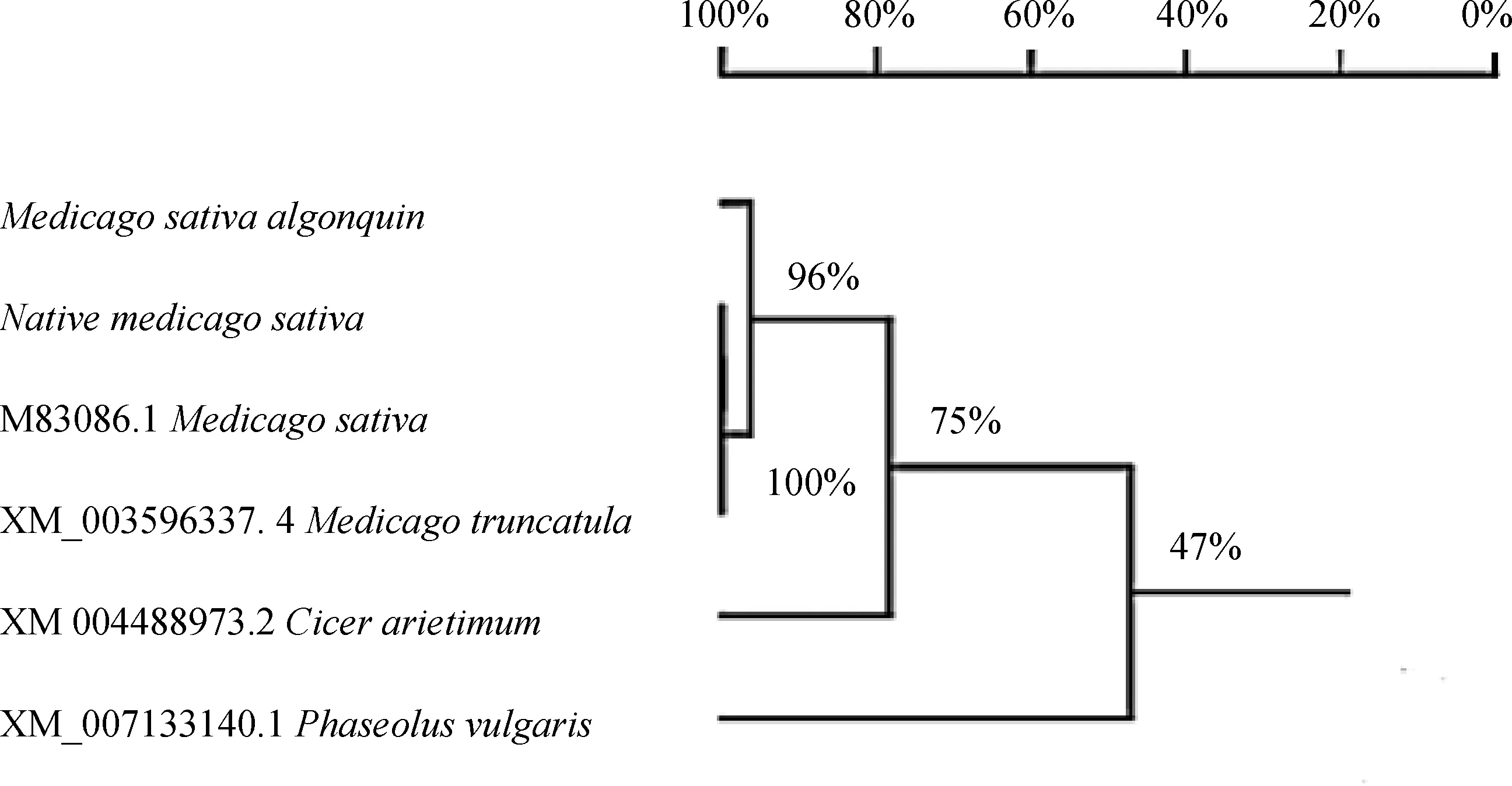
图4 紫花苜蓿6个近缘种的PEPC蛋白同源关系树Fig.4 PEPC proteins sequence homology tree of 6 related species of Alfalfa
3 讨论
PEPC酶不同程度地增强了植物抵御和适应外界胁迫的能力,帮助植物适应生物胁迫和非生物胁迫,同时,植物的PEPC酶活性在外界胁迫下可增强[25-27]。本研究中,两种紫花苜蓿PEPC酶活性随着胁迫时间的延长,大致呈先增加后降低的趋势,当植物感应到胁迫时,会启动胁迫应激机制来抵御和适应外来影响[28]。两种胁迫条件下,两种紫花苜蓿均在胁迫第12 h出现峰值,可能是此时达到了紫花苜蓿自我调节所能承受的极限,PEPC酶活性在此之后则表现出下降的趋势,当受胁迫的紫花苜蓿未到死亡极限时给予复水,紫花苜蓿植株受到的胁迫减轻并脱离胁迫临界点后,PEPC酶活性又开始增强以便应对胁迫。在相同处理条件下,‘阿尔冈金’紫花苜蓿的PEPC酶活性基本上都低于野生紫花苜蓿,可能因为野生紫花苜蓿原本就生长在干热河谷极端恶劣的自然环境中[29],已经适应了干热环境下形成的特殊自我保护机制。两种胁迫条件下在复水前均可观察到一个滞缓期,表明紫花苜蓿PEPC酶对植株复水的反应是一个长期反应,这可能与基因表达强度的减弱有关[30]。两种紫花苜蓿PEPC酶活性在复水后可完全恢复到胁迫前的水平,甚至高于胁迫前的水平,这说明植物PEPC酶对植物的作用是一个可逆过程,这与雷明月等[31]的研究结果一致。
本试验获得的野生紫花苜蓿和‘阿尔冈金’紫花苜蓿的PEPC核酸序列长度分别为739和750 bp,分别编码228和233个氨基酸,在氨基酸序列比对中,两种不同紫花苜蓿PEPC基因氨基酸序列极度保守,具有高度的一致性,这与赵晋锋等[32]的研究结果一致。两种紫花苜蓿PEPC蛋白的分子量、等电点、亲水系数和蛋白质不稳定系数等理化性质比较稳定,与在水稻[33]、大豆[34]和油菜(BrassicanapusL.)[35]等植物上的研究结论相似。
两个紫花苜蓿材料与4个近缘种间PEPC蛋白同源性分析中,野生紫花苜蓿与蒺藜苜蓿和紫花苜蓿之间,以及紫花苜蓿与蒺藜苜蓿之间同源性均为1,相似性较高,说明其氨基酸结构差异比较小;菜豆与其他5个近缘种间差异性较大,相似性均小于0.5,说明他们之间亲缘关系较远。将两个紫花苜蓿材料联合4个近缘种的PEPC蛋白进行系统进化分析,野生紫花苜蓿、紫花苜蓿和蒺藜苜蓿以100%的支持率聚为一组,但不能单纯从它们的序列相似性来推测其PEPC基因具有相似功能,还需要考虑其启动子顺式作用元件和非编码区的差异[36]。而‘阿尔冈金’紫花苜蓿可能适应了相对独立的环境条件,导致其PEPC蛋白发生改变,从而其蛋白活性及功能也随之发生改变。四种苜蓿与鹰嘴豆和菜豆的同源关系均较远,表明PEPC在进化过程中既保留了较强的保守性,又在不同种属间产生了差异[37]。
4 结论
干旱胁迫与干热胁迫都对紫花苜蓿光合酶PEPC活性产生了较大的影响,其中,两种胁迫下野生紫花苜蓿的酶活性基本高于‘阿尔冈金’紫花苜蓿,两种紫花苜蓿PEPC蛋白均为不稳定蛋白和亲水性蛋白,且氨基酸序列保守性较高。

