土一枝蒿药材指纹图谱和含量测定研究*
金倩倩,刘理燕,汪 洋,蒋良梦,孙 佳,郑 林,王永林,△
(1.贵州医科大学民族药与中药开发应用教育部工程研究中心·省部共建药用植物功效与利用国家重点实验室,贵州 贵阳 550004;2.贵州医科大学药学院,贵州 贵阳 550004;3.贵州医科大学贵州省药物制剂重点实验室,贵州 贵阳 550004)
土一枝蒿为菊科植物云南蓍Achillea wilsonianaHeimerl ex Hand.-Mazz.新鲜或干燥的地上部分,又名飞天蜈蚣、野一枝蒿等,主要产于云南、四川、贵州等地,具有解毒利湿、活血止痛等功效,可用于头风痛、牙痛、风湿痹痛、血瘀经闭、腹部痞块、跌扑损伤、蛇虫咬伤、痈肿疮毒等的治疗[1-3]。土一枝蒿是贵州省少数民族用药,收载于《贵州省中药材、民族药材质量标准》(2003年版),其中仅对其性状及显微特征进行了规定[4],相关文献也较缺乏。因此,本研究中参照2020年版《中国药典(四部)》对土一枝蒿药材水分、总灰分、水溶性浸出物进行含量测定,并通过高效液相色谱(HPLC)法对不同产地和批次的土一枝蒿药材进行指纹图谱研究及3种主要成分的含量测定,以期为其质量标准研究提供参考。现报道如下。
1 仪器与试药
1.1 仪器
Ultimate3000型高效液相色谱仪(美国Thermo Fisher Scientific公司),包括Chromeleon色谱数据工作站、系统控制器、柱温箱、低压梯度组件、输液泵、脱气组件、样品室、自动进样器、UV-DAD检测器;AE240型十万分之一电子天平(瑞士Mettler Toledo公司);KQ5200E型超声波清洗器(昆山市超声仪器有限公司)。
1.2 试药
异荭草素对照品、异牡荆苷对照品、槲皮素-4'-O-β-D-葡萄糖苷对照品(均为从土一枝蒿药材中提取分离制备所得,含量均大于98.0%);乙腈为色谱纯;其余试剂为分析纯;水为超纯水。土一枝蒿药材12批(来源及批号见表1),经贵州中医药大学药学院生药实验室孙庆文教授鉴定为菊科蓍属植物土一枝蒿的干燥全草。
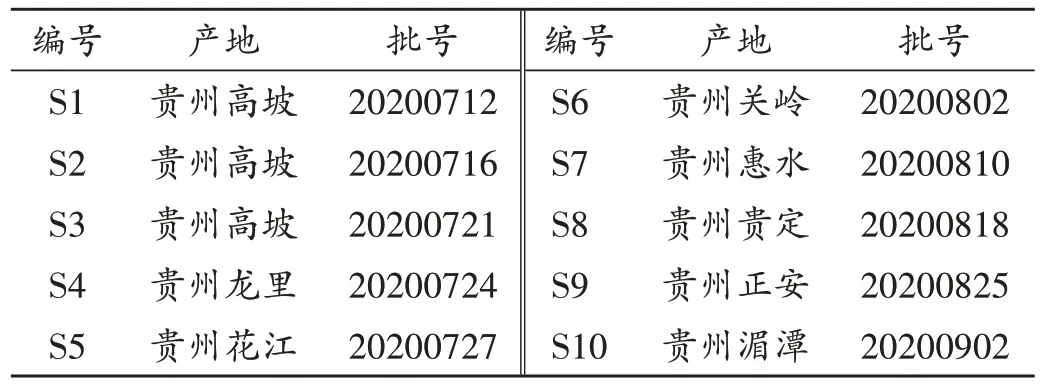
表1 药材样品来源Tab.1 Source information of Achillea wilsoniana samples
2 方法与结果
2.1 水分、灰分、浸出物含量测定
参照2020年版《中国药典(四部)》通则0832水分测定法中的第二法(烘干法)、通则2302灰分测定法和通则2201项下水溶性浸出物测定法进行相应含量测定。结果见表2。
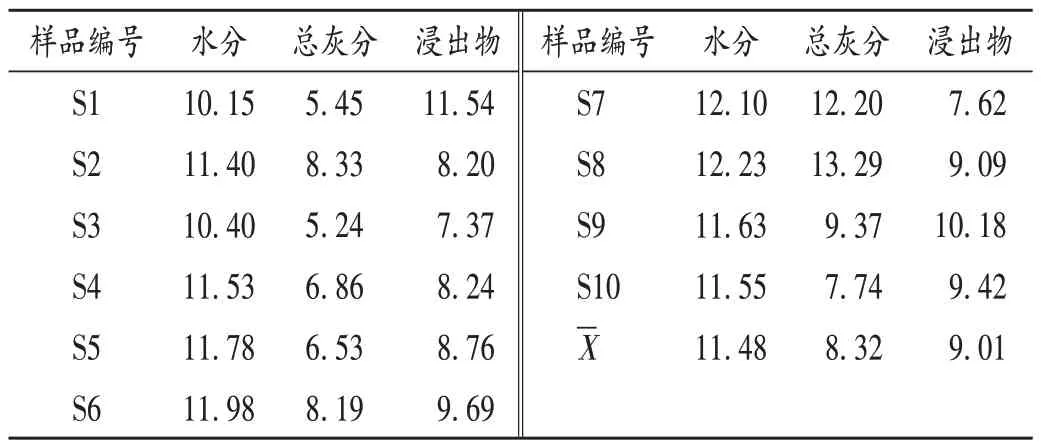
表2 药材样品水分、总灰分、水溶性浸出物含量测定结果(%,n=2)Tab.2 Results of content determination of moisture,total ash and water-soluble extract of Achillea wilsoniana samples(%,n=2)
2.2 HPLC指纹图谱的建立与分析
2.2.1 色谱条件
色谱柱:CAPCELLPAKC18MGⅡ(S-5)柱(250 mm×4.6 mm,5μm);流动相:乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱(0~45 min时13%A,45~46 min时13%A→14%A,46~76 min时14%A,76~77 min时14%A→15%A,77~107min时15%A→20%A,107~113min时20%A→65%A);流速:0.7 mL/min;检测波长:365 nm;柱温:30℃;进样量:10μL。
2.2.2 溶液制备
取异荭草素、异牡荆苷、槲皮素-4'-O-β-D-葡萄糖苷对照品各适量,精密称定,用甲醇溶解制成质量浓度分别为1.101,1.580,1.346 mg/mL的单一对照品贮备液;分别精密量取12.5,5,5 mL,置同一25 mL容量瓶中,加甲醇定容,摇匀,即得质量浓度分别为0.550 5,0.316 0,0.269 2 mg/mL的混合对照品溶液。取药材样品粉末1.0 g,过3号筛,精密称定,置50 mL具塞三角瓶中,精密加入70%甲醇20 mL,称定质量,超声(功率200 W,频率40 kHz)处理15 min,放冷至室温,再次称定质量,加70%甲醇补足减失的质量,摇匀,静置,取上层液,12 000 r/min离心10 min,取上清液,即得供试品溶液。以甲醇为空白对照溶液。
2.2.3 方法学考察
精密度试验:取药材样品(编号S1)适量,按2.2.2项下方法制备供试品溶液,按2.2.1项下色谱条件连续进样测定6次,以异红草素峰(5号峰)为参照峰,计算14个共有峰的相对保留时间和相对峰面积,结果的RSD分别小于0.50%,3.00%(n=6),表明方法精密度良好。
稳定性试验:取2.2.2项下供试品溶液(编号S1),分别于室温下放置0,4,8,18,20,24 h时按2.2.1项下色谱条件进样测定,以异红草素峰(5号峰)为参照峰,计算14个共有峰的相对保留时间和相对峰面积,结果的RSD分别小于0.50%,3.00%(n=6),表明供试品溶液在室温放置24 h内基本稳定。
重复性试验:取药材样品(编号S1)适量,按2.2.2项下方法制备供试品溶液,平行6份,按2.2.1项下色谱条件进样测定,以异红草素峰(5号峰)为参照峰,计算14个共有峰的相对保留时间和相对峰面积,结果的RSD分别小于1.00%,2.00%(n=6),表明方法重复性良好。
2.2.4 指纹图谱建立与相似度评价
指纹图谱建立:取10批药材样品各适量,按2.2.2项下方法制备供试品溶液,按2.1项下色谱条件进样测定,将10批药材样品的HPLC数据导入中药色谱指纹图谱相似度评价系统(2012年130723版),利用中位数法进行多点校正,生成10批药材样品的HPLC叠加指纹图谱(图1)及共有模式的对照指纹图谱(图2),共确定了14个共有峰。通过与混合对照品溶液图谱(图3)比对,确认5号峰为异荭草素,10号峰为异牡荆苷,12号峰为槲皮素-4'-O-β-D-葡萄糖苷。
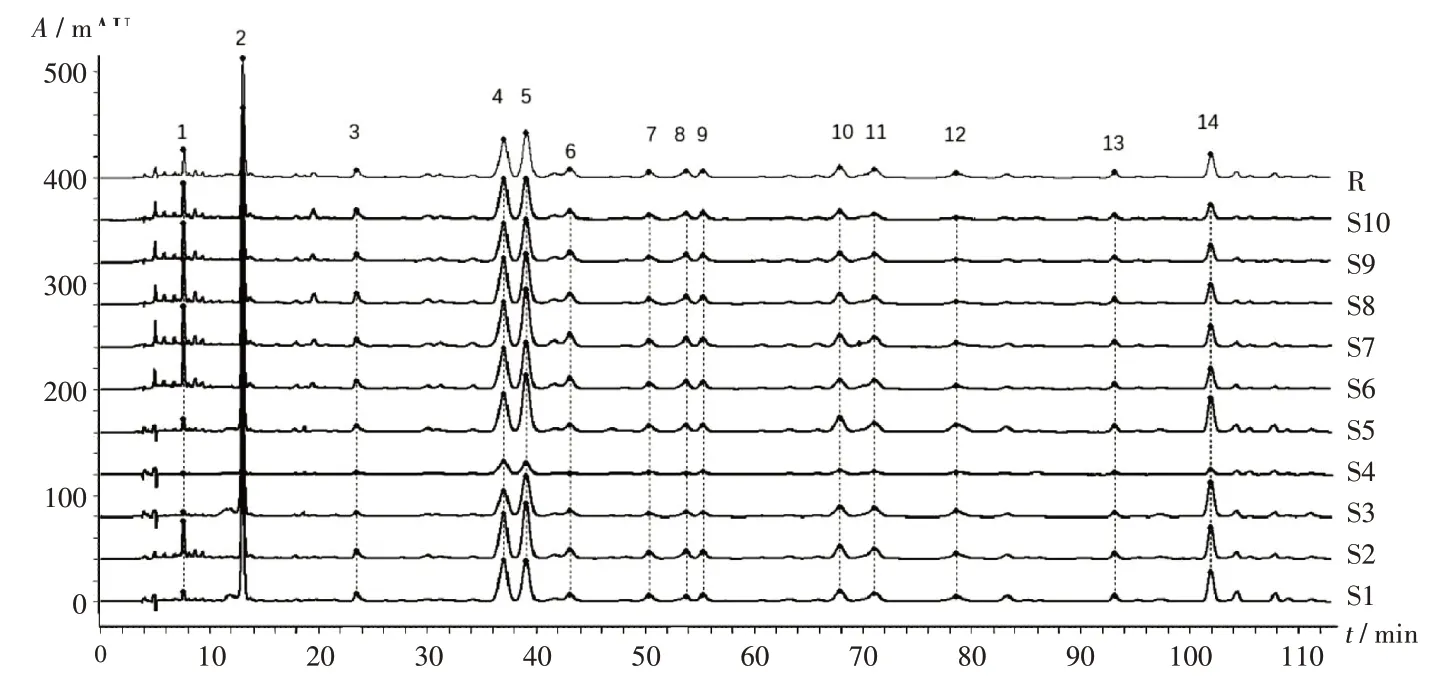
图1 10批药材样品高效液相色谱叠加指纹图谱Fig.1 Superimposed HPLC fingerprints of 10 batches of Achillea wilsoniana samples
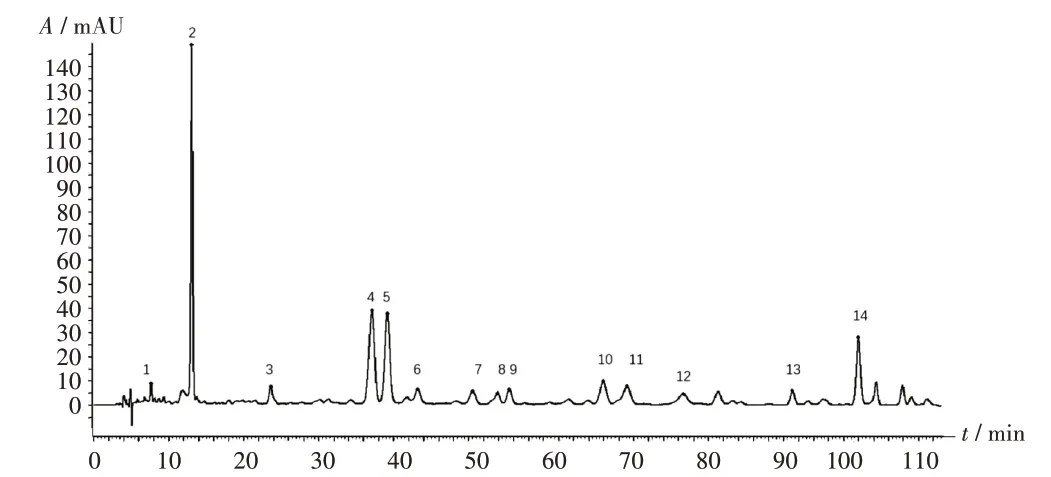
图2 高效液相色谱对照指纹图谱Fig.2 HPLC reference fingerprint
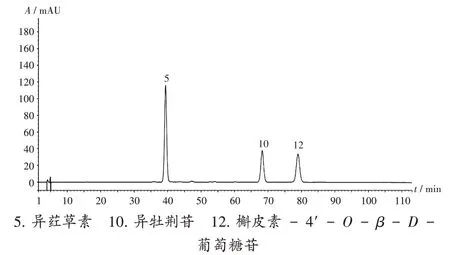
图3 混合对照品溶液高效液相色谱图5.Isoorientin 10.Isovitexin 12.Quercetin-4'-O-β-D-glucosideFig.3 HPLC chromatogram of mixed reference solution
相似度评价:以共有模式为对照图谱,采用中药色谱指纹图谱相似度评价系统(2012年130723版)计算10批样品的相似度。结果S1~S10药材样品相似度依次为0.987,0.997,0.957,0.986,0.941,0.995,0.987,0.995,0.993,0.988,表明不同产地、不同批次样品的相似度较好。
2.3 含量测定
2.3.1 方法学考察
系统适用性试验:取2.2.2项下混合对照品溶液、供试品溶液、空白对照溶液适量,按2.2.1项下色谱条件进样测定,记录色谱图。结果供试品溶液中异荭草素、异牡荆苷、槲皮素-4'-O-β-D-葡萄糖苷色谱峰保留时间与对照品色谱峰一致,各成分分离度均大于1.5,理论板数均大于15 000,且空白对照无干扰。详见图4。
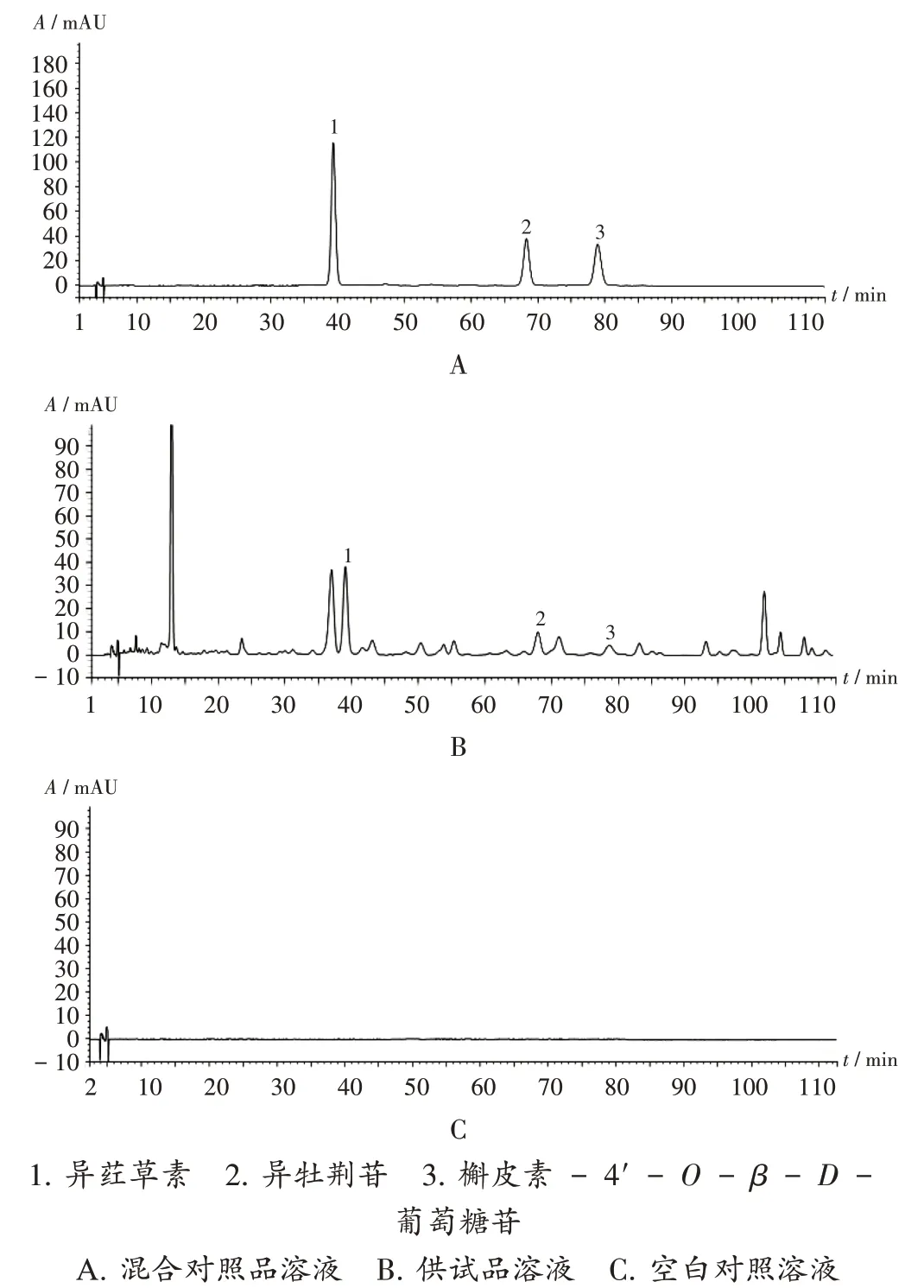
图4 高效液相色谱图1.Isoorientin 2.Isovitexin 3.Quercetin-4'-O-β-D-glucoside A.Mixed reference solution B.Test solution C.Blank control solutionFig.4 HPLC chromatograms
线性关系考察:精密量取2.2.2项下混合对照品溶液适量,逐级稀释成不同质量浓度的系列混合对照品溶液,按2.2.1项下色谱条件进样测定,记录峰面积,以待测成分质量浓度(X,mg/mL)为横坐标、峰面积(Y)为纵坐标进行线性回归,得回归方程,异荭草素为Y1=402.56X1+0.230 5(r=0.999 9)、异牡荆苷为Y2=303.68X2+1.314 5(r=0.999 5)、槲皮素-4'-O-β-D-葡萄糖苷为Y3=309.48X3+0.102 0(r=0.999 8)。结果表明,异荭草素、异牡荆苷、槲皮素-4'-O-β-D-葡萄糖苷质量浓度分别在12.55~200.82μg/mL、7.20~115.28μg/mL、6.14~98.20μg/mL范围内与峰面积线性关系良好。
精密度试验:取样品(编号S1)适量,按2.2.2项下方法制备供试品溶液,按2.2.1项下色谱条件连续进样测定6次,记录峰面积。结果异荭草素、异牡荆苷、槲皮素-4'-O-β-D-葡萄糖苷峰面积的RSD分别为0.82%,0.81%,2.12%(n=6),表明方法精密度良好。
稳定性试验:取2.2.2项下供试品溶液(编号S1),分别于室温下放置0,4,8,18,20,24 h时按2.2.1项下色谱条件进样测定,记录峰面积。结果异荭草素、异牡荆苷、槲皮素-4'-O-β-D-葡萄糖苷峰面积的RSD分别为0.54%,0.67%,2.05%(n=6),表明供试品溶液在室温放置24 h内基本稳定。
重复性试验:取药材样品(编号S1)适量,按2.2.2项下方法制备供试品溶液,平行6份,按2.2.1项下色谱条件进样测定,记录峰面积。结果异荭草素、异牡荆苷、槲皮素-4'-O-β-D-葡萄糖苷峰面积的RSD分别为1.78%,1.95%,2.24%(n=6),表明方法重复性良好。
加样回收试验:取已知含量药材样品粉末(编号S1)约0.5 g,精密称定,各6份,分别加入异荭草素、异牡荆苷、槲皮素-4'-O-β-D-葡萄糖苷对照品0.741 5,0.254 3,0.182 5 mg,按2.2.2项下方法制备供试品溶液,按2.2.1项下色谱条件进样测定,记录峰面积并计算加样回收率。结果见表3。
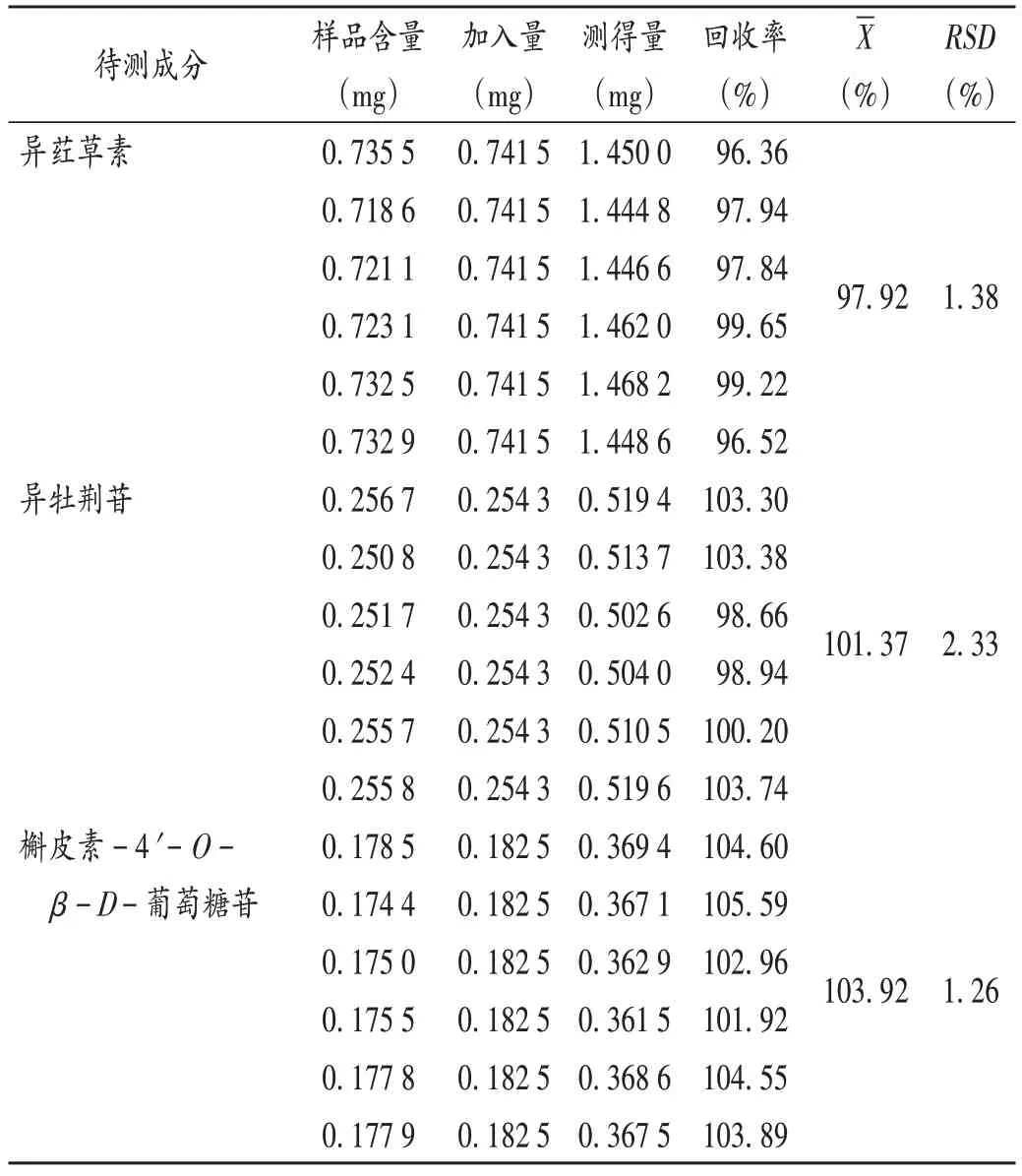
表3 加样回收试验结果(n=6)Tab.3 Results of the recovery test(n=6)
2.3.2 药材样品含量测定
取各批药材样品粉末约1.0g,精密称定,按2.2.2项下方法制备供试品溶液,按2.2.1项下色谱条件进样测定,记录峰面积并按标准曲线法计算样品中3种待测成分含量。结果见表4。
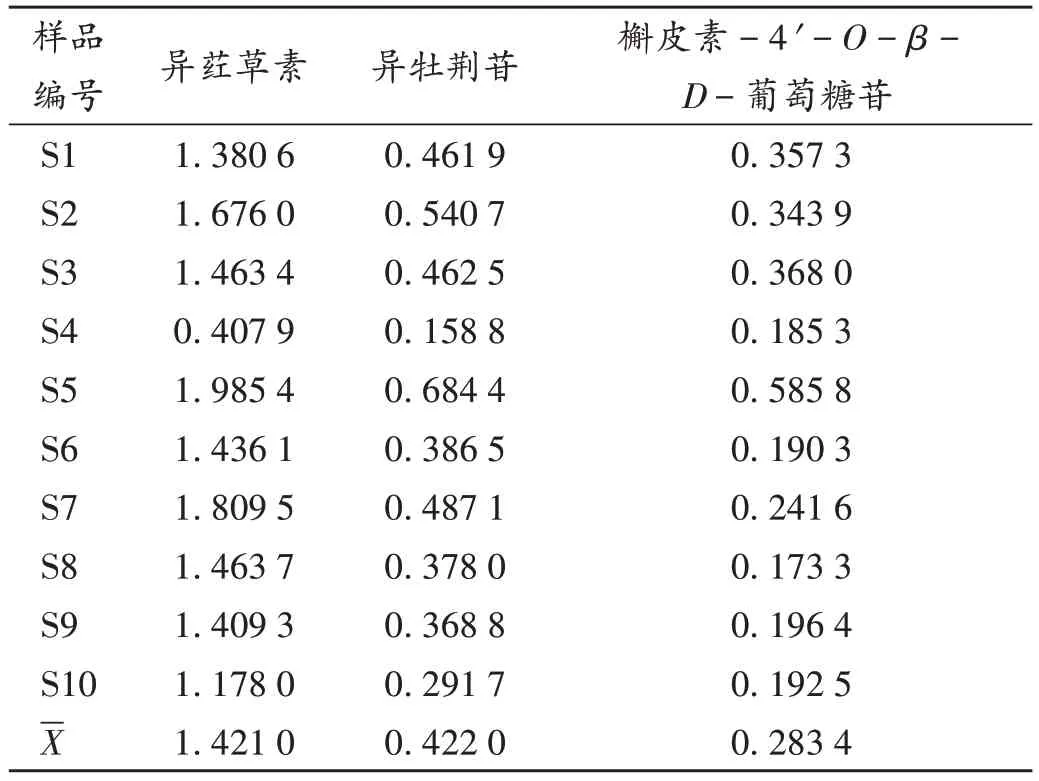
表4 药材样品含量测定结果(mg/g,n=2)Tab.4 Results of the content determination of three components in 10 batches of Achillea wilsoniana samples(mg/g,n=2)
3 讨论
3.1 样品提取方法选择
预试验中分别考察了提取溶剂(30%甲醇、70%甲醇、甲醇、30%乙醇、70%乙醇、乙醇、水)、提取时间(15,30,45 min)、提取方式(超声、回流)对提取效果的影响,在考虑供试品制备方法的高效、简单、方便操作等因素前提下最终确定,提取溶剂为70%甲醇、超声处理15 min为最佳提取方法。
3.2 色谱条件优化
预试验中对不同检测波长进行了考察,发现各待测成分在330,350,365 nm波长处有较大吸收,但在330,350 nm波长处有杂质峰干扰,且基线分离效果不如365 nm,故最终选择365 nm为检测波长;比较了不同色谱柱的分离效果,发现MGⅡC18柱(250 mm×4.6 mm,5μm)具有较高柱效,能较好地分离待测成分与杂质峰;流动相考察了乙腈-0.1%磷酸溶液、甲醇-0.1%磷酸溶液、甲醇-水、乙腈-水,发现以乙腈-0.1%磷酸溶液为流动相时,各色谱峰的峰形及分离度较好;还考察了不同柱温(30℃、35℃、40℃)及流速(0.7,0.8,1.0 mL/min),发现30℃为分析检测的最佳柱温,流速为0.7 mL/min时色谱峰分离效果优于0.8 mL/min及1.0 mL/min,故可确定最佳色谱条件。
3.3 结果分析
有文献报道,土一枝蒿药材中主要含有萜烯类,生物碱类等化学成分,具有抗炎、解热、镇痛、抗菌、血管保护等药用价值[5-13]。国内外文献尚未见其质量控制相关研究报道,在《贵州省中药材、民族药材质量标准》(2003年版)中仅以土一枝蒿药材的性状及显微鉴别作为质量控制指标,不能全面控制药材的质量。因此,本试验中对土一枝蒿药材进行了指纹图谱及含量测定的研究,结果表明,10批不同产地和不同批次土一枝蒿药材相似度均大于0.940,说明贵州省内各产地的药材质量均一性较高。水分与浸出物含量相对总灰分含量而言差异较小,范围较宽,说明贵州省不同产地的土一枝蒿药材中无机成分、杂质、泥沙含量差异较大。不同产地的样品含量存在差异,其中S4样品中异荭草素、异牡荆苷、槲皮素-4'-O-β-D-葡萄糖苷含量较低,S5样品含量较高,除这两批药材外,其余8批土一枝蒿药材中3种成分含量较均衡。由以上结果可知,药材成分含量差异与产地的差异有一定相关性。
综上所述,本研究中建立的HPLC指纹图谱及含量测定的方法简单,准确可靠,样品的收集具有一定代表性,可为土一枝蒿药材的质量控制提供参考。

