失眠认知行为治疗在脑卒中睡眠障碍患者中应用效果分析
黄清明
脑卒中是目前临床十分常见的脑血管意外,主要包括出血性脑卒中和缺血性脑卒中两种,前者即脑出血,后者即脑梗死,与脑出血相比,脑梗死的患病率相对更高[1]。目前认为脑梗死可导致患者大脑神经功能受损,由此会引发一系列肢体、感觉、认知障碍,睡眠障碍则是此类患者发病后的常见并发症之一。此并发症发生考虑与患者生理、心理等多种因素相关[2-3]。与睡眠节律相关的5- 羟色胺(5-HT)、多巴胺(DA)、褪黑素(MLT)等分泌紊乱为其重要发病机制[4]。因此针对此类患者,临床常会在实施积极对症治疗后予以服用相应药物,以改善其神经递质分泌情况[5]。但有学者表示[6],除上述客观性致病因素外,脑卒中睡眠障碍发病还与患者个人心理、认知等主观性因素相关,予以药物干预可一定程度改善患者的神经递质水平,但无法提升患者的治疗依从性,在临床实践中治疗效果并不理想。失眠认知行为治疗为一种用于治疗睡眠障碍的非药物疗法,通过对患者实施积极健康宣教及心理干预,可很大程度上纠正其错误认知,对改变患者睡眠习惯、养成规律作息均有积极意义[7]。本研究主要探讨失眠认知行为治疗在脑卒中睡眠障碍患者中的应用效果。
1 资料与方法
1.1 一般资料 回顾性分析选取2021年3月至2022年3月期间至武陟济民医院接受治疗的260例脑卒中睡眠障碍患者为研究对象,采用抽签法将患者分为药物组和联合组,每组130例,药物组中男70 例(53.85%),女60 例(46.15%),年 龄50 ~80岁,平均年龄(65.25±0.31)岁,脑卒中位置:脑干86例(66.15%)、基底节区44例(33.85%),失眠病程20~50 d,平均病程(35.22±0.14)d;联合组中男73例(56.15%),女57例(43.85%),年龄52~78岁,平均年龄(65.217±0.25)岁,脑卒中位置:脑干90例(69.23%)、基 底 节 区40 例(30.77%),失 眠 病 程23~47 d,平均病程(35.36±0.25)d,两组患者一般资料差异无统计学意义(P>0.05),可对比,本次研究已经获得医院伦理委员会批准 (批准号:20121)。
1.2 选取标准 纳入标准:入组患者均符合《中国急性缺血性脑卒中诊治指南2018》[8]中脑卒中诊断标准;经影像学检查均确认存在缺血性脑卒中病灶;发病后均存在不同程度睡眠障碍,失眠病程均在20 d以上;病情处于稳定期、意识清醒可顺利配合研究;入组患者均已知悉此次研究目的和内容,均已在相关同意书签字确认。排除标准:经临床诊断为脑出血者[9];伴其他病理性精神、认知障碍疾病者;病情处于急性发作期者;已知对本研究所用药物存在过敏史者;依从性差不愿配合此次研究者。
1.3 方法 两组患者均统一接受常规治疗+药物干预,联合组联合应用失眠认知行为治疗,均持续治疗8周后评估疗效。
常规治疗如下:首先结合患者临床症状予以对症处理,包括控制颅内压、调脂、降血压、降血糖等,同时密切关注患者病情变化,予以积极抗凝处理和营养支持治疗等。同时还需为患者构建良好的睡眠环境,将病房内空气温度控制在24~27 ℃,湿度控制在50%~60%,观察患者是否存在头痛、呕吐、尿频、咳嗽、呼吸困难等可影响睡眠的生理因素,若有异常则需对症干预;在患者夜间休息时需尽量关闭病房内不必要的医疗设备,避免造成噪声污染,尽量将诊疗、护理工作集中在日间患者清醒时开展,避免在其休息时实施其他临床干预等。
药物干预方案如下:在以上常规治疗基础上,予以两组服用艾司唑仑片进行治疗,1 mg/次,于每晚睡前30 min以温水送服即可。
失眠认知行为治疗如下:①了解睡眠障碍发生的主要原因,通过一对一与患者进行深入交流,鼓励患者说出内心真实感受,从患者个人叙述中了解失眠的真正原因,并针对失眠原因予以积极疏导;以亲和、通俗语言对患者进行健康宣教,告知患者不必过度担忧,放宽心接受诊疗,同时告知失眠可对其病情产生的不利影响,从主观上帮助患者纠正与睡眠障碍相关的错误认知,提升其治疗依从性。②指导患者每日养成填写睡眠日记的习惯,记录每日午睡时长、夜晚上床时间、入睡困难程度(由易到难对应1~3分)、关灯时间、夜间醒来次数、清晨觉醒时间、每次觉醒时情绪(由平静到不安、焦虑或烦躁对应1~5分)等相关信息。③结合睡眠日记情况,制定限制计划,日间巡房时可多与患者交流,为其设定午睡闹钟,将午睡时间控制在30 min以内,嘱其睡前3 h需避免剧烈运动,睡前2 h避免进食,日常饮食避免摄入含咖啡因等刺激性物质的食物,告知若躺下后20 min仍无困意则可离床,待有睡意再上床,睡眠避免过度活动大脑,不看可令大脑兴奋的书籍、视频,规定每晚上床时间及次日起床时间,帮助患者养成规律作息等。④睡前放松训练,可在睡前为其播放轻音乐,帮助舒缓心境;指导患者呼吸、肌肉放松,吸气后可屏气1~3 s后呼气,呼吸放松时可通过回想日间轻松经历分散注意力,同时嘱患者保持平卧,以此放松全身肌肉,使机体呈瘫软状态下配合呼吸放松和音乐放松助眠。
1.4 观察指标 ①睡眠质量:于治疗1、3、5、8周时采用匹兹堡睡眠质量指数(PSQI)[10]评估其睡眠质量,量表包括7个维度,均按0~3分计分,满分21分,分值越高表示睡眠质量越差。②神经递质:取患者外周静脉血为样本,统一经抗凝、离心处理后将血清样本送入Beckman Coulter 公司提供的AU5800型全自动生化分析仪中检测MLT、5-HT等神经递质水平。③心理状态:于治疗后采用焦虑自评量表(SAS)[11]、抑郁自评量表(SDS)[12]评估两组患者的心理状态改善情况,SAS满分80分,分值越高表示焦虑越严重,SDS满分80分,分值越高表示抑郁越严重。④脑神经功能:于治疗后采用改良Rakin量表(mRS)[13]、改良Barthel指数(MBI)[14]、美国国立卫生研究院卒中量表(NIHSS)评分[15]评估两组患者的脑神经功能改善情况,mRS满分7分,分值越高脑神经功能越差,MBI满分100分,分值越高脑神经功能越好,NIHSS评分满分42分,分值越高脑神经功能越差。⑤生活质量:于治疗后采用简明健康生活状态量表(SF-36)[16]评估两组患者的生活质量,量表含多个维度,本研究仅取生理机能(PF,10~30分)、生理职能(RP,4~8分)、情感职能(RE,3~6分)、精神健康(MH,5~10分)等4个维度进行评估。
1.5 统计学方法 研究数据均纳入SPSS 23.0统计学软件处理,计数资料均以率[n(%)]表示,采用χ2检验,计量资料均符合正态分布,故均以均数±标准差(±s)表示,采用t检验,当P<0.05时各组数据差异有统计学意义。
2 结果
2.1 两组患者治疗后的PSQI评分比较 在不同治疗方案下,联合组治疗1、3、5、8周后,联合组的PSQI评分均低于药物组,差异有高度统计学意义(P<0.001),见表1。
表1 两组患者治疗后的PSQI评分比较(±s) 单位:分
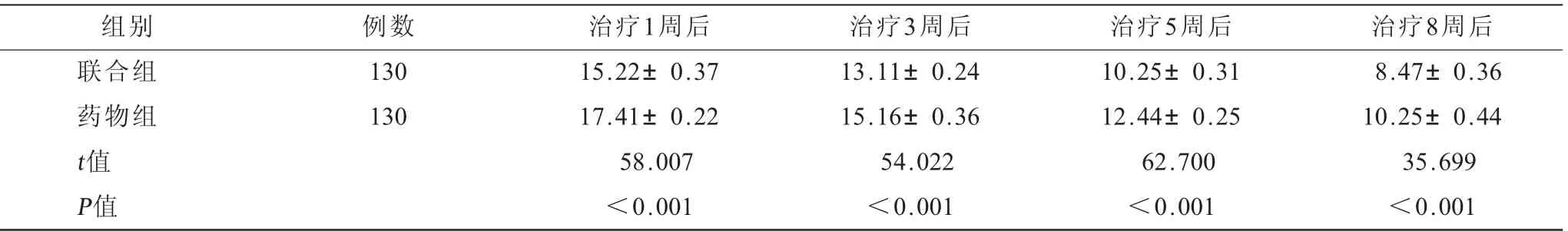
表1 两组患者治疗后的PSQI评分比较(±s) 单位:分
注:PSQI=匹兹堡睡眠质量指数。
组别 例数 治疗1周后 治疗3周后 治疗5周后 治疗8周后联合组 130 15.22±0.37 13.11±0.24 10.25±0.31 8.47±0.36药物组 130 17.41±0.22 15.16±0.36 12.44±0.25 10.25±0.44 t值 58.007 54.022 62.700 35.699 P值 <0.001 <0.001 <0.001 <0.001
2.2 两组患者治疗后的神经递质水平比较 治疗后,联合组的MLT、5-HT水平均高于药物组,DA水平低于药物组,差异有高度统计学意义(P<0.001),见表2。
表2 两组患者治疗后的神经递质水平比较(±s)

表2 两组患者治疗后的神经递质水平比较(±s)
注:MLT=褪黑素,DA=多巴胺,5-HT=5- 羟色胺。
组别 例数 MLT/(ng·L-1) DA/(mg·L-1) 5-HT/(ng·mL-1)联合组 130 62.33±1.46 366.45±5.47 145.32±5.36药物组 130 60.15±1.38 382.45±5.18 142.33±5.17 t值 12.372 24.216 4.578 P值 <0.001 <0.001 <0.001
2.3 两组患者治疗后的心理状态评分比较 治疗后,联合组的SAS、SDS评分均低于药物组,差异有高度统计学意义(P<0.001),见表3。
表3 两组患者治疗后的心理状态评分比较(±s) 单位:分

表3 两组患者治疗后的心理状态评分比较(±s) 单位:分
注:SAS=焦虑自评量表,SDS=抑郁自评量表。
组别 例数 SAS SDS联合组 130 25.11±0.27 25.23±0.41药物组 130 27.16±0.38 27.82±0.33 t值 50.141 56.109 P值 <0.001 <0.001
2.4 两组患者治疗后的脑神经功能评分比较
治疗后,联合组的mRS、NIHSS评分低于药物组,MBI 高于药物组,差异有高度统计学意义(P<0.001),见表4。
表4 两组患者治疗后的脑神经功能评分比较(±s) 单位:分
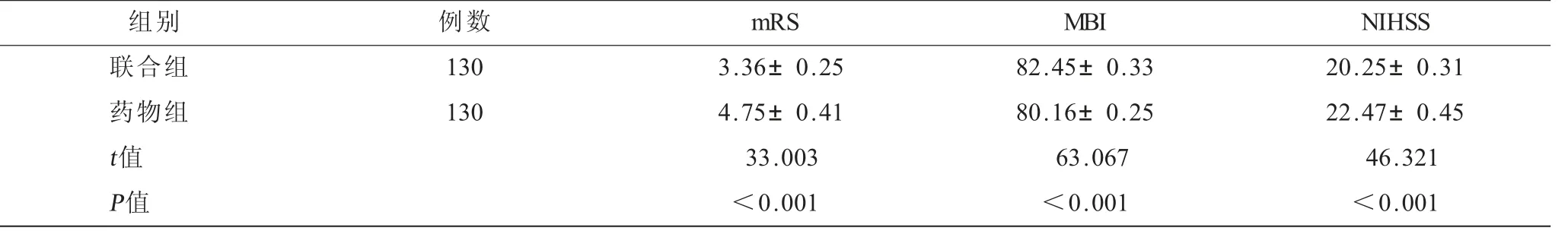
表4 两组患者治疗后的脑神经功能评分比较(±s) 单位:分
注:mRS=改良Rakin量表,MBI=改良Barthel指数,NIHSS=美国国立卫生研究院卒中量表。
组别 例数 mRS MBI NIHSS联合组 130 3.36±0.25 82.45±0.33 20.25±0.31药物组 130 4.75±0.41 80.16±0.25 22.47±0.45 t值 33.003 63.067 46.321 P值 <0.001 <0.001 <0.001
2.5 两组患者治疗后的生活质量评分比较 治疗后,联合组各维度SF-36评分均高于药物组,差异具有高度统计学意义(P<0.001),见表5。
表5 两组患者治疗后的生活质量评分比较(±s) 单位:分

表5 两组患者治疗后的生活质量评分比较(±s) 单位:分
注:PF=生理机能,RP=生理职能,RE=情感职能,MH=精神健康。
组别 例数 PF RP RE MH联合组 130 26.41±0.25 6.65±0.32 5.02±0.41 8.14±0.27药物组 130 24.33±0.31 4.76±0.41 4.11±0.35 6.82±0.36 t值 59.550 41.433 19.247 33.445 P值 <0.001 <0.001 <0.001 <0.001
3 讨论
近年随着我国全面进入老龄化社会,脑卒中的临床患病率越来越高,且随人们生活方式改变,此病发病特征逐渐呈年轻化趋势。由于脑神经功能缺损,脑卒中患者发病后多会存在不同程度认知、行为、意识障碍,此时其生理、心理状态均会受到一定影响,出于对个人疾病及预后的担忧,多数患者后续可能会存在明显的睡眠障碍[17]。作为脑卒中患者较为常见的并发症之一,睡眠障碍可对日常生活产生不利影响,重则可能增加其他心血管不良事件的发生风险,从而影响患者预后。目前临床针对脑卒中睡眠障碍多会通过多种镇静药物治疗,较为常见的药物类型主要有艾司唑仑片,此药为一种短效镇静药,睡前服用可一定程度上促进患者睡眠[18]。但有研究指出[19],脑卒中睡眠障碍为一种慢性病,为获得理想睡眠质量,患者往往需长期、多次服药治疗,长时间用药难免会导致机体发生一些药物副反应,也十分不利于其症状恢复。目前临床认为,失眠认知行为疗法在此类患者的治疗中具有较高应用价值,通过纠正患者错误认知、并实施睡眠行为限制对促使其养成良好睡眠习惯及规律作息均有重要意义[20]。
本研究结果显示,两组患者经统一常规治疗及药物干预均取得一定效果,但相比之下,联合组在联合应用失眠认知行为治疗后的效果更佳,该组治疗后1、3、5、8周后的PSQI评分均低于药物组(P<0.001),提示该组患者的睡眠质量改善更佳。考虑原因如下:失眠认知行为疗法重在找出导致患者失眠的根本原因,并针对具体原因实施个体化健康宣教及心理干预,以此纠正其关于疾病错误认知,帮助其认识到改善失眠对促进病情恢复的重要性,以此提升其接受行为治疗的配合度及依从性。神经递质为支配大脑睡眠觉醒系统的重要介导,当患者的治疗依从性明显提升后,可更好的配合医护人员所实施一系列治疗、干预措施,在谨遵医嘱定时定量用药后,患者的神经递质改善效果更佳,联合组治疗后的MLT、5-HT水平均高于药物组,DA水平低于药物组(P<0.001)。已有的研究证实[21],DA等神经递质也是支配人中枢神经系统的重要物质,经用药改善DA水平后,患者的情绪状态也可得到明显改善,故联合组治疗后的SAS、SDS评分也低于药物组(P<0.001)。除纠正患者认知外,失眠认知行为治疗还会通过行为限制来帮助患者养成良好睡眠习惯并保持规律作息,当机体生理、心理状态均得以改善后,患者也可获得更加理想的治疗效果,本研究中联合组治疗后的mRS、NIHSS评分低于药物组,MBI评分高于药物组(P<0.001),提示在此非药物疗法联合下,患者的脑神经功能恢复情况更佳,相应的,该组患者治疗后各维度SF-36 评分均高于药物组(P<0.001)。王晓娟等[22]在相关研究中证实了失眠认知行为治疗对脑卒中睡眠障碍患者的应用效果,该研究结果显示,经此疗法治疗后,患者的神经递质水平及脑神经功能均优于对照组(P<0.05),与本研究结果具有一致性。
综上所述,在脑卒中睡眠障碍接受常规治疗和药物干预时,联合应用失眠认知行为疗法治疗可增强其治疗效果,对提升患者睡眠质量、促进神经递质水平恢复、改善心理状态及脑神经功能并提高生活质量均有积极意义。

