取卵术后中度卵巢过度刺激综合征合并迟发性重度腹腔内出血保守治疗1例报道及文献复习
郑可茗,陈士岭
(南方医科大学南方医院妇产科生殖医学中心,广州 510515)
体外受精-胚胎移植(IVF-ET)技术是治疗不孕症的有效手段之一,并发症包括卵巢过度刺激综合征(OHSS)、盆腔感染、腹腔内出血等。其中,OHSS是进行卵巢刺激时发生的医源性并发症,根据症状的严重程度可分为轻度、中度及重度。中、重度的OHSS发生率在1%~5%。轻度OHSS表现为程度较轻的腹胀、呼吸困难、恶心呕吐等胃肠道不适及卵巢体积增大。严重OHSS可以表现为严重腹胀,大量腹腔积液、胸腔积液形成,导致血液浓缩、重要脏器血栓形成和功能损害及严重的电解质紊乱[1]。超声引导下经阴道穿刺取卵术(TVOR)是IVF助孕治疗的常规步骤,其操作相对简单可行、安全性高[2]。TVOR术后并发症包括阴道穿刺点出血、卵巢穿刺部位出血、盆腔内脏器穿刺损伤等。TVOR术后腹腔内出血的发生率为0.04%~0.23%[3],血流动力学稳定状态下可选择保守治疗,血流动力学不稳定且(或)出现进一步失血症状需手术治疗者为严重腹腔内出血[4]。多数患者出血症状在TVOR术后24 h内发生,我们在临床诊治了一例IVF控制性促排卵治疗过程中的OHSS患者,在TVOR术后第3天发生严重的腹腔出血及急性贫血,最后经保守治疗出院。现报道本例患者诊治过程,查阅结合相关文献进行讨论,为辅助生殖技术相关并发症的处理提供临床依据。
一、病例资料
患者女,29岁,因正常性生活未避孕2年未孕就诊于我院生殖医学中心。患者身高163 cm,体重43 kg,体质量指数(BMI)16.2 kg/m2,抗苗勒管激素(AMH)10.06 ng/ml,双侧卵巢基础窦卵泡数(AFC)23个。IVF助孕指征为:双侧输卵管慢性炎症;男方少弱畸精子症。
2021年10月20日采用GnRH拮抗剂方案促排卵,促性腺激素(Gn)总量1 075 U,共用11 d;扳机日雌二醇(E2)水平 10 140.21 pmol/L,直径大于10 mm卵泡20个。予促性腺激素释放激素激动剂(GnRH-a)0.2 mg+HCG 2 000 U促卵母细胞成熟。取卵术前:红细胞计数(RBC)4.02×1012/L,血红蛋白(HGB)118 g/L。2021年11月1日9:00am行超声引导下卵巢表面穿刺取卵术,穿刺卵泡20个(左侧8个、右侧12个),获卵19个,仅形成8CI胚胎1个。术后2 h复查经阴道B超提示子宫大小正常,卵巢大小左侧59 mm×45 mm、右侧58 mm×40 mm,陶氏腔液性暗区17 mm×12 mm。
取卵术后第2天常规随诊,患者诉轻度腹胀,血常规[白细胞计数(WBC) 11.40×109/L,红细胞压积(HCT) 0.326 L/L,RBC 3.64×1012/L,HGB 109 g/L,血小板计数(PLT) 250×109/L],肝、肾功能未见明显异常;D-二聚体8.84 μg/ml,纤维蛋白原4.84 g/L;E22 905.9 pmol/L。经阴道B超:子宫大小正常,左侧卵巢59 mm×49 mm、右侧72 mm×43 mm,子宫后方液性暗区64 mm×29 mm,前方液暗区33 mm×26 mm。考虑“中度OHSS”。为预防重度OHSS,决定取消新鲜周期胚胎移植,行全胚冻存。因D-二聚体明显升高,患者属于高危血栓发生人群,故予那屈肝素“速碧林”0.6 ml 皮下注射1次,预防血栓形成。
取卵术后第3天常规随诊,患者10:30am左右突感下腹胀痛,持续性,逐渐加重,伴恶心、呕吐,呕吐物为胃内容物,肛门坠胀感,立即卧床休息;全腹部有压痛、反跳痛和肌紧张,考虑有卵巢扭转、破裂或腹腔出血的可能。生化检查报告:血常规(WBC 8.35×109/L,RBC 2.93×1012/L,HGB 89 g/L,HCT 0.263 L/L,PLT 228×109/L);肝、肾功能以及电解质、凝血四项均正常范围内;纤维蛋白原(FbgC)3.66 g/L,D-二聚体 3.25 μg/ml。行经阴道彩超:子宫前位,大小形态正常;左卵巢83 mm×56 mm,右卵巢82 mm×44 mm,内见多个液性弱回声;子宫直肠窝可见游离液性暗区为20 mm;双侧髂窝内见液性暗区,深度分别为22 mm(右)、39 mm(左);肝肾隐窝见游离液性暗区44 mm;左上腹见游离液性暗区37 mm。于当日中午收入妇产科住院部,下午行CT全腹平扫:子宫体积稍增大,双侧附件区明显增大并多发类圆形病变,考虑多发卵泡形成,部分见卵泡囊出血;周围盆腔积血,腹盆腔大量积液。予持续心电监护,按OHSS常规处理,予白蛋白、多巴胺等扩容处理及补液治疗;每间隔4 h复查血常规、间隔12 h复查凝血四项、D-二聚体等检查,因血红蛋白进行性下降停用低分子肝素,考虑诊断中度OHSS合并腹腔内大出血,估计出血量约在1 800 ml左右;考虑卵巢增大、质地脆,手术止血困难,故暂予保守治疗;予输红细胞3 U,血浆200 ml后复查血红蛋白最低值为HGB 73 g/L,再次予输红细胞2 U,之后多次监测血红蛋白无明显下降,多次复查D-二聚体值在3.53~19.89 μg/ml范围内,未用低分子肝素,患者无血栓事件发生,继续予对症支持治疗。经过住院6 d治疗后症状缓解,复查血常规(HGB 92 g/L),办理出院。
出院后随诊患者病情平稳,症状无反复。患者于取卵后49 d月经来潮,双侧卵巢恢复正常大小,无腹腔积液,血常规未见明显异常(HGB 134 g/L)、D-二聚体0.16 μg/ml。2022年2月冷冻胚胎移植一枚8CI胚胎,未孕。
二、讨论
1.OHSS相关的危险因素分析:OHSS病理生理机制主要是由于血管内皮生长因子(VEGF)的过度分泌导致卵巢和腹膜毛细血管通透性增加,液体从血管内转移到第三腔隙所致[5]。其发生主要与HCG水平相关,高危因素包括年轻患者、低BMI、多囊卵巢综合征、基础AFC数目多、高AMH水平、控制性卵巢刺激(COS)后雌二醇峰值水平高[5-7]。OHSS的治疗重在预防,在进行卵巢刺激前识别易患OHSS的高风险女性。拮抗剂方案、冷冻胚胎可有效降低OHSS发生,其他方法还包括GnRH-a触发卵母细胞成熟,以及使用多巴胺受体激动剂、葡萄糖酸钙、阿司匹林以及二甲双胍[8-10]。轻度OHSS具有自限性,未妊娠患者的OHSS症状通常随下一个月经周期消失,妊娠患者症状可能会持续到妊娠早期[5]。轻、中度OHSS一般无需处理,重度OHSS患者需进行补液扩容、维持电解质紊乱、抗凝和必要时穿刺引流腹水或胸水等对症治疗[11]。OHSS患者静脉血栓栓塞症(VTE)风险增加,进行预防性抗凝治疗可降低88%的VTE风险[12-13]。
本例患者术前AMH水平高(10.06 ng/ml)、AFC数量多(23个)、低BMI,为OHSS高风险。尽管仅给予Gn100 U/d,患者仍出现卵巢高反应,E2峰值14 188.22 pmol/L,发育卵泡数29个。采用GnRH-a+HCG扳机,获卵19个,行TVOR第2天后患者出现轻度腹胀症状;B超提示双侧卵巢增大,盆腔积液;D-二聚体(8.84 μg/ml)、纤维蛋白原(4.84 g/L)水平升高,考虑“中度OHSS”。予低分子肝素抗凝治疗预防血栓形成,嘱患者高蛋白饮食、适当饮水。
2.取卵后腹腔出血的诊断和分析:当出现弥漫性腹痛、乏力症状,超声提示盆腔内有中等至大量液体,手术治疗术中发现或CT扫描证实出血部位可诊断为腹腔内出血;若患者出现心血管系统不稳定及(或)血红蛋白水平及红细胞压积下降引起临床症状,需要手术干预,则该并发症程度定义为严重腹腔内出血[4]。无症状患者取卵后24 h正常失血量为(232±130) ml[14]。一项关于中、重度OHSS及严重腹腔内出血的危险因素的大数据回顾文献报道,年轻女性、助孕指征为输卵管因素、采用GnRH-a方案、取卵数量多以及新鲜胚胎移植后临床妊娠与OHSS及腹腔内出血风险增加相关[3]。低BMI值、多囊卵巢综合征已明确证实与卵巢出血存在相关性,多囊卵巢综合征患者群体卵巢出血的发生率高达4.5%[15]。其他与卵巢出血风险相关的因素还包括既往多次取卵史、既往盆腔手术史、操作时重复穿刺、肝素化生理盐水冲洗卵泡等[16-18]。Ragni等[19]研究发现,取卵后4~6 h内患者红细胞计数、血红蛋白浓度及盆腔液体量与术前存在差异,取卵术后72 h患者失血量无明显增加。TVOR后出血症状一般在24 h内出现,主要表现为腹痛、失血引发的一系列贫血症状,33.3%卵巢出血患者在取卵术后1 h内出现症状,93.3%患者在24 h内出现出血症状,6.7%的患者在24 h后没有出现临床症状,因此文献还提出“迟发性出血(late onset bleeding)”这一概念,但没有进一步具体阐述[4]。
本文检索总结了文献报道的5例TVOR术后出现迟发性腹腔内出血的患者临床特征(加上本例患者,共6例;表1)。其中2例TVOR后出现延迟性腹腔内出血的患者既往有长期抗凝药物使用史,取卵术前16 h停用抗凝药物,并在术后12 h开始使用肝素,分别在取卵后2 d、3 d出现剧烈腹痛[20]。1例因卵巢位置异常采用超声引导下经子宫肌层及经腹取卵术,6 d后患者出现了大量阴道出血,考虑是取卵操作破坏动脉壁的连续性而导致子宫动脉假性动脉瘤形成破裂导致[21]。假性动脉瘤是医源性损伤导致动脉穿刺部位一层或多层动脉壁缺损而与动脉管腔相通形成充满血液的空腔。1例患者有Ⅷ凝血因子缺乏症,在TVOR术后7 d出现腹痛及阴道流血[22];另1例患者术前凝血功能正常,既往有原发性血小板增多病史,低分子肝素半衰期短,预防性用药剂量低,术后监测间接反映患者肝素含量的抗凝血a因子浓度为0,因此,该文献作者认为出现延迟性腹腔出血可能是由于血小板增多症导致的血小板功能障碍,而不考虑肝素的使用导致[23]。
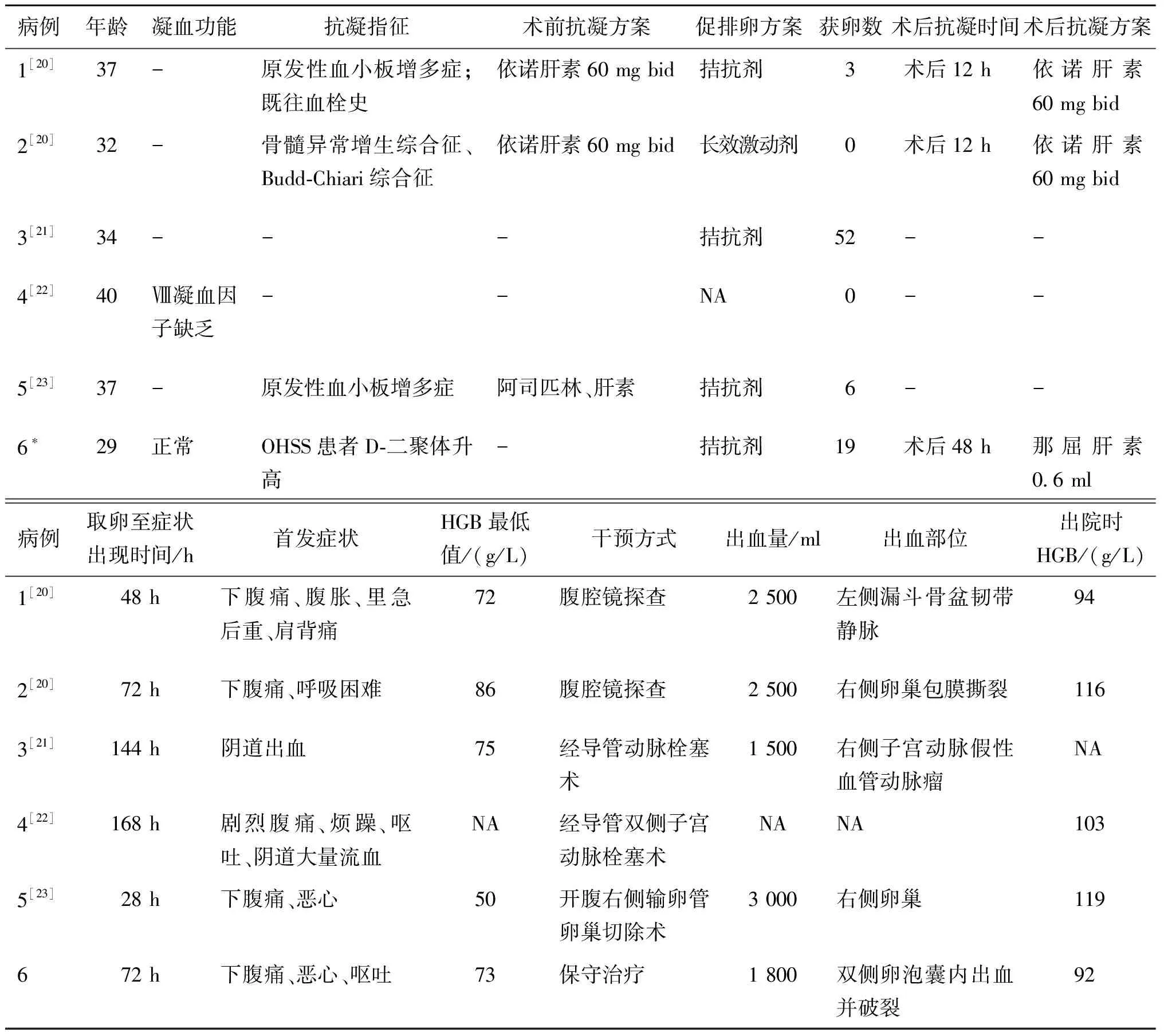
表1 总结6例TVOR后发生迟发性腹腔出血患者的临床特征
在原发性血小板增多症患者群体中TVOR后延迟出血似乎更常见,血小板功能障碍及其伴随的出血倾向可能与延迟性出血有关。既往研究发现,术后早期使用肝素与术后出血二次手术探查的显著增加有关[24]。对比患有原发性血小板增多症患者术后使用肝素与不使用肝素情况,发现使用肝素的患者症状延迟的时间更加显著,肝素可能是导致发生延迟性出血的原因。另外,凝血功能障碍、盆腔内结构的异常、取卵操作穿刺部位的选择可能是导致延迟性腹腔内出血的危险因素。
3.本文报道病例的诊治分析:本例患者于取卵后第2天应用低分子肝素的次日出现剧烈腹痛,血常规提示血红蛋白快速下降。排除卵巢扭转诊断,主要考虑诊断中度OHSS合并腹腔内大出血,估计出血量约在1 800 ml左右。考虑出血来源主要为卵巢黄体囊肿破裂口出血或与原有取卵穿刺点凝块脱落后出血有关,与低分子肝素应用可能有关。考虑到COS后卵巢增大、质地脆,手术止血难度大,故决定予保守治疗。取卵术后第4天行腹腔穿刺术抽出20 ml陈旧性暗红色液体,提示腹腔内活动性出血已经停止。取卵术后第5天经输血治疗后患者血红蛋白降至最低值73 g/L,红细胞压积(HCT)下降至最低值0.214 L/L,D-二聚体较前升高7.69 μg/ml,考虑与入院时予多巴胺扩容治疗所致红细胞被稀释相关;心电监护下患者生命体征平稳,凝血功能正常,3P试验阴性,无弥漫性血管内凝血(DIC)征象,继续输血治疗。取卵术后第6天血红蛋白(80 g/L)、HCT(0.238 L/L)逐渐上升,D-二聚体升高至19.89 μg/ml,患者主观症状缓解,遂决定继续目前保守治疗方案。继续检测下血红蛋白、HCT逐渐上升,D-二聚体降至10.04 μg/ml。
发生OHSS时机体出现血液高凝状态[25]。OHSS患者血液浓缩体现在白细胞数量增加,HCT上升[5],然而本例患者多次复查血常规提示血红蛋白下降,HCT下降,说明患者的血液浓缩状态不足以弥补血容量的丢失。当OHSS患者并发出血性疾病,机体产生保护性反应,D-二聚体及纤维蛋白酶原在OHSS基础上进一步升高[26]。本例患者出现症状后复查发现血浆纤维蛋白原、血浆D-二聚体水平并未上升而是较前下降,可能是由于在出现腹痛症状前曾予肝素抗凝治疗,抗凝治疗可能导致卵巢表面血凝块脱落后出血点不发生自凝或者延缓自凝时间,血液在盆腹腔内缓慢蓄积至一定程度后引发明显的腹膜刺激征,延迟腹痛症状出现的时间,失血症状逐渐加重,导致严重的腹腔内出血。
OHSS患者获卵数多,雌二醇峰值水平高,卵巢体积增大会造成卵巢血管扩张、组织脆弱,卵巢出血风险大[27]。因此,对于诊断OHSS的患者,突然出现剧烈腹痛时应警惕腹腔内出血、卵巢扭转的发生。但由于腹腔内出血该类并发症的罕见性,目前暂未见比较OHSS与非OHSS患者出血风险的相关临床研究。TVOR穿刺出血点可随时间自发愈合,使用肝素治疗是否增加出血风险,仍需要更多临床资料进一步证实。
4.TVOR后腹腔出血的处理:大部分患者行TVOR后失血量无明显改变,一般机体可代偿TVOR引起的失血,可选择保守治疗[19]。TVOR后严重腹腔内出血患者通过输血、补液等保守治疗也可获得满意的疗效[28]。其他治疗方式包括介入、腹腔镜手术治疗及开腹手术治疗。
取卵术后约有三分之一的患者因血栓形成倾向需要接受抗凝治疗[29]。国内学者报道2例TVOR后当天发生OHSS合并卵巢出血患者,1例为腹腔镜手术治疗后第2天予低分子肝素治疗;另1例患者通过多次输血、白蛋白、低分子肝素等对症支持保守治疗出院,均获得满意疗效[27]。肝素的使用对于出血已控制的OHSS合并腹腔内出血患者未引起负面效果,说明肝素使用时机的重要性。肝素是否使腹腔内出血症状恶化、延长患者住院时间,如何平衡血栓形成风险的预防以及出血性疾病的治疗仍需要更多的探索。
综上所述,OHSS与腹腔内出血的高危因素都与卵泡数量、BMI、PCOS有关。当患者考虑诊断OHSS,出现严重腹痛、血常规提示血红蛋白进行性下降、HCT下降、D-二聚体与纤维蛋白酶原降低等表现时,应考虑合并腹腔内出血的发生。使用肝素治疗OHSS导致的高凝状态,可能会导致腹腔迟发性出血,因此应该延长术后观察及随访时间。对于取卵术后高危出血患者,不应该单依据D-二聚体这一指标判断是否有血栓风险,应谨慎使用低分子肝素治疗,降低出血的风险。对于TVOR术后出现延迟发生严重腹腔内出血患者,酌情选择保守治疗可获得满意疗效。

