石墨相氮化碳基材料光催化还原除铀研究进展
秦泽敏
(国能新朔铁路有限责任公司,鄂尔多斯 017000)
0 引 言
核能因具有高的能量密度和低的二氧化碳排放量,被认为是化石燃料的替代品,具有很好的发展前景[1]。铀(uranium, U)是一种重要的核燃料[2-3],核能工业的快速发展会导致大量的铀通过采矿废水等途径释放到环境中[4-5],铀的生物毒性和放射性毒性会对周边的生态系统和环境构成威胁。因此,在含铀废水排放前进行适当处理至关重要。目前研究较多的处理方法有离子交换[6]、膜滤[7]、吸附[8]等,但以上方法均有局限性,例如离子交换法在树脂生产过程中可能会产生大量的污染,膜滤法电能消耗较高,而吸附法则存在吸附后产生的含铀吸附剂处理不当可能会造成铀的二次污染的问题。因此,发展高效、清洁的废水除铀新技术变得非常有意义。
光催化法(photocatalysis, PC)是一种新兴的、有效的含铀废水处理方法[9],因具备高效、无二次污染、低成本、可重复利用等优点而受到了关注[10-14]。目前光催化除铀的研究多集中在新型光催化剂的开发上[15-17]。而在诸多光催化剂中,g-C3N4基催化剂被认为是理想的光催化除铀材料[16,18],具有制备简便、制备成本低、能带结构合适、稳定性及光电性能出色等特点。g-C3N4是一种无毒无害的光催化剂,可以通过尿素、硫脲、三聚氰胺等富含氮元素的前驱体通过一步热缩合反应制备[13,19-20],是一种具有三-s-三嗪骨架结构的二维聚合物,通过氨基相互连接[21]。截至2022年7月,已经有大量文章报道了采用g-C3N4基光催化剂光催化还原去除水中U(VI),大约占到光催化除铀文章总数的30%以上,并呈现逐年增长的态势(见图1)。

图1 g-C3N4基材料光催化还原去除水中U(VI)的文献检索情况。(a)数据基于“Web of Science”数据库,检索关键字 “photocatalytic, reduction, U(VI), g-C3N4”;(b)g-C3N4基光催化剂光催化还原去除水中U(VI)文献占比情况Fig.1 Researches on g-C3N4based materials photocatalytic reduction of U(VI). (a) Data is based on a search result from “ Web of Science ” using keywords “photocatalytic, reduction, U(VI), g-C3N4 ”; (b) proportion of photocatalytic reduction of U(VI) from water by g-C3N4 based materials in field of photocatalytic reduction of U(VI)
本文综述了光催化还原除铀的机理以及应用于光催化还原去除水中U(VI)研究的g-C3N4基光催化剂。基于前人的研究成果,总结了目前的研究进展,并以此提出了g-C3N4基材料光催化去除水中U(VI)存在的问题,展望了未来的发展前景。
1 g-C3N4光催化除铀原理
铀是多价态的,其中+VI和+IV可以稳定存在于水体中[22]。六价铀(U(VI))易溶于水且毒性较高,而四价铀(U(IV))难溶且毒性较低。因此将U(VI)还原为难溶的U(IV)是一种适当的处理含铀废水方法[23]。在光催化除铀中,U(VI)首先被吸附在催化剂表面,当光催化剂被光照射时,价带(valence band, VB)上的电子跃迁到导带(conduction band, CB)上形成光电子,光电子会将吸附在光催化剂表面的U(VI)还原为U(IV),从而达到去除水中U(VI)的目的[24-26],具体原理见图2。
图3(a)归纳总结了U(VI)被还原为U(VI)的标准氢电极电位(normal hydrogen electrode, NHE)[27],图3(b)是g-C3N4能带结构[21],从图3(b)中可以看出,g-C3N4的导带位置位于-1.1 V,远低于U(VI)还原电位,所以g-C3N4光催化还原去除水中铀在热力学上是可行的。

图2 光催化除铀(U(VI))机理图Fig.2 Mechanism diagram of photocatalytic reduction of U(VI)

图3 铀还原过程中的氧化还原电位(a)和g-C3N4的能带结构(b)[21]Fig.3 Redox potential of U(VI) reduction (a) and band structure diagram of g-C3N4 (b)[21]
2 g-C3N4基光催化剂
虽然g-C3N4光催化还原除铀在热力学上是可行的,但由于块状g-C3N4存在光生电子和空穴会快速复合、易发生团聚、表面活性差等缺陷,会影响其光催化还原除铀性能。为了克服块状g-C3N4固有的局限,提出了很多块状g-C3N4改性方法以提高其光催化除铀性能。
2.1 一元g-C3N4催化剂
一元g-C3N4催化剂主要是通过对g-C3N4掺杂、表面修饰、提高比表面积等形式进行改性,以提高g-C3N4光催化除铀性能。
2.1.1 掺杂
在众多g-C3N4改性策略中,掺杂是增强g-C3N4光催化除铀性能最常规也是最可控的方法。通过在g-C3N4晶体结构中掺杂金属或非金属元素,形成晶格缺陷,有利于形成更多活性中心,从而起到加快电荷分离、提高光吸收能力以及氧化还原性能等作用[16,28]。
Xue等[29]以NH4Br溴源,采用混合煅烧尿素和NH4Br的方法制备了溴掺杂的g-C3N4(CNBr),得到的催化剂相比于块状g-C3N4具有更窄的禁带宽度(见图4(a)),更大的光吸收范围,更强的光生载流子转移能力(见图4(b)),所以将其应用于光催化除铀实验中,相比于块状g-C3N4去除效率提升了2.2倍。

图4 CN和CNBr的能带结构(a)和光致发光谱(b)[29]Fig.4 Band structure diagram (a) and photoluminescence (b) of CN and CNBr[29]
Wu等[30]使用乙醇溶解尿素和磷酸三丁酯,蒸干后焙烧,得到引入磷的g-C3N4(P-introduced g-C3N4, PC3N4)。通过密度泛函理论(density functional theory, DFT)理论计算,在g-C3N4引入P后,可能取代N、C1、C2三种位点,计算P原子得到取代N、C1、C2的吉布斯自由能分别为-2 287.71(N位点)、-2 304.31(C1位点)和-2 304.29(C2位点)Hetree,表明C原子会优先被P取代,且C1比C2更有利于取代掺杂,从图5分子轨道和能量中可以看出无论是C1还是C2位点,与初始的g-C3N4相比,HOMO与LUMO之间的带隙都有所缩小。改性后的P3C3N4相比于块状g-C3N4光催化除铀效率提升了2.75倍,这是由于引入P后g-C3N4的电子结构发生了明显的变化,带隙变窄,可见光吸收能力增强,光生载流子转移能力增强,光催化除铀机理图见图6。
Lu等[13]使用H3BO3溶液溶解硫脲,蒸干后焙烧,得到硼杂化的g-C3N4(B-g-C3N4)。改性后的B2-g-C3N4相比于块状g-C3N4光催化除铀效率提升了2.54倍。硼的掺杂使B-g-C3N4的带隙变窄,在可见光的照射下更容易激发产生光生电子-空穴对,提升了光催化除铀性能。
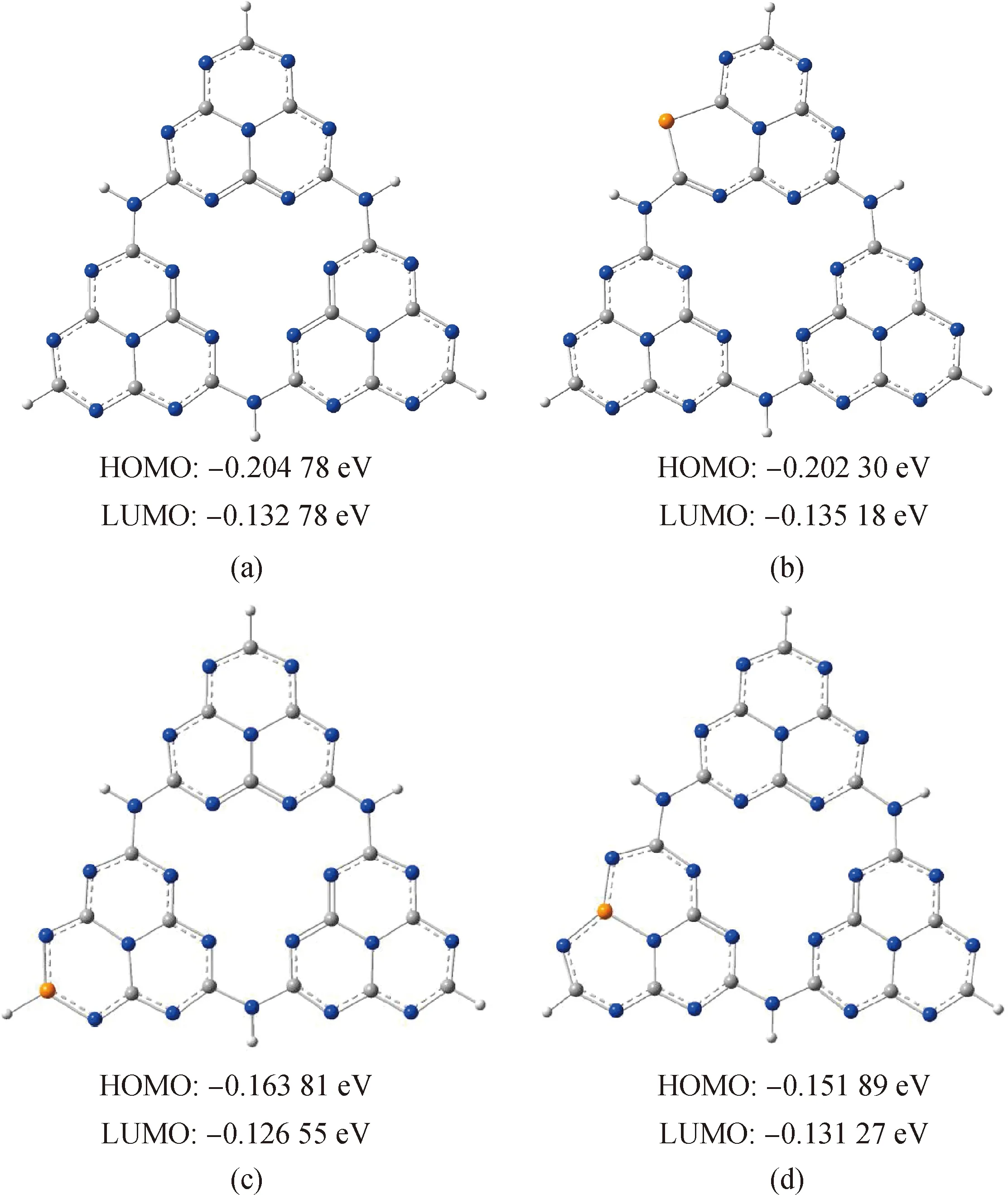
图5 分子轨道和能量。g-C3N4 (a),被P取代N (b)、C1 (c)、C2 (d)的PC3N4 (HOMO:最高已占分子轨道;LUMO:最低未占分子轨道)Fig.5 Molecular orbital energies and structures of g-C3N4 (a) and PC3N4 with the substitutional P for N (b) or C1 (c) & C2 (d) (HOMO: highest occupied molecular orbital; LUMO: lowest unoccupied molecular orbital)
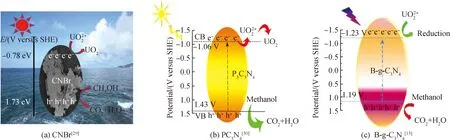
图6 CNBr[29] (a),PC3N4[30](b)和B-g-C3N4[13](c)的光催化机理图Fig.6 Photocatalytic mechanism diagram of CNBr[29] (a), PC3N4[30] (b) and B-g-C3N4[13] (c)
2.1.2 表面修饰
通过官能团修饰被认为是提高g-C3N4光催化活性的重要策略之一,这些官能团可以提高催化剂的光吸收能力,调节催化剂的能带结构并可以作为高效的耗电子俘获剂来提高光催化除铀效率。
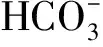

图7 原始和羧化g-C3N4的分子轨道和能量结构(从左到右依次是BCN、CCN-5、CCN-20,羧基含量依次增加)Fig.7 Molecular orbital energies and structures of raw and carboxylated g-C3N4 (From left to right, it is BCN, CCN-5, CCN-20, and the carboxyl group content increases in turn)
Gao等[31]采用直接煅烧尿素和金属-有机框架材料混合物的方式,合成了含有杂原子(Zn+C)和氰基(—CN)共修饰的多孔g-C3N4纳米片(DCNNS)光催化剂。DCNNS的光催化除铀效率相比于块状g-C3N4提高了~6.09倍。这是由于改性后的DCNNS具有大量的纳米孔,为了加速传质提供了更多的反应点位和扩散通道;氰基的存在提升了g-C3N4的光响应范围,同时作为强吸收电子基团提高了载流子的分离效率。
2.1.3 提高比表面积
通过热聚合焙烧工艺得到的块状g-C3N4比表面积小,所能提供的反应活性位点比较少,所以通过合成多孔g-C3N4,提高g-C3N4孔隙度以及比表面积,可以增加g-C3N4表面的活性位点,提升g-C3N4光催化除铀性能。
Wang等[32]采用硬模板法合成了介孔g-C3N4(MCN),将氰酰胺溶液在70 ℃下进行搅拌,在溶液中加入12 nm的SiO2,混合物在70 ℃下过夜搅拌蒸干,将混合物在氮气的保护下550 ℃加热聚合4 h,将得到的黄色粉末置于4 mol/L的NH4HF2溶液中处理24 h,移除粉末中的SiO2,具体步骤见图8。得到的MCN1.0光催化除铀效率相较于块状g-C3N4提高6.75倍。效率的提高主要是因为MCN材料较大的比表面积提供了更多的活性位点,光利用效率和光生载流子的分离效率均得到了显著提高。

图8 MCN样品制备示意图Fig.8 Sample preparation diagram of MCN
蒋丽等[33]采用SiO2和双氰胺超声溶解于去离子水中,在70 ℃下加热12 h蒸干,在550 ℃加热聚合4 h,将得到的黄色粉末置于100 mL的1 mol/L HF中,超声24 h,得到三维大孔g-C3N4。表征结果表明,三维大孔g-C3N4比表面积显著增加,具有良好的三维贯通性(见图9),对可见光的吸收明显增强。三维大孔g-C3N4相较于块状g-C3N4具有更高的光催化除铀活性,去除效率是块状g-C3N4的5.9倍。

图9 样品的SEM和TEM照片。(a,b)块状g-C3N4,(c,d)三维大孔g-C3N4Fig.9 SEM and TEM images of bulk g-C3N4 (a, b) and 3D macroporous g-C3N4 (c, d)
2.2 二元g-C3N4基异质结催化剂
构建二元异质结是提升g-C3N4光催化除铀性能的主要手段,二元光催化剂基于两种半导体的不同能带结构可以分为四种类型:(1)Type-I型异质结(跨立型排列),(2)Type-II异质结(错开型排列),(3)Type-III异质结(破隙型排列),(4)Z型异质结。不同二元异质结类型能带排列结构如图10所示。
在光催化除铀领域Type-II型异质结受到了最多的关注,因其组成的两个半导体之间独特的能带排列结构有利于载流子的分离,在典型的Type-II异质结中,半导体1(SC1)的导带和价带都低于半导体2(SC2),同时两种半导体的带隙相互重叠,这种独特的排列结构允许在不同的半导体材料中积累带有相反电荷的载流子,从而降低了载流子复合的概率,促进光催化反应[34-36]。
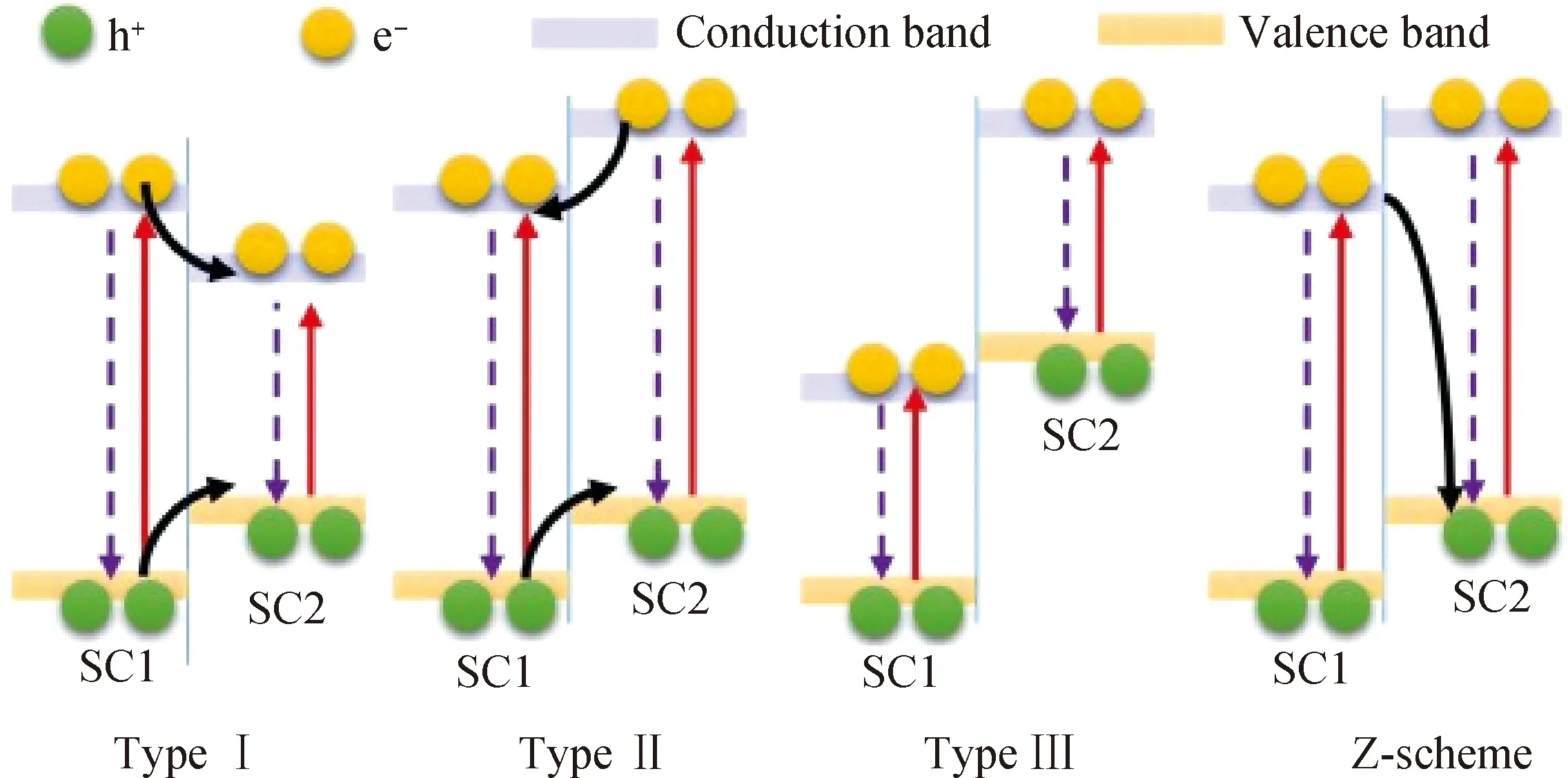
图10 不同二元异质结类型能带排列结构Fig.10 Different types of heterojunction band alignments
Wang等[36]以硫脲和钨酸作为前驱体(见图11(a)),采用煅烧法制备了g-C3N4/WS2(CN/WS2)。通过TEM照片(见图11(b)、(c))可以看出,g-C3N4呈现出了类似石墨烯的片状结构,在g-C3N4/WS2中,WS2掺杂到了g-C3N4薄片中,而这种紧密结合的结构有利于提高光催化反应活性,而WS2的加载保持了g-C3N4片状结构。通过不同配比g-C3N4/WS2催化剂的光催化还原除铀实验结果(见图11(d))可以看出,CN/WS2-5体现出了最高的去除效率,是块状g-C3N4的3.1倍。g-C3N4/WS2能带结构见图11(e),由图可以看出CN/WS2是Type-II型催化剂,g-C3N4在光照的条件下产生光生电子-空穴对,由于g-C3N4的CB比WS2的CB更负,所以光生电子会从g-C3N4的CB迁移到WS2的CB,在WS2的CB将U(VI)还原为U(IV)。
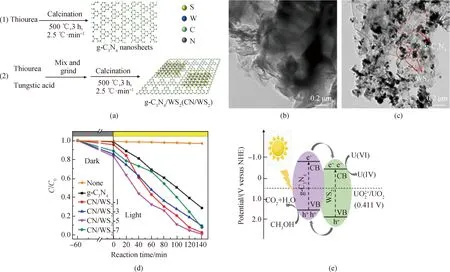
图11 g-C3N4和g-C3N4/WS2的合成示意图(a);g-C3N4(b)和g-C3N4/WS2(c)的TEM照片; 不同配比g-C3N4/WS2的光催化除铀结果(d);以及g-C3N4/WS2光催化除铀机理图(e)Fig.11 Schematic diagram of synthesis of g-C3N4 and g-C3N4/WS2 (a); TEM images of g-C3N4 (b) and g-C3N4/WS2 (c); removal efficiency of different ratio g-C3N4/WS2 (d); and mechanism diagram of g-C3N4/WS2 (e)
Li等[17]采用三聚氰胺热缩聚的方法合成g-C3N4,然后采用溶剂热法合成CdS/g-C3N4(CdS/CN)。根据总态密度和分波态密度可以看出,CdS/CN是Type-II型异质结(见图12(a))。所以光生电子会从CB低的g-C3N4流向CB相对较高的CdS,在CdS的表面发生U(VI)的还原反应(见图12(b))。
Z型异质结两个半导体的排列结构与Type-II型异质结类似,但在光反应中SC1的光生电子会与SC2的光生空穴中和,SC1光生空穴会在其VB累积,因此SC1的VB会保持高的氧化水平,SC2光生电子会在其CB累积,因此SC2的CB会保持高的还原水平。基于这种独特的内部电荷转移机制,Z型异质结相对于Type-II型异质结优势在于可以保持两个半导体的高氧化和高还原效率。
Liu等[37]采用尿素在600 ℃焙烧2 h制备g-C3N4,混合不同比例的TiO2,加入去离子水配成g-C3N4/TiO2水溶液,在80 ℃加热5 h蒸干至粉状,然后400 ℃煅烧2 h,冷却后研磨成粉,得到g-C3N4/TiO2复合光催化剂。通过对比g-C3N4,TiO2以及g-C3N4/TiO2不同复合体光催化除铀速率,可以看出去除速率最高g-C3N4/TiO2-1(k=0.222 2)的去除速率分别是块状g-C3N4(k=0.003 3)和TiO2(k=0.135 9)的67.3倍和1.64倍(见图13(a))。这是由于g-C3N4/TiO2-1复合体光催化剂在TiO2的CB上产生的光生电子可以迁移到g-C3N4表面,与g-C3N4VB上的光生空穴复合猝灭,g-C3N4CB上的光生电子将U(VI)还原为U(IV)。这样的电荷转移机制减少了g-C3N4/TiO2光生载流子复合,有助于提升光催化除铀效率。
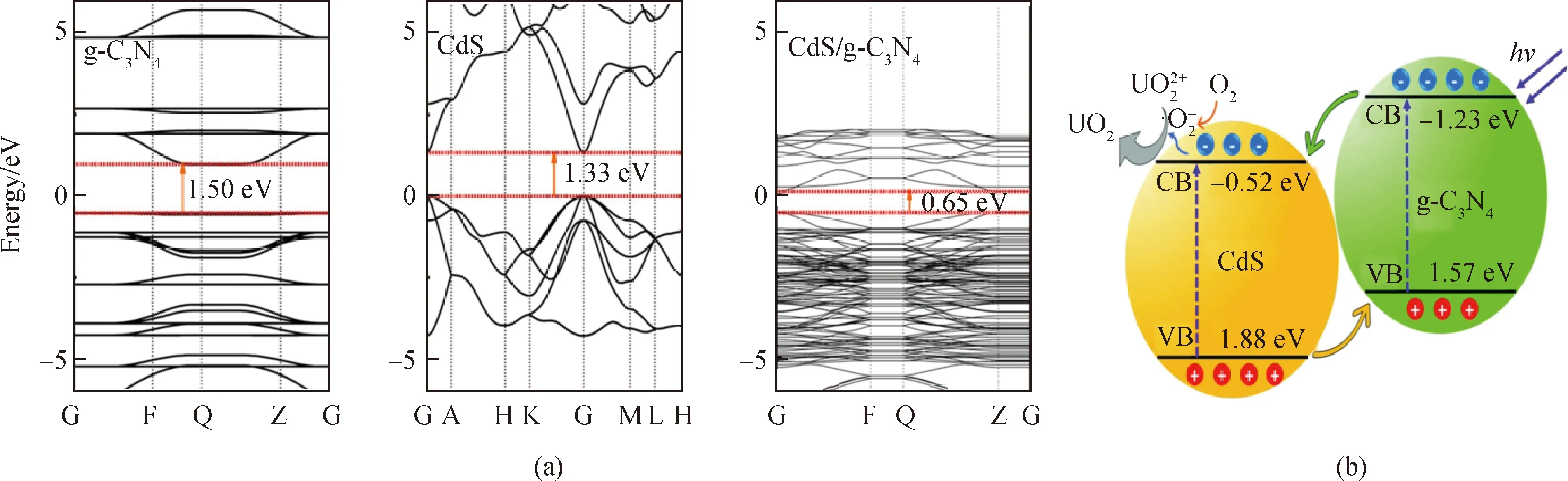
图12 g-C3N4、CdS和CdS/g-C3N4的 DFT能带结构计算图(a)和CdS/g-C3N4的光催化除铀机理图(b)Fig.12 DFT band structure calculation of g-C3N4、CdS and CdS/g-C3N4 (a) and photocatalytic uranium removal mechanism diagram of CdS/g-C3N4 (b)
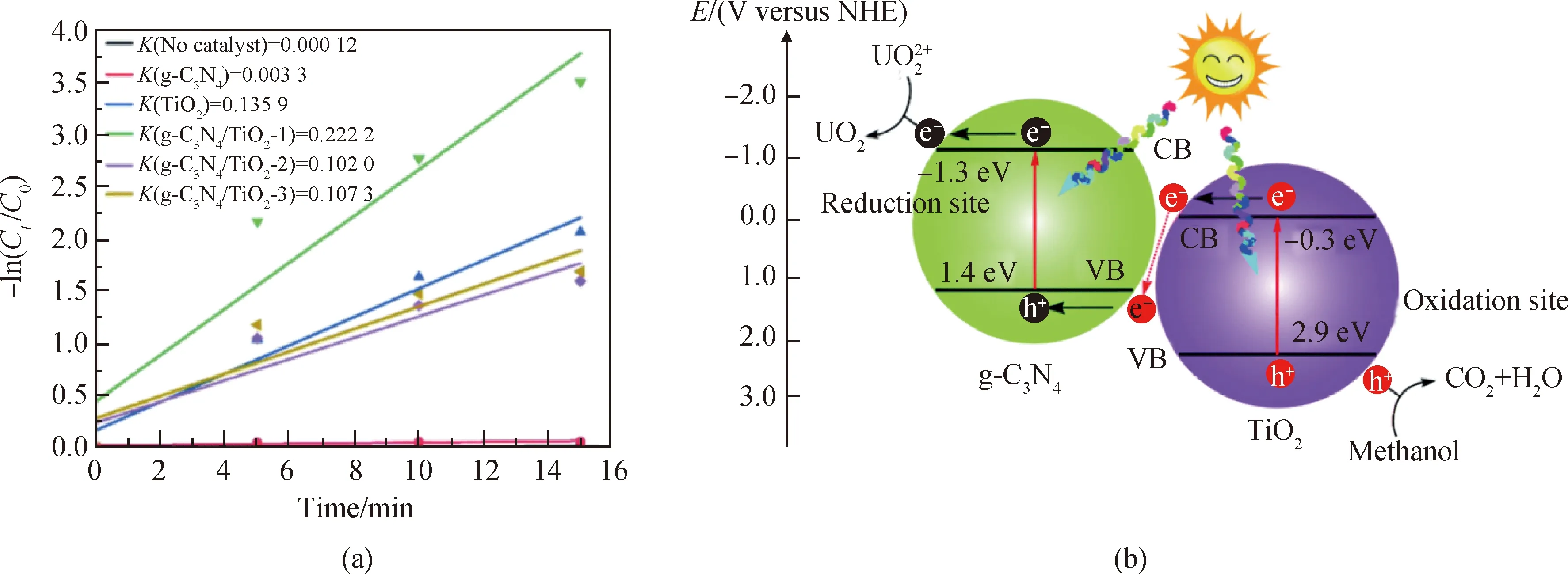
图13 TiO2、g-C3N4和g-C3N4/TiO2的光催化还原除铀反应速率常数(a); 以及g-C3N4/TiO2在模拟太阳光照射下的去除机理图(b)Fig.13 Rate constant (k) of U(VI) photocatalytic reduction by TiO2, g-C3N4 and g-C3N4/TiO2 (a); and diagram of proposed mechanism of g-C3N4/TiO2 nanostructures under simulated sunlight irradiation (b)
2.3 三元g-C3N4基异质结催化剂
在g-C3N4基光催化剂光催化除铀的报道中,Liu等[14]通过引入贵金属Ag合成了g-C3N4/Ag/TiO2三元催化剂。贵金属Ag的引入主要是由于贵金属的费米能级通常低于半导体材料,当贵金属沉积于半导体材料上时,半导体材料在光照情况下产生的光生电子可快速向贵金属迁移,从而使材料的整体费米能级降低。从光致发光光谱的结果来看(见图14(a)),相比g-C3N4/TiO2,引入贵金属Ag形成三元催化剂,可以有效地降低光生电子-空穴复合速率。从去除效果来看(见图14(b)),g-C3N4/Ag/TiO2三元催化剂光催化除铀的去除率达到了99%,远高于单体或者二元复合催化剂。图14(c)是g-C3N4/Ag/TiO2光催化除铀的机理图,g-C3N4、Ag和TiO2的禁带宽度分别为2.7 eV、0.3 eV和3.2 eV,在光照的情况下,g-C3N4、Ag和TiO2都可以产生光生电子-空穴对,其中Ag可吸收可见光,从而可以被局部表面等离子体共振激活,此外Ag纳米颗粒可以产生一个很强的原位表面电场,激发g-C3N4和TiO2产生更多的光生电子-空穴对,而Ag产生的光生电子会移动到g-C3N4的VB与光生空穴发生复合,TiO2表面的光生电子会移动到Ag表面与Ag产生的光生空穴发生二次光生载流子的复合,最终在g-C3N4的CB发生U(VI)的还原反应。

图14 样品的光致发光光谱(a);不同催化剂的光催化除铀效率(b);g-C3N4/Ag/TiO2的光催化除铀机理图(c)Fig.14 Photoluminescence spectra of the sample (a); photocatalytic uranium removal efficiency of different catalysts (b); and mechanism diagram of photocatalytic removal of uranium by g-C3N4/Ag/TiO2 (c)
3 结语与展望
光催化还原技术因其高效、无二次污染、成本低、可重复利用等优点被认为是一种有效的铀去除方法,而g-C3N4具有制备简便、制备成本低、能带结构合适、稳定性及光电性能出色等优点,是一种理想的光催化除铀材料,因此本文对光催化除铀的机理以及应用于光催化除铀研究的g-C3N4基材料进行了综述。
虽然目前对于g-C3N4基光催化剂在光催化除铀方面取得了一些研究进展,但距离实际应用还有很大差距,仍然有一些问题亟待解决。
(1)光催化除铀是利用光催化剂吸收光能激发产生光生电子将含铀废水中易溶的U(VI)还原为难溶的U(IV)实现铀的去除,然而被还原的难溶U(IV)会沉积在光催化剂的表面,占据光催化剂活性位点使除铀效率下降,因此如果在空间上分离光催化剂活性位点和铀沉淀位点,可以实现光催化除铀的连续高效运行。光电催化法可以有效地解决光催化法的上述缺陷,因此开发固定型g-C3N4基光催化剂对于光电催化除铀连续高效运行具有重要意义。
(2)目前对于光催化除铀的研究,以合成水为主,主要研究单一无机离子或者有机离子的影响。虽然研究单一离子对U(VI)去除影响以及探究影响机制是有益的,但实际含铀废水的情况和合成水有很大的不同,实际水可能是大量的无机物、有机物以及微生物等的混合物,不同成分之间可能存在协同或者抵消作用,因此面向实际含铀废水的g-C3N4基光催化剂开发应该在今后的研究中得到重视。
(3)水处理成本是判断水处理技术是否可以大范围使用的重要考量因素,而g-C3N4基光催化剂在光催化除铀的研究中很少对此进行阐述。建议在今后的研究中,应该从g-C3N4基光催化剂合成成本、催化剂耐久性、再生费用等角度进行成本效率评价。
值得欣慰的是,在现有的g-C3N4基光催化剂光催化除铀的研究中,2020年以后发表的文章占比在80%以上。在可预见的未来,g-C3N4基材料光催化除铀技术将会变成一个很有前景的铀污染治理技术,将成为g-C3N4基材料光催化产氢以及光催化二氧化碳还原之外,另外一个重要的应用场景。
——潘桂棠光生的地质情怀

