液相色谱法分析植物多糖中单糖组成及含量
王 成, 李真真, 邵世华, 甄荣英, 刘英学, 马红伟, 袁 梅, 张丽燕, 王 芳, 蒋永毅
(青岛菲优特检测有限公司,山东青岛 266100)
多糖是由单糖和寡糖缩合而成的多聚物,在植物样本中广泛分布,植物多糖是植物细胞代谢产生的聚合度大于10的聚糖[1]。植物多糖具有抗肿瘤、降血糖、降血脂、提高机体免疫力等多种生物活性,且多糖的生物活性与其分子量和单糖组成紧密相关,多糖的单糖组成为植物多糖研究中的重要参数[2]。检测多糖中单糖的组成及含量时,通常采用酸水解和酶水解的方法破坏糖苷键,将多糖水解成单糖,再对单糖进行检测[1 - 3]。酸水解用于较难水解的单糖,酸水解反应比较剧烈,可以水解大部分多糖,但反应过程中容易发生降解[2]。目前多糖中单糖组成的检测方法有液相色谱-质谱法[2]、糖腈乙酸酯衍生化-气相色谱法[4]、1-苯基-3-甲基-5-吡唑啉酮(PMP)柱前衍生-液相色谱法[1,2]、3-氨基-9-乙基咔柱前衍生-液相色谱法等[5]。与质谱相比液相色谱的紫外检测器不易被污染,因此维护成本较低,其中PMP衍生柱前衍生法应用最为广泛[6 - 8]。由于多糖水解过程容易出现水解不充分、在酸作用下水解生成的单糖发生降解等情况[2],因而使用PMP衍生-液相色谱法分析单糖时常出现回收率低、稳定性差等问题而影响检测的准确性。为此,本研究以海带多糖为样本,对多糖水解时间、PMP衍生物稳定时间等因素进行探究,旨在找到单糖组成及含量分析的关键点,提高该方法的准确性和稳定性。
1 材料与方法
1.1 实验材料与仪器
标准品L-古罗糖醛酸、D-甘露糖醛酸、D-甘露糖、鼠李糖、葡萄糖、半乳糖、岩藻糖(标准品纯度>95%,上海安谱实验科技股份有限公司);三氟乙酸、1-苯基-3-甲基-5-吡唑啉酮(PMP)、NaOH、HCl、(分析纯,中国医药集团有限公司);三氯甲烷、甲醇、乙腈(色谱纯,Merck Millipore)。本实验中使用的样品为市售海带。
岛津LC-20A液相色谱仪,带紫外检测器(岛津企业管理(中国)有限公司);电热鼓风干燥箱(上海一恒科学仪器有限公司);TDZ5-WS离心机(湘仪离心机仪器有限公司);电子天平(XSE205,梅特勒-托利多国际贸易有限公司);真空干燥箱(DZF-6051,上海一恒科学仪器有限公司)。
1.2 分析方法
1.2.1 色谱条件色谱柱:UG120 C18(4.6 mm×250 mm×5 μm),检测波长:254 nm,柱温:40 ℃,进样量:20 μL。流动相A:0.05 mol/L KH2PO4溶液,加4 mol/L NaOH溶液调pH值为6.8;流动相B:乙腈[8]。流动相洗脱程序为:0~25 min,85%~60%A;25~30 min,60%~85%A;30~36 min,85%A。
1.2.2 单糖水解及衍生方法的研究(1) 三氟乙酸水解时间对水解效率的影响:精密称取0.2 g烘干后的海带样品于25 mL水解管中,加入10 mL 4 mol/L三氟乙酸,充氮后放入110 ℃烘箱中,分别水解0、0.5、1、1.5、2 h,冷却后加入4 mol/L NaOH溶液调pH值至中性,加水定容到25 mL,取1 mL于10 mL离心管中,加0.3 mol/L NaOH溶液1 mL,加0.5 mol/L PMP(甲醇)1 mL,70 ℃水浴70 min,冷却后加0.3 mol/L HCl 1 mL,加水定容到10 mL。取2 mL加入4 mL三氯甲烷净化,离心后过膜待测[8 - 10]。
(2) 单糖水解损失率对比:精密量取0.5 mL 1 mg/mL标准品溶液于25 mL水解管中,加入10 mL 4 mol/L三氟乙酸,充氮后放入110 ℃烘箱中,分别水解0、0.5、1、1.5、2 h,冷却后加入4 mol/L NaOH溶液调pH值到中性,加水定容到25 mL,取1 mL于10 mL离心管中,加0.3 mol/L NaOH溶液1 mL,加0.5 mol/L PMP(甲醇)1 mL,70 ℃水浴70 min,冷却后加0.3 mol/L HCl 1 mL,加水定容到10 mL。取2 mL 加入4mL三氯甲烷净化,离心后过膜待测。
(3)真空干燥除酸单糖的热损失率研究:精密量取0.05 mL 100 mg/L标准品溶液于10 mL离心管中,加入2 mL甲醇后放入60 ℃真空干燥箱中,烘干后加0.3 mol/L NaOH溶液0.5 mL,加0.5 mol/L PMP(甲醇)0.5 mL,70 ℃水浴70 min,冷却后加0.3 mol/L HCl 0.5 mL,加水定容到5 mL。取2 mL加入4 mL三氯甲烷净化,离心后过膜待测。
(4) PMP单糖衍生物稳定性实验:将10 mg/L标准品溶液分别在衍生后6、12、14、16、18、20 h进样分析。
2 结果与分析
2.1 水解用酸的选择
用于水解多糖的酸有盐酸、硫酸和三氟乙酸,盐酸通常用于低聚糖的酸解制备,但在高温条件下盐酸具有强氧化性,会破坏多糖和已经水解下来的单糖,水解损失率较大,反应不易控制[1]。但是对于较难水解的单糖可以选择用盐酸水解,如壳寡糖中的氨基葡萄糖[11]。硫酸也具有强氧化性,而且还可与单糖发生反应。三氟乙酸氧化性不强,对多糖的破坏较小,其带有-CF基团,可以吸引更多氢离子,催化促进多糖的水解[1]。海带等植物样品中L-古罗糖醛酸、D-甘露糖醛酸、D-甘露糖、葡萄糖、半乳糖、岩藻糖的含量较高,且这些单糖比较容易水解,多糖水解成单糖后,单糖在酸的作用下会发生降解[2],导致检测结果偏低。为了降低海带样品的单糖水解损失率,选择三氟乙酸对样品进行水解。
2.2 水解时间对水解效率的影响
图1为海带样品水解时间对水解效率的影响,由图1可以看出,海带样品中游离单糖只有葡萄糖和半乳糖,且含量较小。随着水解时间的增加,L-古罗糖醛酸、D-甘露糖醛酸、D-甘露糖、葡萄糖、半乳糖、岩藻糖的含量显著增加。L-古罗糖醛酸和D-甘露糖醛酸最难水解,水解2 h时含量达到最大值,含量分别为8.53±0.21%和24.69±1.35%,且显著高于1.5 h的含量,其含量分别为7.62±0.58%和22.73±0.85%。D-甘露糖和葡萄糖水解2 h时含量达到最大值,含量分别为1.07±0.87%和1.36±0.65%,但水解1.5 h后继续水解含量增加不显著。1.5 h时含量分别为0.86±0.12%和1.31±0.24%,半乳糖和岩藻糖最容易水解,水解1 h后含量没有显著增加。由此可以得出,各单糖的水解速率是不同的,确定水解时间时要综合考虑各单糖的水解速率,由图1可以得出,2 h时海带样品水解最为充分。
本实验旨在研究单糖在高浓度三氟乙酸和高温条件的降解比率。由图2可以看出L-古罗糖醛酸和岩藻糖水解时含量显著降低,水解0.5 h时L-古罗糖醛酸和岩藻糖的含量分别为90.5±2.09%和95.9±0.51%,水解2 h时分别降解到68.48±0.44%和91.6±2.11%,其它单糖没有发生降解。因此可以得出,多糖水解成单糖后随着水解时间的延长,游离单糖在三氟乙酸的作用下会发生降解,这与Matthew J等人的研究结果一致[2]。L-古罗糖醛酸的稳定性最差,但植物样品中L-古罗糖醛酸的水解速率较慢,减缓了L-古罗糖醛酸单糖的降解,对结果准确性影响不大。图1中海带岩藻糖在水解1 h时含量为11.18±1.09%,水解2 h后含量显著下降到10.05±1.35%(P<0.05),也是由于水解后游离的岩藻糖在三氟乙酸的作用下发生降解导致的。
D-甘露糖,鼠李糖,葡萄糖和半乳糖在水解0.5 h时含量显著升高,L-古罗糖醛酸,D-甘露糖醛酸和岩藻糖在水解0.5 h时含量显著降低,因此在水解初期,单糖在三氟乙酸的作用下可发生相互转化[2]。但相互转化比率较低,不超过10%,由单糖相互转化引入的实验误差是可以接受的[9]。因此水解时间的确定需要分析各单糖的水解速率和水解后的降解速率,综合考虑得出海带样品的最佳水解时间为2 h。

图1 海带样品水解时间对水解效率的影响Fig.1 Effect of hydrolysis time on hydrolysis efficiency of kelp
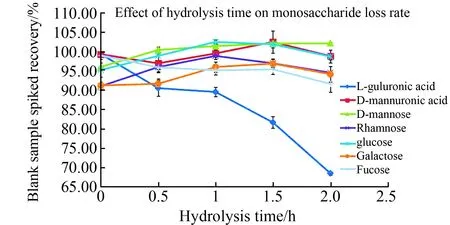
图2 水解时间对单糖损失率的影响Fig.2 Effect of hydrolysis time on loss rate of standard substance
2.3 水解后三氟乙酸去除方式的选择
PMP需要在弱碱性条件下与单糖发生衍生,因此水解后需要去除三氟乙酸。目前去除三氟乙酸的方法有两个,一是加碱中和除酸[6],二是真空干燥除酸[5]。图3为加碱除酸和真空干燥除酸对单糖损失率的影响,从图中可以看出采用真空干燥除酸时单糖的损失较大,说明单糖在干燥状态下的热稳定性不好,其中L-古罗糖醛酸和D-甘露糖醛酸全部降解,其它5种单糖的加标回收率为32.12%~46.67%。加碱中和除酸的空白加标回收率较好,为100.01%~103.20%。因此海带样品水解后应采用加碱中和的方式去除三氟乙酸。
2.4 PMP衍生物稳定性分析
图4为PMP衍生物稳定性分析,从图4可以看出,12 h前7种单糖PMP衍生物没有发生降解,12 h后7种单糖的空白加标回收率显著下降(P<0.05),14 h时7种单糖的回收率为61.20±1.45%~98.20±1.09%。岩藻糖的PMP衍生物降解比率最大,20 h后加标回收率只有44.29±1.35%。由此可以得出,样品完成衍生后要在12 h之内完成上机分析,分析一针样品需要36 min,12 h可分析20针样品,因此同时衍生的样品数量不要超过20个。

图3 加碱除酸和真空干燥除酸对单糖损失率的影响Fig.3 Effect of deacidification manners (adding alkali and vacuum drying) on monosaccharide loss rate
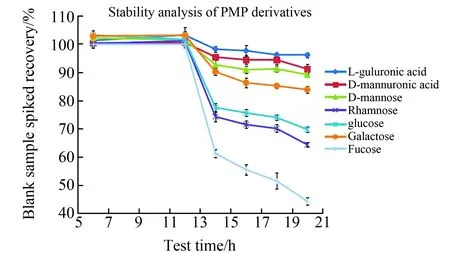
图4 PMP衍生物稳定性分析Fig.4 Stability analysis of PMP derivatives
2.5 方法检出限、精密度及准确性分析
本研究对高效液相色谱法分析单糖的精密度进行评价,表1为7种单糖标准品(20 mg/L)连续进样的相对标准偏差(RSD)和标准曲线r2。从表2可以看出,7种单糖连续进样6针的RSD均小于2%,说明该方法稳定性较好。GB/T 27404-2008《实验室质量控制规范食品理化检测》中规定:对于确证方法的标准曲线相关系数不应低于0.99[12]。在线性范围5~100 mg/L内标准曲线r2均大于0.999,可以得出该方法的线性较好。液相分析时有杂质干扰,因此将5倍信噪比设为检出限,10倍信噪比设为定量限,7种单糖5倍信噪比的检测浓度为0.8~1 mg/L,与王凤芹等人的结果接近[12,13],换算至样品中单糖的检出限为100~125 mg/kg。对海带样品进行加标回收实验,加标水平为0.5%,样品加标回收率为81.5%~91.2%,表明方法的准确性较好。

表1 单糖衍生物的标准方程、相关系数、检测限及回收率
2.6 本文方法与文献方法结果对比
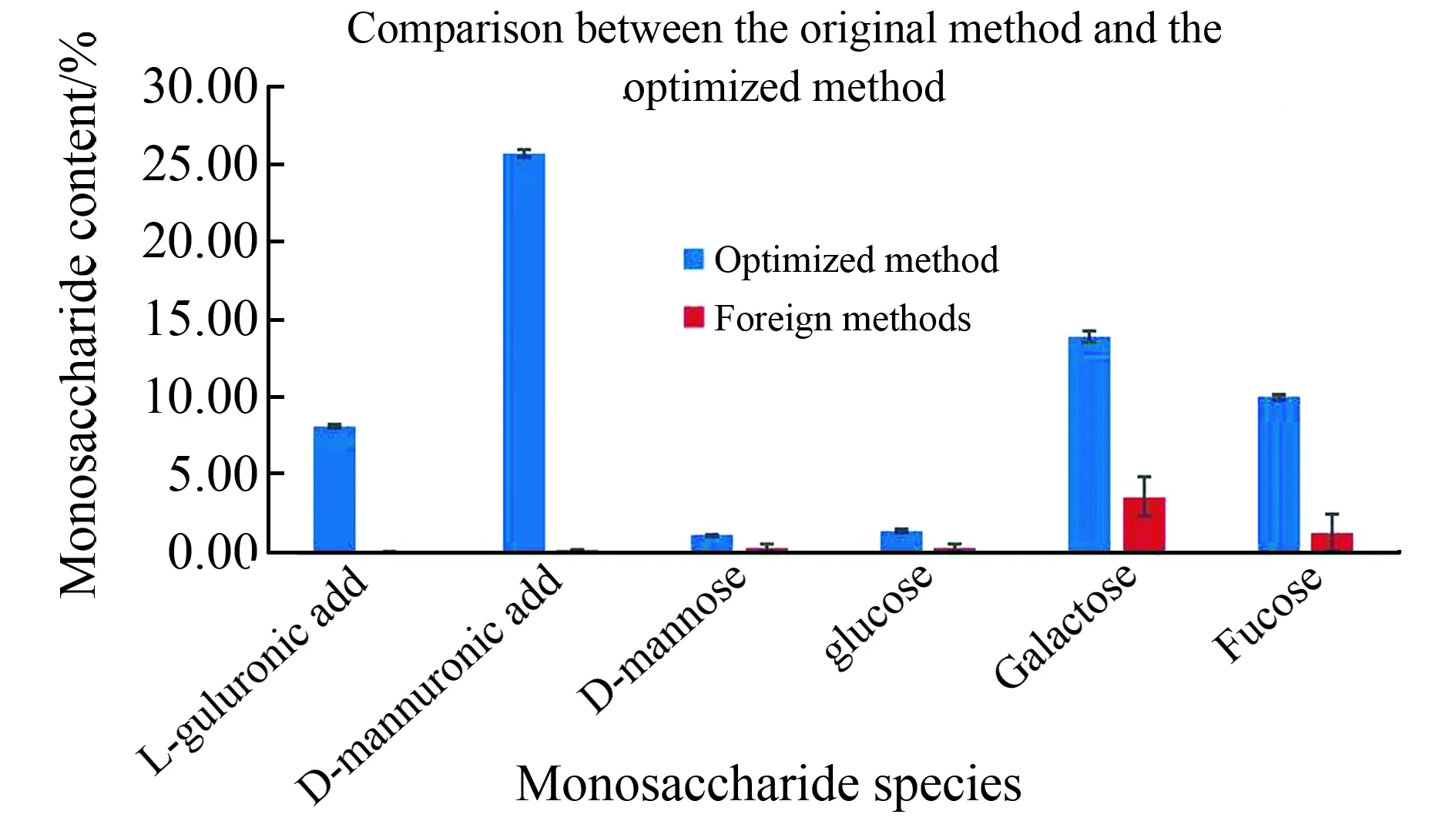
图5 文献方法与本文方法单糖检测结果对比Fig.5 Comparison of monosaccharide detection results between the literature method and the optimized method
图5为液相色谱法分析海带中单糖组成及含量文献方法和本文方法的对比,文献方法是参考Lv等人检测茶中多糖[7]和Liu等人检测茯苓多糖[8]的方法。文献方法的前处理加入三氟乙酸后放入沸水浴中加热6 h,冷却后取出0.5 mL,加入2 mL甲醇后放入60 ℃真空干燥箱中烘干,真空干燥除酸后进行PMP衍生。由图1可以看出,使用文献方法检测时L-古罗糖醛酸和D-甘露糖醛酸全部降解。本文方法的两种单糖检测结果分别为8.21±0.12%和25.76±0.29%。本文方法检测D-甘露糖、葡萄糖、半乳糖、岩藻糖的含量显著高于原有方法(P<0.05)。使用文献方法时岩藻糖含量为1.28±1.24%,本文方法的含量为10.08±1.28%,由图5可以看出,文献方法检测的D-甘露糖、葡萄糖、半乳糖、岩藻糖误差大于本文方法,本文优化后方法的数据平行性较好,适用于海带样品多糖的检测。
3 结论
分析植物类样品中单糖组成的关键控制点为:水解用酸,水解时间和单糖PMP衍生物稳定时间。本实验通过优化海带样品中单糖的PMP柱前衍生化-液相色谱测定方法条件,找到了多糖水解单糖分析过程中的关键控制点。解决了单糖分析时常出现回收率低、稳定性差等问题。为多糖样品中单糖组成分析提供了新的方法优化模式,可应用于其它植物或动物多糖样品中单糖组成的分析。

