分散液液微萃取/气相色谱-质谱法测定水中多氯联苯
王 兴, 史 丽, 赵 阳, 杨 艳
(北京市科学技术研究院资源环境研究所,北京 100089)
多氯联苯(Polychlorinated Biphenyls,PCBs)是人工合成的一类联苯环上的氢原子被氯原子取代之后的化合物,通常按氯原子数或氯的百分含量加以标号。在我国,习惯按联苯上氢被氯取代的个数分为一氯至十氯联苯。PCBs的异构体共有209种,以PCB1至PCB209命名区分。该类化合物由于具有良好的耐热性、不可燃性、化学惰性以及低蒸气压和高介电常数等特点,曾被广泛地用于电力设备的绝缘介质和油漆等器件中[1 - 3]。然而,PCBs具有持久性、远距离传输性、生物积累性和生物毒性等特点,对环境和人类安全都存在着巨大的威胁,为此《持久性有机污染物的斯德哥尔摩公约》将其列为首批需要消除的12种持久性有机污染物之一,目前已停止使用[4 - 6]。我国水体中的PCBs主要来源于含PCBs的工业、城市废水排放以及大气降水。对黄河、长江、珠江三大水系及其它一些水系环境中的调查显示,我国水域中PCBs浓度在几十至几百μg/L之间,所以对水体中PCBs检测方法的进一步研究十分必要[7 - 10]。
水中PCBs萃取的传统方法主要为液液萃取与固相萃取,但方法需要的样品量较大。同时,传统方法存在操作步骤繁琐、耗时长、需要使用大量有机溶剂,对环境不友好等缺点[11,12]。因此,开发省时高效、有机溶剂用量少的微萃取技术一直是研究热点。与固相微萃取、单滴液相微萃取、中空纤维膜液相微萃取等微萃取技术相比,基于均相萃取和浊点萃取的分散液液微萃取(Dispersive Liquid-Liquid Microextraction,DLLME)具有操作简单快速、仪器设备要求简单、耗材成本低廉等优点,具有较好的应用前景[13,14]。
本文选择毒性较强的12种类二噁英类PCBs(PCB77、81、105、114、118、123、126、156、157、167、169、189),联合国GEMS/Food中规定的7种PCBs指示性单体(PCB28、52、101、118、138、153、180),以及(GB/T 14848-2017)《地下水质量标准》中需要监测的八氯联苯(PCB194)、九氯联苯(PCB206)共计20种PCBs为对象,使用分散液液微萃取进行分离富集,采用气相色谱-质谱法测定,实现了对水样中20种痕量PCBs检测的要求。
1 材料与方法
1.1 仪器与试剂
7890A气相色谱仪(美国安捷伦);5977B质谱仪(美国安捷伦);CR-GIII冷冻离心机(日本日立)。
标准物质:20种多氯联苯标准物质以及内标物(PCB77-d6)均购自百灵威(美国AccuStandard),质量浓度为100 mg/L。二氯甲烷、三氯甲烷、四氯化碳、氯苯、甲醇、乙腈、丙酮均为色谱纯(美国赛默飞世尔);实验用水为超纯水(美国Milli-Q)。
1.2 样品制备
水样经0.45 μm滤膜过滤后,移取10 mL于15 mL离心管中,将1 mL丙酮,20 μL二氯甲烷注入离心管中,涡旋2 min,室温静置5 min后,4 ℃、8 000 r/min离心10 min,吸取下层有机相10 μL,加入0.2 μL内标物后进行后续分析。
1.3 仪器条件
1.3.1 气相色谱条件色谱柱:HP-5MS柱(30 m×0.25 mm×0.25 μm,美国安捷伦);程序升温:120 ℃保持1 min,20 ℃/min升到180 ℃,再以5 ℃/min升到280 ℃,保持20 min;进样方式:不分流进样1 min;进样量:1.0 μL;进样口温度:270 ℃;传输线温度:270 ℃;柱流量:1.2 mL/min。
1.3.2 质谱条件电子轰击离子(EI)源,EI温度:250 ℃;离子化能量:70 eV;选择离子模式(SIM)扫描。各化合物选择离子见表1。
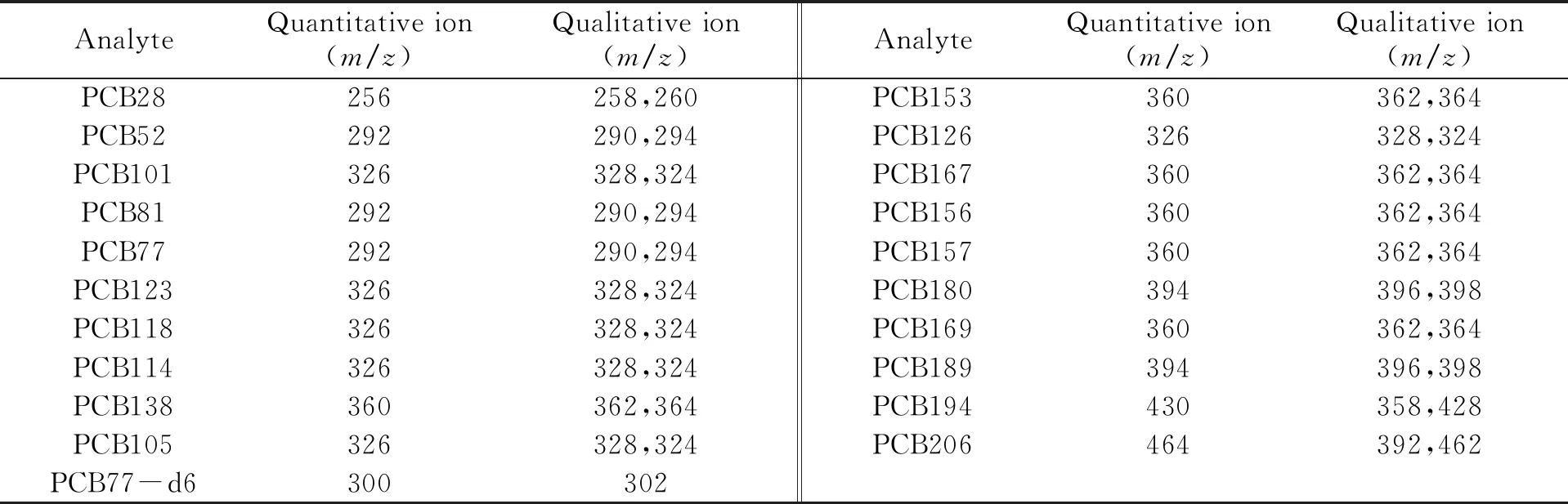
表1 PCBs的选择离子参数
2 结果和讨论
2.1 分散液液微萃取条件优化
2.1.1 萃取剂和分散剂种类的选择萃取剂需选择不溶于水或在水中溶解度低、可与分散剂混合后在水溶液中形成稳定的两相系统,并对目标化合物溶解度高且密度大于水的有机溶剂。分散剂需选择能同时与水和萃取剂互溶的有机溶剂,可使萃取剂在水相中形成细小的液滴,并使溶液形成稳定的乳浊液体系,从而增大萃取剂与目标化合物的接触面积,获得较高的萃取效率[15]。此外,有研究表明水中低氯代的PCBs较高氯代PCBs的萃取效率更低[16]。分别考察了二氯甲烷、三氯甲烷、四氯化碳、氯苯作为萃取剂(20 μL),以及甲醇、乙腈、丙酮作为分散剂(1 mL)对PCB28(200 μg/L)的萃取能力。结果表明三氯甲烷与丙酮的组合PCB28回收率最高(91.4%),四氯化碳/丙酮(88.1%)、二氯甲烷/丙酮(85.6%)的回收率次之。尽管三氯甲烷与四氯化碳的萃取效率更高,但与二氯甲烷区别并不显著,由于二氯甲烷在环境分析实验室更加常见,且对环境与健康的危害更小,因此采用二氯甲烷/丙酮的组合作为后续实验的萃取剂和分散剂。
2.1.2 萃取剂体积的选择分别选用含有不同体积二氯甲烷(10.0、20.0、30.0、40.0、50.0 μL)的丙酮溶液(1.0 mL)对PCB28(100 μg/L)进行萃取,考察萃取剂体积对萃取效率的影响。如图1所示,回收率随萃取剂体积的增大而增大,当萃取剂体积超过20 μL后,PCB28的回收率变化不大,说明在萃取剂体积为20 μL时,形成的细微液滴与水中PCBs具有较大的接触面积,可以达到萃取要求。故选用20 μL作为最佳萃取剂体积。
2.1.3 分散剂体积的选择考察丙酮体积分别为0.50、0.75、1.00、1.25、1.50 mL时,对PCB 28(100 μg/L)的萃取效率(二氯甲烷体积20.0 μL)。如图2所示,回收率随分散剂体积的增大而增大,当丙酮体积为1 mL时,回收率达到最大。加入分散剂体积超过1 mL后,回收率略有降低,原因可能是PCB28溶于水相的浓度增大导致[17]。因此选用1 mL作为最佳分散剂体积。

图1 萃取剂体积对回收率影响Fig.1 Effect of extractant volume on recovery

图2 分散剂体积对回收率影响Fig.2 Effect of dispersant volume on recovery
2.2 方法的线性范围、检出限和精密度
配制浓度分别为10.0、20.0、50.0、100、200、500 μg/L PCBs水溶液,按照优化条件进行萃取与测定。结果显示,PCBs浓度在10.0~500 μg/L范围内呈现良好的线性关系,相关系数均可达0.999。如表2所示,按实验方法测定浓度为10 μg/L的多氯联苯水溶液,平行测定7份,得到方法检出限,检出限在0.7~1.8 μg/L之间。多氯联苯的选择离子扫描总离子流图见图3,表明各目标化合物在色谱柱上获得了良好的分离效果,可满足检测要求。
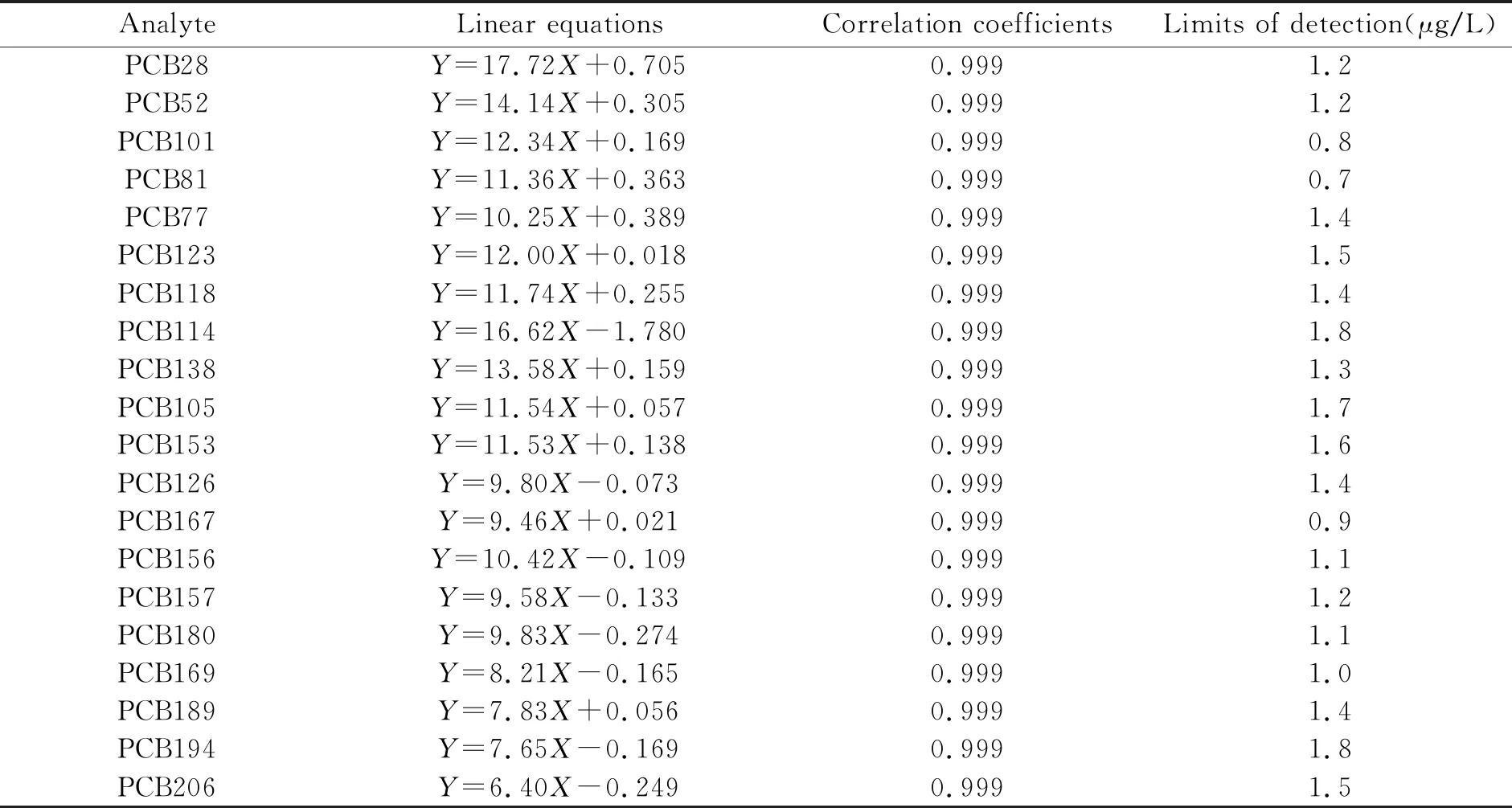
表2 PCBs的回归方程、相关系数和检出限(n=7)
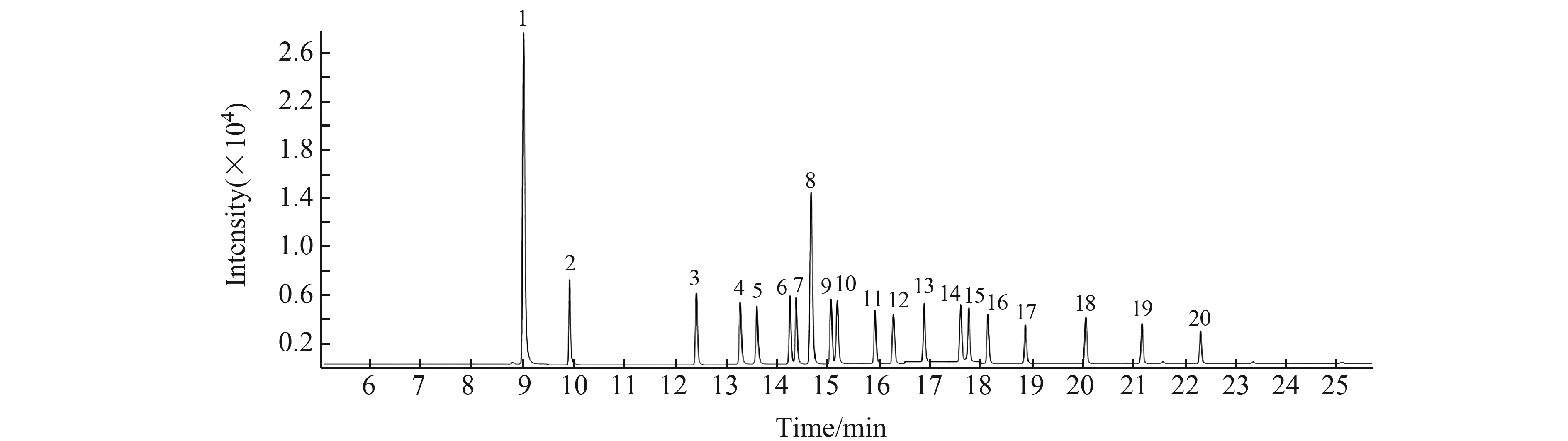
图3 多氯联苯总离子流图Fig.3 Chromatogram for standard sample of PCBs1.PCB28;2.PCB52;3.PCB101;4.PCB81;5.PCB77、PCB77-d6;6.PCB123;7.PCB118;8.PCB114;9.PCB138;10.PCB105;11.PCB153;12.PCB126;13.PCB167;14.PCB156;15.PCB157;16.PCB180;17.PCB169;18.PCB189;19.PCB194;20.PCB206.
在方法测定范围内,选择100 μg/L浓度点加标进行6次重复测定,PCBs的相对标准偏差(RSD)及回收率见表3。结果表明,PCBs的RSD为2.2%~7.1%,回收率在83.6%~104%之间,能够满足水中PCBs的测定需求。
2.3 实际水样分析
实际样品使用地表水、生活污水、工业废水,在最佳萃取条件下,对水样及其样品加标进行萃取与测定,
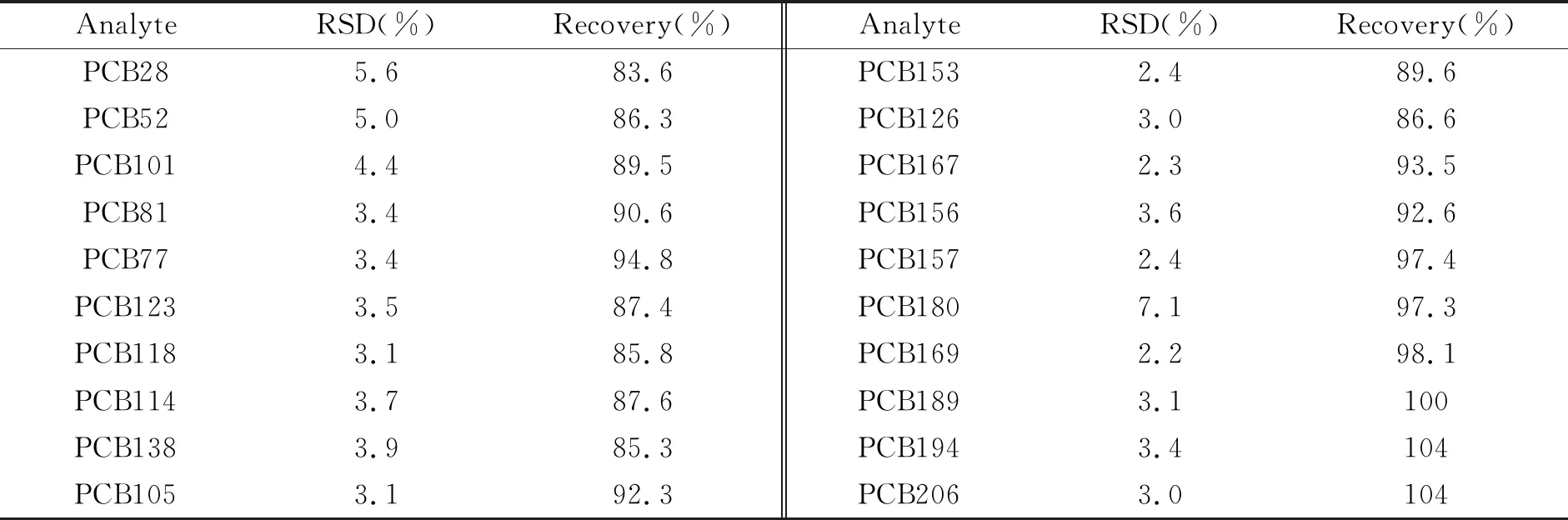
表3 PCBs的相对标准偏差和回收率
其中地表水加标量为20.0 μg/L,生活污水加标量为100 μg/L,工业废水加标量为450 μg/L。由于水样中均未检出PCBs,故采用样品加标计算相对标准偏差与回收率(表4),各化合物相对标准偏差与回收率分别在1.6%~9.7%与72.0%~115%之间,表明方法能够满足实际样品的测定。

表4 实际样品PCBs的相对标准偏差和回收率
3 结论
本文采用分散液液微萃取与气相色谱-质谱法联用,测定了水中20种多氯联苯,并对影响萃取效率的因素进行了优化。本方法前处理具有操作简单、有机溶剂用量少、萃取时间短等优点。方法在10.0~500 μg/L范围内,相关系数均达0.999以上,检出限为0.7~1.8 μg/L,同时具有较好的精密度和准确度。对实际样品加标的相对标准偏差为1.6%~9.7%,回收率为72.0%~115%,表明该方法适用于环境水样中多氯联苯的测定。

