氧糖剥夺/再灌注损伤小胶质细胞通过上调胸腺素β4影响PI3K/AKT信号通路*
熊娟 庞月珊 吴忧 任海波
(南充市中心医院 1.特需医疗科;2.老年科;3.神经外科,四川 南充 637000)
急性脑梗死在全世界都具有较高发病率、高致残率和高死亡率。急性脑缺血发生后,脑中血管神经单元受到损伤,及时恢复脑血流是目前主要治疗措施之一,但可能诱发缺血/再灌注损伤。缺血再灌注损伤后小胶质细胞迅速活化,可释放炎性介质及细胞因子再次损伤脑组织[1]。活化的小胶质细胞同样在血管生成中起着重要的作用[2],但研究小胶质细胞对脑血管的影响较少。Tβ4是由43个氨基酸构成的多肽具有广泛的生物活性,包括神经保护[3],诱导中枢和外周神经系统的血管生成[4]。研究显示外源性Tβ4可通过PI3K/AKT/eNOS信号通路刺激内皮祖细胞定向迁移[5],在急性和慢性缺血模型中对内皮祖细胞都起到保护作用[6]。PI3K/AKT信号通路是血管新生重要的信号通路,其激活后可以上调下游的mTOR、eNOS、HIF1α和VEGF等表达促进血管新生[7-10]。PI3K/AKT通路在中枢神经系统损伤和修复中起到核心作用。全脑缺血后小胶质细胞高表达Tβ4[11],且Tβ4与PI3K/AKT通路相关[5, 12-13],胶质源性的Tβ4是否通过PI3K/AKT通路参与局灶脑缺血/再灌注损伤后的修复尚不清楚。本研究旨在探讨缺血再灌注/损伤后小胶质细胞中Tβ4的表达变化及其对PI3K/AKT通路的影响。
1 材料与方法
1.1 实验动物 21只成年雄性SPF级SD大鼠,体重(200±20) g (上海西普尔-必凯实验动物有限公司,动物许可证号:SCXK(沪)20130016)。大鼠被饲养在特定的无病原体的条件下,自由获得食物和水。动物实验获得四川省实验动物学会伦理委员会批准(2021-05),并按照动物实验机构指导原则进行。
1.2 局灶脑缺血/再灌注损伤模型、细胞氧糖剥脱/再灌注损伤模型 参考文献制作局灶脑I/R模型[14],动物随机分为假手术组(Sham组)(n=6)、模型组(I/R组)(n=15)。先用3.5%水合氯醛(1 mL/100 g)腹腔注射麻醉大鼠。取仰卧位,备皮消毒后沿颈正中线切开皮肤2~3 cm,钝性分离皮下组织及右侧颈总、颈内、颈外动脉。用丝线暂结扎颈外动脉,经总动脉,并在颈总动脉远端置线并打结,便于固定栓线。夹闭颈内动脉,用眼科剪在颈总动脉两个绑线间剪个小口,插入栓线,打开夹闭颈内动脉的动脉夹,栓线插入到距离颈内、颈外分叉口18~20 mm处,直到出现轻微阻力,表明大脑前动脉和大脑中动脉起源处被阻断,消毒缝合切口并置于37℃恒温实验台上,直至苏醒。缺血2 h后,轻轻向外提拉线栓10 mm,实现再灌注。假手术组织切开钝性分离,不结扎血管和植入线栓。行为测试参照Zea-longa评分法[14]评价模型是否成功,9只成模大鼠再灌注后分别于24(I 2 h/R 24 h)、48(I 2 h/R 48 h)、72 h(I 2 h/R 72 h)麻醉处死大鼠取脑进行后续实验(n=3)。OGD/R模型是根据文献[15]制作,将制备好的BV2细胞(购于中国典型培养物保藏中心细胞共享平台)6×105/mL接种于无血清无糖DMEM培养基中并置于 1% O2、5% CO2、94% N2的三气培养箱中分别孵育2、4、6 h;再灌注时,首先去掉无血清无糖的 DMEM 培养基,再加入含10%血清的DMEM F12胶质细胞培养基中,分别在24、48、72 h进行检测。
1.3 Tβ4 shRNA转染 使用转染效率较高的Tβ4 shRNA序列:正义链5′-GGTTGGATCAAGTTTAA AT-3,反义链 5′-ATTTAAACTTGATCCAACC-3′。对照shRNA由一个混乱的序列组成,不能针对任何已知的细胞mRNA。免疫荧光分析评价检测基因干扰后Tβ4表达,然后将细胞用于OGD/R造模。分为对照组、OGD/R组、shRNA Tβ4+Control组、shRNA Tβ4+OGD/R组、Control shRNA+Control组、Control shRNA+OGD/R组。对照组细胞置于含10%血清的DMEM F12胶质细胞培养基中37℃、5% CO2培养箱中培养。
1.4 蛋白免疫印迹实验 使用添加蛋白酶和磷酸酶抑制剂RIPA裂液提取细胞蛋白。采用BCA法测定蛋白质浓度,蛋白变性,并按50 ug/孔标准向12%的SDS-PAGE分离胶加入样本并进行电泳1 h,转膜45 min。脱脂奶粉封闭 2 h,洗膜后与稀释的兔抗AKT、兔抗磷酸化AKT (Ser473)、兔抗PI3K、兔抗磷酸化PI3K (1∶800,CST)和小鼠抗β-actin(1∶1000,碧云天生物技术公司)一抗共孵育4℃过夜;复温1 h,洗膜后与辣根-过氧化物酶标记二抗(碧云天生物技术公司)室温孵育 1 h。膜上滴加ECL曝光液,在Bio-Rad仪对条带进行扫描并使用“Quantity one”软件分析。
1.5 细胞免疫荧光、免疫组化实验 细胞免疫荧光:去掉培养基,加入4%多聚甲醛固定10~15 min,使用PBS反复清洗3次清洗后加入Tβ4一抗4℃孵育过夜(1∶400, SANTA CRUZ), 复温1 h,洗涤后使用山羊抗小鼠FITC抗体(1∶1000,碧云天生物技术公司)避光室温孵育2 h, DAPI染核色(100 ng/mL) 10 min,最后显微镜荧光显微镜成像。免疫组织化学:将大鼠麻醉后经心脏灌注生理盐,再灌注4%多聚甲醛,取大脑经过固定、脱水后石蜡包埋。将病变部位大脑切成6 μm厚的切片。经常规脱蜡水化,室温用3%双氧水作用10 min灭活内源性过氧化物酶。将Tβ4抗体按1∶200稀释,4℃孵育过夜,洗涤后脱脂奶粉封闭2 h,再次洗涤后加入HRP标记的二抗,室温静置30 min,加DAB显色液,显色5~10 min,用苏木精复染2 min,乙醇分化、脱水、透明,树脂胶封片。OLYMPUS PM20显微镜和TCFY-2050病理系统下观察和成像。使用ImageJ对免疫组化图片和免疫荧光图片进行量化。
1.6 统计学分析 使用GraphPad Prism 9.1软件进行数据分析并做统计图,两两比较采用Unpairedttest检验。以P<0.05为差异有统计学意义。
2 结果
2.1 I/R损伤后大脑皮质Tβ4表达水平升高 免疫组化检测脑组织中Tβ4的表达结果显示,与假手术相比,大鼠局灶性脑缺血/再灌注的24、48、72 h大脑皮层均有Tβ4表达增多,根据细胞形态可初步推断Tβ4在神经元和胶质细胞高表达,梗塞部位以及梗塞周围Tβ4的表达以胶质细胞为主(图1A)。对免疫组化进行平均光密度值统计分析发现,与Sham组比较,I 2 h/R 48 h Tβ4表达水平显著升高 (P< 0.0001),见图1B。
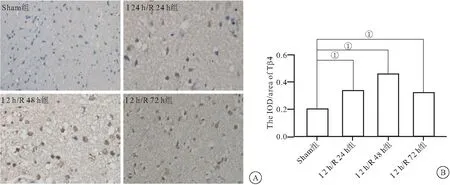
图1 局灶脑缺血2 h/再灌注24、48、72 hTβ4表达情况 Figure 1 The expression of Tβ4 at focal cerebral ischemia 2h/reperfusion 24, 48, 72 h注:A.各组大鼠脑皮质Tβ4表达情况(标尺=50 μm);B.各组平均光密度值。与Sham组比较,①P<0.05
2.2 BV2细胞在氧糖剥夺/再灌注损伤后高表达Tβ4 免疫荧光法检测BV2细胞OGD/R损伤后Tβ4蛋白的表达结果显示,与对照组相比,氧糖剥夺2、4、6 h复氧48 h组Tβ4表达较多, 其中OGD 6 h/ R 48 h组表达最多(P<0.0001)。OGD 2 h/R 72 h和OGD 4 h/ 24 h组与对照组比较差异无统计学意义(P>0.05)。OGD 2 h、OGD 4 h和OGD 6 h组Tβ4都是再灌注后48 h达到峰值,表明Tβ4蛋白表达与氧糖剥夺/再灌注的时间有一定的相关性。见图2。故我们选择在该实验中Tβ4表达相对较多的OGD 6 h/R 48 h组进行后续干预实验。
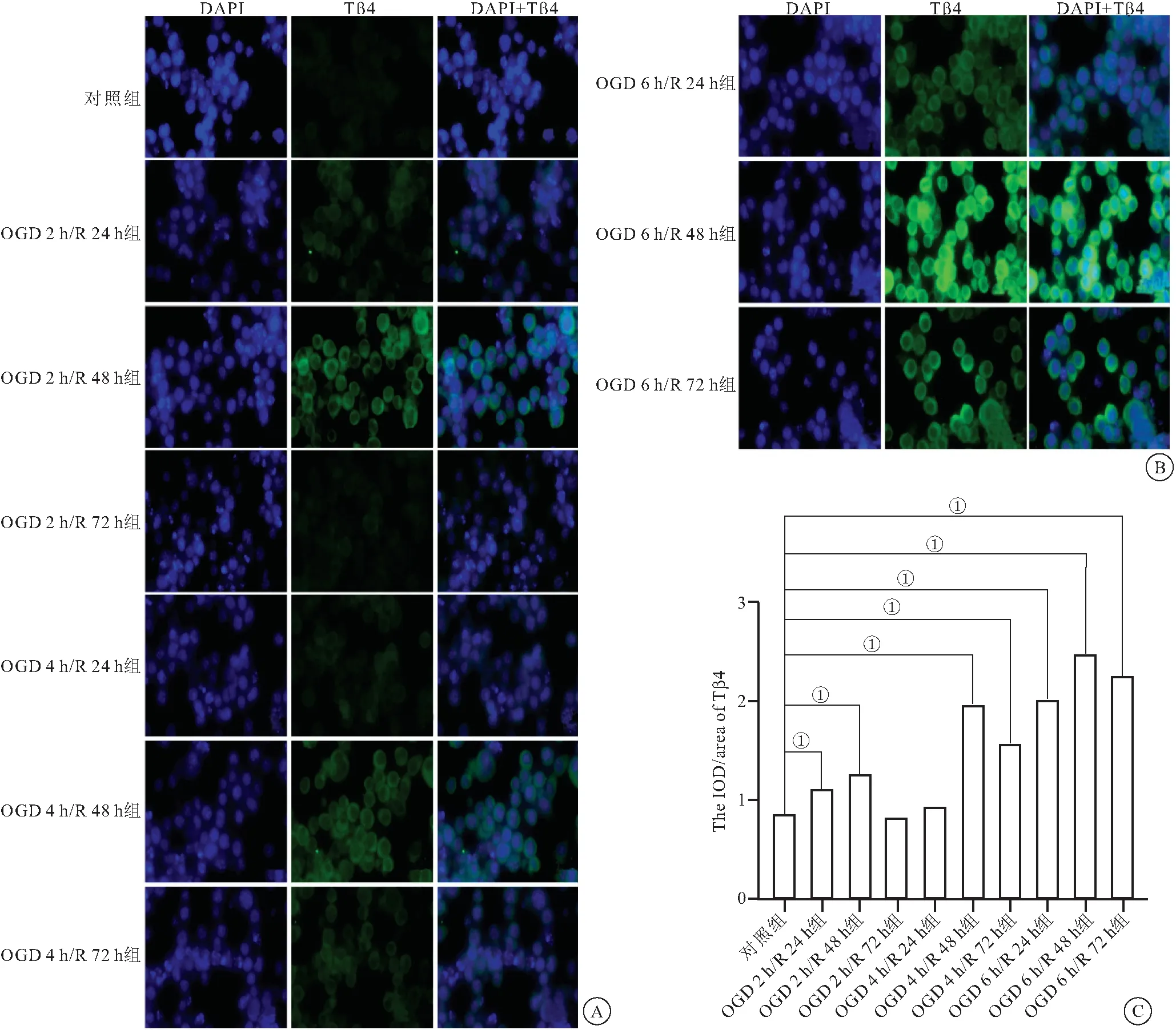
图2 Tβ4在不同组的BV2细胞中表达Figure 2 The expression of Tβ4 in BV2 cells in different groups 注:A、B为Tβ4免疫荧光染色(标尺=50 μm);C.平均光密度。与对照组比较,①P < 0.05
2.3 BV2细胞表达的Tβ4调节PI3K/AKT信号通路表达 为了验证BV2表达的Tβ4对PI3K/AKT通路的影响,我们选择在该研究中Tβ4表达相对较多的OGD 6 h/R 48 h组进行干扰。结果显示,使用shRNA Tβ4干扰BV2 细胞在进行氧糖剥夺/再灌注实验,其中Tβ4蛋白表达明显下降,差异具有统计学意义(P<0.05),见图3A、B。使用对照序列转染组与OGD 6 h/R 48 h组比较,差异无统计学意义(P>0.05)。同时使用WB方法检测PI3K/AKT通路蛋白表达发现,与对照组相比,OGD 6 h/R 48 h组p-PI3K/PI3K比值显著升高(P<0.05),而Tβ4 shRNA OGD 6 h/R 48 h组的p-PI3K/PI3K比值较OGD 6 h/R 48 h组明显降低(P<0.05),见图3C、D。与对照组相比较,OGD 6 h/R 48 h组p-AKT/AKT比值较高(P<0.05),但Tβ4 shRNA干预后,降低了p-AKT/AKT比值(P<0.05),见图3E。结果表明,BV2细胞在OGD/R损伤后高表达的Tβ4可能调控PI3K/AKT信号通路。
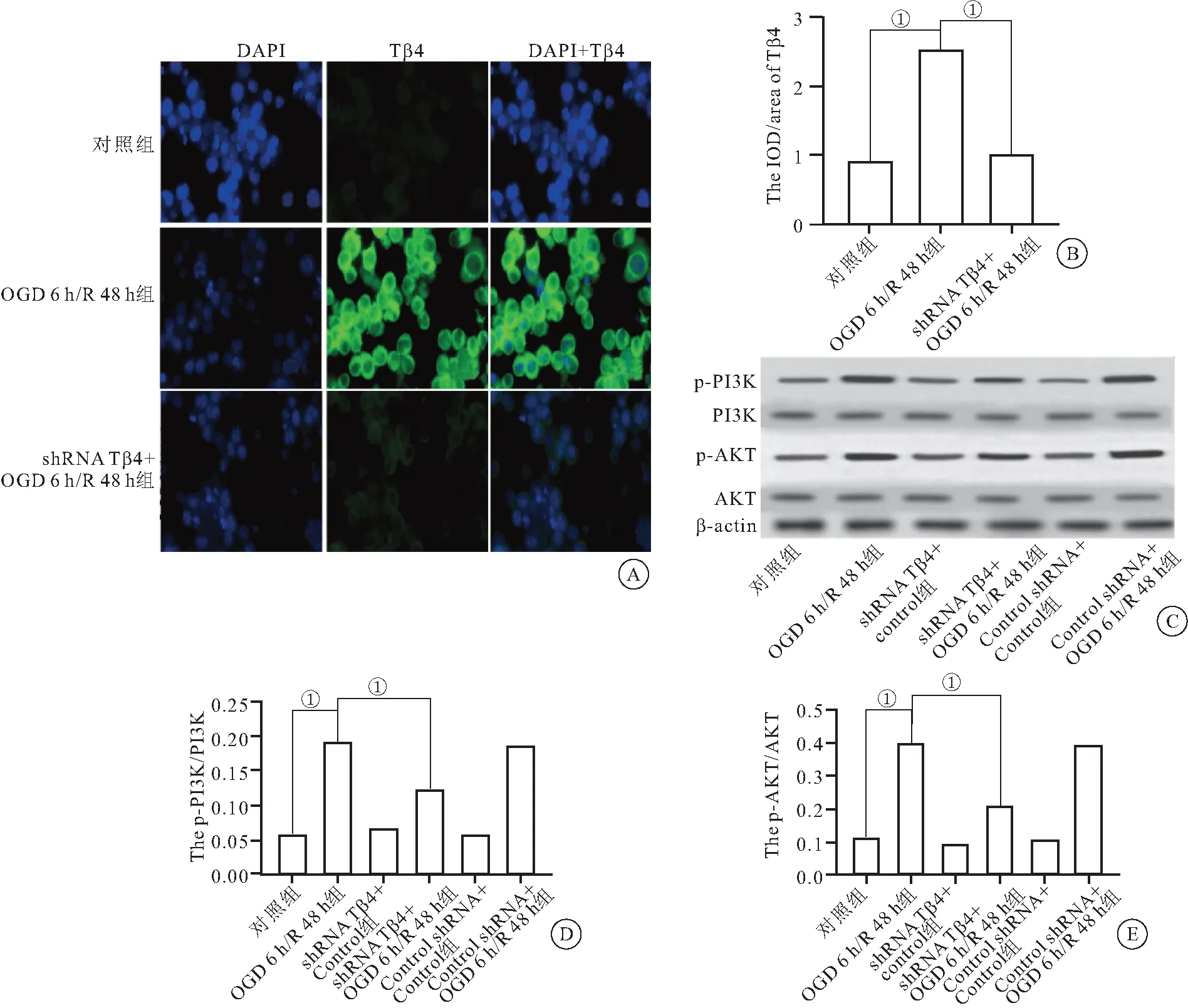
图3 BV2细胞表达的Tβ4 对PI3K/AKT 通路影响Figure 3 The effect of Tβ4 expressed in BV2 on PI3K/AKT pathway注:A、B为Tβ4基因干扰后Tβ4蛋白表达情况及平均光密度值(标尺=50 μm);C.WB检测p-AKT、 AKT、p-PI3K、PI3K、β-actin表达;D、E分别为p-AKT/AKT、p-PI3K/PI3K统计分析。与对照组比较,①P<0.05
3 讨论
小胶质细胞是中枢神经系统的巨噬细胞,可参与免疫调节[16]和脑组织发育[17]。传统上认为小胶质细胞的活化在缺血性脑卒中是有害的,抑制小胶质细胞活化治疗脑卒中的方法得到广泛研究。然而,越来越多的证据表明,小胶质细胞的激活对神经发生、血管生成和突触重塑也至关重要,促进脑缺血后的功能恢复[18]。目前小胶质细胞对卒中后血管生成的影响已经成为研究热点[18-20]。Kubota等[21]研究显示在缺失小胶质细胞的小鼠视网膜中,血管的分支明显减少。Ding等[2]认为活化的小胶质细胞可导致内皮细胞紧密连接破坏,同时促进内皮生长因子分泌促进新生血管的形成。Zhu等[19]研究也发现小檗碱通过AMPK信号通路调节小胶质细胞极化促短暂性大脑中动脉闭塞模型血管生成。
局灶脑缺血/再灌注损伤后,在脑缺血区域周围有小胶质细胞增多[22],但该区域小胶质细胞与血管生成的关系尚不清楚。Tian等[23]观察到BV2小胶质细胞显著促进毛细血管样管形成和脑微血管内皮细胞迁移,并且这种作用与酪氨酸蛋白激酶A相关。在本研究中,我们发现局灶脑缺血/再灌注损伤后位于大脑皮质区周围区域的小胶质细胞Tβ4水平较高,尤其是在I 2 h/R 48 h组,同时我们体外实验证实BV2细胞在OGT/R造模后同样有Tβ4高表达。使用shRNA 干扰Tβ4表达后,p-PI3K、p-Akt表达也相应减少,但PI3K/AKT通路的表达并未完全受到抑制,说明Tβ4不是缺血/再灌注损伤后影响PI3K/AKT通路的唯一因子。Kim等[24]也观察到全脑缺血后可诱导海马齿状回小胶质细胞Tβ4高表达,与本研究结果相似。综上可知,脑缺血再灌注损伤后小胶质细胞有Tβ4表达,并且可能参与PI3K/AKT通路调节。
PI3K/AKT信号通路是调节内皮细胞生存能力及血管再生的关键通路[25-26],也是参与局灶脑缺血/再灌注损伤修复的关键通路。Trenkwalder等[13]研究发现,肌肉注射Tβ4治疗14 d,血管生成增加,且与PI3K/AKT通路相关。此外,另一项研究也表明Tβ4可以通过激活AKT/eNOS促进血管生成[27]。Tβ4激活PI3K/AKT通路后,可调控eNOS表达,进而刺激内皮祖细胞的定向迁移和分化[5,12,27]。研究显示Tβ4不仅能增强内皮祖细胞的活力、血管生成能力和迁移能力,还能使内皮祖细胞高表达血管内皮生长因子A、血管紧张素及血管生成素受体促进血管生成[28]。Tβ4也能通过激活内皮蛋白水解系统,抑制内皮细胞粘附,促进内皮细胞的迁移和毛细血管形成[29]。综上,我们推测局灶脑缺血/再灌注损伤后小胶质细胞高表达Tβ4也可能通过调节PI3K/AKT信号通路影响血管生成,促进局灶脑缺血/再灌注损伤的修复。接下来我们将进一步研究Tβ4对PI3K/AKT通路下游信号因子及血管生成的影响,进一步揭示小胶质细胞对局灶脑缺血/再灌注损伤后血管生成的影响机制。
4 结论
局灶脑缺血/再灌注损伤后,大脑皮质小胶质细胞高表达Tβ4,并且小胶质细胞高表达的Tβ4可能通过PI3K/AKT影响脑缺血/再灌注损伤的修复。

