硫酸镍钴锰溶液中除氟工艺研究①
陈 亮
(湖南长远锂科股份有限公司,湖南 长沙 410205)
近年来,新能源汽车行业快速发展。高镍三元材料已成为主流动力电池正极材料[1],不久将有大批量高镍三元电池报废,对报废后的三元电池进行回收有利于镍钴锰锂等资源循环利用。从废旧动力电池回收镍钴锰的过程中,因前处理过程中存在正极粉与集流体分离不彻底,以及收集、存储、运输过程造成的污染等问题,在湿法提取镍钴锰时浸出液中存在铜、铁、铝、钙、镁等杂质离子。目前,除钙、镁的方法有溶剂萃取法和化学沉淀法。溶剂萃取法除钙镁工艺通常采用P204萃取除钙和P507萃取除镁[2-7],该工艺具有产品品质好的优点,产出的硫酸镍、硫酸钴及硫酸锰可直接用于合成三元前驱体,但存在工艺流程长、投资大、生产成本高、废水量多等问题;化学沉淀法工艺采用氟化物与钙、镁离子生成难溶氟化物沉淀[8-10],然后过滤除去杂质离子,该工艺无需将镍钴锰单独分离回收,工艺流程短、投资少、生产成本低,但采用氟化物除钙、镁过程中会引入大量氟,影响前驱体品质,对设备腐蚀较大,后续废水处理成本较高。
本文采用Al2(SO4)3·18H2O从镍钴锰溶液中除氟,该工艺是一种经济环保的除氟工艺:解决了化学沉淀法除钙、镁时溶液中含氟高的问题;除氟过程中不引入其他金属杂质;镍钴锰损失率较低;氟进入沉淀渣中,可有效解决氟对设备的腐蚀问题,避免了含氟废水的产生;除氟后的镍钴锰溶液可直接作为前驱体生产的原材料。整个工艺简单,能耗低,有价金属损失率低,有助于提升企业效益,具有良好的工业应用前景。
1 实 验
1.1 实验材料
实验原液为废旧三元锂离子电池硫酸浸出除钙、镁后液,其主要化学成分如表1所示。除氟剂为山东蓝鼎生产的Al2(SO4)3·18H2O,其铝含量为8.5%。反应过程中用1 mol/L氢氧化钠溶液调节反应pH值。

表1 实验原液组成 g/L
1.2 实验原理与方法
Al2(SO4)3·18H2O是一种经济实用、效果良好的混凝除氟剂,在许多国家和地区广泛使用。Al2(SO4)3·18H2O混凝除氟过程包括多个化学反应和物理过程,影响除氟效果的因素也很多。Al2(SO4)3·18H2O水解的主要产物是Al(OH)3溶胶,研究表明,在30 h之内,这种溶胶可基本保持凝絮状态。采用硫酸铝除氟可能存在以下3种机理[11-13]:

式(1)为化学反应,F-与加入的Al3+发生反应形成沉淀物,除去氟离子;式(2)为物理吸附,铝盐高价阳离子水解产物通过静电作用吸附废水中的F-;式(3)生成配位体,F-与Al3+形成络合物AlFx3-x,夹杂在硫酸铝的水解产物Al(OH)3中沉降下来。
取一定量的镍钴锰溶液加入三口烧瓶中,将烧瓶置于水浴锅中加热到设定温度,加入液碱调节反应初始pH值至设定值后加入一定量Al2(SO4)3·18H2O,搅拌反应一段时间,反应过程需加入液碱以维持初始pH值稳定。反应完成后,过滤得到除氟后液,除氟渣用纯水淋洗后烘干。分别分析除氟后液及除氟渣中氟、铝、镍、钴、锰含量,按渣计算镍、钴、锰损失率,其中金属损失率为镍钴锰总损失率。
1.3 分析方法
采用电感耦合原子发射光谱仪(Thermo,iCAP7200)分析Ni、Co、Mn、Al含量;采用氟离子选择电极法(雷磁,PHS-3C)分析F含量。
2 实验结果与讨论
2.1 反应初始pH值对除氟效果的影响
反应时间120 min、反应温度40℃、氟铝物质的量比为4,反应初始pH值对除氟效果的影响如图1所示。

图1 反应初始pH值对除氟效果的影响
由图1(a)可知,溶液中氟浓度随着反应初始pH值增大先降低后升高,在pH值为5.5时,溶液中氟浓度降至最低,为103.98 mg/L;溶液中铝浓度随着pH值升高而逐渐降低,当pH值为6.0时,铝浓度最低,为9.16 mg/L。由图1(b)可知,pH值4.5~5.5范围内,溶液中金属损失率随着pH值增大缓慢升高,继续升高pH值,溶液中金属损失率迅速升高;镍损失率随着pH值增大而逐渐升高。pH值大于6.0后,溶液中镍、钴、锰3种金属都会开始生成相应的氢氧化物沉淀,金属损失率会升高,所以pH值不宜过高。为了保证溶液中铝、氟浓度较低,同时降低金属损失率,综合考虑,选择反应初始pH值为5.5。
2.2 Al2(SO4)3·18H2O加入量对除氟效果的影响
反应初始pH值5.5,其他条件不变,Al2(SO4)3·18H2O加入量对除氟效果的影响如图2所示。
由图2(a)可知,Al2(SO4)3·18H2O加入量分别为7.6 g和9.1 g时,溶液中氟浓度均在120 mg/L以下,溶液中铝浓度均在20 mg/L以下,说明除氟效果较好且引入的铝不需要进一步脱除。由图2(b)可知,金属总损失率及镍损失率都随Al2(SO4)3·18H2O加入量增加先减小后增大,最低点出现在加入量7.6 g时。综合考虑,Al2(SO4)3·18H2O加入量为7.6 g比较合适,此时氟铝物质的量比为5。

图2 Al2(SO4)3·18H2O加入量对除氟效果的影响
2.3 反应温度对除氟效果的影响
氟铝物质的量比为5,其他条件不变,反应温度对除氟效果的影响如图3所示。
由图3(a)可知,随着反应温度升高,溶液中氟浓度逐渐降低,溶液中铝浓度逐渐升高。从图3(b)可知,溶液中金属损失率及镍损失率都随反应温度升高先增大后减少再增大,在反应温度60℃时,金属损失率及镍损失率达到最大,说明温度越高,金属越容易损失。综合考虑,适宜的反应温度为40℃。

图3 反应温度对除氟效果的影响
2.4 反应时间对除氟效果的影响
反应温度40℃,其他条件不变,反应时间对除氟效果的影响如图4所示。
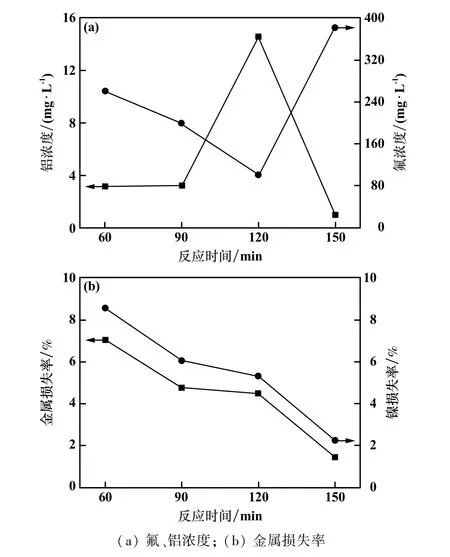
图4 反应时间对除氟效果的影响
由图4(a)可知,反应时间对溶液中铝浓度影响不大,尽管在120 min时出现一个高峰,但对应的铝浓度仅14.58 mg/L;反应时间对溶液中氟浓度影响较大,反应时间120 min时,溶液中氟浓度最低,为100.21 mg/L。由图4(b)可知,反应时间对金属损失率和镍损失率影响较大,其变化趋势相似,均随反应时间增加而降低,反应时间150 min时两者损失率均最低。为了保证溶液中除氟比较干净、同时减少溶液中金属的损失,反应时间选择120 min。
2.5 综合实验
通过除氟单因素实验,综合考虑经济、能耗等因素,选择除氟工艺条件为:反应初始pH值5.5、氟铝物质的量比为5、反应温度40℃、反应120 min,在该条件下进行了综合实验,结果如表2所示。

表2 综合实验结果
由表2可知,在该工艺条件下,溶液中氟、铝浓度分别为130.32 mg/L、8.71 mg/L;溶液中金属损失率为4.90%。说明在该工艺条件下,以Al2(SO4)3·18H2O为沉淀剂除氟效果较好,无需再次除铝,且金属损失率较低。
3 结 论
1)采用Al2(SO4)3·18H2O从硫酸镍钴锰溶液中除氟是可行的,该工艺流程较短、技术可行、除氟效果好。
2)Al2(SO4)3·18H2O除氟的适宜条件为:反应温度40℃、反应时间120 min、反应初始pH值5.5、氟铝物质的量比为5,此条件下除氟后溶液中氟离子浓度从初始的3.22 g/L降至130.32 mg/L,引入的铝离子浓度为8.71 mg/L,镍钴锰金属总损失率为4.90%。

