以废旧NCM523型电池正极材料浸出液制备NiCo2O4和Li2CO3研究①
王子钰,王碧侠,李存刚,汪 攀,李 磊,李卓阳
(西安建筑科技大学 冶金工程学院,陕西 西安 710055)
锂离子电池因绿色环保、能量密度高、环境适应性强而得到广泛应用[1-2],随之而来是产生大量废旧电池[3]。废旧电池正极材料中含有丰富的Ni、Co[4-5],是重要的二次资源。目前多采用湿法冶金工艺从废旧锂离子电池材料中回收有价金属,即电极材料经酸浸、再对酸浸液除杂后从中回收相应金属[6-7]。
超级电容器作为近年来发现的新型储能设备,因其良好的循环性能和充放电性能备受关注,清洁、高效的能源储存系统为解决能源快速消耗和自然环境恶化这两大问题提供了方案[8-9]。其中储能性能与电极材料密切相关,在众多电极材料中,三元金属氧化物NiCo2O4同时具备Ni2+和Co2+,活性位点数量多、活性强,因此电导率远高于单元金属氧化物Co3O4和NiO,且毒性低、耐腐蚀性强,成为研究热点[10]。制备NiCo2O4大多采用液相法,包括共沉淀法[11]、水热法[12]、电沉积法[13]和溶胶-凝胶法[14]等。相比于其他方法,水热法通过高压促进离子水解等反应,具有操作简单、易控制、成本低、产物纯度高、节能环保等优势[15-16]。
本文首次将废旧锂离子电池正极材料的湿法回收与电极材料NiCo2O4的水热合成相结合,避免复杂的金属离子分离操作,实现Ni、Co的高效回收及循环利用。在前期工作基础上[17],针对NCM523型废旧锂离子电池正极材料硫酸浸出液,采用水热-煅烧法制备NiCo2O4材料。由于C2O4-的络合能力强,可与Ni2+、Co2+形成草酸盐沉淀,且不与Li+发生沉淀络合反应,因此以草酸为沉淀剂,考察了表面活性剂种类及水热、煅烧条件对产物形貌的影响,以期为废旧锂离子电池正极材料中Ni、Co的高效回收提供参考。
1 实验部分
1.1 实验原料与设备
NCM523型废旧锂离子电池正极材料硫酸浸出液经KMnO4沉淀法去除Mn2+,所得溶液即为本实验主要原料,其主要元素组成见表1。
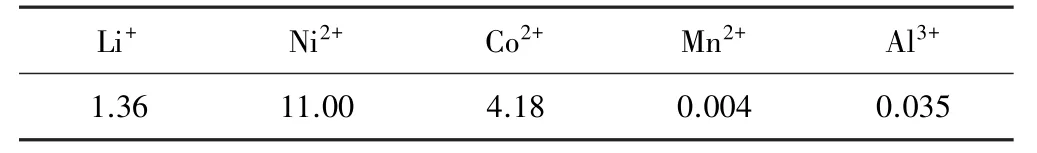
表1 NCM523型电池正极材料硫酸浸出液组成 g/L
实验试剂包括硫酸镍、硫酸钴、草酸、无水乙醇、碳酸钠、聚乙二醇2000(PEG-2000)、聚乙烯吡咯烷酮(PVP)、柠檬酸钠、十六烷基三甲基溴化铵(CTAB)、六次甲基四胺(HMT)等,均为分析纯;实验用水为自制蒸馏水。
实验设备包括SPJX-4-13型马弗炉、101-2AB型恒温干燥箱、SHZ-D型循环水真空泵、JJ-1型精密增力电动搅拌器、100-3型反应釜。
1.2 实验原理与方法
室温下,按Ni、Co化学计量比1∶2在50 mL浸出液中补加NiSO4·6H2O和CoSO4·7H2O,搅拌均匀后加入1.5 g表面活性剂,继续搅拌30 min后加入草酸15 g,混合均匀后在水热反应釜内于一定温度下反应一段时间。反应完成后,抽滤,分离出的固体沉淀即NiCo2O4前驱体。此前驱体经无水乙醇和去离子水(1∶3)混合液洗涤后,于60℃下干燥5 h,再经高温煅烧、研磨得到产物粉末;滤液经加热浓缩后以过量饱和Na2CO3溶液回收其中的Li+。
草酸电离出氢离子和草酸根离子,草酸根离子与镍、钴离子发生反应,生成不溶性的草酸盐沉淀,其反应方程式如下:
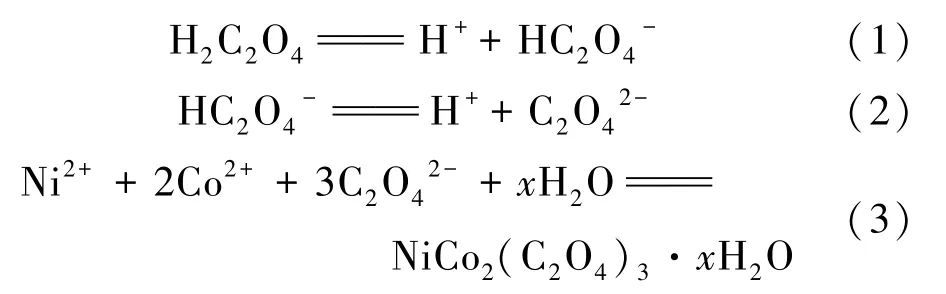
前驱体草酸盐沉淀在空气气氛下进行煅烧,变为尖晶石结构的NiCo2O4产物,其焙烧反应式如下:
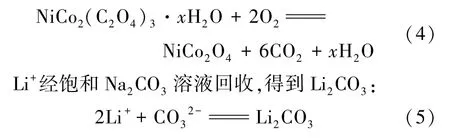
杂质Al3+与草酸溶液的反应吉布斯自由能随时间的变化如图1所示。由图1可知,137℃时,反应的吉布斯自由能为0,反应达到平衡,140℃时,反应的吉布斯自由能为-1.058 kJ/mol,且Al3+浓度为0.001 3 mol/L,反应可以忽略不计;杂质Mn2+在溶液中的浓度为0.000 07 mol/L,含量微小,且在最终产品NiCo2O4中并未检测出锰的存在,可忽略不计。
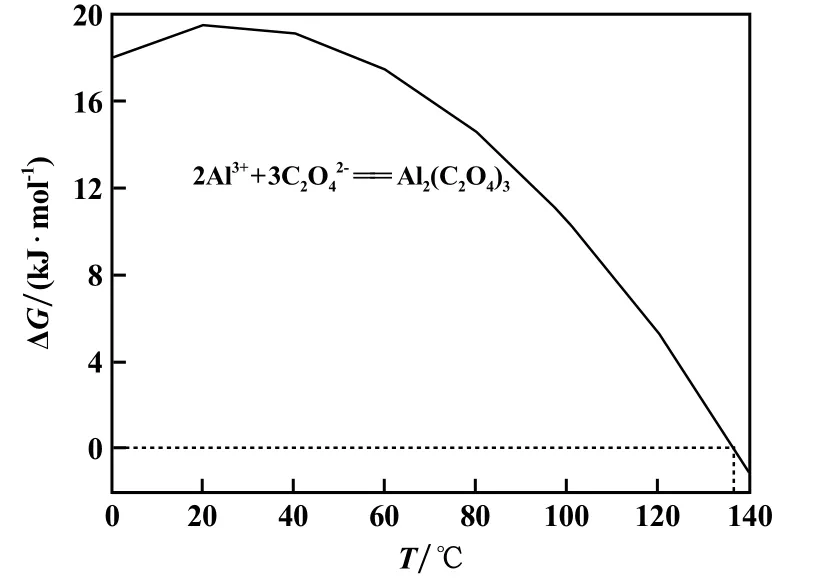
图1 Al3+与草酸溶液的反应吉布斯自由能随温度的变化
在水热反应过程中,通过添加表面活性剂PEG-2000、PVP、柠檬酸钠、CTAB和HMT对产物NiCo2O4的结构及形貌进行改善。PEG-2000是一种非离子型表面活性剂,也可以当作软模板剂,诱导晶体的定向排列及生长,在一定程度上可以防止团聚[18];PVP是一种水溶性高分子聚合物,同样属于非离子型表面活性剂,物理性能非常稳定,溶于水后无法电离,主要起到分散和吸附作用,在PVP分子结构中,吡咯烷酮基团具有亲水性,可与纳米颗粒表面作用,聚乙烯主链基团具有疏水性,作用于尾部基团,调整吸附头部基团之间的距离,可以作为稳定剂和结构导向剂[19];柠檬酸钠是一种阳离子表面活性剂,有较强的络合能力,控制调节产物的尺寸、形貌及结构;CTAB是一种阳离子表面活性剂,能有效降低水的表面张力,在溶液中水解电离出的CTA+阳离子与溶液中的阴离子形成离子对,晶核选择性地吸附在生长面上,有利于产物的均匀形成[20];HMT作为配体,表现出极大的多功能性,允许不同的配位模式,同时也是良好的氢键受体,使产物附着于HMT上,改善产物的框架结构[21]。
1.3 分析方法
采用电感耦合等离子体发射光谱仪(ICP-OES,型号Agilent 5110)分析浸出液中各金属元素含量,采用X射线衍射仪(XRD,型号D8 ADVANCE A25)和场发射扫描电子显微镜(SEM,型号Gemini SEM 300)分别分析产物的物相组成和微观形貌。
2 实验结果与讨论
2.1 表面活性剂种类对产物形貌的影响
在5组50 mL浸出液中分别加入PEG-2000、PVP、柠檬酸钠、CTAB和HMT,用量均为1.5 g,对照组不添加表面活性剂,以上混合液在160℃下水热反应4 h,所得前驱体在350℃下煅烧,表面活性剂种类对产物形貌的影响如图2所示。

图2 加入不同添加剂所得产物的SEM图
从图2可以看出,不添加表面活性剂时产物呈不规则块状团聚物,体积大且不均匀;添加PVP和柠檬酸钠对产物形貌影响不大,但颗粒团聚现象明显;添加PEG-2000和CTAB,产物分别呈链状与块状结构,产物形貌有一定改变,但颗粒大小不均且仍有小规模团聚现象;添加HMT,产物形貌呈相对均匀的条状结构,颗粒清晰且分散性较好。因为HMT分子为正四面体结构,包含4个N原子,每个N原子分别与3个亚甲基(CH2)相连接,N原子上带有孤对电子,可以选择性地吸附在产物的横向晶面上,降低产物表面能,使产物纵向生长[21]。后续实验选择HMT为表面活性剂。
对以HMT作添加剂时的回收产物进行XRD和EDS分析,结果如图3和图4所示,表2为产物的EDS元素分析结果。
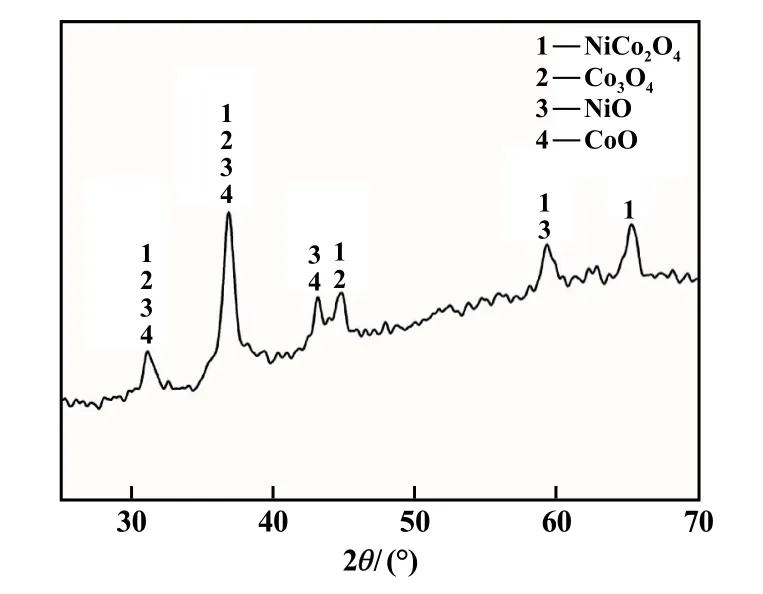
图3 HMT作添加剂时回收产物的XRD图谱
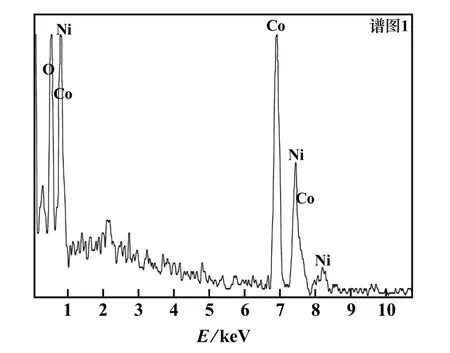
图4 HMT作添加剂时回收产物的EDS图谱
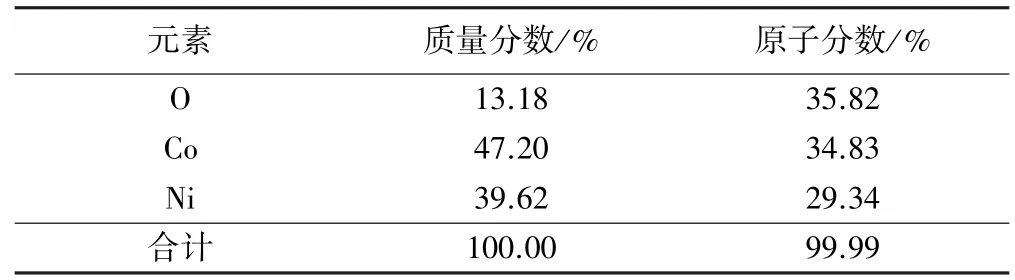
表2 采用HMT作添加剂时回收产物的元素EDS分析结果
由图3和图4可以看出,产物中除NiCo2O4外,也存在Co3O4、NiO和CoO等,NiCo2O4可看作是Ni元素取代了Co3O4中的部分Co元素[22]。由表2可以看出,产物中Ni、Co的原子分数比接近1∶1,推测是反应进行不完全、氧化物掺杂所致,同时可以看出,产物中只含有Ni、Co、O这3种元素,添加剂HMT并不会将杂质元素带入产物中。
2.2 水热温度对产物形貌的影响
以HMT为表面活性剂,加入量30 g/L,水热反应时间4 h,所得前驱体在350℃下煅烧,水热温度对产物形貌的影响如图5所示。

图5 不同水热温度下所得产物形貌
从图5看出,水热温度为100℃时,产物为大小不均匀的短棒颗粒,表面松散、粗糙,孔隙明显;温度升高至120℃时,表面孔隙有所改善,棒状颗粒变长;当温度升高至140℃时,颗粒表面相对光滑、致密,分散均匀;当温度升高至160℃和180℃时,棒状颗粒变短并团聚在一起。这是由于低温时分子的运动速率较慢,成核速率大于生长速率导致反应不完全;而随着水热温度升高,分子的热运动加快,其生长速率加快,水热反应更加彻底,晶体发育完全,尺寸变大;但温度过高,反应过快易形成过多晶核,生长时间不足,造成尺寸变小且团聚在一起。综合考虑,水热反应温度以140℃为宜。
2.3 水热反应时间对产物形貌的影响
水热反应温度140℃,其他条件不变,水热反应时间对产物形貌的影响如图6所示。

图6 不同水热时间下所得产物SEM
从图6可见,水热反应2 h和3 h,产物纵向生长不完全,有许多棒状大颗粒,即中间产物NiCo2(C2O4)2[23];水热时间延长至4 h,反应比较完全,产物形貌清晰均匀,按照表面活性剂HMT所调控的方向生长;水热时间延长至5 h和6 h时,棒状颗粒变粗,团聚现象明显,部分产物由于反应时间过长氧化成金属氧化物,导致杂相产生。综合考虑,选择水热反应时间4 h。
2.4 煅烧温度对产物NiCo2O4形貌的影响
水热反应时间4 h,其他条件不变,煅烧温度对产物形貌的影响如图7所示。

图7 不同煅烧温度下所得产物SEM
从图7看出,煅烧温度200℃时,产物团聚明显,有少量粗大的棒状颗粒出现;煅烧温度250℃时,产物大部分变为粗大的棒状颗粒,尺寸不均匀,这是因为煅烧温度过低,镍、钴草酸盐前驱体转换不完全[22];煅烧温度300℃时,产物由大小均一的棒条状颗粒组成,分散性较好,颗粒表面平滑;煅烧温度350℃时,产物形貌变化不大,但产物颗粒表面出现附着物;煅烧温度400℃时,产物变为大小不一的条状颗粒,且团聚现象明显,这是因为NiCo2O4的热稳定性低,焙烧温度过高,产物分解形成热衍生的NiO相[23]。选择焙烧温度
300℃。
对300℃下煅烧所得产物进行XRD和EDS分析,结果如图8~9所示,表3为产物的EDS元素分析结果。
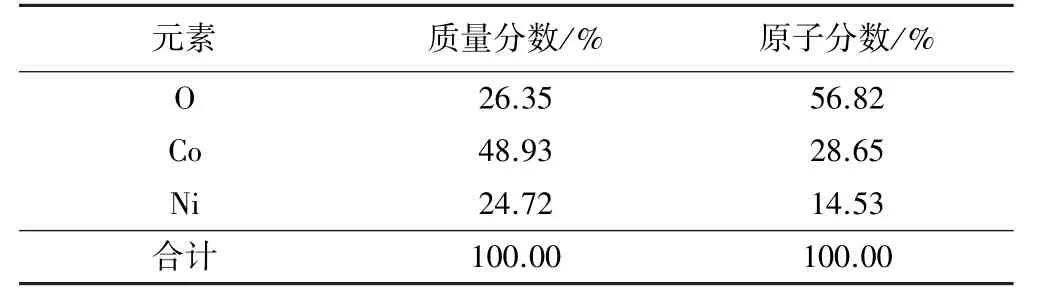
表3 煅烧产物EDS元素分析结果
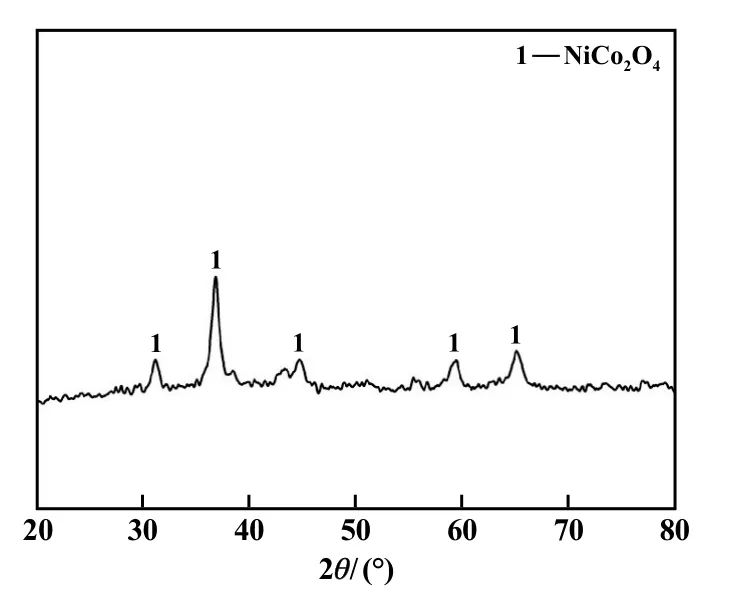
图8 煅烧产物XRD图谱
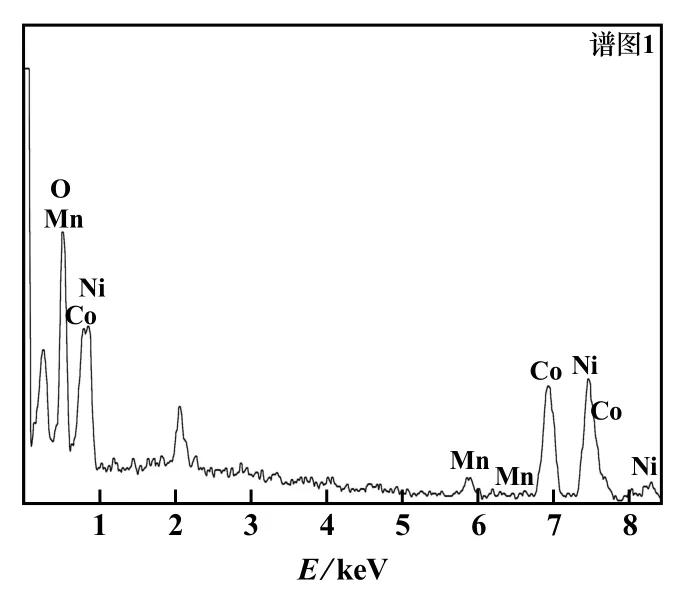
图9 煅烧产物EDS图谱
由图8和9可以看出:2θ为31.2°、36.8°、44.8°、59.0°、64.8°的5个衍射峰较高且尖锐,且与NiCo2O4标准卡片相一致,且EDS图谱中表明产物只含有Ni、Co、O这3种元素,EDS元素分析结果表明Ni和Co的原子分数比接近1∶2,表明所得产物为NiCo2O4。
2.5 锂的回收
对水热法制备NiCo2O4前驱体之后的母液加热浓缩,加入过量饱和Na2CO3溶液,控制溶液pH=7、温度80℃、搅拌时间2 h,通过沉淀回收溶液中锂,析出的沉淀经冷却、过滤、烘干,其SEM和XRD图谱分别如图10~11所示。

图10 沉淀法回收产物的SEM图谱
图10中,产物颗粒为大小不一的棒状结构,长度在10~50μm之间,结构较为清晰,分散均匀。图11衍射峰与标准PDF卡片相吻合,表明产物为Li2CO3;谱图中无杂峰出现,表明Li2CO3结晶度良好。
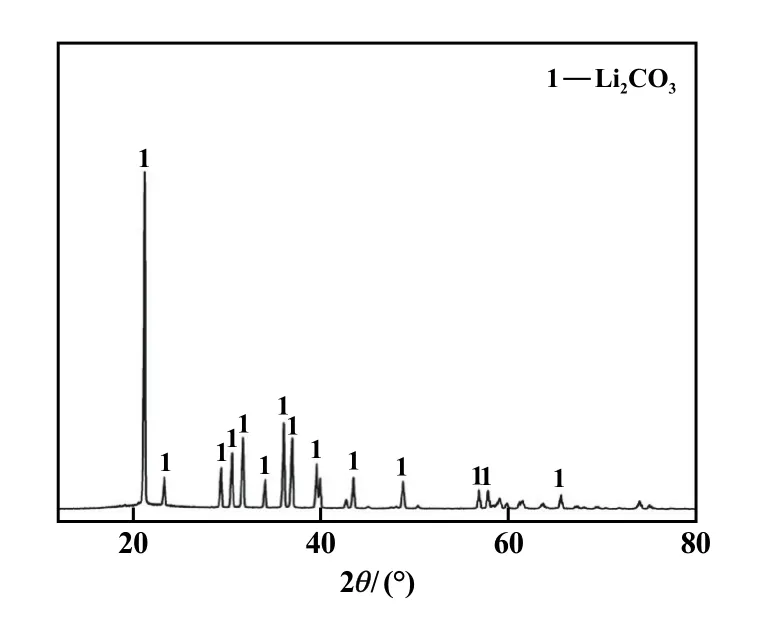
图11 沉淀法回收产物的XRD图谱
3 结 论
1)NCM523型锂离子电池正极材料的硫酸浸出液经除杂净化后,得到硫酸盐溶液,以草酸作沉淀剂(加入量30 g/L)、HMT作表面活性剂,在140℃下水热反应4 h得到前驱体草酸盐沉淀,再将沉淀产物在300℃下煅烧2 h,制得NiCo2O4,实现了Ni、Co的同步回收。
2)用Na2CO3沉淀法可将水热母液中的锂以Li2CO3形式初步回收。

