鸢尾糖基转移酶编码基因ItUGT349和ItUGT419克隆及特性研究
张李兵,李 静,陶无恙,黄梓璐,陈嘉杰,段礼新,季爱加
鸢尾糖基转移酶编码基因和克隆及特性研究
张李兵,李 静,陶无恙,黄梓璐,陈嘉杰,段礼新,季爱加*
广州中医药大学 中药学院国际中医药转化医学研究所,教育部中医药防治肿瘤转化医学研究国际合作联合实验室,广东 省中医药防治肿瘤转化药学研究重点实验室 广东 广州 510000
克隆获得鸢尾糖基转移酶基因和,并对其进行生物信息学分析、基因差异表达检测和蛋白原核表达等特性分析。以鸢尾转录组中筛选到的基因全长开放阅读框(open reading frame,ORF)设计特异性引物,进行PCR扩增,经测序后获得基因序列并进行生物信息学分析;通过荧光定量PCR(real-time PCR,qRT-PCR)进行基因差异表达检测;最后构建pET-32a(+)原核表达载体在大肠杆菌中表达蛋白。PCR扩增和的ORF长度分别为1461、1488 bp,编码蛋白相对分子质量大小分别为53 830、54 910。荧光定量PCR显示,的表达量在叶片中最高,而在花器官中表达最高。进化树表明,ItUGT419与三萜类糖基转移酶聚类在一起,ItUGT349与三萜、黄酮和木质素等多种类型的糖基转移酶聚类到一支。ItUGT349和ItUGT419在大肠杆菌中均成功的表达出可溶性蛋白。通过和基因全长ORF克隆,并对其进行序列分析,基因差异表达检测及原核表达等研究,为后续进一步鉴定其催化功能奠定基础。
鸢尾;糖基转移酶;基因克隆;生物信息学分析;原核表达;qRT-PCR
鸢尾科植物鸢尾Maxim.广泛分布于世界各地,具有悠久的民间用药历史,其主要化学成分黄酮类和三萜类化合物对多种疾病如癌症、炎症及病毒感染等均具有很好的疗效,具有极高的药用价值,《中国药典》2010年版正式将其收录[1]。目前已从鸢尾中分离出多种三萜及其皂苷类化合物,特别是一系列结构新颖的鸢尾醛型三萜,其结构特征在于一个多取代环己烷的C-11位上连有一个侧链,C-6位连有一个羟丙基可被糖基化[2];在抗肿瘤和抗癌方面表现出良好活性[3]。
糖基化是植物次生代谢过程中十分重要的一类化学反应;在尿苷二磷酸(UDP)依赖性糖基转移酶(UGTs)的作用下,将UDP活化的糖作为主要的供体分子转移到特定的受体分子,形成糖苷键,产生多种多样的糖苷类化合物[4]。被糖基化的化合物可显著提高水溶性、化学稳态以及转运能力等, 也能促进其在某些特定的植物细胞或组织中进行储存和积累[5]。植物中的UGTs是一个基因超家族,已在许多植物中被克隆和表征功能[6-8]。此外在模式植物拟南芥L.中,已经报道了120个基因[9];双子叶植物大豆L.中报道182个基因[10];单子叶植物水稻L.中有180个基因被报道[11]。由于UGTs家族成员众多,且催化底物复杂,其基因功能仍有许多未知。有研究指出,UGTs在C端均具有一个高度保守基序PSPG box(putative secondary plant glycosyl-transferase),该保守基序被认为是UDP-糖供体结合的区域;而在N端的序列变异则十分显著,其可能具有对萜类、黄酮类和甾体类等不同的底物进行选择性结合的功能[12-14]。
目前植物中关于催化三萜类化合物糖基化的糖基转移酶基因已有不少报道;如从王不留行中克隆的从燕麦中克隆的和从大豆中克隆的、、等;其编码糖基转移酶蛋白均可对三萜骨架或侧链进行糖基化修饰[15-17]。鸢尾中存在着众多结构新颖的三萜及皂苷类成分,但相关糖基转移酶的研究却未见报道。本研究通过对鸢尾转录组数据进行分析,筛选并克隆了2条糖基转移酶基因(和),并通过生物信息学分析、基因差异表达分析;推测其可能具有催化三萜类底物糖基化的功能。最后在大肠杆菌中进行了蛋白体外表达研究,为进一步鉴定其催化功能、解析鸢尾中三萜类成分生物合成途径奠定基础。
1 材料
本研究所用植物材料于2019年6月取自中国科学院植物研究所,经广州中医药大学中药学院季爱加副研究员鉴定为鸢尾Maxim.。选取生长年限2年,生长健壮,处于盛花期的鸢尾植物,各组织部位取材后立即置于液氮速冻,置于−80 ℃冰箱备用。
2 方法
2.1 RNA提取及反转录
采用液氮研磨法,使用植物总RNA提取试剂盒(北京兴华越洋生物科技有限公司)按试剂盒操作说明提取鸢尾各部位总RNA。将提取的总RNA 进行琼脂糖凝胶电泳检测,并使用核酸定量仪检测RNA浓度。参照TakaRa公司的PrimeScriptTMII 1stStrand cDNA Synthesis Kit(TakaRa公司,6210A)试剂盒中的操作说明合成cDNA链。
2.2 ItUGTs基因克隆
从鸢尾转录组数据中筛选到2条潜在的糖基转移酶基因,命名为和。根据其全长开放阅读框(open reading frame,ORF)序列,使用Vector NTI设计引物,引物由生工生物工程(上海)股份有限公司合成,引物序列信息见表1。以高保真酶Phanta Max Super-Fidelity DNA Polymerase(Vazyme,P505-d1)对候选基因片段进行PCR扩增反应,反应体系为2 ×Phanta Max Buffer 25 μL,dNTP Mix 1 μL,高保真酶1 μL,正反向引物各1 μL,cDNA模板1 μL,超纯水补足至50 μL。反应程序为95 ℃预变性3 min;然后95 ℃、15 s,57 ℃、15 s,72 ℃、90 s,32个循环;终延伸72 ℃,5 min。PCR产物经电泳、切胶回收纯化后连接pLB-T载体并转化至大肠杆菌DH5α感受态细胞中,涂布含氨苄抗性的LB固体平板;于37 ℃恒温培养箱中,暗培养12~15 h。挑取单菌落小摇5~6 h,进行菌液PCR阳性鉴定,将阳性菌液送至生工生物工程上海股份有限公司测序。
2.3 ItUGTs生物信息学分析
使用NCBI在线工具ORF Finder (https:// www.ncbi.nlm.nih.gov/orffinder)搜索和糖基转移酶基因序列的开放阅读框;经ProtParam(https://web.expasy.org/protparam/)网站获得预测蛋白的理化性质。通过CELLO v 2.5(http://cello.life.nctu.edu.tw/)获得蛋白亚细胞定位信息;利用在线工具SignalP-5.0(http://www. cbs.dtu.dk/ services/SignalP/)和TMHMM(http:// www. cbs. dtu. dk/ services/TMHMM/)预测蛋白信号肽和跨膜区。通过SOPMA(https://npsa- prabi.ibcp.fr/cgi-bin/secpred_sopma.pl)预测蛋白二级结构,再经SWISS-MODEL(https://swissmodel. expasy.org/ interactive)进行同源模建,获得蛋白的三维结构。通过NCBI-cdd(https://www.ncbi. nlm.nih.gov/cdd)在线工具和pfam(http:// pfam.xfam.org/)网站预测蛋白的结构域范围,利用DNAMAN软件进行序列比对。再使用MEGA 7.0软件构建系统发育进化树;已知功能糖基转移酶蛋白序列[14,18]从NCBI(https://www. ncbi.nlm.nih.gov/)数据库下载。

表1 引物序列
2.4 ItUGTs基因qRT-PCR分析
参照TakaRa公司的qRT-PCR反转录试剂盒(TakaRa公司,RR047A)中的操作说明合成cDNA链,用于qPCR反应的模板。参照艾科瑞生物公司的SYBR Green Pro Taq HS预混型qRT-PCR试剂盒说明书,使用QuantStudio 5实时荧光定量PCR仪进行检测,将鸢尾各组织部位cDNA稀释20倍作为qRT-PCR反应体系模板,以为内参基因(引物序列见表1);每个基因3个生物学重复,3个技术重复。反应体系10 μL:2×SYBR Green Pro Taq HS Premix,5.0 μL;正反向引物各0.2 μL;荧光染料0.2 μL;模板cDNA 1 μL;超纯水3.4 μL。反应条件:95 ℃,30 s;40个循环(95 ℃,5 s;64 ℃,34 s)。使用2−△△Ct法计算基因在不同组织部位中的相对表达量。使用IBM SPSS 2.0软件进行表达差异的统计分析,<0.01表示显著性差异。
2.5 ItUGTs基因原核表达
参照南京诺唯赞生物科技有限公司的快速重组克隆试剂盒(ClonExpress II)盒说明书对候选基因片段进行PCR扩增。扩增产物经胶回收纯化后,采用双酶切(EcoRI,XhoI)进行pET32a载体线性化,通过同源重组酶将二者重组,同源产物转化至大肠杆菌DH5α,涂布于含氨苄抗性的平板上,过夜培养(37 ℃),经菌液PCR鉴定,选取阳性菌液送测序,将测序正确的菌液活化,提取质粒,获得带目的基因的表达载体质粒。
通过热激法将重组质粒转入宿主菌BL21(DE3) 感受态,挑取阳性克隆菌于LB 液体培养基(含100 mg/L氨苄抗生素)中进行震荡培养,4~6 h后通过紫外分光光度计检测菌液密度至OD值为0.5~0.6时,加入终浓度0.1 mmol/L IPTG,18 ℃、180 r/min,诱导培养18 h。4 ℃、4000 r/min 离心10 min 收集菌体,弃上清。在菌体中加入20 mL的50 mmol/L Tris-HCl(pH 8.0)重悬菌体,蛋白破碎前加入1 mmol/L PMSF,超声破碎。4 ℃、12 000 r/min离心30 min,分离上清及沉淀。进行SDS-PAGE。
3 结果与分析
3.1 ItUGTs基因克隆
以1.0%琼脂糖凝胶电泳检测PCR扩增产物,可见和均为1条清晰条带(图1),片段大小在1500 bp左右,与预期大小相符。阳性克隆测序结果与转录组序列比对,结果一致。基因的ORF长度为1461 bp,编码486个氨基酸,命名为UGT707D1;基因的ORF长度为1488 bp,编码495个氨基酸,命名为UGT92N1。
3.2 ItUGTs的序列分析
3.2.1 ItUGTs蛋白理化性质 经ProtParam在线工具预测,ItUGT349和ItUGT419相对分子质量分
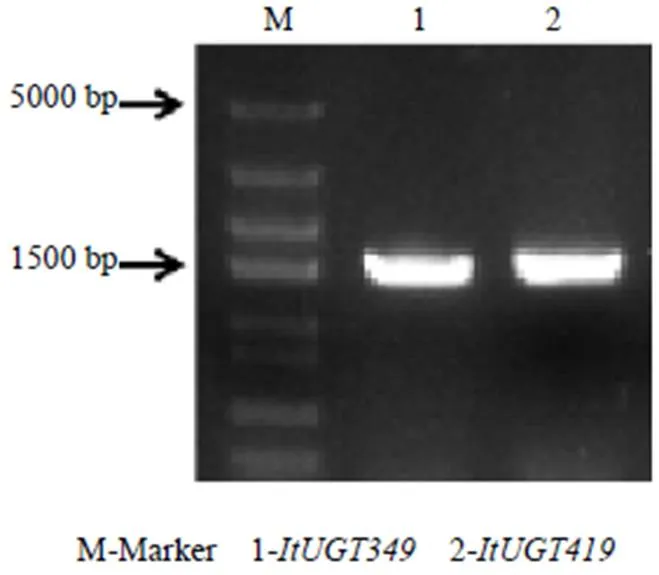
图1 PCR产物凝胶电泳图
别为53 830和54 910,理论等电点分别为4.94、4.92,不稳定系数为53.69、49.58,表明ItUGT349和ItUGT419均属于不稳定酸性蛋白。
3.2.2 ItUGTs跨膜区及信号肽分析 亚细胞定位预测表明,2个ItUGTs均定位于细胞质。通过在线工具TMHMM预测蛋白跨膜区,发现2个ItUGTs均不含有跨膜螺旋区(图2),为膜外蛋白。利用在线工具SignalP-5.0对ItUGTs进行信号肽预测,发现ItUGT349具有信号肽(图2),为分泌蛋白;ItUGT419不具有信号肽,为非分泌蛋白,二者可能具有不同的生物学功能。
3.2.3 ItUGTs蛋白二级结构及三维建模 二级结构分析表明,ItUGT349和ItUGT419均以α螺旋和无规卷曲为主要组成元件,其具体预测信息见表2。
使用在线工具SWISS-MODEL预测ItUGT349和ItUGT419蛋白三维结构。ItUGT349蛋白与蒺藜苜蓿三萜UDP-葡萄糖基转移酶(UGT71G1)具有42.70%的序列相似性,以该蛋白(PDB ID:2acw.1)A链[19]为模板,通过同源建模构建ItUGT349蛋白的三级结构,建模范围为2~485位氨基酸,全球性模型估测值(GMQE值)为0.68,三维建模质量良好(图3)。ItUGT419蛋白与美洲商陆糖基转移酶(UGT3)具有32.83%的序列相似性,以该蛋白(PDB ID:6lzx.1)A链[20]为模板,通过同源建模构建ItUGT419蛋白的三级结构,建模范围为4~488位氨基酸,GMQE值为0.67,三维建模质量良好。

A、B-ItUGTs跨膜区预测 C、D-ItUGTs信号肽分析

表2 ItUGTs蛋白二级结构预测
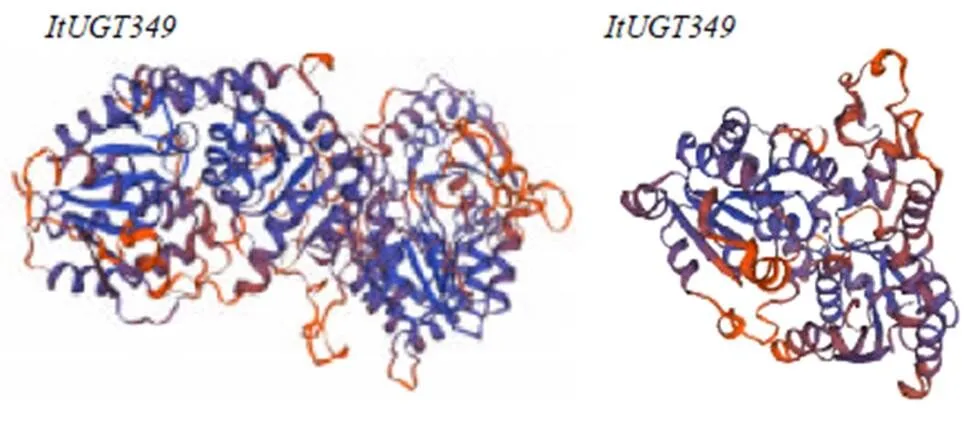
图3 鸢尾ItUGTs蛋白三级结构预测
3.3 ItUGTs的系统发育与结构域分析
根据糖基转移酶的底物催化特异性,将拟南芥、大豆、人参、蒺藜苜蓿、栀子等植物中已表征功能的糖基转移酶与ItUGT349和ItUGT419进行系统发育分析(图4)。结果显示,ItUGT419聚类在第3支(Group III),与人参和麦蓝菜中的三萜类糖基转移酶聚类在一起;而ItUGT349聚类在第2支(Group II),与已知功能的三萜类,黄酮类等糖基转移酶聚类在一起。
使用NCBI-CD-Search和Tbtools工具对其结构域进行预测,发现ItUGT349和ItUGT419与已知功能的三萜类糖基转移酶具有相同的结构域(GTB-type superfamily)。进一步使用pfam在线软件对其结构域序列进行分析,并使用DNAMAN进行多序列比对(图5),发现ItUGT349和ItUGT419与三萜类糖基转移酶的氨基酸序列具有较高的一致性,结构域全长约150个氨基酸。在与黄酮类糖基转移酶的序列比对中发现,其结构域较三萜类的更长,约330个氨基酸;ItUGT349和ItUGT419在C端区域较为保守,在N端存在大片段的缺失。
3.4 ItUGTs的组织差异表达分析
以鸢尾为内参基因,通过qRT-PCR检测和基因在鸢尾根状茎、叶片和花中的差异表达情况,结果见图6,在叶片中有最高表达;在花中的表达量最高。
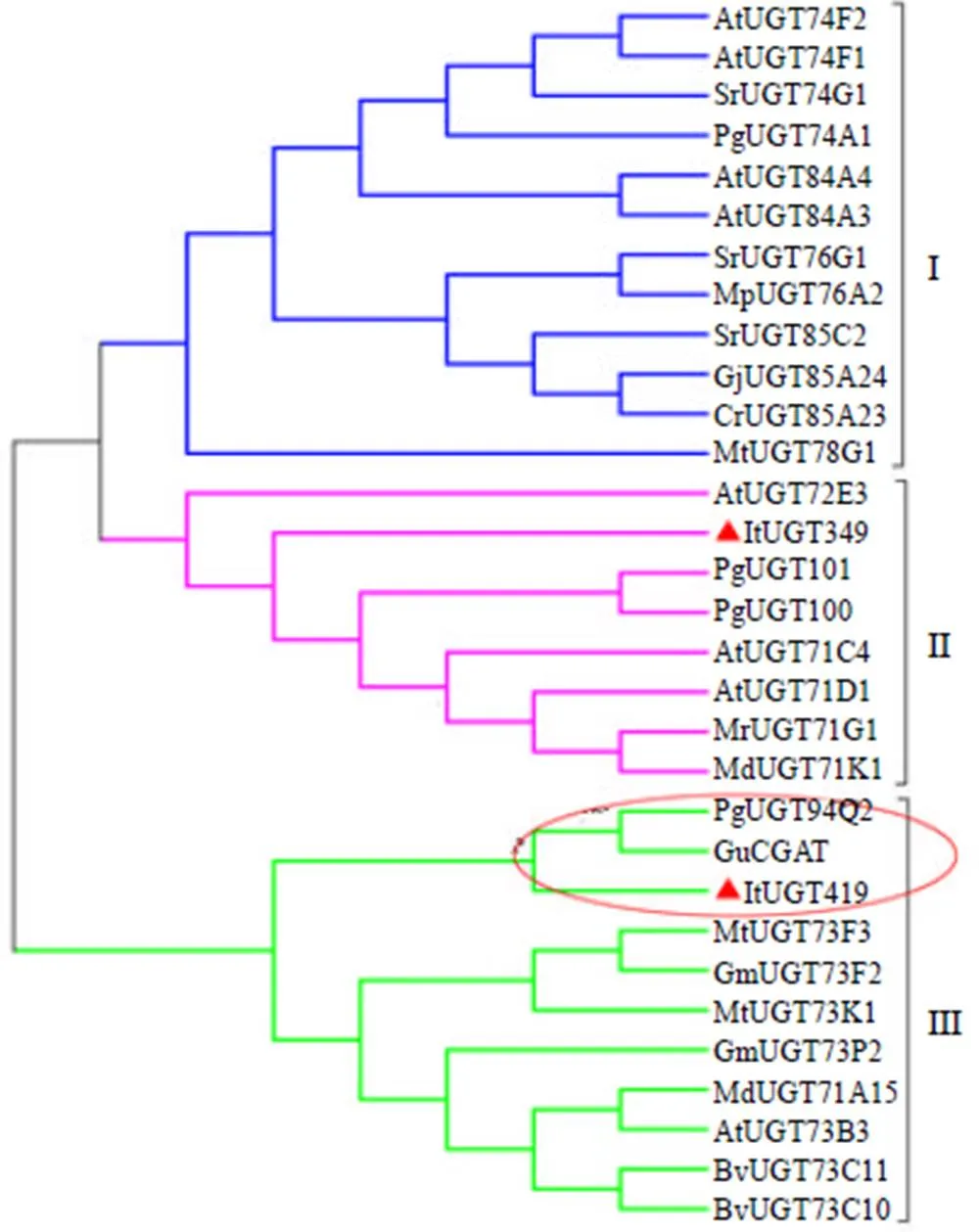
AtUGT-拟南芥 SrUGT-甜叶菊 PgUGT-人参 MpUGT-蒺藜苜蓿 GjUGT-栀子 GuCGAT-麦蓝菜 GmUGT-大豆 BvUGT-欧洲山芥
3.5 ItUGTs的原核表达
将构建好的重组质粒pET32a(+)-ItUGT349、pET32a(+)-ItUGT419转入宿主菌BL21(DE3),通过菌液PCR筛选转化阳性菌液进行IPTG诱导表达。在IPTG的诱导作用下,和在大肠杆菌体系中进行异源表达,经SDS-PAGE检测蛋白的表达情况,结果见图7。ItUGT349重组蛋白相对分子质量理论值为74 230,通过与空载表达情况对照,发现成功表达出较大量的可溶性蛋白;ItUGT419重组蛋白大小理论值为75 310,通过与空载表达情况对照,发现可溶性蛋白达较少,蛋白主要表达在沉淀中。
4 讨论
糖基转移酶是植物次生代谢产物的结构修饰酶,可催化三萜、黄酮、甾体生物碱等众多化合物进行糖基化修饰。药用植物中的主要次生代谢产物通常为其药效物质基础,糖基化修饰对药效成分生化活性及药理作用具有显著的影响。如穿心莲中经糖基化修饰后生成的新穿心莲内酯,其水溶性增加了数倍[21]。人参中含有的多种人参皂苷,其糖基化修饰的差异会使得同种皂苷产生不同甚至截然相反的药理作用[22]。当前对糖基转移酶的研究还有很多未知,一直是国内外研究热点。鸢尾作为一种传统的药用植物,其中含有多种三萜及其皂苷类成分,具有重要的药理活性[1-3]。本研究基于鸢尾转录组数据,筛选并克隆了2条糖基转移酶基因,经进化树分析,初步推测ItUGT349和ItUGT419可能以三萜类化合物作为底物进行糖基化反应,但ItUGT349可能具有更宽泛的底物选择性。有研究指出,糖基转移酶的底物选择性与N端结构域序列的差异高度相关[23-25]。如从茶树中分离得到的糖基转移酶CsUGT78A14可专一性的催化黄酮类化合物的糖基化反应;而另一个糖基转移酶Cs UGT72AM1则可催化黄酮醇、花青素、木质素等多种底物进行糖基化反应,二者C端序列高度保守但在N端则存在显著差异[26-27]。进一步对鸢尾糖基转移酶ItUGT349 和ItUGT419结构域序列进行分析发现ItUGT349和ItUGT419的N端结构域与三萜类的糖基转移酶相似度更高,较黄酮类的糖基转移酶则存在大片段的缺失,其可能导致对黄酮类底物的选择性降低。

PhF3GT-矮牵牛F3GT Cp3GT-葡萄柚3GT CsUGT-茶树UGT FiF3GT-连翘F3GT PfF3GT-紫苏F3GT PjGAT-竹节参GAT

采用单因素方差分析,*P<0.01 存在显著性差异
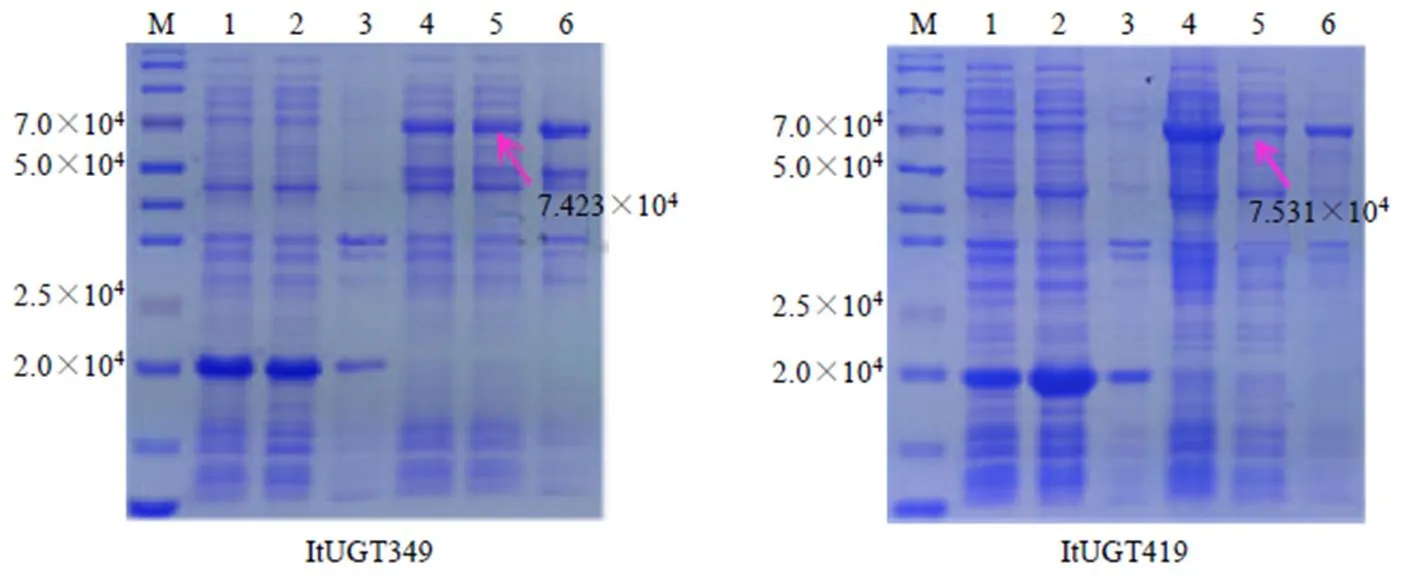
M-Marker 1~3依次为BL21(DE3)-pET32a(+)全蛋白、可溶性蛋白、沉淀 4~6依次为ItUGTs全蛋白、可溶性蛋白、沉淀
吴世丹[28]对鸢尾中的几种重要的三萜类成分进行了含量分析,发现其在叶片中含量非常高,而根状茎中的含量较低。通过荧光定量PCR检测和基因在鸢尾根状茎、叶片和花组织中的表达情况;和基因差异表达与鸢尾各组织中三萜类化合物的积累趋势较为一致,故推测ItUGT349和ItUGT419糖基转移酶更可能参与鸢尾地上部分组织中的糖基化反应。进一步验证糖基转移酶基因功能,需要通过蛋白原核表达,获得相应的酶蛋白,并与各种类型的底物进行体外酶促反应;其中可溶性融合蛋白的成功表达对后续鉴定酶的功能至关重要。
本研究通过构建ItUGT349和ItUGT419原核表达载体,在大肠杆菌中进行蛋白表达,ItUGT349和ItUGT419均表达出可溶性蛋白,但ItUGT419可溶性蛋白表含量较低。有研究指出,融合蛋白可能会以包涵体的形式聚集在沉淀中,这与蛋白是否含有跨膜区及是否为分泌蛋白有关[29];除此之外,蛋白的溶解性还与基因序列、蛋白空间结构、表达载体、菌株及诱导条件等有关[30]。本课题组在诱导表达过程中对诱导培养的温度和诱导剂(IPTG)的使用量等参数进行了摸索,依然不能很好的提高ItUGT419的可溶性蛋白含量;下一步将继续优化表达系统或使用发酵罐增大菌体的诱导量,来获得较大量的ItUGT419可溶性蛋白,为后续体外酶促反应鉴定酶功能提供足够的酶蛋白。
利益冲突 所有作者均声明不存在利益冲突
[1] 雷启荣, 罗君, 赵琳珺, 等. 鸢尾的化学成分和药理作用的研究进展 [J]. 中国民族民间医药, 2011, 20(12): 41-42.
[2] Taillet L,. Isolation and structure determination of three epoxidized iridals from[J]., 1999, 52(8): 1597-1600.
[3] 顾卫卫, 谢国勇, 荆英姗, 等. 鸢尾醛型三萜的分布和生物活性研究进展 [J]. 现代药物与临床, 2016, 31(1): 122-130.
[4] Vogt T, Jones P. Glycosyltransferases in plant natural product synthesis: Characterization of a supergene family [J]., 2000, 5(9): 380-386.
[5] Plaza M, Pozzo T, Liu J Y,. Substituent effects onantioxidizing properties, stability, and solubility in flavonoids [J]., 2014, 62(15): 3321-3333.
[6] Gachon C M, Langlois-Meurinne M, Henry Y,. Transcriptional co-regulation of secondary metabolism enzymes in: Functional and evolutionary implications [J]., 2005, 58(2): 229-245.
[7] Bowles D, Lim E K, Poppenberger B,. Glycosyltransferases of lipophilic small molecules [J]., 2006, 57: 567-597.
[8] Bowles D. A multigene family of glycosyltransferases in a model plant,[J]., 2002, 30(2): 301-306.
[9] Li Y, Baldauf S, Lim E K,. Phylogenetic analysis of the UDP-glycosyltransferase multigene family of[J]., 2001, 276(6): 4338-4343.
[10] Shibuya M, Yan G J, WU X X,. Identification and characterization of glycosyltransferases involved in the biosynthesis of soyasaponin I in[J]., 2010, 584(11): 2258-2264.
[11] Caputi L, Malnoy M, Goremykin V,. A genome-wide phylogenetic reconstruction of family 1 UDP-glycosyltransferases revealed the expansion of the family during the adaptation of plants to life on land [J]., 2012, 69(6): 1030-1042.
[12] Paquette S, Møller B L, Bak S. On the origin of family 1 plant glycosyltransferases [J]., 2003, 62(3): 399-413.
[13] Ross J, Li Y, Lim E,. Higher plant glycosyltransferases [J]., 2001, 2(2): REVIEWS3004.
[14] 郭思远, 尹艳, 石颖慧, 等. 滇重楼糖基转移酶基因的克隆和原核表达 [J]. 中国实验方剂学杂志, 2021, 27(8): 126-134.
[15] Meesapyodsuk D, Balsevich J, Reed D W,. Saponin biosynthesis in. cDNAs encoding beta-amyrin synthase and a triterpene carboxylic acid glucosyltransferase [J]., 2007, 143(2): 959-969.
[16] Louveau T, Orme A, Pfalzgraf H,. Analysis of two new Arabinosyltransferases belonging to the carbohydrate-active enzyme (CAZY) glycosyl transferase Family1 provides insights into disease resistance and sugar donor specificity [J]., 2018, 30(12): 3038-3057.
[17] Sayama T, Ono E, Takagi K,. The Sg-1 glycosyltransferase locus regulates structural diversity of triterpenoid saponins of soybean [J]., 2012, 24(5): 2123-2138.
[18] 李媛. 穿心莲糖基转移酶的基因克隆及功能研究 [D]. 济南: 山东中医药大学, 2019.
[19] Shao H, He X Z, Achnine L,. Crystal structures of a multifunctional triterpene/flavonoid glycosyltransferase from[J]., 2005, 17(11): 3141-3154.
[20] Maharjan R, Fukuda Y, Nakayama T,. Crown-ether-mediated crystal structures of the glycosyltransferase PaGT3 from[J]., 2020, 76(Pt 6): 521-530.
[21] Li Y, Lin H X, Wang J,. Glucosyltransferase capable of catalyzing the last step in neoandrographolide biosynthesis [J]., 2018, 20(19): 5999-6002.
[22] 梁会超, 王庆华, 巩婷, 等. 人参皂苷生物合成相关糖基转移酶研究基本策略及进展 [J]. 药学学报, 2015, 50(2): 148-153.
[23] Lairson L L, Henrissat B, Davies G J,. Glycosyltransferases: structures, functions, and mechanisms [J]., 2008, 77: 521-555.
[24] Chang A, Singh S, Phillips G N Jr,. Glycosyltransferase structural biology and its role in the design of catalysts for glycosylation [J]., 2011, 22(6): 800-808.
[25] 袁帅. 虎眼万年青属糖基转移酶的挖掘及其在糖苷多样性中的应用 [D]. 北京: 北京协和医学院, 2018.
[26] Zhao X C, Dai X L, Gao L P,. Functional analysis of an uridine diphosphate glycosyltransferase involved in the biosynthesis of polyphenolic glucoside in tea plants () [J]., 2017, 65(50): 10993-11001.
[27] Jiang X L. Four flavonoid glycosyltransferases present in tea overexpressed in model plantsandfor functional identification [J]., 2018, 1100/1101: 148-157.
[28] 吴世丹. 川射干三萜环化酶基因克隆和生化功能验证 [D]. 广州: 广州中医药大学, 2020.
[29] Patnaik P R. Investigation of induction effect on the steady state performance of a continuous fermentation for recombinant β-ga1actosidase [J]., 2001, 36(11): 1069-1074.
[30] 靳保龙, 崔光红, 党伯岳, 等. 丹参二萜合酶基因CPS4的原核表达体系优化及活性蛋白纯化 [J]. 中国实验方剂学杂志, 2014, 20(10): 94-98.
Genes clone and features analysis of glycosyltransferase genesandfrom
ZHANG Li-bing, LI Jing, TAO Wu-yang, HUANG Zi-lu, CHEN Jia-jie, DUAN Li-xin, JI Ai-jia
Guangdong Provincial Key Laboratory of Translational Cancer Research of Chinese Medicines, Joint International Research Laboratory of Translational Cancer Research of Chinese Medicines, International Institute for Translational Chinese Medicine, School of Pharmaceutical Sciences, Guangzhou University of Chinese Medicine, Guangzhou 510000, China
To clone the glycosyltransferase genesandfromand conduct bioinformatics analysis, gene differential expression analysis and protein prokaryotic expression analysis.Gene-specific primers were designed based on the open reading frame (ORF) of, which were screened from the transcriptome data; And the gene products were obtained by PCR amplification. After sequencing identification, bioinformatics analysis was performed. Moreover, the different expression of both genes among various tissues were detected by real-time qPCR. Finally, the target gene was constructed into the prokaryotic expression vector pET-32a (+) and the soluble proteins were obtained in.The length of open reading frame (ORF) ofandwere 1461 bp and 1488 bp, respectively; And the molecular weight of the encoding proteins were 53 830 and 54 910. The fluorescence quantitative PCR results showed that the expression level ofwas highest in leaves, whilewas highly expressed in flowers. The phylogenetic tree showed that ItUGT419 was clustered with the UGTs, which were related to triterpene biosynthesis; And ItUGT349 was clustered with the UGTs, which were involved in the biosynthesis of triterpene, flavonoids and lignin. Finally, ItUGT349 and ItUGT419 were successfully expressed in.The full-length ORF cloning, sequences analysis, differential gene expression detection and prokaryotic expression ofandlay a foundation for the subsequent identification of their catalytic function in.
Maxim.; glycosyltransferase; gene cloning; bioinformatics analysis; prokaryotic expression; qRT-PCR
R286.12
A
0253 - 2670(2023)01 - 0254 - 08
10.7501/j.issn.0253-2670.2023.01.027
2022-05-06
国家自然科学基金青年基金项目(82003895);广东省基础与应用基础研究基金项目(2019A1515110594,2020A1515010926);广东省级大学生创新训练项目(S202110572094,S202110572055)
张李兵,男,硕士研究生,研究方向为药用植物功能基因组学。
通信作者:季爱加,女,副研究员,药用植物功能基因组学。E-mail: ajji@gzucm.edu.cn
[责任编辑 时圣明]