先心病患儿心脏手术围术期TOI、FTOE水平及其与术后转归的关系
熊曌雪,郑景浩
(上海交通大学医学院附属上海儿童医学中心小儿心胸外科,上海 200000)
先天性心脏病(先心病)为常见先天性疾病,近年流行病学调查显示,全球1万名新生儿中有先心病患儿75~90例。手术是先心病的主要治疗手段,虽然目前手术技术及术后管理较既往更为优化,但术后死亡病例并不少见[1]。因此,分析先心病术后死亡高危因素,预测死亡风险,并予以积极地防控措施,对先心病管理有重要意义。目前,我国尚未对先心病手术风险评估及围术期管理作统一要求,患儿预后不良的高危因素也存在争议[2]。近年研究[3]发现,脑组织血氧饱和度指数(cerebral oxygenation index,TOI)、脑组织氧摄取分数(fractional tissue oxygen extraction,FTOE)等指标能通过评估脑组织氧供及氧耗平衡,间接评估先心病患儿术后神经功能损伤,对预测患儿预后有利。本研究旨在探讨先心病患儿心脏手术围术期TOI、FTOE水平及其与术后转归的关系。
1 资料与方法
1.1 一般资料
选取2020年1月至2021年12月上海交通大学医学院附属上海儿童医学中心收治的486例行心脏手术治疗的先心病患儿为研究对象,根据术后28 d转归分为死亡组(n=33)和生存组(n=453)。本研究经院伦理委员会审核批准,患儿家属知情同意。纳入标准:(1)术前经心脏超声及心脏增强CT检查确诊为先心病,且符合《先天性心脏病外科治疗中国专家共识》[4-9]中先心病诊断标准,并参考该共识行择期体外循环先心病根治术(包括室间隔缺损修补术、肺动脉狭窄矫治术、法洛四联症矫治术等);(2)年龄<16岁;(3)围术期检查资料完整。排除标准:(1)既往开胸手术治疗史;(2)合并严重染色体异常;(3)合并原发性癫痫、脑外伤等脑功能障碍疾病;(4)术中死亡。
1.2 方法
所有患儿行择期体外循环及主动脉阻断先心病根治术。采用小儿心脏外科年度胸外科和心血管外科研讨会制定的RACHS-1评分[10]评估手术复杂程度,完善检查,积极纠正内环境紊乱,并给予强心、利尿、抗感染、营养支持等对症治疗。术后呼吸机辅助通气,在患儿血流动力学稳定、血气分析正常、自主呼吸有力后过渡撤机,并维持水电解质及酸碱平衡,根据《先天性心脏病外科治疗中国专家共识》判断术后早期(30 d)并发症发生情况。术前(入院后2~3 d)及术后7 d,使用近红外光谱脑部血氧饱和度监护仪(美国CAS Medical Systems公司)监测TOI,同时使用心电监护仪监测右上肢经皮血氧饱和度(SpO2),6 h/次,记录各指标每次监测的平均值,计算FTOE=(SpO2-TOI)/SpO2×100%。
1.3 观察指标
(1)影响先心病患儿术后死亡的单因素;(2)影响先心病患儿术后死亡的多因素;(3)不同转归患儿围术期TOI、FTOE变化情况;(4)TOI、FTOE对先心病患儿术后死亡的预测价值。
1.4 统计学分析
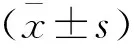
2 结果
2.1 影响先心病患儿术后死亡的单因素分析
不同性别、主要心脏疾病、术前是否使用血管活性药物支持、术前是否使用呼吸机辅助治疗、术中延迟关胸与否、术后机械通气情况、术后30 d内急性肾损伤与否及肺部感染与否的先心病患儿术后死亡率比较,差异无统计学意义(P>0.05);日龄<30 d、RACHS-1评分3~4级、体外循环阻断时间≥60 min的患儿术后死亡率更高(P<0.05)。见表1。
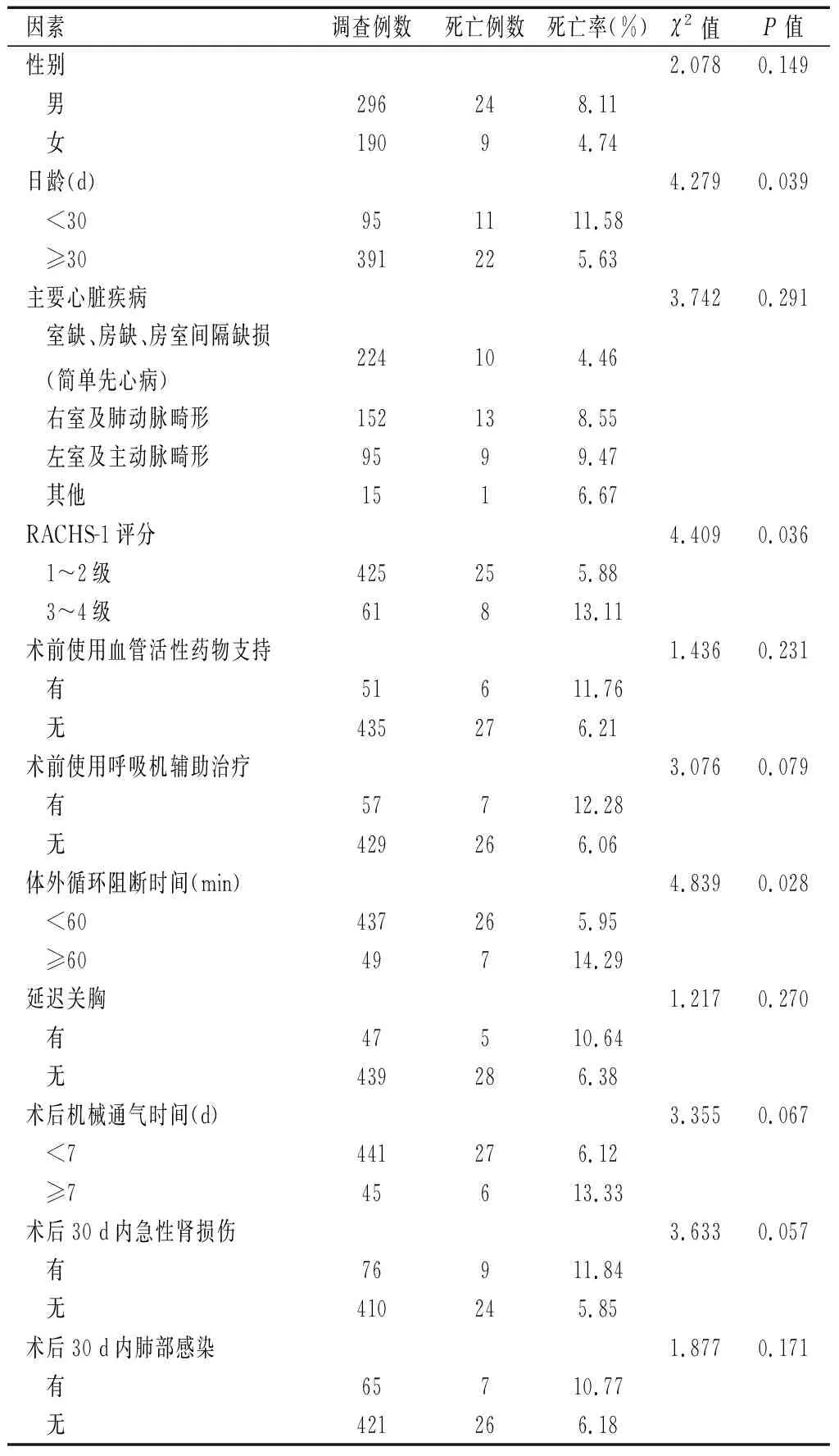
表1 影响先心病患儿术后死亡的单因素
2.2 影响先心病患儿术后死亡的多因素分析
回归分析显示,日龄<30 d、RACHS-1评分3~4级、体外循环阻断时间≥60 min均为先心病患儿术后死亡的危险因素(P<0.05)。见表2。

表2 先心病患儿术后死亡的多因素分析
2.3 不同转归患儿围术期TOI、FTOE变化情况比较
术后7 d,两组患儿TOI、FTOE均较术前升高(P<0.05),且生存组高于死亡组(P<0.05)。见表3。

表3 不同转归患儿围术期TOI、FTOE变化情况比较
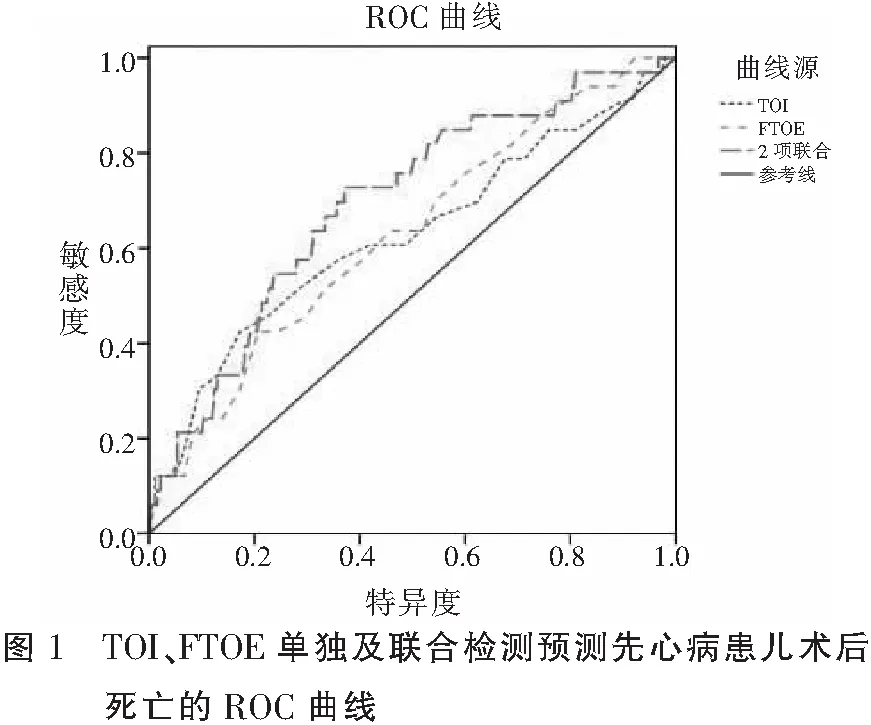
2.4 TOI、FTOE对先心病患儿术后死亡的预测价值
ROC曲线分析显示,术后7 d,TOI、FTOE单独及二者联合检测对先心病患儿术后死亡均有较高预测价值(P<0.05)。见表4及图1。

表4 TOI、FTOE对先心病患儿术后死亡的预测价值
3 讨论
RACHS-1评分是国际上用来评估先心病手术复杂程度的重要工具,近年研究[11]指出,其对预测先心病手术死亡及重大并发症有利。Yu等[12]指出,根据RACHS-1评分制定先心病手术风险等级,不同风险等级患儿手术死亡率为0.26%~62.00%,表明RACHS-1评分对预测先心病患儿手术死亡风险有重要价值。本研究单因素分析发现,RACHS-1评分3~4级的患儿术后死亡率更高;回归分析也显示,RACHS-1评分3~4级是先心病患儿术后死亡的危险因素(P<0.05),与上述报道一致。年龄与先心病手术预后的关联性仍存在争议,有研究者[13]认为年龄越小、越早行先心病手术治疗的患儿,心肌重构能力更佳,预后更好。也有研究者[14]认为,新生儿等年龄偏小的患儿,生长发育不成熟,围术期血流动力学不稳定,术后不良预后的风险更高。日龄<30 d是先心病患儿术后死亡的危险因素(P<0.05),可能与年龄过小、过早行手术治疗的患儿病死风险更高有关。
目前临床认为,行心脏手术者,体外循环时间越长,预后越差,尽量缩短体外循环时间也是心脏手术管理的重要方向[15]。本研究发现,体外循环阻断时间≥60 min为先心病患儿术后死亡的危险因素(P<0.05)。另外,近年研究[16]指出,延迟关胸是影响先心病患儿预后的重要因素,延迟关胸提示患儿手术复杂程度高、体外循环时间长,术后并发症及病死风险更高。但本研究单因素分析显示术中延迟关胸与否与先心病患儿术后死亡风险无关,可能是一方面与纳入样本量不足,结果存在偏倚;另一方面与延迟关胸是改善血流动力学不稳定的措施,不能直接判断患儿预后死亡风险。宋晓琪等[17]通过单中心12年大数据汇总分析指出,术后住院死亡危险因素包括年龄、身高、手术史、超声心动图检查及实验室检查结果等多项因素,也提示影响先心病术后转归的风险因素复杂,单一因素难以直接判断,需要结合多因素综合评估。但本研究纳入样本量有限,得到的结论还需后续大样本单中心研究的支持。
另有文献[18]报道,先心病患儿术后脑组织氧供及氧耗平衡障碍越严重且维持时间越长,神经发育系统将受到严重影响,预后不良风险极高。TOI、FTOE利用近红外光谱脑部血氧饱和度监护仪监测,具有无创、实时、准确等优点,近年在心脏手术的脑保护措施中广泛应用[19]。本研究结果显示,两组生存组和死亡组患儿术后7 d的TOI、FTOE均较术前升高(P<0.05),且生存组高于死亡组(P<0.05),提示心脏手术可纠正患儿体循环供氧,术后患儿脑组织氧供及氧耗平衡得到一定改善,且脑组织氧供需平衡更佳者术后预后也更好,而脑组织氧供需平衡不良,术后神经功能障碍风险更高,预后更差[20]。术后7 d,TOI、FTOE单独及二者联合检测对先心病患儿术后死亡均有较高预测价值(P<0.05),提示术后监测TOI、FTOE可通过评估患儿脑组织氧供需平衡,间接评估患儿神经功能障碍风险,预测预后死亡情况,对指导临床诊疗有利。
综上,先心病患儿术后死亡风险与日龄、手术复杂程度、体外循环阻断时间等因素有关,术后7 d TOI、FTOE对预测患儿术后不良预后有利,可为临床诊疗提供新方向。

