原子分子论确立过程及其科学价值
赵存梅 莫尊理 张华敏
(西北师范大学 甘肃 兰州 730070)
一、问题的提出
《义务教育化学课程标准(2022年版)》的教学建议中鼓励和倡导教师可以利用化学实验、科学史实、新闻报道等多种素材作为导入课堂的情境。[1]化学作为一门从原子、分子水平上研究物质的科学,让学生更充分、完整地理解原子分子的本质、原子分子论确立的过程及其体现出的科学精神和科学思维之极其重要。因此有必要梳理清楚原子分子论确立的来龙去脉,凝练其中的科学价值和教学价值,为一线的教学提供可借鉴的化学史素材。
二、原子分子论的发展历史梳理
原子论是哲学家与科学家之间围绕“构成物质的终极单位究竟是什么?”这一问题而展开思考与研究的一种学说,[2]其历史发展可谓精彩纷呈,充满哲学思辨。作为进入化学学科的“门槛”,原子分子的教学不只是让学生体会到微观粒子的存在,更是要让学生从化学学科的角度得到科学思想与精神的启蒙,梳理其确立的历史过程,凝练其科学价值。
通过梳理原子分子论的确立过程,整理出具有代表性的四个不同时期的原子分子论,[3,4]如表1 所示,以时间线为顺序呈现不同时期人们对微观世界的探索与认识。
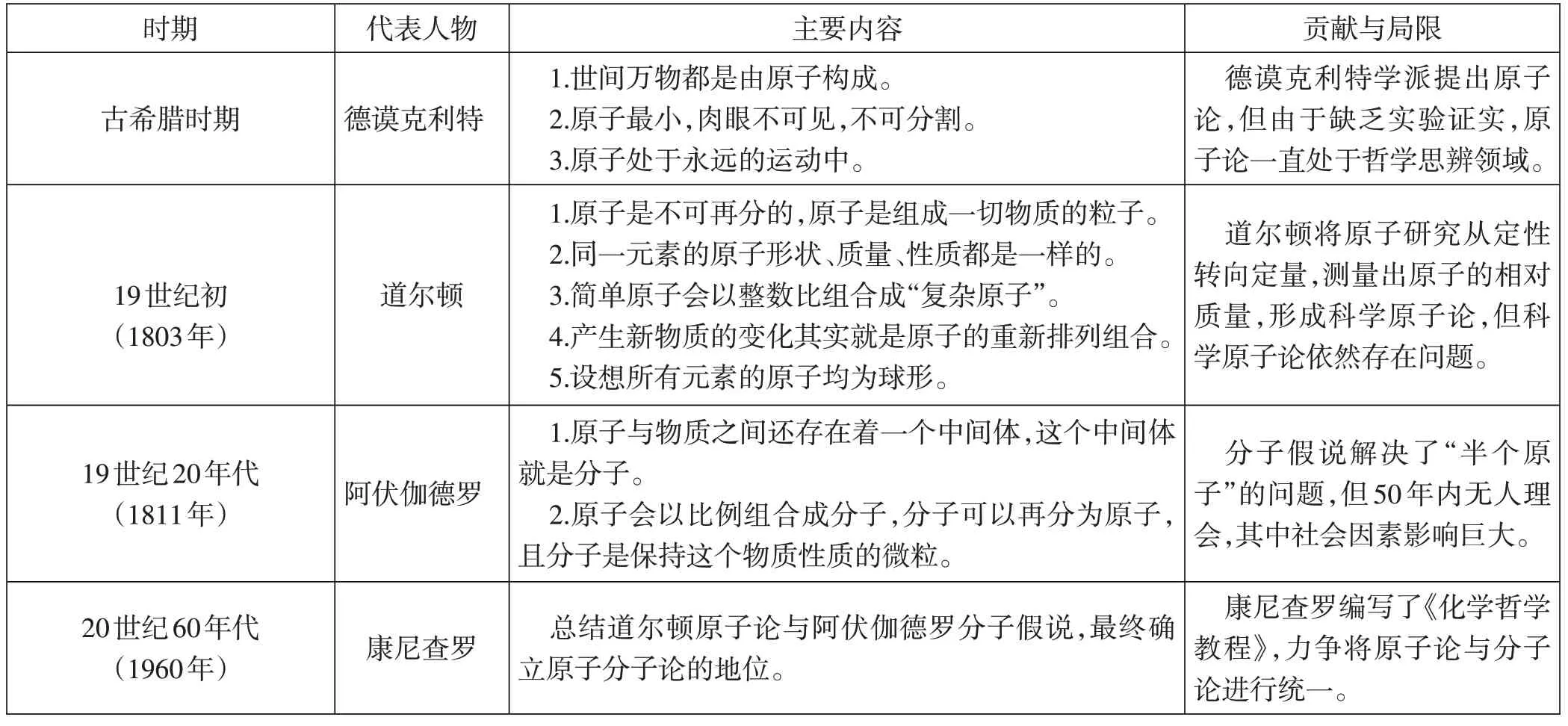
表1 原子分子论的历史资料
三、原子分子论确立过程的科学价值
通过对原子分子论的提出、发展及确立过程的简单梳理,发现其从假说到客观事实的发展过程中蕴含着丰富的科学价值,对发展学生的学科理解有重要的启示作用。
1.结合了科学的思考与规范的实验
科学史前进的每一步都离不开思维的指导与实践的检验,原子分子论的确立就是个典型的例证。道尔顿从18世纪后半叶开始对气象学进行研究,他不断积累理论知识,在思考气体的物理性质究竟是怎么样的同时,开始积极探索,通过做实验来考察气体性质,最终在理论的指导与实验的验证下,提出气体分压定律、倍比定律等一系列著名论断。这些发现为原子论的建立提供了理论基础,甚至可以说,道尔顿如果没有对气象学孜孜不倦的研究,那么他可能很难提出原子学说,近代化学的新时期也很难由他开启。阿伏加德罗亦是如此,他的分子假说,不仅划清了原子与分子的界限,而且还指明分子与原子之间的关系:分子是由原子构成的。之所以能得出这样的结论,是因为阿伏加德罗将道尔顿与盖·吕萨克(Joseph Louis Guy-Lusack,1778—1850)之间的争论进行细致地对比与研究,通过科学合理的推理,引入分子的概念将“半个原子”矛盾进行了化解,在此基础上,阿伏伽德罗进行了大量的实验,利用实验去检验其思考的问题,发现气态物质化合反应时具有简单的整数比,基于这个实验结论,他对盖·吕萨克的分子假说进行修正并提出:同温同压下,相同体积的任何气体所含有的分子数目是相等的。
化学作为一门以实验为基础的自然科学,科学思考与规范实验缺一不可,原子分子论的确立无疑为这一规律提供了强有力的佐证。其实纵观整个科学史发展的脉络,每一次科学理论的发展均是如此,就原子分子论而言,对该理论发展做出贡献的科学家(无论是物理学家还是化学家)均通过科学思考与规范实验相结合,一步步推理、一步步验证得到结论。因此,原子分子论的确立科学、准确、客观地描述了从原子论到分子学说的过程,其提出意义重大。
2.渗透着科学本质观思想
亚里士多德将实体(即物质的本质)作为研究哲学的对象,认为研究实体的哲学才是第一科学。[5]由此可见要想了解科学,必须从科学本质观入手。而科学本质观教育是国际科学教育的重要目标,体现在世界各国的科学课程改革文件中(如美国、英国、加拿大、南非、澳大利亚)。我国最新修订的《普通高中化学课程标准(2017年版)》中多次强调要促进学生对科学本质的理解。[6]然而学生对科学本质的认识现状不容乐观,高中化学科学本质教育现状并不理想,还需要广大一线教师在实践中从各个层面上提高认识。[7]因此,从初中化学学习中注重启蒙与培养学生的科学本质意识势在必行,原子分子论的确立从各阶段渗透着科学本质观思想,教师可充分挖掘其价值。
首先,原子分子论发展的每个阶段都具有暂时性。从早期的留基伯与德谟克里特对原子的认识,到道尔顿原子论的提出;从道尔顿与盖·吕萨克之间的学术争论,到阿伏伽德罗分子学说的提出。分子学说从不被认可到其地位的确立,这个波澜壮阔的历史进程并不是直接连续的,而是具有间接性和暂时性。每位科学家都在前人研究的基础上创造性地提出自己的观点,由此推动了科学的进步。
其次,原子分子论的建立史具有一定的创造性。道尔顿在亨利定律(Henry’s Law)的基础上,通过对气象学的观察创造性地提出了原子假说,并将研究方法由定性转向定量,这种创造性的做法无疑给原子分子论的研究提供了新的研究思路。
第三,原子分子论的建立史脱离不了主观性。从本体论上讲,主观性是一种存在方式,即事物借助于主体正在被感知或经验而存在的方式。[8]阿伏伽德罗的分子假说一经问世,便遭到贝采利乌斯的反对,尽管当时的卤代反应(特别是三氯醋酸的成功制取)已经证明贝采利乌斯的电化二元论是片面的,但分子论建立后很长的一段时间内,道尔顿、贝采利乌斯等人仍不承认其地位,这种主观性的认识蒙蔽了他们的双眼,在一定程度上阻碍了科学前进的脚步。
3.蕴含着丰富的学科思维
思维是人脑对客观事物的间接反映,其借助已有的知识与经验,对未知事物进行推测最终达到对事物本质的认识,它包含分析、综合、归纳、演绎等诸多过程。学科思维是某一门具体的学科在发展演变的过程中渗透出来的独一无二的思想,其涉及在学科提出问题、解决问题的过程中所采取的各种方法、手段、路径等。任何一门学科都有其独一无二的学科思维,化学学科也不例外。把学科思维过程作为化学过程的核心,重视学生在知识学习过程中的反省性思维或批判性思维,是培养化学学科思维的基本途径。[9]原子分子论的确立蕴含着丰富的化学学科思维。首先,道尔顿的原子论就是建立在其对气体性质的观察与思考的基础上,通过总结归纳得到的理论。其次,化学是一门在分子、原子层面研究物质的组成、性质、结构与变化规律,创造新物质的自然科学。[10]因此在化学教学中,通过梳理原子分子论的确立过程,可培养学生的微粒观,让学生认识到物质是由微粒构成的,既培养了学生的学科思维能力,也能让学生达到对化学学科本源性的认识。
4.诠释了理性的质疑——批判精神
恩格斯曾非常肯定地指出:“怀疑—批判”的头脑是科学家的一个“主要仪器”。[11]由此可见科学理论发展的过程中理性的质疑与批判是不可或缺的。原子分子论的确立过程充满质疑与批判的声音,如果我们将其想象成一幅横向铺展开的画卷,那么这幅画卷上一定布满科学家的大胆质疑、理性批判的足迹。科学史的发展向来是存在矛盾就会出现质疑的声音,不断出现矛盾就会出现不断地质疑,直到这个科学理论变得清晰、完整,这是科学理论发展的自然规律。原子分子论发展的过程中就产生过两次重要的质疑与纷争。
第一次是道尔顿与盖·吕萨克之间关于“半个原子”的纷争。道尔顿的原子论提出来还未真正在科学界立足,盖·吕萨克就针对原子论的内部矛盾提出了自己的质疑:道尔顿认为元素是由最小的微粒——原子构成的,这就意味着原子是最小的,是无法再分的。但同时他又认为化合物是由“复杂原子(Compound atom)”构成的,“复杂原子”意味着其由更小的原子构成,意味着“复杂原子”可分,那么复杂原子和原子的关系是什么?原子究竟可不可分?这2个原子论内部逻辑上的矛盾就连道尔顿自己都无法解释。
针对道尔顿原子论中的这一“漏洞”,盖·吕萨克立足于气体实验,创造性地提出了重要假说——同温同压下,相同体积的任何气体中含有的原子数目是一样的。若这一假说成立,那么原子就不得不“被分割”。如1体积的氢气与1体积的氯气化合后生成2体积的氯化氢,每个氯化氢“原子”由半个氢与半个氯组成,这就是“半个原子”的由来。道尔顿对此观点坚决反对,因此,原子论又一次“陷入僵局”,而这次争议恰恰为阿伏伽德罗提出分子学说奠定了基础。道尔顿原子论视角下的化学反应如图1所示:
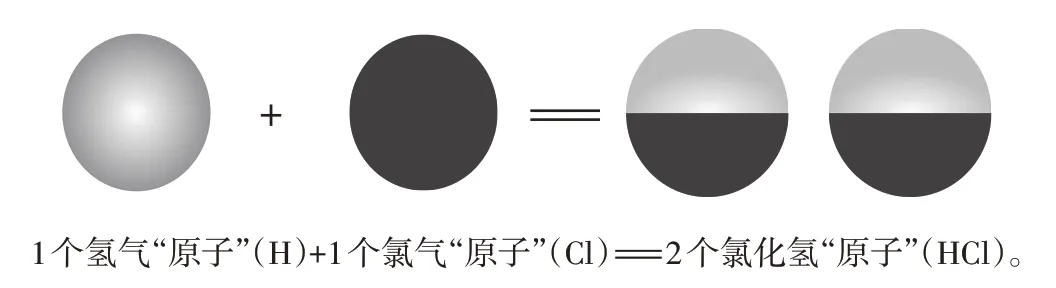
图1 道尔顿原子论视角下的化学反应
“半个原子”的纷争并没有阻碍原子论的进一步发展,阿伏伽德罗在原子论的基础上引入了分子的概念,阐明了分子与原子的区别与联系。引入分子后的化学反应如图2所示:
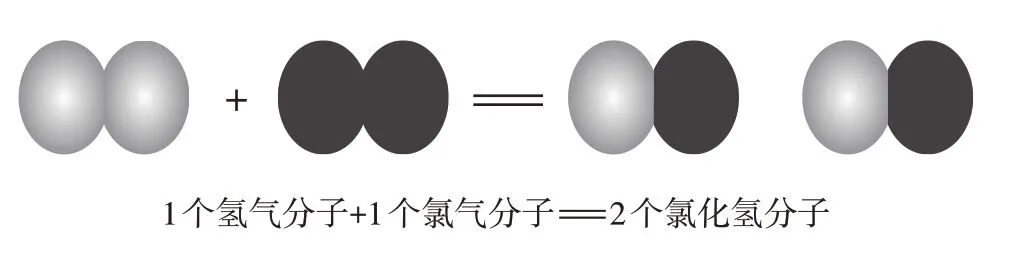
图2 引入分子概念后的化学反应
原子分子论确立过程中,第二次较大的质疑则发生于阿伏伽德罗分子学说与贝采利乌斯的电化二元论之间。阿伏伽德罗的分子学说提出后,遭到贝采利乌斯质疑,他们的争论点在于:阿伏伽德罗的分子学说认为原子会以比例组合成分子,分子可以再分为原子,且分子是保持这个物质性质的微粒。而贝采利乌斯提出的电化二元论认为不同的原子带不同的电荷,因而具有相互吸引力;同种原子带相同的电荷,会相互排斥,根据这一假说,单质气体分子是不可能形成多原子分子的。显然科学的进步证明贝采利乌斯的观点过于片面,但不得不承认的是,在原子分子发展的进程中,科学家基于事物本身的矛盾进行大胆的质疑精神尤为重要,其揭示了科学理论进步的艰辛历程,也证明理论本身存在的矛盾才是推动理论发展的根本所在。
批判性思维是创造性思维的前提和基础,是学会创造性思维的重要途径。[12]在实际的教学中以原子分子论确立过程为素材,将其贯穿到原子分子教学中,有利于培养学生批判性思维与系统思维,激发学生创造的潜能,同时在学生心中树立勤奋好学的科学家形象。

