石墨炉原子吸收法(GFAAS) 测定水样中Cu2+和Cr3+的质量浓度
代智慧
(朔州师范高等专科学校,山西 朔州 036002)
铜(Cu)元素和铬元素(Cr3+)都属于人体所必需的微量元素,人体长期缺少这两种元素时就会引起各种疾病[1-2]。但是,当Cu和Cr元素在人体中达到或超过一定的限值时,也会给人体带来非常严重的伤害[3]。例如:Cu过量会引起机体出现肌痛、腹痛、腹泻,酸中毒,诱发胰腺炎和休克等症状。如果Cr超标,身体便会出现一些皮肤和呼吸道系统病变等问题。我国《生活饮用水卫生标准》(GB 5749—2006)中有严格要求,生活饮用水及地面水中的Cu和Cr的质量浓度分别不能超过1.0 mg·L-1和0.05 mg·L-1[4]。但是,在日常生活中,人们经常使用的饮用水设备中难免会使用一些不合格的配件,这很可能会导致饮用水中的重金属离子含量超标,饮用这样的水会对人身体产生伤害。如果环境中的河水或湖水等受到重金属Cu和Cr的污染,重金属Cu和Cr也会在水中的鱼类体内富集,大量食用后同样会使人体内重金属含量超标,对健康极为不利。准确检测出饮用水及环境水样中Cu和Cr的浓度就变得很有现实意义。当今社会,在众多金属离子检测方法中,石墨炉原子吸收法(GFAAS)因其具有使用量较少、操作简单、测试快捷及灵敏度高等优点[5-11],是检测水中重金属的最实用的一种方法。
因此,采用石墨炉原子吸收法分别对三种常见的饮用水(桶装水、直饮水机净化水和自来水)及湖水中的Cu和Cr含量进行了测定。除此之外,还通过加标回收实验对该方法的准确性及精确度进行了测试。
1 材料与方法
1.1 仪器与试剂
原子吸收分光光度计(TAS-990型,北京普析通用有限公司);电热恒温鼓风干燥箱(101-0型,北京科伟永兴仪器有限公司);具塞(磨口)刻度管(50 mL,天津科密欧有限公司);分子生物型超纯水机(AFZ-2001-V型,重庆颐洋有限公司);型台式离心机(TD5G,青岛聚创环保集团有限公司)。
Cu标准储备溶液(1 mg·mL-1,国家标准物质研究中心);Cr标准储备溶液(1 mg·mL-1,国家标准物质研究中心);浓HNO3(AR,嘉兴市精博化学品有限公司)。0.500 0 mol·L-1稀HNO3的配制:准确量取32.00 mL浓HNO3置于1 000 mL的容量瓶中,加水稀释并定容,轻轻摇匀后备用。铜标准使用溶液:准确吸取Cu标准储备液1.00 mL于100.00 mL容量瓶中,加0.500 0 mol·L-1的稀HNO3至刻度线,稀释成质量浓度为10 μg·mL-1的铜标准使用液。从中移取10.00 mL于100 mL容量瓶中,再加0.500 0 mol·L-1稀HNO3至刻度线,稀释成1μg·mL-1的铜标准使用液,摇匀,封口待用。C r标准使用溶液(0.1μg·mL-1)制备方法同前。桶装饮用水(市售)。
1.2 水样中Cu和Cr含量的测定
1.2.1 水样的采集与处理
利用洁净且干燥的采样瓶分别采集桶装水(B)、直饮水机净化水(C),自来水(D)以及湖水(E)四种不同水样(表1),然后用移液管吸取等量的水样至离心管中,装有水样的离心管在离心机上离心20 min后取出,取上层清液转移至洁净干燥的具塞管中,封口待测。

表1 四种不同的水样
1.2.2 标准曲线的绘制
1)Cu标准曲线的绘制:准确移取质量浓度为1 μg·mL-1的Cu标准使用液0.00、0.50、1.00、2.00、3.00和4.00 mL分别转移到6只相同体积的容量瓶中(50 mL),然后加稀HNO3(0.500 0 mol·L-1)至刻度后摇匀,封口膜封口待用。所得到的6个不同的Cu标准溶液质量浓度(C)分别为0.00、10.00、20.00、40.00、60.00和80.00 μg·L-1。将配好的6个不同浓度的溶液依次用移液枪准确移取10 μL进行测定吸光度,利用测得的吸光度值A和溶液的准确浓度C来绘制Cu标准曲线。
2) Cr标准曲线的绘制:准确移取质量浓度为0.1 μg·mL-1的Cr标准使用液0.00、1.00、2.00、3.00、4.00和5.00 mL分别转移到6个相同体积的容量瓶中(50 mL),同样加稀HNO3(0.500 0 mol·L-1)至刻度线后摇匀,封口膜封口待用。所得到的6个不同的Cr的标准浓度分别为0.00、2.00、4.00、6.00、8.00和10.00 μg·L-1。Cr标准曲线绘制方法同(1)。
1.2.3 水样分析及加标实验
1) 水样分析:利用移液枪准确移取10 μL不同的水样分别平行测定3次,利用得到的吸光度值,分别对样品的两种重金属离子进行分析。
2) 加标实验:取20.00 mL水样于具塞管中,然后准确移取1.00 mL标准溶液到具塞管,摇匀。最后,移液枪移取10 μL水样注入石墨炉中,测试其吸光度值后根据标准曲线得到实际浓度,计算其回收率。
2 结果与分析
2.1 Cu和Cr标准曲线
首先,利用Cu和Cr标准溶液的不同浓度C对应的吸光度A分别绘制了Cu和Cr标准曲线。图1为Cu标准曲线和Cr标准曲线。图1(a)中可以看到,实验得到Cu标准溶液的回归曲线方程为:
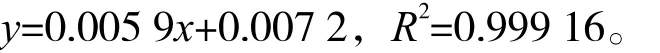
图1(b)中看到Cr标准溶液的回归曲线方程为:y=0.003 8x-0.000 4,R2=0.999 37。以上两个回归曲线方程的相关系数R2都接近于1,说明Cu和Cr的标准曲线符合要求,可用于准确计算重金属离子的浓度。
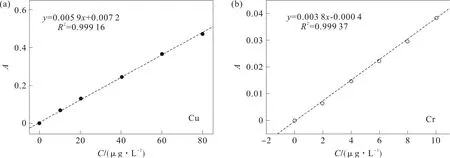
图1 (a) Cu标准曲线;(b) Cr标准曲线
2.2 不同水样中Cu和Cr含量分析及加标实验
接下来,对收集到的四种不同水样进行了预处理,后通过仪器直接测试它们的吸光度。图2为收集的不同水样中Cu和Cr含量的检测结果。从图2(a)可以看到,桶装饮用水(B)和家用自来水(D)两个样品中均未检测出含有铜,这是由于二者中的Cu2+非常低导致仪器无法检出。但是,直饮水机净化水(C)和湖水(E)都检出了铜离子,Cu2+平均质量浓度分别为9.168和2.904 µg·L-1,RSD分别为1.610%和6.667%。让人很意外的是,直饮水机净化水比湖水中的铜含量要高,主要原因可能是由于校园直饮水机所用到的不锈钢中含有少量铜的成分,长时间使用过程中铜会溶出,以Cu2+的形式出现在饮用水中。但我们不必过于担心,两种水中检出的铜含量均未超过GB 5749—2006《生活饮用水卫生标准》中要求的生活饮用水中c(Cu)≤1 mg·L-1的限值[4]。图2(b)为四种不同水样中Cr含量的实验检测结果。从图中可以看出,桶装饮用水(B)和湖水(D)中都未检出铬,这也是因为两种水中的Cr3+浓度非常低导致仪器无法检出。而直饮水机净化水(C)和家用自来水(D)检出了平均质量浓度分别为5.693和6.833 µg·L-1的Cr3+,RSD分别为9.434%和10.465%。直饮水机净化水除了检出Cu含量外还检出了Cr含量,这意为着直饮水机中的不锈钢中还含有铬的成分。此外,家用自来水中也检出了一定浓度的Cr3+,可能来源于水龙头里含有微量的Cr。不过,大家不用担心,水样中检测出的Cr3+均未超过GB 5749—2006《生活饮用水卫生标准》中生活饮用水中c(Cr)≤0.05 mg·L-1的限值[4]。

图2 (a) 四种水样中的Cu质量浓度;(b) Cr质量浓度
最后,为了验证实验结果的准确度和判断试验方法的精密度,还在直饮水机净化水和湖水中进行了Cu加标回收实验。表2为直饮水机净化水和湖水两种不同水样中的Cu加标回收实验结果。从表中可以看到,两种水样加标回收率在94.3%~97.4%之间,直饮水机净化水和湖水的平均加标回收率分别为96.3%和96.7%,由此说明本实验使用的方法准确可靠。

表2 Cu加标回收实验
3 结 论
正利用石墨炉原子吸收分光光度计分别测定了四种不同水样(桶装饮用水、直饮水机净化水、自来水和湖水)中的Cu2+和Cr3+含量,经过检测后可知四种水样中Cu2+和Cr3+浓度均未超过我国规定的限值。铜加标回收实验说明该方法操作简便、数据准确可靠,可广泛推广到其它重金属含量方面的检测。

