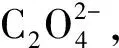氰化尾渣浸出液光催化制备草酸亚铁及再生的研究
党晓娥,张 婷
(1.西安建筑科技大学冶金工程学院; 2.陕西省黄金与资源重点实验室)
引 言
焙烧氰化尾渣是难处理金精矿经焙烧、氰化浸金后产出的大宗固体废物[1]。焙烧过程中由于部分铁矿物发生熔融或再结晶,导致部分金被致密赤铁矿二次包裹[2-3],造成氰化过程中金浸出率偏低,氰化尾渣含金偏高,金品位一般在2 g/t以上。此外,氰化尾渣中还含有25 %~45 %铁和30~80 g/t银等有价元素,是一种重要的二次资源。目前,此类渣以堆存为主,仅有极少数企业采用高温氯化挥发[4-6]、铜精矿-氰渣协同熔炼[7]及磁化焙烧[8-9]等火法工艺处理,但火法工艺存在流程长、能耗大、生产成本高等缺点,限制了其工业化应用。常规酸法[10-11]浸出除铁处理温度虽低于火法,但酸耗大,浸出选择性差,目前尚未见有工业化应用实例。本项目组开发出固体草酸常压络合除铁富集金银等有价金属的技术[1,12],利用草酸的酸性和草酸根离子对Fe(Ⅲ)的络合性协同高效浸出赤铁矿,同时利用草酸根离子易与二价金属阳离子形成难溶草酸盐的性质抑制相应矿物的浸出,实现浸出液的净化。该技术除铁效果好,且时间短,但除铁过程会产出大量含有草酸铁配合物的浸出液。为杜绝浸出液对环境的污染,必须资源化利用浸出液。
草酸铁配合物具有强光化学活性,目前多作为光敏剂用于降解工业废水中的有机物[13-14]及垃圾渗滤废水。其原理是利用草酸铁配合物光催化过程产生的强氧化性羟基自由基·OH将水体中的有机物降解为CO2和H2O,是一种高级氧化技术。如果光催化过程中不添加过硫酸盐[15]和H2O2[16],则草酸铁配合物中的铁最终以FeC2O4形式沉淀析出。FeC2O4是制备纳米磁性材料、超级电容器用多孔材料及生产锂电池用磷酸亚铁锂正极材料所需的主要原料,也是制备纳米Fe2O3、Fe3O4及其他复合催化剂的原料。此外,α-FeC2O4具有n型半导体的特性,被成功用作光催化[17-19]和Fenton氧化的双功能催化剂[18]。
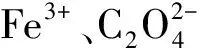
1 试验部分
1.1 试验原料
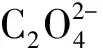
1.2 浸出液光催化
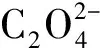
1.3 总铁和总浓度的分析
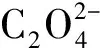
1.4 铁沉淀的表征
采用TD-3500型X射线衍射仪对铁沉淀组成进行表征;采用JSM-650LV型扫描电镜对铁沉淀微观形貌进行表征。
2 结果与讨论
2.1 Fe3+-H2C2O4-H2O体系中Fe3+和的形态分布
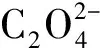
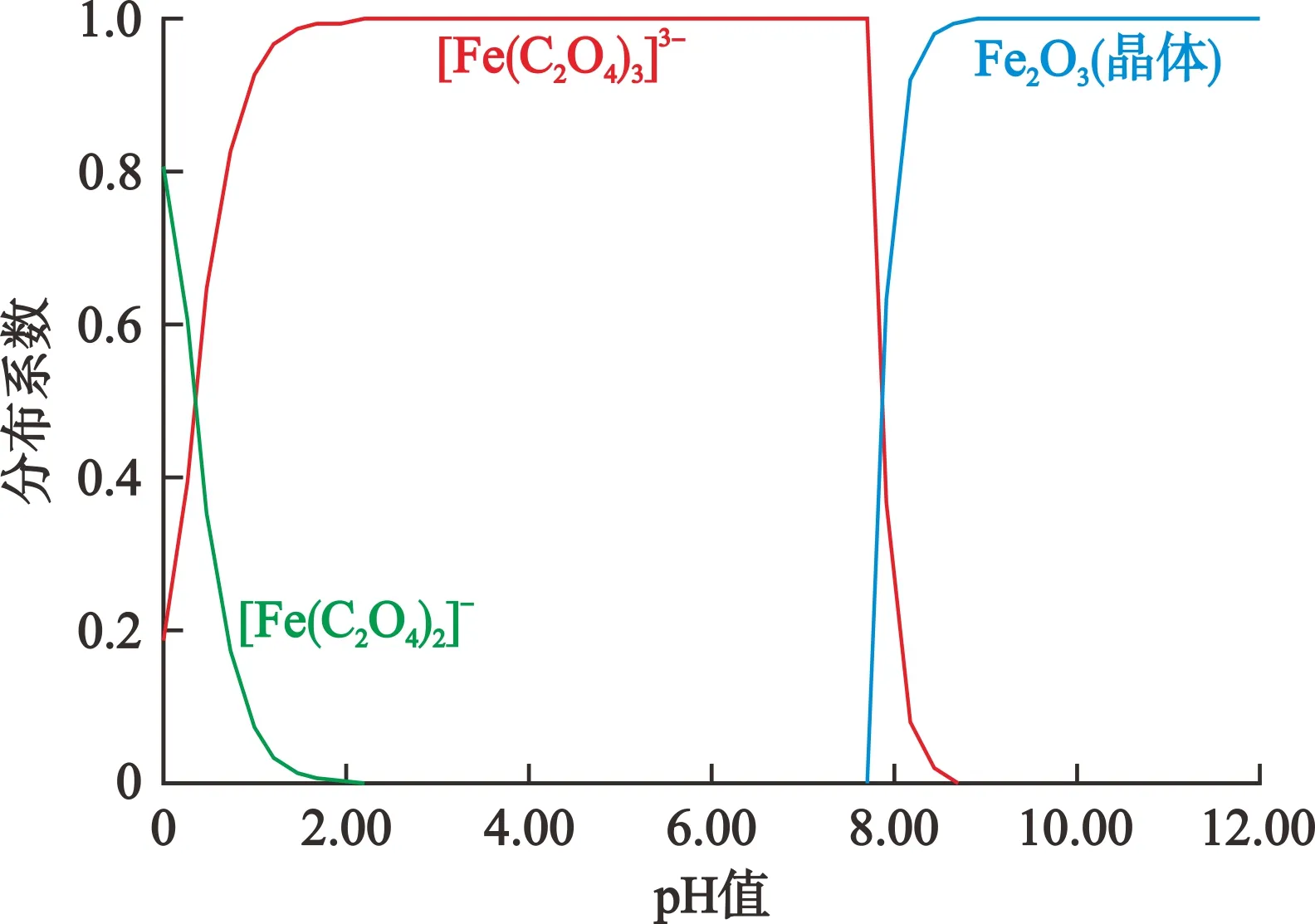
图1 Fe3+在Fe3+-H2C2O4-H2O体系中的形态分布(25 ℃)
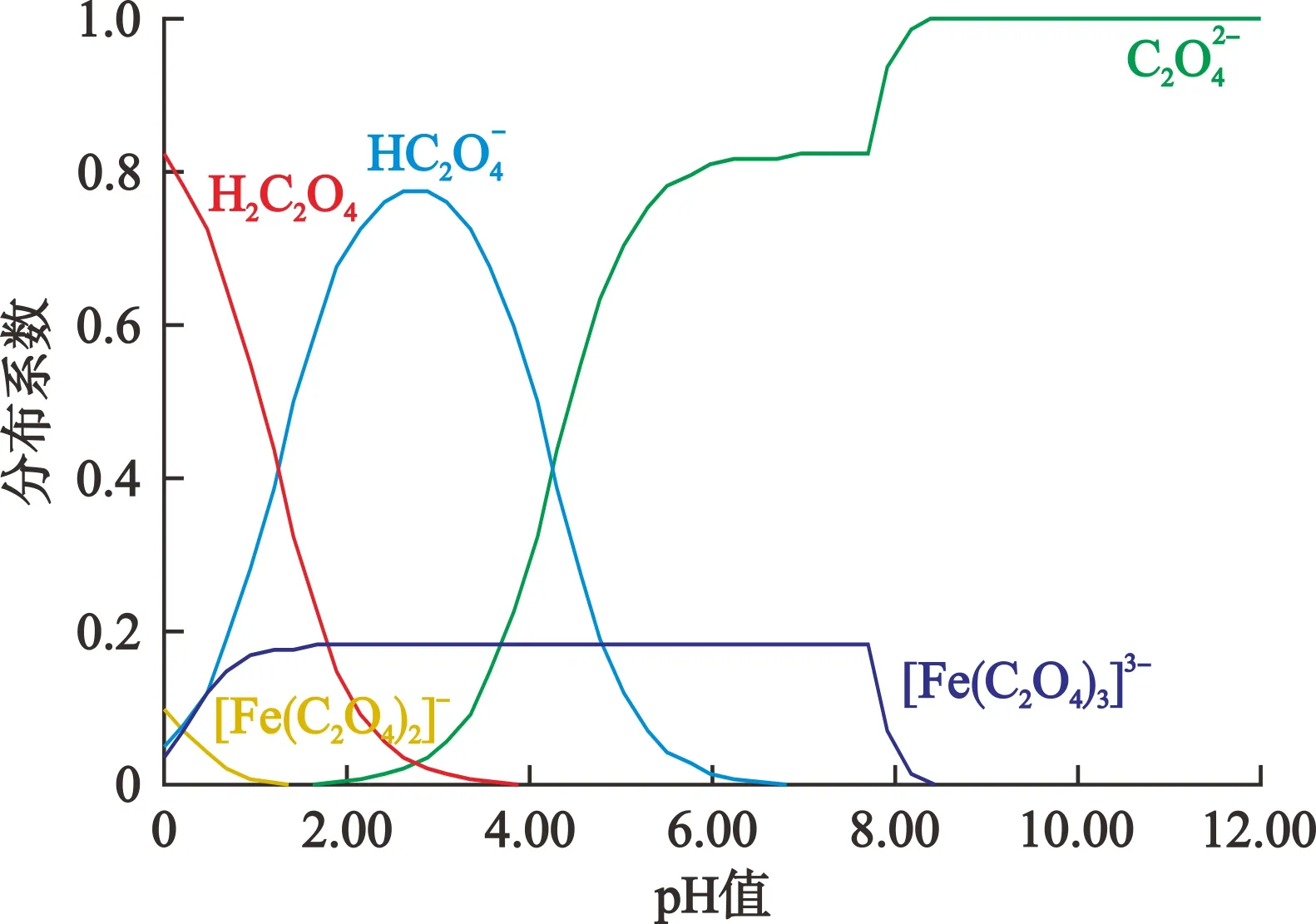
图在Fe3+-H2C2O4-H2O体系中的形态分布(25 ℃)
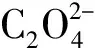
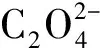
2.2 Fe3+-H2C2O4-H2O体系电位-pH图
由于浸出液中的Fe3+以[Fe(C2O4)3]3-和[Fe(C2O4)2]-形式存在,且二者都具有光化学活性,在光化学反应过程中伴随氧化还原反应的发生。因此,借助HYDRA-MEDUSA软件绘制了Fe3+-H2C2O4-H2O体系电位-pH图,结果见图3。
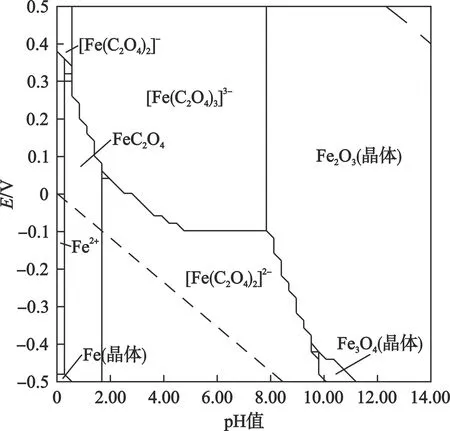
图3 Fe3+-H2C2O4-H2O体系电位-pH图(25 ℃)
由图3可知:在Fe3+-H2C2O4-H2O体系中,[Fe(C2O4)3]3-可被还原成FeC2O4和[Fe(C2O4)2]2-2种产物。pH值在0.28~1.66时,其还原产物为FeC2O4;pH值在1.66~7.84时,其还原产物为[Fe(C2O4)2]2-。由于Fe3+还原过程会伴随H2C2O4的氧化消耗,因此[Fe(C2O4)2]2-最终也会转化成FeC2O4沉淀析出。
由于浸出液光催化后液要返回氰化尾渣除铁过程进行再利用,因此光催化过程暂不考虑添加其他化学试剂。鉴于试验过程中日光光源的不稳定性,后续试验拟以人造氙灯光源提供浸出液光催化过程所需要的能量。
2.3 浸出液静态光催化
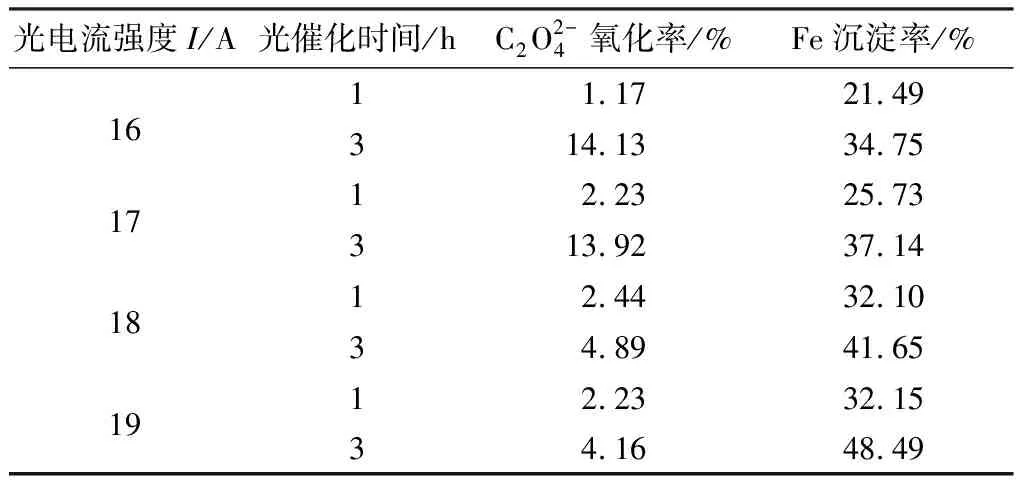
表1 光电流强度对浸出液静态光催化效果的影响
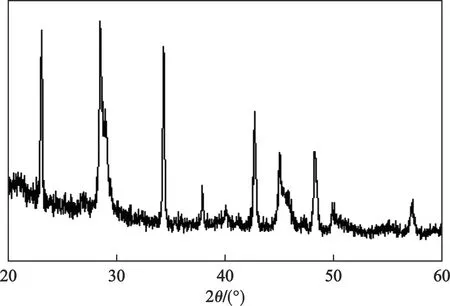
图4 铁沉淀X射线衍射谱图

a—16 A b—17 A c—18 A d—19 A
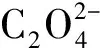
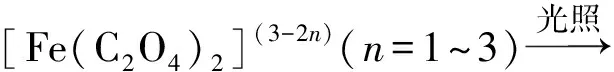

(1)
(2)
(3)
(4)
(5)
(6)

(7)
(8)
(9)
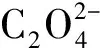
由图4可知:浸出液光催化过程产出的淡黄色沉淀中并未检测到其他杂质的衍射峰,所有衍射峰均为β-FeC2O4·2H2O(PDF22-0635)的特征衍射峰,峰型尖锐,晶型发育也比较完善。
由于浸出液静态光催化效果较差,要提高其光催化效果,试验选择动态光催化,即对浸出液进行搅拌。
2.4 浸出液动态光催化
2.4.1 磁力搅拌强度
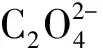
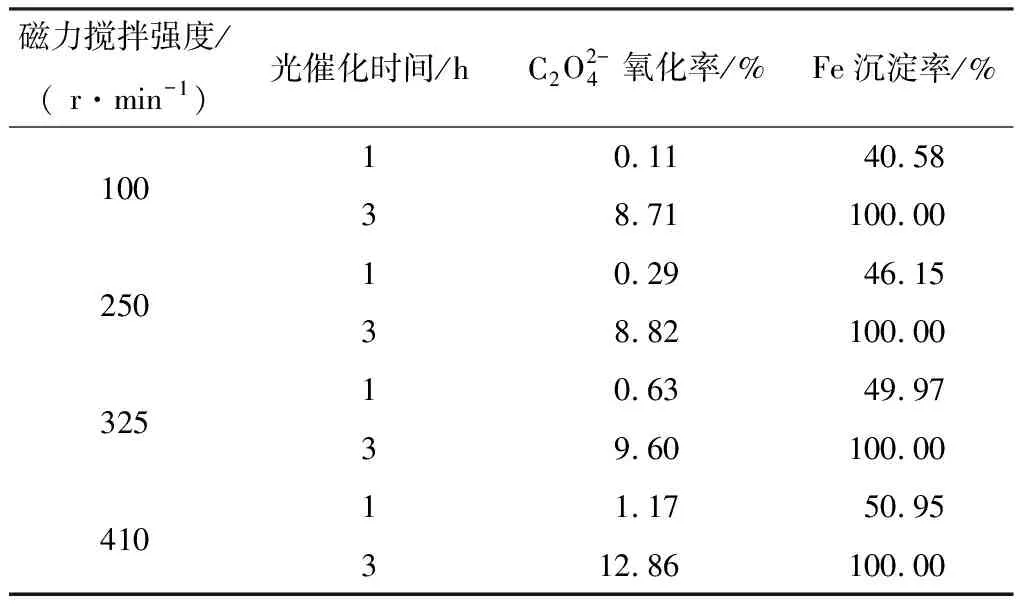
表2 磁力搅拌强度对浸出液光催化效果的影响(I=16 A)
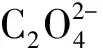
由表2和图6可知:磁力搅拌虽可提高草酸铁配合物的光催化反应速度及光催化效果,但β-FeC2O4·2H2O沉淀形貌被破坏,且搅拌强度越大,形貌破坏越严重,获得的β-FeC2O4·2H2O粒度越小,最终以无规则形状析出。因此,要获得晶型完整的β-FeC2O4·2H2O,光催化过程最好在静态状态下进行,但光催化效率会有所降低。

a—100 r/min b—250 r/min c—325 r/min d—410 r/min
2.4.2 电流强度
在磁力搅拌(搅拌强度 250 r/min)状态下,光电流强度对浸出液光催化效果的影响见表3。铁沉淀微观形貌见图7。
由表3和表1对比发现:浸出液在磁力搅拌下光催化3 h,铁完全以β-FeC2O4·2H2O形式沉淀析出,而浸出液在静态下光催化3 h,铁沉淀率未超过50 %。这是因为磁力搅拌可强化传质过程,从而使浸出液在磁力搅拌下的光催化效果远优于在静态下的光催化效果。
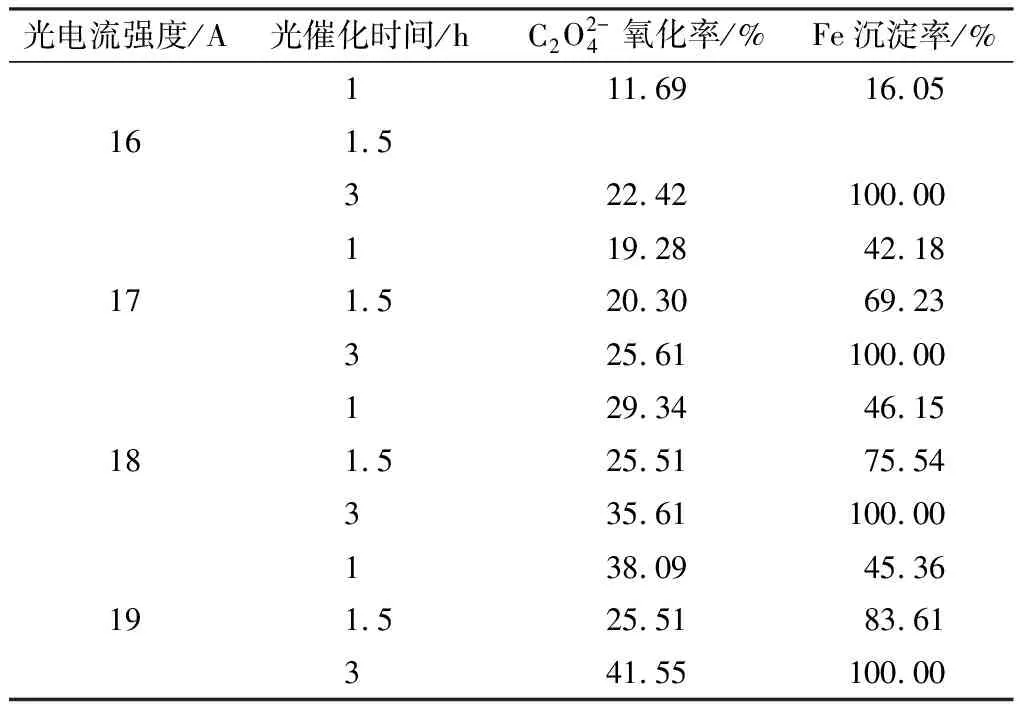
表3 光电流强度对浸出液光催化效果的影响
由图7可知:随着光电流强度的增加,β-FeC2O4·2H2O粒度有所减小。这是因为提高光电流强度,入射光强度增大,光化学反应速度加快,单位时间内[Fe(C2O4)3]3-被还原成FeC2O4粒子的数量增加,即β-FeC2O4·2H2O的形核速度大于其生长速度,导致光催化过程产出更多的β-FeC2O4·2H2O粒子,与之相应形成的β-FeC2O4·2H2O粒度越小,比表面积越大,表面能越高,则粒度较小的β-FeC2O4·2H2O吸附在粒度较大的β-FeC2O4·2H2O微粒表面,最终形成的β-FeC2O4·2H2O粒度分布比较宽。浸出液在光电流强度为19 A条件下进行光催化时,β-FeC2O4·2H2O粒度有所增大,这可能是因为光电流强度越强,浸出液吸收的光能越多,从而更多的光能被转化成热能,使浸出液温度有所升高,导致β-FeC2O4·2H2O的生长速度大于其形核速度,有利于β-FeC2O4·2H2O晶粒的长大。浸出液温度如超过90 ℃,则β-FeC2O4·2H2O将会转化成α-FeC2O4·2H2O[23]。

a—16 A b—17 A c—18 A d—19 A
3 结 论