温度对铜渣和磷矿协同联产制备磷铁影响的实验研究
谢仁齐,黄润,刘利,张金柱
(贵州大学材料与冶金学院,贵州省冶金工程及过程节能重点实验室,贵州 贵阳 550025)
磷铁是指P(15%~30%)、Fe(50%~70%)的合金物,常温下其化学性质比较稳定,不溶于酸、不生锈、无磁性,其分子式一般为Fe3P、Fe2P、FeP、FeP2[1]。磷铁可生产高级防腐油漆涂料磷铁粉[2],也可用来生产正极材料LiFePO4[3]。此外,磷铁还可用来生产磷酸氢二钠和磷酸三钠等磷酸盐,制备FePO4(蓝铁矿)、FezP电极材料的前驱体[4]。
磷矿是一种不可再生、替代,具有战略意义的非金属矿资源[5]。我国现已探明磷矿储量约为330亿t,然而,我国磷矿特点是:富矿少,贫矿多,绝大多数(90%左右)是中低品位磷矿(P2O5<30%)[6]。铜渣是铜矿经过熔融造锍、精炼铜后产生的渣[7],我国每年产生的铜渣量大约为2000万t,累计堆积已有3亿t[8]。大量的铜渣堆积不仅占用土地,而且含的有害元素会对环境造成污染。
基于此,本研究提出采用中低品位磷矿和铜渣协同联产还原直接制备磷铁的方法,剩余的渣可用作生产水泥的原料,也可替代硅灰石另作其他用途。
1 实验
1.1 实验原料
实验所用的原料为磷矿和铜渣,石墨(纯度>99%),甲基纤维素(粘结剂),硼砂(B2O3),硼砂(B2O3)主要作用是作为熔化剂,降低物质的熔化温度。磷矿和铜渣的化学组成见表1。磷矿与铜渣的物相组成见图1。
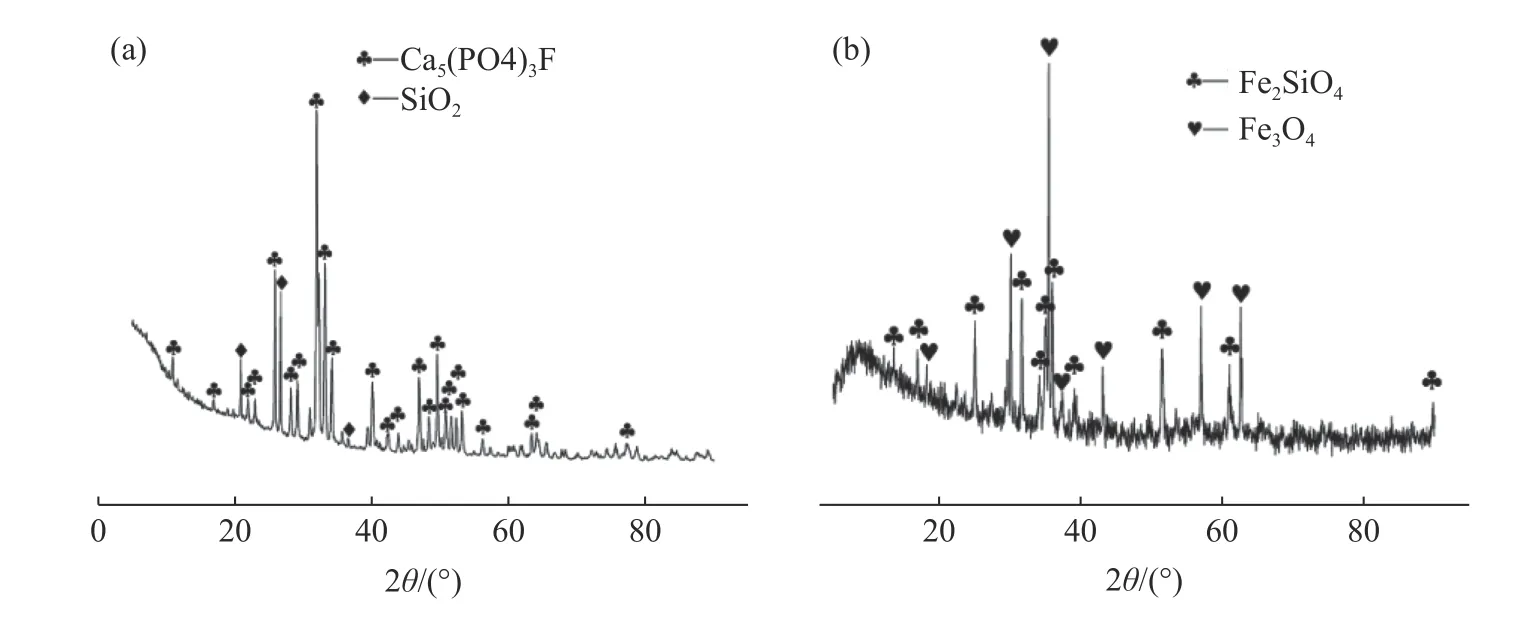
图1 a:磷矿XRD;b:铜渣XRDFig.1 a:XRD of phosphate ore; b:XRD of copper slag

表 1磷矿和铜渣的化学成分/%Table 1 Chemical composition of copper slag and phosphate ore
1.2 实验步骤
分别计量称取6.22 g磷矿,13.78 g铜渣,2.42 g石墨和少量的硼砂(助熔剂)与少量甲基纤维素(粘结剂),进行充分均匀混合后在圆柱形模具上进行制样,压样机的压强设定为15 MP,压后得到大约高13 mm,宽30 mm,重量为23.89 g的样品。在温度为105℃的烘箱中进行干燥24 h,干燥后的试样放进石墨坩埚中,使用推杆把坩埚推到KSS-1600℃高温节能管式炉中间恒温区。合上法兰后打开氩气瓶阀门,以600 mL/min Ar进行通气10 min左右开始加热升温,在升温过程中保持40 mL/min Ar通气,升温速率为4℃/min。升到设定温度后保温60 min,以4℃/min降温到800℃,关掉电源随炉冷却到室温。取出试样进行分离、研磨至0.074 mm左右,使用XRD,SEM和EDS(SUPRA 40)进行相关表征。其实验流程见图2。
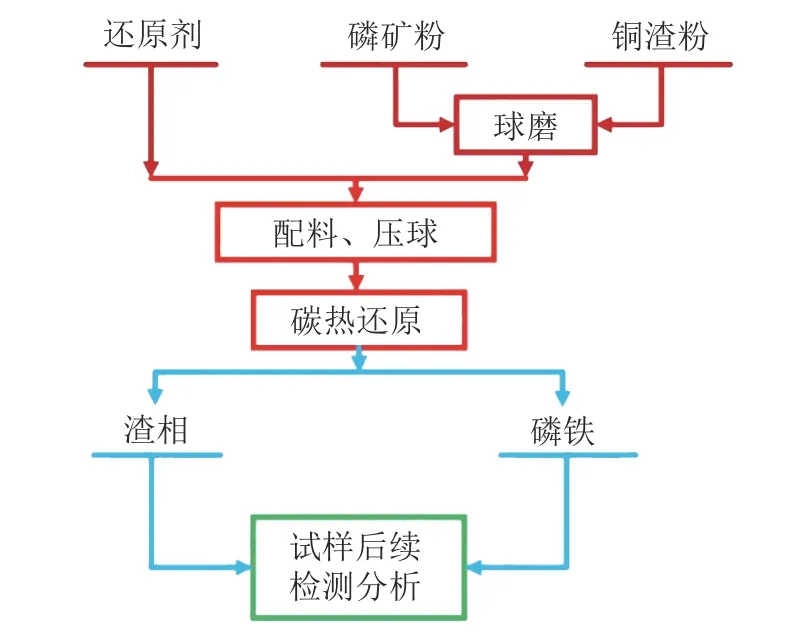
图2 中低品位磷矿与铜渣制备磷铁的工艺流程Fig.2 Process of middle low-grade phosphorus ore andcopper slag for preparation of ferrophosphorus
1.3 分析方法
碳热还原过程中,碳会夺取氧化物中的氧,形成气体溢出,在高温下,某些元素也会发生挥发,进而导致试样会发生失重,试样的失重率由式(1)计算:
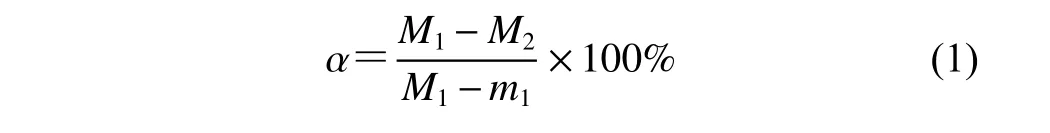
式中:α为还原产物失重率;M1为还原前磷矿和铜渣的质量;M2为还原后磷矿和铜渣的质量;m1为甲基纤维素质量。
2 结果与讨论
2.1 热力学分析
2.1.1 生成磷铁的反应吉布斯自由能
图3是磷矿、铜渣与磷铁发生反应的吉布斯自由能,由a图可知,常压低温下磷矿很难发生自身分解和被还原反应,这可能是因为磷矿的晶型结构为六方柱状,集合体为粒状、致密块状和结核状等复杂形状导致磷矿低温下难以发生分解及被还原。在大约为1400℃时反应开始进行,随着温度的升高,最可能发生大量反应的是:
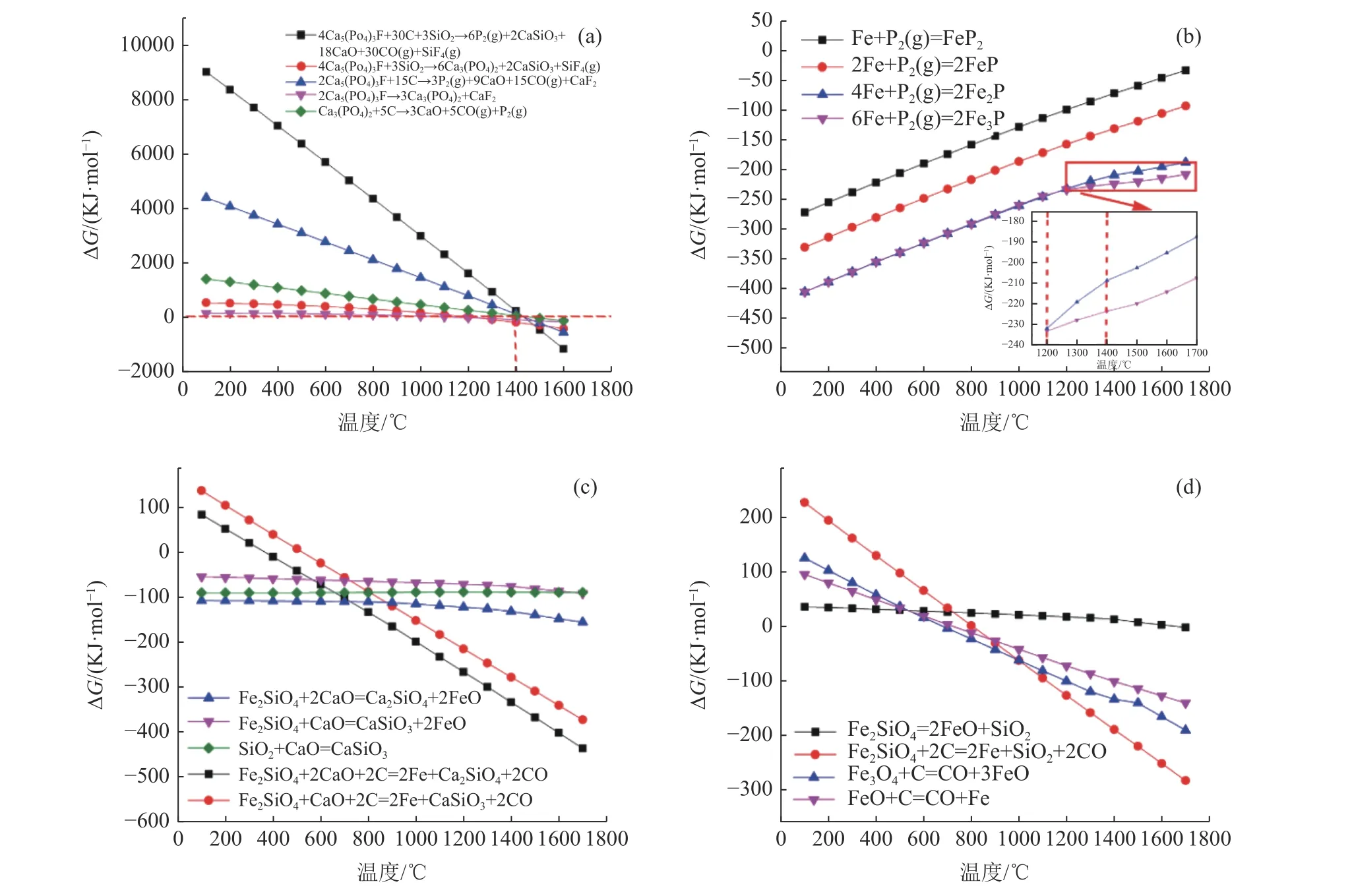
图3 a:磷矿可能发生分解反应的吉布斯自由能;b:生成磷铁的吉布斯自由能;c和d:铜渣可能发生分解反应的吉布斯自由能Fig.3 a:Gibbs free energy for possibledecomposition of phosphate ore; b:Gibbs free energy to form ferrophosphorus;c and d:Gibbsfreeenergy for possible decomposition of copper slag

图b是磷与铁反应生成不同的磷铁,所有生成磷铁的反应随着温度的升高反应难进行。在温度<1700℃条件下,反应过程中可能生成FeP、Fe2P、Fe3P、FeP2。使用热力学软件模拟分析可知,在一定条件下FeP、Fe2P、Fe3P、FeP2会发生不同程度的热解,其中Fe2P、Fe3P的热解稳定性相对较高[9]。从图c和d可知,即使在很高的温度下,铜渣中的Fe2SiO4也很难发生自身分解反应,这是因为铁橄榄石的结构复杂,密度高,内部结构坚硬,很难进行磨矿且化学性质稳定。而当体系中存在一定量的C或者CaO时,在一定温度下Fe2SiO4即可发生大量分解反应。这是由于CaO的添加,改变了整个体系的碱度,破坏铁橄榄石的结构,把铁橄榄石中的氧化亚铁置换出来,同时提高氧化亚铁的活性,进而在较低温下便可开始发生还原反应[10]。据c和d图结合相图[11]分析可知,当体系中同时存在一定量的碳与氧化钙时,铁橄榄石在相对较低温下就可发生反应生成最终生成Fe、CaSiO3(硅灰石)及CO。
2.1.2 温度对生成磷铁、Fe及磷的影响
为探究不同温度对生成磷铁的影响,在一定温度下进行热力学模拟得到磷铁、金属铁及单质磷见图4。在低温时生成的磷铁较少,随温度的升高反应生成磷铁逐渐增加,在1300℃左右达到极高值;而随温度继续升高,生成磷铁开始出现下降的趋势。体系中生成金属铁在前段温度1100℃出现上升,在1100~1300℃时生成的金属铁降低,往后又继续表现出升高的趋势。而体系中产生的单质磷含量很少,磷含量与温度出现线性相关的趋势。这是因为1100℃前主要是铜渣中的磁铁矿被C大量还原产生金属铁,同时产生的金属铁与磷发生反应产生磷铁。在1100~1300℃期间,铜渣中的铁橄榄石也开始发生还原反应产生金属铁,磷铁反应得到加强,生成磷铁的量增多导致金属铁量出现一定的降低,在1300℃时生成磷铁反应接近完成。继续温度升高,反应生成的磷铁开始发生逆向反应,进而导致磷铁的量在下降而金属铁与磷出现增加。
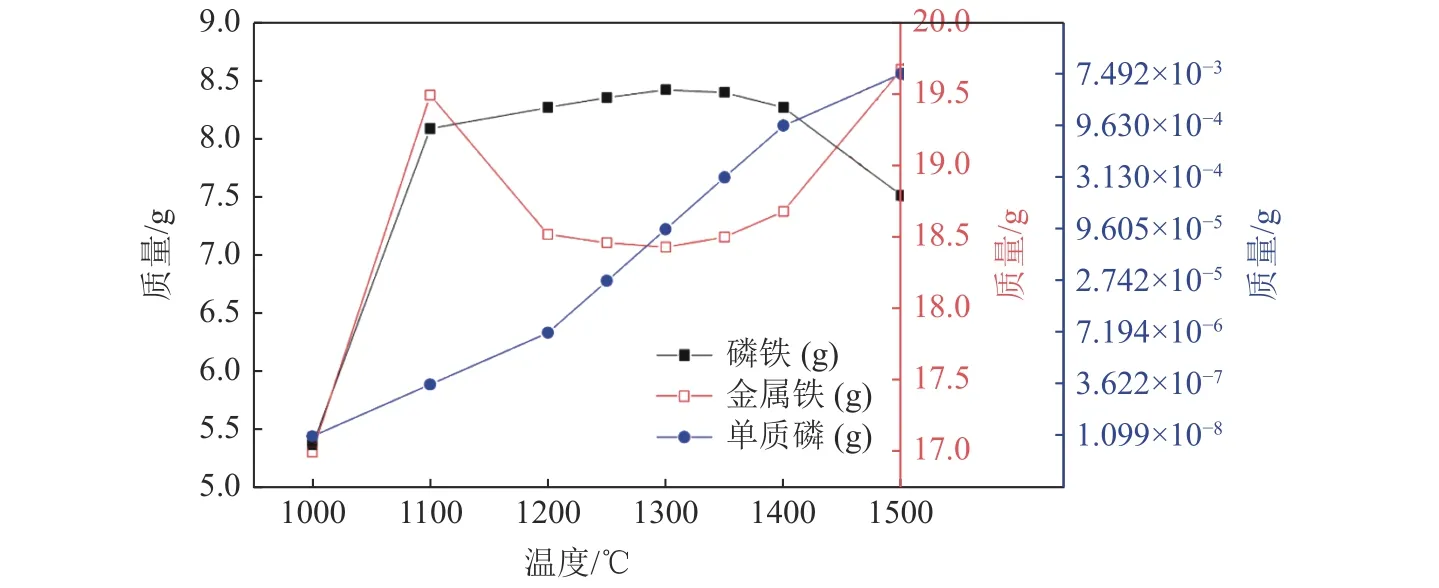
图4 不同温度下获得到磷铁、金属铁和单质磷Fig.4 Ferrophosphorus,metallic iron and phosphorus element were obtained at different temperatures
2.2 还原后失重率及生成磷铁量
为探讨碳热还原中低品位磷矿及铜渣制备磷铁的情况,对不同温度下试样的失重率及生成磷铁的影响进行探究,得到结果见图5。在温度为1200℃时,失重率较大,达39.5%左右,随着温度升高,试样的失重率为32.7%左右。低温时,分离得到磷铁较少,随着温度的升高量增加,在1350℃时接近最高为7 g左右;而随着温度增加到1400℃时,分离得到磷铁的量出现降低。低温时失重率高,高温失重率低,这是因为在还原过程中,碳与磷矿和铜渣发生反应产生大量气体并扩散出去,同时碳还原磷矿产成磷(g),而低温时体系液相少,铁和磷发生反应生成的磷铁较弱,磷来不及与铁大量接触反应生成磷铁而以气体的形式扩散出去,进而导致在低温时试样失重率很高;随着温度的升高,体系中液相增多,磷、铁扩散加快,磷挥发较少,生成磷铁的量多从而试样的失重率变低;随着温度的继续升高,生成磷铁的反应接近完成,故于1350℃时生成磷铁的量出现了一个较大值[12];而随着温度继续升高到1400℃时,由于生成Fe3P、Fe2P的热解性较弱,于是开始发生少量分解反应生成金属铁和磷,从而导致生成的磷铁降低[9]。

图5 不同温度下试样失重率及生成磷铁Fig.5 Weight lossratio and formation of ferrophosphorus at different temperature
2.3 微观结构分析
为观察高温还原生成磷铁的微观形貌变化,将不同温度下还原制得磷铁试样进行处理后经SEM进行扫描,得到的微观形貌及面扫见图6。在1200℃较低温度下,铁元素分布在整个区域中且较密集,磷元素的分布区域与铁的分布区域出现部分重合,表明此时生成的磷铁中含有金属铁。随温度升高到1300℃,磷与铁元素的分布区域绝大部分出现重合,而此时铁元素分布区域与1200℃相比的密集度稍微降低,碳和氧元素元素分布区域较为明显。温度继续升高到1350℃,铁和磷元素基本出现完全重合,说明此时生成的磷铁化合物较多,碳元素分布的区域更加显著且与铁和磷元素分布的区域不重合,说明碳是单独存在。随着温度继续升高到1400℃,磷与铁元素的分布区域的重合程度出现降低,说明反应生成的磷铁降低,这可能是因为在此时温度生成的磷铁出现了分解导致的结果。

图6 1200℃、1300℃、1350℃、1400℃温度下磷铁的微观形貌与面扫图Fig.6 Micromorphology and surfacescan of ferrophosphorus at temperatures of 1200℃,1300℃,1350℃and 1400℃
从微观形貌图中可知,在低温时试样表面出现少量的孔洞,而随着温度的升高,出现的孔洞增多。这是因为在低温时,反应速率慢,反应不完全,产生气体少。而在高温时,反应速率得到加强,反应速率快,反应更加的完全,生成大量的气体。而在反应结束后冷却过程中,气体来不及扩散而被包裹在已熔融的磷铁相中,最终形成了孔洞。
从面扫图中可知,灰色(a)部分形成的是磷铁化合物,深灰色(b)部分主要是金属铁,黑色点或者孔洞(c)是碳,白色(d)的亮点含有少量的氧。对试样表面不同衬度进行打点分析,得到的结果见表2。衬度a主要含有磷和铁,其他元素基本没有,说明生成的磷铁化合物较纯,同时不同温度下,磷及铁元素的含量差别不大,从原子比上来看可能形成Fe3P、Fe2P且含有金属铁。衬度b主要是金属铁,其中含有少量的碳且随温度的升高铁含量有所降低而碳含量有所增加,这是因为一方面高温时形成液相增多,物质扩散速率加快;另一方面反应得到的金属铁含量增多,生成的磷铁反应加强。衬度c是打在黑色点或者孔洞处,主要是碳且随着温度的升高,碳含量增大,铁含量出现降低的现象,结合失重率来看,高温时产生大量气体同时还原得到产物增多阻碍气体向外扩散,进而导致碳发生沉积而失重率降低碳含量增多现象。衬度d是打在白色亮点上,可看出其中氧含量相对较多且随着温度的升高含量出现降低的趋势,这是因为在低温时反应较弱、不完全而高温时反应增强、完全的结果。
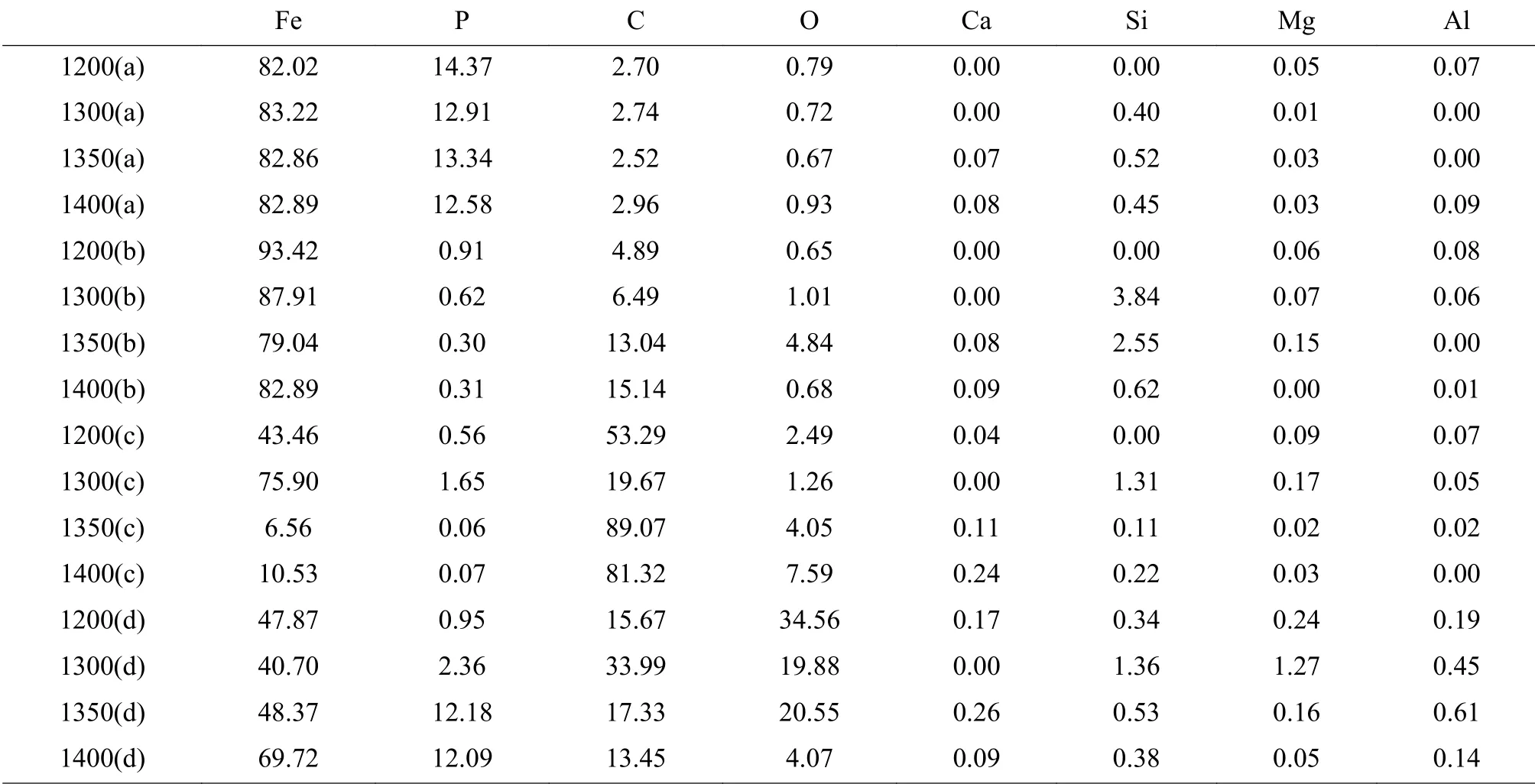
表 2不同温度下点扫描结果/%Table 2 Spot scan resultsat different temperatures
2.4 还原后物相分析
2.4.1 还原后磷铁物相分析
为探究不同温度下还原制备得到磷铁的物相变化,对不同温度下测得的磷铁XRD结果见图7。在1200℃时出现了Fe3P、Fe与C的图谱,碳的峰值相对较强且与金属铁和磷铁的峰出现了一处重合,磷铁的峰值也比较强。这是因为在此时发生了固相反应,温度低反应较弱、不完全导致出现了残碳,同时在此时的温度已开始反应形成了Fe3P但形成的量较少。随温度升高到1250℃,出现的物相没有发生变化,仅仅是碳和磷铁化合物的峰值出现了相应的变化。此过程中发生的主要反应为:
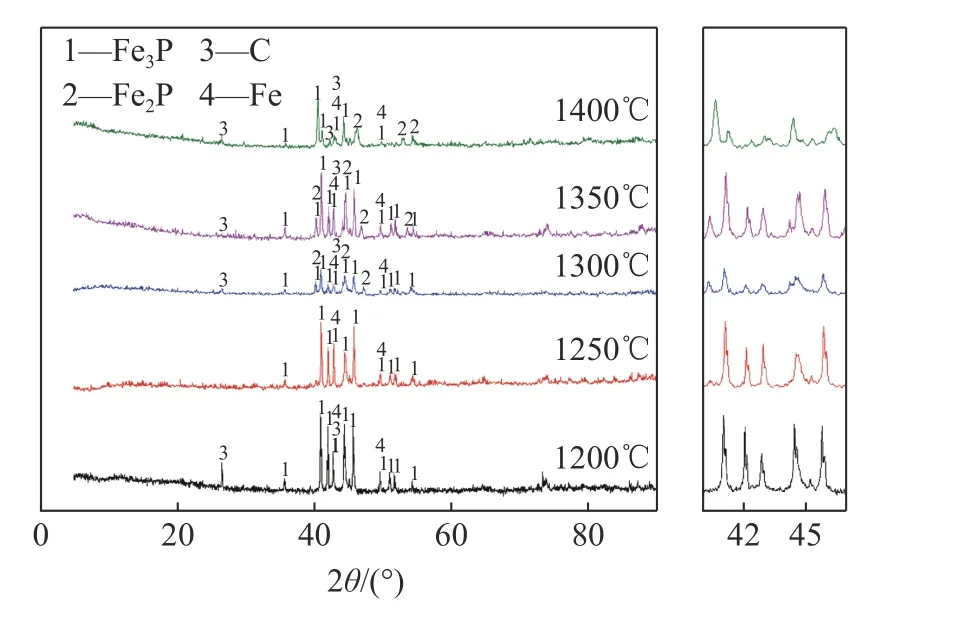
图 7还原后生成磷铁XRDFig.7 Diagram of ferrophosphorus XRD after reduction

随着温度的继续升高到1300℃,开始出现了新的物相磷二铁(Fe2P)图谱,此时其峰值比较弱。随温度的继续升高,体系中出现的物相没有发生变化,出现的Fe2P的峰增多且相较与1300℃时较强,说明此时生成Fe2P的反应发生剧烈,故得到的Fe2P量也增多。而随着温度升高到1400℃,可看出除了碳的峰值出现了增强外,Fe2P、Fe3P、Fe的峰值都出现了相应的减弱,这是因为在此时的温度下,磷铁已开始发生了部分分解,从而导致反应生成的量在减少,而碳的峰值在增强是因为布多尔反应发生逆向进行导致C发生了沉积而造成碳含量增多,进而导致失重率在降低。此过程中发生的主要反应如下:

2.4.2 还原后渣相物相分析
为研究还原分离磷铁后得到渣相的成分,对不同温度下的渣进行物相分析得到结果见图8。在1300℃之前得到的渣相基本无峰,据相图分析可知,在此之前得到的渣相为玻璃态[13];随着温度的升高氟磷酸钙大量分解,体系中的氧化钙增多,开始出现了CaSiO3的峰且峰值较弱,在1400℃时出现了新的物相硅酸铝,而此时偏硅酸钙的峰增多且增强,同时可知渣相中的主要物质为硅酸盐,物相是CaSiO3含带少量的硅酸铝(Al2SiO5)。发生的主要反应如下:

图8 还原后渣相XRDFig.8 XRD of slag after reduction

3 结论
(1)碳热还原磷矿和铜渣制备磷铁,在T<1300℃时,主要物相为Fe3P;在T>1300℃时,物相为Fe3P和Fe2P,其中含有少量的金属铁。
(2)在R(CaO/SiO2)=1.0,C=12%,t=60 min及不同温度条件下,经实验结果分析可知,在温度1350℃时失重率为32.4%,制得磷铁量最多7.03g。
(3)经高温还原焙烧反应后,得到的磷铁与渣易分离。还原温度T<1300℃时,渣相为玻璃态,还原温度T>1300℃冷却形成晶体,物相结合热力学模拟分析得到,最终生成渣的成分主要是硅酸盐类,其物相以偏硅酸钙(CaSiO3)为主和含有少量的硅酸铝(Al2SiO5)。

