特发性免疫性血小板减少症患儿血清中ITGB3和PRDX6水平及临床意义*
岐 锦,王 静,姚秀坤
山西省儿童医院(山西省妇幼保健院):1.营养科;2.血液科,山西太原 030002;3.山西医科大学,山西太原 030002
特发性免疫性血小板减少症(ITP)是一种以血小板(PLT)破坏、巨核细胞成熟障碍为特征的自身免疫性疾病[1]。ITP多见于儿童,目前,激素治疗和脾脏切除是治疗ITP的主要方案,但少数患儿仍出现复发或对药物不敏感等情况,使颅内出血等并发症发生风险增加。因此,发现合适的生化指标判断患儿的病情及预后对早期临床干预至关重要。整合素β3(ITGB3)是一种跨膜糖蛋白受体,由788个氨基酸组成,主要存在于PLT和巨核细胞表面,具有调控细胞黏附、凋亡及迁移和介导细胞与细胞外基质的连接等功能[2]。研究表明,ITGB3能够诱导血小板生成素活化,激活休眠中的造血干细胞(HSC),维持HSC活性,促进PLT合成[2]。过氧化物酶(PRDX)6属于非硒代谷胱甘肽过氧化物酶家族,其编码基因位于染色体1q24,相对分子质量约为25 000,主要存在于细胞质中,参与氧化应激、细胞凋亡及新陈代谢等过程[3]。研究表明,PRDX6失活能够促进巨核细胞凋亡,导致分化为PLT的数量下降,加速慢性ITP进展[3]。目前ITGB3和PRDX6在ITP中的报道少见,且与疾病严重程度和预后关系尚不清楚。因此,本研究旨在探讨ITP患儿血清中ITGB3和PRDX6水平及与疾病严重程度和预后的关系。
1 资料与方法
1.1一般资料 选取2018年3月至2021年8月山西省妇幼保健院收治的73例ITP患儿作为ITP组,同时选取70例相同年龄层来院体检的健康儿童作为对照组。ITP组中男32例、女41例,年龄1~11岁、平均(6.27±1.96)岁;对照组中男31例、女39例,年龄2~10岁、平均(6.33±1.78)岁。两组的年龄、性别差异均无统计学意义(P>0.05),具有可比性。ITP患儿纳入标准:(1)符合ITP诊断标准[4];(2)均为首次诊断ITP,且病程<4周;(3)既往未接受过激素或丙种球蛋白类药物治疗。排除标准:(1)伴有凝血功能障碍疾病,如:弥漫性血管内凝血、血友病及先天性凝血因子缺乏症等;(2)肝、肾功能障碍;(3)伴有先天或后天性免疫功能异常。本研究经山西省妇幼保健院伦理委员会批准,所有研究对象家属均签署知情同意书。
1.2方法
1.2.1血液指标的检测方法 所有研究对象均于空腹状态下采集10 mL静脉血置于抗凝管中。其中5 mL血液标本通过离心机(生产厂家:美国Labnet公司;型号:SCI-12)离心,离心条件为6 000 r/min(4 ℃)、离心半径10 cm、离心时间5 min,收集上清液,采用MC-6600全自动血常规分析仪(生产厂家:深圳市美思康电子有限公司)检测PLT计数,通过酶联免疫吸附试验检测血清中ITGB3和PRDX6水平。严格遵照试剂盒说明书进行操作。剩余的5 mL血液标本采用全光谱流式细胞仪(生产厂家:Cytek公司;型号:Aurora 3L)检测CD4+T细胞 /CD8+T细胞比值。将标本使用乙二胺四乙酸二钠进行抗凝,每个试管均加入20 μL的单克隆抗体,混匀后室温避光染色10~15 min,使用磷酸盐缓冲液洗涤1遍,弃上清液后加入磷酸盐缓冲液重悬细胞0.5 mL,之后加入肝素抗凝,用流式细胞仪检测。
1.2.2ITP严重程度分级 (1)轻度:PLT计数为(20~100)×109/L,小瘀斑和出血点较少。(2)中度:PLT计数为(10~20)×109/L,大瘀斑(直径>5 cm)和出血点较多,伴有牙龈、鼻、消化道反复出血,偶见血尿、血便及咳血表现。(3)重度:PLT计数<10×109/L,全身广泛大瘀斑和出血点,伴有牙龈、口腔及咽部持续性出血,偶见内脏出血或颅内出血[5]。
1.2.3ITP的治疗方法及预后评估 (1)对于PLT计数≥20×109/L且无内脏出血者,采用地塞米松(生产企业:广东华南药业集团有限公司;批准文号:国药准字H44024469)治疗,静脉注射,剂量为1 mg/(kg·d),最大剂量≤15 mg。当PLT计数恢复正常后,采用泼尼松(生产企业:华中药业股份有限公司;批准文号:国药准字H42021394)治疗,口服,初始剂量为1.5~2.0 mg/(kg·d),逐渐减量至停用。(2)对于PLT计数<20×109/L或伴有内脏出血者,采用地塞米松联合丙种球蛋白(生产企业:华兰生物工程股份有限公司;批准文号:国药准字S10970034)治疗。地塞米松用法、用量与(1)中一致。丙种球蛋白的剂量为400 mg/(kg·d),静脉注射。当血PLT计数恢复正常后,采用泼尼松口服,用法、用量与(1)中一致。(3)若(1)和(2)在经过2周治疗后,尚未达到理想疗效,则采用甲泼尼龙(生产企业:天津天药药业股份有限公司;批准文号:国药准字H20020223)实施冲击治疗,剂量为10 mg/(kg·d),连续使用5 d,再次评估PLT计数,采用(1)或(2)中的治疗方案。此外,在治疗期间进行针对性的饮食管理,如:改善饮食结构、低钠低胆固醇饮食、多食用含铁的绿叶蔬菜及增加摄入含有凝血止血成分的食物(银耳、红枣、红衣花生及荷叶等)。治疗周期为4周,若PLT计数未升高,且临床症状未改善,则判断为预后不良[5]。

2 结 果
2.1两组研究对象血液指标的比较 ITP组PLT计数、CD4+T细胞/CD8+T细胞比值及血清中ITGB3、PRDX6水平均较对照组明显下降(P<0.05),见表1。

表1 两组研究对象血液指标的比较
2.2不同严重程度ITP患儿各项血液指标的比较 重度患儿PLT计数、CD4+T细胞/CD8+T细胞比值及血清中ITGB3、PRDX6水平均低于中度及轻度患儿,差异均有统计学意义(P<0.05);中度患儿PLT计数、CD4+T细胞/CD8+T细胞比值及血清中ITGB3、PRDX6水平低于轻度患儿,差异均有统计学意义(P<0.05)。见表2。

表2 不同严重程度ITP患儿各项血液指标的比较
2.3血清中ITGB3、PRDX6水平与PLT计数、CD4+T细胞/CD8+T细胞比值的相关性 血清中ITGB3、PRDX6水平与PLT计数、CD4+T细胞/CD8+T细胞比值均呈正相关(r>0,P<0.05),见表3。

表3 血清中ITGB3、PRDX6水平与PLT计数、CD4+T细胞/CD8+T细胞比值的相关性
2.4不同预后情况的ITP患儿血清中ITGB3、PRDX6水平差异 经治疗,预后良好患儿64例,预后不良患儿9例。预后不良患儿血清中ITGB3、PRDX6水平较预后良好患儿明显下降(P<0.05),见表4。

表4 不同预后情况的ITP患儿血清中ITGB3、PRDX6水平比较
2.5血清ITGB3、PRDX6水平对ITP患儿预后不良的诊断价值 以ITP患儿是否出现预后不良为前提绘制ROC曲线。ITGB3、PRDX6判断ITP患儿预后不良的最佳截断值分别为105.31 pg/mL、28.98 pg/mL,曲线下面积(AUC)分别为0.786、0.741(Z=3.824,P<0.05;Z=2.841,P<0.05)。两指标联合检测判断ITP患儿预后不良的AUC为0.852(Z=6.799,P<0.05),其灵敏度和特异度分别为88.89%和78.12%。见表5和图1。

表5 血清ITGB3、PRDX6水平对ITP患儿预后不良的诊断价值
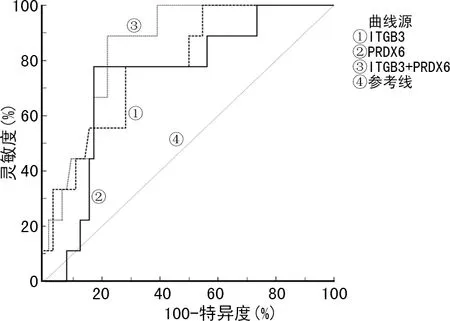
图1 血清ITGB3、PRDX6水平诊断ITP患儿预后不良的ROC曲线
3 讨 论
儿童ITP的具体发病机制与机体免疫失耐受所致的血小板破坏及生成不足有关。皮肤黏膜出血、牙龈出血及鼻出血是ITP的主要临床表现,严重者可能出现内脏出血或颅内出血,危及患者生命。目前,PLT计数是判断ITP严重程度的常用指标,但也有其局限性,而针对ITP的预后评估尚无法做出有效判断。因此,为了帮助临床在早期采用更加合理的治疗方案,探索合适的生化指标辅助评估ITP的预后情况是必要的。
ITGB3又称CD61,是一种Ca2+依赖的异源二聚体复合物,相对分子质量为(90~110)×103,其编码基因位于17号染色体,包括αvβ3 和αⅡbβ3两种类型,参与调节胚胎发育、伤口愈合、凝血止血及免疫应答等病理生理过程[6]。BERTRAM等[7]发现,在拮抗ITGB3后,小鼠脑血管内皮细胞大量凋亡,血管密度减低,血管生成相关因子沉默,从而导致颅内出血。在ITGB3基因缺失的小鼠中,循环血管生成细胞分化减少,同时对损伤的内皮细胞下膜的黏附性降低,无法与纤维蛋白原结合,提高了血管渗血或出血的风险[6]。本研究结果表明,ITP组血清中ITGB3水平较对照组明显下降(P<0.05),提示ITGB3可能是影响ITP发病的重要因素。其原因可能是抗PLT自身抗体能够特异性识别PLT表面的ITGB3,抗体与ITGB3结合后,诱导巨噬细胞将其吞噬分解,使血清中的ITGB3水平降低[8]。本研究结果显示,随着ITP严重程度的增加,血清中ITGB3水平逐渐降低(P<0.05),提示ITGB3可能参与了ITP的进展。其机制可能是血清中ITGB3水平降低后,其自身的ICY 结构域失活,发生去磷酸化,阻碍信号转导蛋白和细胞骨架蛋白肌球蛋白在糖蛋白(GP)Ⅱb /Ⅲa结构域中积聚,从而使PLT活性丧失,加重ITP病情[8]。此外,ITGB3失活能够诱导内皮细胞凋亡,使血管通透性增加,同时,内皮细胞凋亡使机体凝血系统异常,PLT合成受阻,导致血清中PLT计数下降[2,9]。
PRDX6是仅含有1个保守半胱氨酸(Cys)残基的PRDX超家族成员,包含224个氨基酸,同时具有磷脂酶A2(PLA2)和谷胱甘肽(GSH)过氧化物酶功能,在抵御细胞膜表面氧化应激损伤方面发挥重要作用[10]。VRBENSKY等[10]研究发现,当PRDX6失活时,白细胞介素-1表达增加,促进肿瘤坏死因子释放,抑制花生四烯酸合成,阻碍PLT激活,并诱导血管内皮细胞凋亡。动物实验表明,在PRDX6基因敲除的大鼠体内,炎症细胞浸润程度增加,促进活性氧(ROS)释放,抑制PLT生长因子活性,提高大鼠肺泡出血风险[11]。本研究结果表明,ITP组血清中PRDX6水平较对照组明显下降(P<0.05),提示PRDX6可能在ITP发病过程中起到重要作用。其原因可能是PRDX6基因启动子沉默,无法转录合成PRDX6,造成血清中PRDX6水平下降,但其具体调控机制尚不清楚[12]。本研究结果表明,随着ITP严重程度的增加,血清中PRDX6水平逐渐降低(P<0.05),提示PRDX6可能在ITP进展具有调控作用。其原因可能是PRDX6下调后能够激活丝/苏氨酸激酶(AKT)信号通路,促进促凋亡蛋白Bad磷酸化,诱导PLT失活,促进ITP进展[12]。此外,PRDX6活性降低能够使ROS大量合成,促进线粒体去极化,使内环境处于氧化还原状态,各种凋亡相关蛋白被激活,促进PLT凋亡[13]。
本研究结果表明,血清中ITGB3、PRDX6水平与PLT计数、CD4+T细胞 /CD8+T细胞比值均呈正相关(P<0.05),提示血清中ITGB3、PRDX6水平能够在一定程度上反映机体免疫应答状态和血液中PLT含量。其机制可能是ITGB3水平降低能够促进内皮细胞凋亡,使细胞间黏附分子-1(ICAM-1)下调,抑制CD4+T细胞活性,导致CD4+T细胞 /CD8+T细胞比值失衡,诱导B淋巴细胞产生识别PLT的特异性抗体,破坏血管内的PLT[14]。PRDX6下调后无法消耗ROS,导致机体内ROS水平明显上升,使CD4+T细胞对有丝分裂原不应答,抑制其分裂、增殖,使CD4+T细胞/CD8+T细胞比值下降,同时,过量的ROS通过氧化应激反应使巨核细胞的细胞膜受损,无法分化PLT,导致PLT计数下降[15]。本研究中预后不良患儿血清中ITGB3、PRDX6水平均较预后良好患儿明显下降(P<0.05),提示ITGB3和PRDX6水平可能影响ITP患儿的预后情况,对辅助临床早期筛查具有重要意义。ROC曲线显示,ITGB3和PRDX6联合检测判断ITP患儿预后不良的AUC明显高于ITGB3、PRDX6单一检测的AUC,灵敏度和特异度分别为88.89%和78.12%,提示两指标联合检测能够提高对ITP患儿是否发生预后不良的诊断价值,同时,联合检测的灵敏度明显高于单一指标检测,有利于早期筛查可能发生预后不良的患儿,为临床早期进行针对性治疗提供可靠支持。
综上所述,ITP患儿血清中ITGB3和PRDX6水平降低。同时,血清中ITGB3和PRDX6水平能够反映机体免疫应答状态和PLT计数。这两指标联合检测对ITP患儿是否发生预后不良具有良好的诊断效能,且灵敏度较高,为临床早期针对性治疗提供帮助。但受试验设备的限制,血清中ITGB3和PRDX6水平变化的具体机制尚不清楚,需要在后续的基础实验中进一步证实。

