芪归银方对左氧氟沙星大鼠半体内抗耐药铜绿假单胞菌的PK/ PD 分析
张婉乔 李颜伶 吴 珺 刘清泉 徐 广 秦 铭 吉 莉 马 群
1.北京中医药大学中药学院,北京 102488;2.北京中医药大学生命科学学院,北京 102488;3.首都医科大学附属北京中医医院中医科,北京 100010
铜绿假单胞菌(Pseudomonasaeruginosa,PA)为革兰氏阴性菌,具有耐药性强,耐药机制复杂的特点,耐药PA 所致的重症肺炎死亡率较高[1-3]。左氧氟沙星(Levofloxacin,LVFX)是氟喹诺酮类抗菌药物,可用于治疗由PA 引发的各种感染性疾病[4-5]。近年来LVFX抗菌活性下降,PA 对LVFX 的耐药率始终保持在30.0%以上[6-8]。
芪归银方由黄芪、当归、金银花、青蒿和虎杖五味中药组成,具有攻补兼施、扶正透邪之功。前期研究表明,芪归银方与抗生素联用能够提高抗生素对多重耐药菌感染的治疗效果[9-14]。本研究通过建立并评价LVFX 单用及LVFX 联用芪归银方后的药动学/药效学(pharmacokinetic/pharmacodynamics,PK/PD)模型,探索芪归银方对LVFX 抗PA 的影响。
1 材料
1.1 药品与试剂
黄芪、当归、金银花、青蒿和虎杖(北京三和药业有限公司,批号:90541102、93451002、90280901、9305 1001、90510501),北京中医药大学中药资源与鉴定系杨瑶珺教授鉴定为正品;左氧氟沙星片[第一三制药(北京)有限公司];左氧氟沙星标准品、盐酸环丙沙星(上海源叶生物技术有限公司,批号:W14M11H113063、Y04D8C49703);甲醇、乙腈、甲酸均为质谱级。
1.2 仪器
ACQUITY 型超高效液相色谱系统(美国Waters公司),XevoTQ-SMicro 型三重四级杆质谱仪(美国Waters 公司),SorvallST8R 型高速冷冻离心机(美国Thermo 公司),XW-80A 型旋涡混合仪(海门市其林贝尔仪器制造有限公司),CM-24 型水浴氮吹仪(北京成萌伟业科技有限公司),LERD-Tech 型恒温培养箱[立德泰勊(上海)科学仪器有限公司],DNM-9602G 型酶标分析仪(北京普朗新技术有限公司)。
1.3 实验动物与菌株
SPF 级Wistar 雄性大鼠6~7 周龄,体重240~260 g,购于北京维通利华实验动物技术有限公司,许可证号SCXK(京)2016-0006;饲养条件:室温(23±2)℃,相对湿度为(60±5)%。本研究通过动物实验伦理学审核(BUCM-4-2021113001-4079);多重耐药铜绿假单胞菌临床分离株(No.1912109)由北京中医药大学东直门医院检验科提供。
1.4 大鼠灌胃液的制备
1.4.1 芪归银方灌胃液 黄芪、金银花、当归、青蒿和虎杖(12∶3∶2∶3∶2)加去离子水提取3 次,合并水提液,浓缩至生药浓度为1.0 g/ml,加乙醇至醇浓度为60%,4℃静置24 h。上清液挥发至无醇味后干燥,得提取物浸膏。按临床处方量将提取物浸膏加蒸馏水稀释得1 g/ml 生药浓度的灌胃液。
1.4.2 LVFX 灌胃液 取LVFX,按临床处方量加蒸馏水稀释得0.01 g/ml 浓度的灌胃液。
1.5 超高效液相色谱-串联质谱分析方法的建立
1.5.1 溶液的制备LVFX 标准品1.0 mg,置于10 ml 容量瓶中,加甲醇定容。使用前,加甲醇稀释至浓度为0.2、0.4、1.0、2.0、4.0、10.0、20.0、40.0 μg/ml 的LVFX系列标准溶液备用。同法配制浓度为5 μg/ml 的环丙沙星(Ciprofloxacin,CPFX)内标液,4℃保存备用。
1.5.2 检测条件 ACQUITY UPLC CSH C18(2.1 mm×100 mm,1.7 μm),流速0.4 ml/min,柱温40℃,进样体积1 μl。流动相0.1%甲酸水(A)-乙腈(B),梯度洗脱:0~0.1 min,90%→85%A;0.1~3.0 min,85%→20%A;3.0~3.5 min,20%→90%A。质谱条件:电喷雾离子源,正离子模式,离子对选择LVFX m/z=362.239 5~261.176 7,锥孔电压44 V,碰撞能量22 eV;CPFX m/z=332.165 1~245.191 9,锥孔电压42 V,碰撞能量20 eV。毛细管电压2.5 kV,离子源温度150℃,去溶剂气温度350℃,去溶剂气流速650 L/h,多反应监测模式检测。
1.6 实验分组及处理
1.6.1 实验分组和样品采集 大鼠适应性喂养3 d 后,分为空白组、单用组、联用组,每组5 只。单用组灌胃0.01 g/ml LVFX(0.003 0 ml/g 大鼠);联用组先灌胃1 g/ml 血药浓度的芪归银方(0.011 5 ml/g 大鼠),再灌胃0.01 g/ml VFX(0.003 0 ml/g 大鼠);空白组灌胃等量蒸馏水。末次给药前12 h 禁食不禁水,末次给药后0、0.25、0.50、1.00、1.50、2.00、4.00、8.00、12.00、24.00 h眼眶取血,4℃3 500 r/min 离心15 min(离心半径6.6 cm)分离血清,56℃水浴30 min,灭活,-80℃保存。
1.6.2 血清样品预处理与分析 取含药血清20 μl,加5 μl 甲醇、5 μl 内标液混匀,50 μl 甲醇沉淀蛋白,涡旋1 min,4℃14 000 r/min 离心15 min 取上清液,氮气吹干后加入1 ml 初始比例的流动相复溶,涡旋30 s,离心,取上清液。
1.7 统计学方法
采用SPSS 21.0 软件进行数据分析。计量资料用均数±标准差()表示,比较采用t 检验;计数资料用例数或百分率表示。以P <0.05 为差异有统计学意义。
2 方法与结果
2.1 线性范围
取空白血清20 μl,分别加入LVFX 系列标准溶液各5 μl,内标液5 μl,配成内标溶液终浓度为25 ng/ml,LVFX 终浓度分别为200、100、50、20、10、5、2、1 ng/ml 的系列浓度血清样品。按“1.6.2”项下进样测定,以LVFX 峰面积As 与内标峰面积Ai 的比值(Y)对LVFX 浓度(X)作权重回归。LVFX 在血清中标准曲线方程为Y=0.113 2X+0.140 0,r=0.999。
2.2 精密度试验
取空白血清20 μl,加入LVFX 标准溶液5 μl,配置5、20、100 ng/ml 的样品,每个浓度5 个样品,处理后连续进样5 次,得日内精密度,连续进样5 d,得日间精密度。结果显示,LVFX 在大鼠血清中的日内精密度平均RSD 值为7.70%,日间精密度平均RSD值为7.56%。
2.3 稳定性试验
制备LVFX 5、20、100 ng/ml 的血清样品各5 份,分别在室温25℃放置4 h,-80℃冰箱冷冻14 d 及-20℃冰箱冷冻-室温解冻反复冻融3 次,处理后进样。结果显示,3 种条件下平均RSD 值分别为7.00%,4.83%和6.88%。
2.4 提取回收率
制备5、20、100 ng/ml 的LVFX 血清样品各5 份,进样分析,结果显示高、中、低三个浓度下LVFX 平均提取回收率为81.03%~93.46%,平均RSD 值为7.28%。
2.5 基质效应
①配制LVFX 低、中、高浓度分别为5、20、100 ng/ml的甲醇溶液各5 份;②配制LVFX 浓度为5、20、100ng/ml的空白血清样品各5 份,处理后测定,基质效应=响应值②/响应值①×100%[20]。结果显示基质效应范围为86.74%~92.00%,平均RSD 值为3.18%。
2.6 PK 实验及结果
处理后的血清样品按“1.5”项下进样分析,采用DAS 2.0 软件计算PK 参数,采用SPSS 21.0 软件进行统计分析。结果显示,单用组与联用组曲线下面积(area under the curve,AUC)、最大血药浓度(Cmax)、平均滞留时间[MRT(0-t)]、达峰时间(Tmax)和清除率比较,差异有统计学意义(P <0.05)。见图1、表1。
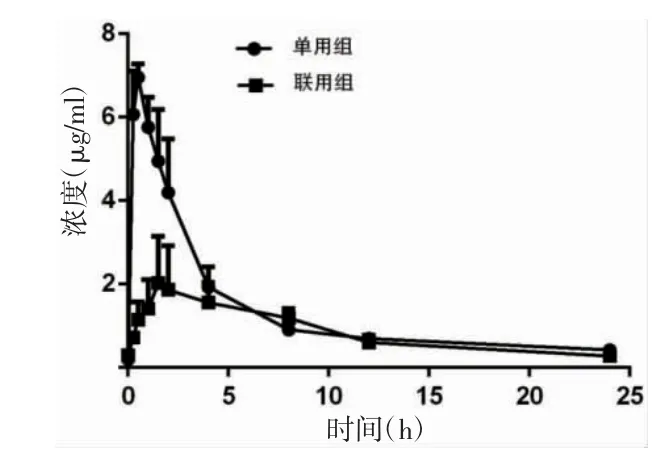
图1 单用组及联用组大鼠血清中平均药物浓度-时间曲线
表1 单用组及联用组PK 参数(n=5,)
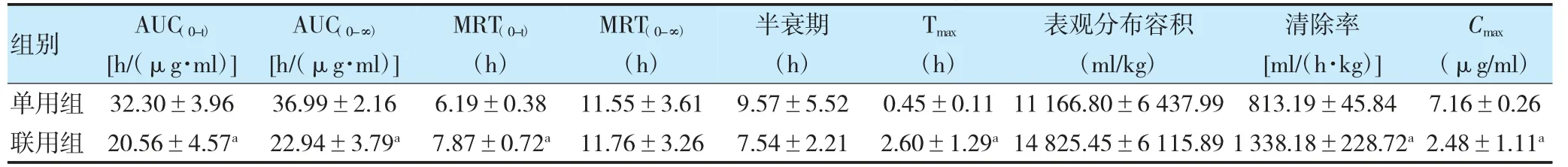
表1 单用组及联用组PK 参数(n=5,)
注 与单用组比较,aP <0.01。PK:药代动力学;AUC:曲线下面积;MRT:平均滞留时间;Tmax:达峰时间;Cmax:最大血药浓度
2.7 PD 实验及结果
2.7.1 最低抑菌浓度(minimal inhibitory concentration,MIC)测定 采用肉汤稀释法测定单用组及联用组对耐药PA 的MIC 值。结果显示,单用组MIC 为8 μg/ml,联用组MIC 为4 μg/ml。
2.7.2 抑菌率测定 取PA 单个菌落接种并培养后,配制1.5×108CFU/ml 的PA 菌液。用MHB 培养基稀释得1×106CFU/ml 的PA 肉汤培养基混合液。取50 μl各时间点的血清于96 孔板中,每孔中加入PA 肉汤培养基混合液50 μl,3 个平行孔。另设含空白血清的阳性和阴性对照孔平行对照。37℃培养24 h 后测定各孔吸光度值,计算含药血清对PA 的抑菌率。结果显示,单用组和联用组的抑菌率初始值4.49%和37.40%,在给药24 h 后的血清抑菌率为7.69%和32.91%。见图2。
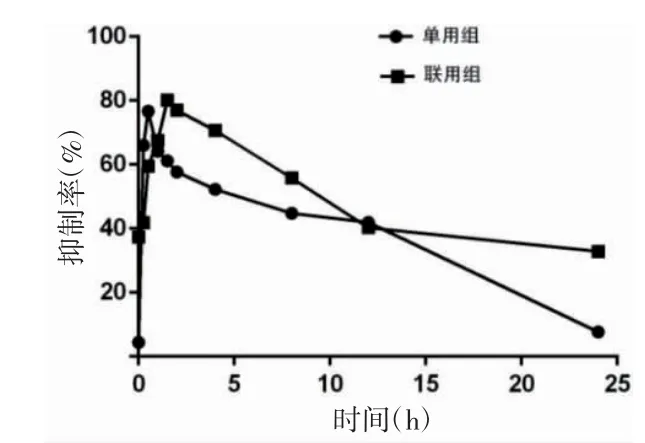
图2 单用组及联用组大鼠血清抑菌效应-时间曲线
2.8 PK/PD 模型的建立
计算大鼠血清半体内各时间点平均孔内浓度Ci和各个时间点血清的半体内AUC24h值(AUC24h=Ci×24),采用Phoenix WinNonlin 软件拟合半体内参数AUC/MIC 与抑菌效果,以标准偏差和变异系数评估模型拟合精度,以最小信息化准则(akaike information criterion,AIC)值评估模型拟合优度,确定最优模型。结果显示,单用组采用无基线SigmoidEmax 模型(E0=0)拟合效果较好,AIC 值为73.08;联用组采用有基线SigmoidEmax 模型拟合效果较好,AIC 值为47.39。以血清抑菌率为药效指标,通过Phoenix WinNonlin 软件拟合得到两组的PK-PD 参数,见表2。单用组半体内PK/PD 模型为E=(63.80×C2.96)/(0.94+C2.96);联用组半体内PK/PD 模型为E=34.72+(57.88×C3.04)/(66.63+C3.04)。
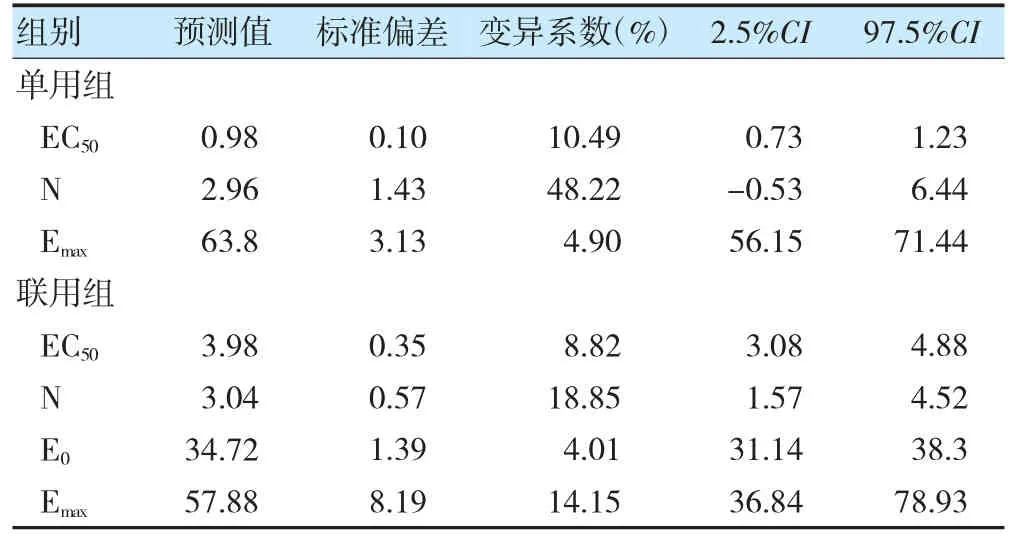
表2 以血清抑菌率为药效指标的PK-PD 参数
3 讨论
本研究结果中LVFX 单用时的Tmax及Cmax与文献[15-16]报道基本一致,提示本研究结果准确可信。本研究结果显示,联用芪归银方虽然减慢了LVFX 在大鼠体内的吸收速度和程度,但可使其在体内的平均滞留时间延长,控制LVFX 在体内的释放速度;联用芪归银方后血清抑菌率的初始值较高,达峰时间较长,给药24 h 后抑菌率继续保持在30%以上。芪归银方中黄芪提取物、青蒿精油、虎杖中分离的醌类化合物和当归总黄酮醇提液对大肠埃希菌、沙门菌、枯草芽孢杆菌、金黄色葡萄球菌等有抑制作用;且金银花能破坏PA 生物膜的形成,达到抑菌效果[17-26]。芪归银方联用对LVFX 抗耐药PA 的优势除了协同作用外,可能与其中中药成分的抑菌作用有关。同时,PK/PD 模型显示大鼠体内LVFX 不同时间点的血药浓度与其抑菌率有一定的相关性,芪归银方可能通过影响LVFX 在大鼠体内的血药浓度从而增强LVFX 对耐药PA 的抑制效果。

