石墨烯量子点复合材料的制备及其对抗坏血酸的荧光检测
赵宝茹,王健恺,黄鑫,王悦,杜小雨,张永,马文辉
石墨烯量子点复合材料的制备及其对抗坏血酸的荧光检测
赵宝茹1,王健恺1,黄鑫1,王悦1,杜小雨1,张永2,马文辉1*
(1.齐齐哈尔大学 化学与化学工程学院,黑龙江 齐齐哈尔 161006;2.齐齐哈尔大学 材料科学与工程学院,黑龙江 齐齐哈尔 161006)
设计并制备了一种在纯水系中荧光增强识别抗坏血酸(AA)的石墨烯量子点复合材料NB-GQDs@MOF-5,利用TEM、FT-IR和XRD对其形貌和结构进行了表征,结果表明NB-GQDs与MOF-5成功复合。荧光检测结果表明,在纯水体系中,NB-GQDs@MOF-5可在考察的有机小分子及阳离子范围内专一性地识别AA,滴加AA后引起荧光增强8.1倍,检出限为0.039μmol/L。
石墨烯量子点;MOF-5;荧光识别;抗坏血酸
抗坏血酸(AA)是一种重要的营养物质,其在保障人体健康方面发挥着不可替代的作用,其含量的增加或缺乏均会引起不良反应,其检测方法主要有液相色谱法[1]、电化学法[2]和荧光法[3]等。荧光探针法用于AA的检测虽有灵敏度高、选择性好、成本低、操作简单等优点,但大多数有机小分子探针因毒性大、水溶性差而在实际应用中存在许多限制[4-5]。石墨烯量子点(GQDs)集量子限域、尺寸效应等于一体,还兼具良好的生物相容性、优异的发光性能等优势,在化学传感、超级电容器和医学治疗等领域具有良好的应用前景[6-8]。金属有机骨架材料(MOF)具有巨大的比表面积、超高的孔隙率、可调的孔尺寸、可修饰的官能团等特点,这使其在气体吸附与分离、催化、荧光检测等领域有着广泛应用[9-11]。将GQDs与MOF结合制备新型复合材料用于荧光检测具有潜在的研究空间。本文以柠檬酸、硼砂和乙二胺为原料,采用水热法制备N、B共掺杂的石墨烯量子点(NB-GQDs),后与MOF-5的前体溶液进行复合制备得到了新型石墨烯量子点复合材料(NB-GQDs@MOF-5)。光谱实验表明,在纯水体系中其能够高选择性和高灵敏性检测AA。
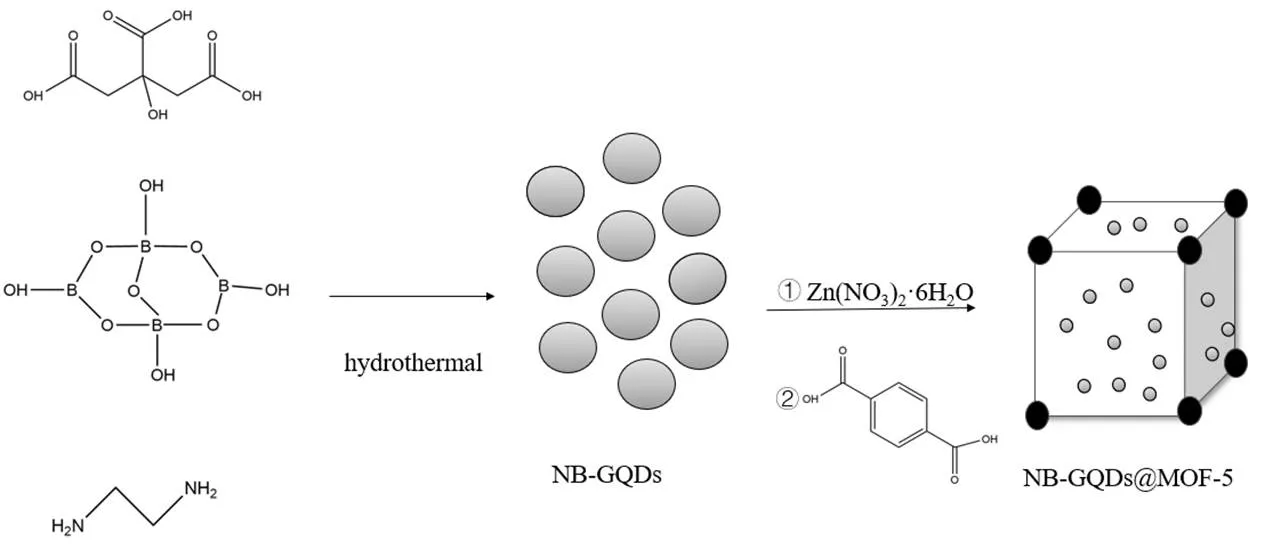
图1 NB-GQDs@MOF-5的合成路线
1 实验部分
1.1 主要试剂与仪器
柠檬酸,分析纯,哈尔滨化工化学试剂厂;硼砂,分析纯,天津市科密欧化学试剂有限公司;对苯二胺,分析纯,郑州兴隆化工有限公司;对苯二甲酸,分析纯,天津市元立化工有限公司;六水合硝酸锌,分析纯,沈阳化学试剂厂;葡萄糖,分析纯,天津市科密欧化学试剂有限公司;抗坏血酸,分析纯,北京成宇化工有限公司;氨基酸,分析纯,北京百灵威科技发展有限公司;MD55-5M透析袋(MW:1000),北京索莱宝科技有限公司;其他试剂均为市售分析纯;阳离子均为硝酸盐。
H-7650型透射电子显微镜,日本日立公司;D8-FOCUS X-射线衍射仪,德国布鲁克公司;Spectrum One傅里叶变换红外光谱仪,美国珀金埃尔默公司;ESCALAB 250Xi X射线光电子能谱仪,美国赛默飞公司;TU-1901双光束紫外可见分光光度计,北京普析通用仪器有限责任公司;LS55荧光分光光度计,美国珀金埃尔默公司。
1.2 NB-GQDs@MOF-5的合成
NB-GQDs和MOF-5分别参照文献[12, 13]制备。将77 mg NB-GQDs分散在30 mL的N,N-二甲基甲酰胺中,超声分散后加入1210 mg(4.06 mmol)六水合硝酸锌和340 mg(2.04 mmol)对苯二甲酸,于25℃下反应3 h后将反应液过滤,分别用N,N-二甲基甲酰胺、无水乙醇、蒸馏水反复洗涤三次,真空干燥得浅紫色粉末NB-GQDs@MOF-5。
1.3 NB-GQDs@MOF-5的光谱性能测试
配制浓度为30 mg/L的NB-GQDs@MOF-5测试液,等量移取3 mL,分别加入浓度为0.1 mol/L的小分子及阳离子(丝氨酸、酪氨酸、脯氨酸、白氨酸、缬氨酸、葡萄糖、K+、Na+、Zn2+、Co2+、Ni2+、Pb2+),充分摇匀,利用荧光分光光度计测试荧光光谱。
2 结果与讨论
2.1 NB-GQDs@MOF-5的形貌和结构表征
通过TEM、FT-IR、XRD和XPS等手段研究了NB-GQDs@MOF-5的形貌结构特征。图2为NB-GQDs、MOF-5和NB-GQDs@MOF-5的TEM图,可以看出,NB-GQDs粒径均匀分布,MOF-5具有立方体结构,尺寸在100 nm左右,NB-GQDs@MOF-5与MOF-5具有相似的形貌,并可以明显的观察到NB-GQDs的存在,证明了NB-GQDs与MOF-5成功复合。

图2 NB-GQDs(a), MOF-5(b), NB-GQDs@MOF-5(c)的TEM图像
图3为NB-GQDs, MOF-5及NB-GQDs@MOF-5的XRD图谱(插图为NB-GQDs及NB-GQDs@MOF-5局部放大图)。NB-GQDs@MOF-5在2=6.82°, 9.58°, 13.68°, 15.44°等位置出现了MOF-5的特征峰,分别对应MOF-5的(200), (220), (400), (420)晶面。表明NB-GQDs的掺杂并没有影响MOF-5本来的晶型,MOF-5的骨架没有发生改变。并且在23.5°处出现了石墨烯结构的衍射峰,对应石墨烯结构的(002)晶面[14-15],证明NB-GQDs与MOF-5成功复合。
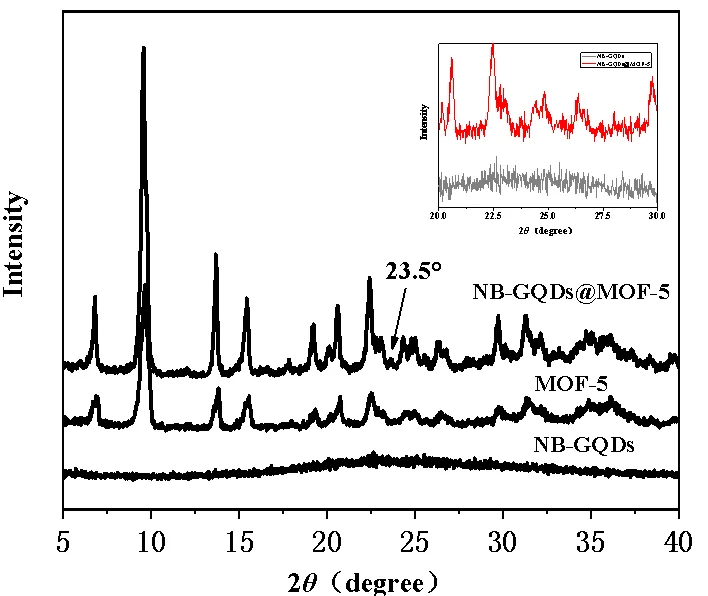
图3 NB-GQDs, MOF-5, NB-GQDs@MOF-5的XRD谱图
图4为NB-GQDs, MOF-5及NB-GQDs@MOF-5的FT-IR光谱图。图4中NB-GQDs@MOF-5在478.5 cm-1的吸收峰归属于Zn—O的伸缩振动。1102.50 cm-1归属于B—C的伸缩振动峰,1152.52 cm-1归属于B—O—H的伸缩振动峰,1310.60 cm-1归属于C—N—C的伸缩振动峰,1391.78 cm-1是B-O的伸缩振动峰。1505.60 cm-1, 1658.97cm-1, 3429.61cm-1分别是C=N, N—C=O, O/N—H的伸缩振动峰[12]。制备的NB-GQDs@MOF-5同时具有NB-GQDs和MOF-5的特征吸收带,证明NB-GQDs与MOF-5成功复合。
2.2 NB-GQDs@MOF-5对AA的识别
图5是NB-GQDs@MOF-5的荧光滴定光谱(插图:荧光强度(440nm)与AA(333.33~1333.33μmol/L)浓度关系图)。向NB-GQDs@MOF-5(30mg/L)溶液中加入AA,随着AA浓度的增加体系荧光强度增强,当AA浓度达到1333.33μmol/L时,荧光强度增至最大;当AA的浓度范围为333.33~1333.33μmol/L时,体系荧光响应与AA浓度呈良好的线性关系2= 0.9912,其线性拟合方程为= 43.0001-50.2017,最低检出限公示LOD = 3/(为检测20个空白样的标准差;为线性拟合方程的斜率)得其检出限为0.039μmol/L。
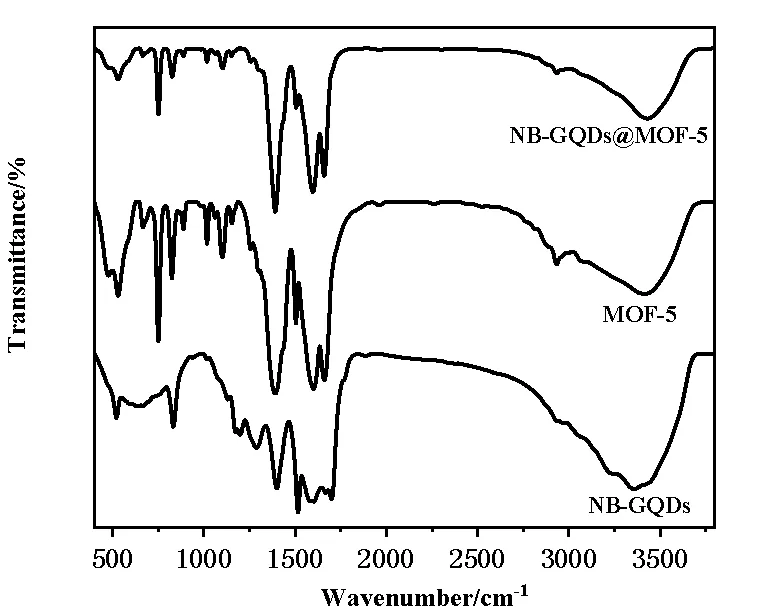
图4 NB-GQDs@MOF-5的红外光谱图
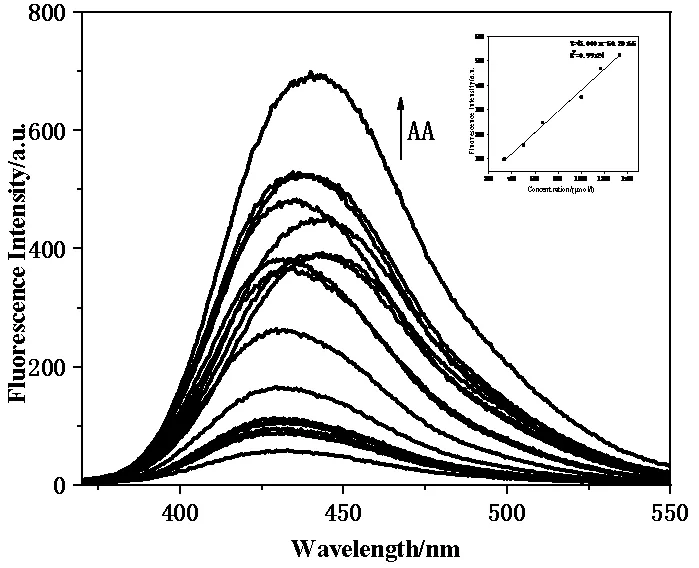
图5 不同浓度的AA(0~1666.7μmol/L)存在时 NB-GQDs@MOF-5(30 mg/L)的荧光光谱
从选择性和竞争实验(图6,黑色条表示NB-GQDs@MOF-5对不同分子及离子的荧光响应,白色条表示加入AA到含有NB-GQDs@MOF-5和这些分子及离子体系中的荧光变化)可以看出,在考察的有机小分子及阳离子范围内(丝氨酸、酪氨酸、脯氨酸、白氨酸、缬氨酸、葡萄糖、K+、Na+、Zn2+、Co2+、Ni2+、Pb2+),仅AA引起NB-GQDs@MOF-5体系的荧光显著增强,其他分子及离子的存在并未明显干扰NB-GQDs@MOF-5对AA荧光增强响应。因此,NB-GQDs@MOF-5对AA具有良好的的选择性。此外,根据文献[16-17]推测,NB-GQDs@MOF-5对AA识别机理可能是,NB-GQDs和AA存在空间效应和氢键作用,并且MOF-5的多孔结有利于AA的富集。
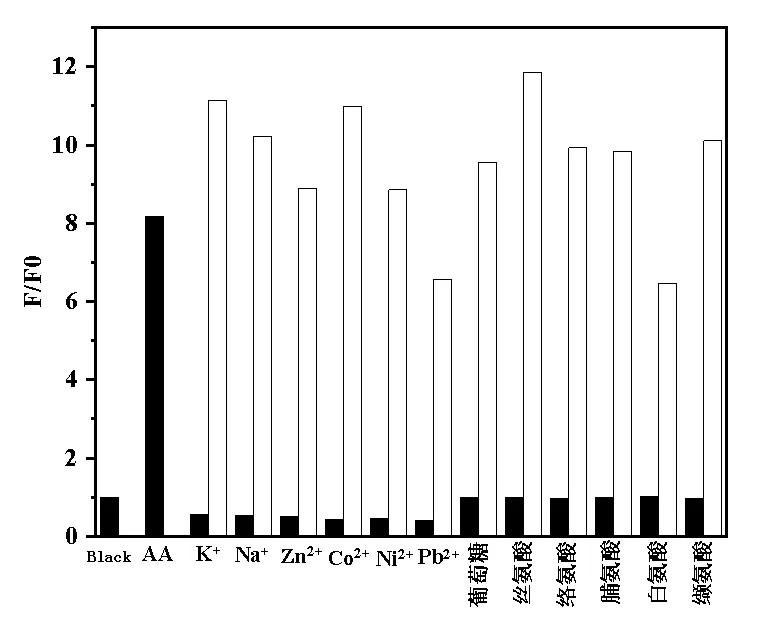
图6 NB-GQDs@MOF-5对不同分子 及离子的荧光响应及竞争实验
3 结论
将N、B共掺杂的石墨烯量子点与MOF-5复合得到新型荧光材料,利用TEM、XRD、FT-IR和XPS对其形貌结构进行了表征。在纯水体系中,NB-GQDs@MOF-5对AA荧光增强识别,检测限0.039μmol/L,且抗干扰能力较强。
[1]WABAIDUR S M, ALOTHMAN Z A, KHAN M R. A rapid method for the simultaneous determination of L-ascorbic acid and acetylsalicylic acid in aspirin C effervescent tablet by ultra performance liquid chromatography-tandem mass spectrometry[J]. Spectrochimica Acta Part A Molecular & Biomolecular Spectroscopy, 2013, 108: 20-25.
[2]SKROVANKOVA S, MLCEK J, SOCHOR J, et al. Determination of ascorbic acid by electrochemical techniques and other methods[J]. International Journal of Electrochemical Science, 2015, 10(3): 2421-2431.
[3] MA X, LIN S J, DANG Y F, et al. Carbon dots as an "on-off-on" fluorescent probe for detection of Cu(II) ion, ascorbic acid, and acid phosphatase[J]. Analytical & Bioanalytical Chemistry, 2019, 411(25): 6645-6653.
[4] MATSUOKA Y, YAMATO M, YAMADA K I. Fluorescence probe for the convenient and sensitive detection of ascorbic acid[J]. Journal of Clinical Biochemistry & Nutrition, 2016, 58(1): 16-22.
[5] YAN X, HE L, ZHOU C, et al. Fluorescent detection of ascorbic acid using glutathione stabilized Au nanoclusters[J]. Chemical Physics, 2019, 522: 211-213.
[6] KALITA H, PALAPARTHY V S, BAGHINI M S, et al. Electrochemical synthesis of graphene quantum dots from graphene oxide at room temperature and its soil moisture sensing properties[J]. Carbon, 2020, 165: 9-17.
[7] ZHANG S, LI Y, SONG H, et al. Graphene quantum dots as the electrolyte for solid state supercapacitors[J]. Journal of Materials Science: Materials in Electronics, 2016, 6: 19292.
[8] HENNA T K, PRAMOD K. Graphene quantum dots redefine nanobiomedicine [J]. Materials Science and Engineering: C, 2020,110.
[9] WU D, ZHANG P F, YANG G P, et al. Supramolecular control of MOF pore properties for the tailored guest adsorption/separation applications[J]. Coordination Chemistry Reviews, 2021, 434(2012): 213709.
[10] WANG Y, CHEN L, HOU C C, et al. Multiple catalytic sites in MOF-based hybrid catalysts for organic reactions[J]. Organic & Biomolecular Chemistry, 2020, 18(42): 8508-8525.
[11] HAO Y Q, CHEN S, ZHOU Y L, et al. Recent Progress in metal-organic framework(MOF) based luminescent chemodosimeters[J]. Nanomaterials, 2019, 9(7): 974.
[12] LIU Y, LI W, WU P, et al. Hydrothermal synthesis of nitrogen and boron co-doped carbon quantum dots for application in acetone and dopamine sensors and multicolor cellular imaging[J]. Sensors and Actuators, 2019, B281(FEB.): 34-43.
[13] D BUSO, JASIENIAK J, LAY M, et al. Highly luminescent metal-organic frameworks through quantum dot doping[J]. Small, 2012, 8(1): 80-88.
[14] WU Z P, WANG M X, ZHOU L J, et al. Framework-solvent interactional mechanism and effect of NMP/DMF on solvothermal synthesis of [Zn4O(BDC)3]8[J]. Transactions of Nonferrous Metals Society of China, 2014, 24(11): 3722-3731.
[15] HAFIZOVIC J, BJØRGEN M, OLSBYE U, et al. The inconsistency in adsorption properties and powder XRD data of MOF-5 is rationalized by framework interpenetration and the presence of organic and inorganic species in the nanocavities[J]. Journal of the American Chemical Society, 2007, 129(12): 3612-3620.
[16] NGO Y, JIN S C, HUR S H. Aminoboronic acid-functionalized graphitic carbon nitride quantum dots for the photoluminescence multi-chemical sensing probe[J]. Dyes and Pigments, 2019, 168:180-188.
[17] LI Y, YE W, CUI Y, et al. A metal-organic frameworks@ carbon nanotubes based electrochemical sensor for highly sensitive and selective determination of ascorbic acid[J]. Journal of Molecular Structure, 2020, 1209: 127986.
[18] ZHU X H, ZHAO T B, NIE Z, et al. Non-Redox modulated fluorescence strategy for sensitive and selective ascorbic acid detection with highly photo luminescent nitrogen-doped carbon nanoparticles via solid-state synthesis[J]. Analytical Chemistry, 2015, 87(16): 8524-8530.
Preparation of graphene quantum dot composites and fluorescence detection of ascorbic acid
ZHAO Bao-ru1,WANG Jian-kai1,HUANG Xin1,WANG Yue1,DU Xiao-yu1,ZHANG Yong2,MA Wen-hui1*
(1.College of Chemistry and Chemical Engineering, Qiqihar University, Heilongjiang Qiqihar 161006,China;2.College of Materials Science and Engineering, Qiqihar University, Heilongjiang Qiqihar 161006,China)
A graphene quantum dot composite NB-GQDs@MOF-5 was designed and prepared for the fluorescence recognition of ascorbic acid (AA) in pure water system. The morphology and structure of NB-GQDs were characterized by TEM, FT-IR and XRD. The results showed that the NB-GQDs was successfully combined with MOF-5. The fluorescence detection results exhibited that in pure water system, NB-GQDs@MOF-5 could specifically identify AA among the organic small molecules and cations. The addition of AA led to a 8.1-fold fluorescence enhancement with a detection limits of 0.039 μmol/L.
graphene quantum dot;MOF-5;fluorescence recognition;ascorbic acid
2021-09-28
黑龙江省自然科学基金联合引导项目(LH2020E126);齐齐哈尔大学研究生创新科研项目资助(YJSCX2019041,YJSCX2020003);黑龙江省表面活性剂与工业助剂重点实验室开放课题基金资助项目(BMHXJKF002)
赵宝茹(1997-),女,黑龙江拜泉人,在读硕士,主要从事材料化荧光探针研究,1170941686@qq.com。
O657.3
A
1007-984X(2022)02-0062-04

