Fe3O4/活性炭的制备及其对Cr(Ⅵ)的吸附研究
刘小丹,颜永斌,林 诗
(1.湖北工程学院新技术学院,湖北 孝感 432000;2.湖北工程学院 化学与材料科学学院,湖北 孝感 432000)
铬是污染水体中常见的重金属元素之一,其主要来源于铬矿、机械、金属冶金、电镀、制革、医药和化工等工业所排放的“三废”[1-2]。它是一种对人体有害的元素,在水体环境中主要是以Cr(III)和Cr(VI)两种价态存在,且会相互转化。铬离子常见的去除方法有化学沉淀法[3]、离子交换法[4]、膜分离法[5]、絮凝法[6]和吸附法。吸附法具有操作简单、原料来源广泛、设备成本较低、去除效率高、吸附容量大、吸附速率快、吸附剂再生性能好、对环境友好等优点[7]。除此之外,还可以对吸附剂进行物理改性或化学改性,通过吸附剂的物理或化学改性,可以有效提高吸附剂的孔隙率和比表面积[8],从而提高对废水中的Cr(VI)的吸附能力和吸附效率[9]。因此,通过改性制备出性能优异的吸附剂是处理废水中Cr(VI)的有效途径之一。
活性炭的吸附能力强,物理化学性质稳定,耐酸碱、耐高温,因此,被广泛应用于食品、医药、化工、金属冶金和水污染处理等各领域。活性炭比表面积大,内部孔隙结构发达,吸附能力强,吸附废水中的Cr(VI)离子效率高[10-13]。但是活性炭吸附废水中的Cr(VI)之后,会出现回收困难的问题。因此,制备磁性四氧化三铁/活性炭,用磁分离方法简单、高效、安全地分离回收磁性活性炭,可以解决一般活性炭吸附废水中的重金属离子后分离回收困难的问题。
1 实验方法
1.1 原料和试剂
活性炭、六水合氯化铁、七水合硫酸亚铁、氢氧化钠、二苯碳酰二肼、重铬酸钾、丙酮、pH计、傅立叶变换红外光谱仪、X射线衍射仪、扫描电子显微镜、可见紫外分光光度计。
1.2 磁性Fe3O4/活性炭的制备
取摩尔质量比为1∶2的FeSO4·7H2O和FeCl3·6H2O,加入一定量的去离子水搅拌溶解,恒温70 ℃。称取一定量的经过预处理的活性炭加入其中,同时滴加4 mol/L的NaOH调节溶液的pH值,持续搅拌30 min,经过滤、洗涤、烘干后,将试样研磨过100目筛,即得到磁性Fe3O4/活性炭。
1.3 改性前后活性炭的表征方法
1.3.1 扫描电镜分析
取改性前后的活性炭制样,喷金,装样,设置扫描电镜测试的工作电压为5 kv、放大倍数为1500倍,在扫描电镜上进行测试,观察改性前后活性炭的表面形态变化。
1.3.2 X射线衍射分析
取适量改性前后的活性炭制样、装样,设置X射线衍射仪的2θ角测定范围为20° ~ 80°,在X射线衍射仪上进行测试。
1.3.3 红外光谱分析
在红外灯的照射下,取适量样品与KBr混合,充分研磨后压片,再进行测试。
1.4 磁性Fe3O4/活性炭的吸附实验
向离心管中加入含50 mL Cr(VI)溶液和一定量的Fe3O4/活性炭,改变溶液的Cr(VI)初始浓度、活性炭投加量、吸附温度、吸附时间、pH值(用0.1 mol/L的HCl和0.1 mol/L的NaOH调节),置于恒温振荡器中振荡,吸附平衡后过滤取上层清液,加入显色剂和酸度剂,测其吸光度。将测得的吸光度值代入到标准曲线拟合方程中计算,可以得到溶液中Cr(VI)剩余浓度,再计算活性炭对Cr(VI)的吸附量和去除率,从而确定改性活性炭吸附的最佳实验条件。按下式计算吸附量q和去除率η[14-15]:
q=(C0-Ct)V/m
(1)
η=(C0-Ct)/C0×100%
(2)
式中:C0为溶液中Cr(VI)离子的初始浓度,mg/L;Ct为某时刻剩余Cr(VI)离子的浓度,mg/L;V为溶液体积,L;m为吸附剂的质量,g;q为吸附量,mg/g;η为去除率,%。
1.5 磁性Fe3O4/活性炭的回收和再生利用
在实际废水处理过程中,对吸附剂进行回收可以有效避免对环境的二次污染。回收后的吸附剂进行再生,可以实现吸附剂的循环利用,降低废水处理成本。因此,本文将制备的Fe3O4/活性炭进行了回收和再利用实验。
将磁性Fe3O4/活性炭加入到模拟废水中,控制pH值、吸附温度,振荡吸附后,把反应后的烧杯置于磁铁上,通过磁铁吸附吸附剂中的磁性Fe3O4来加速沉降,弃取上清后,下层固体在80 ℃下烘干后称量。按公式(3)计算磁性Fe3O4/活性炭回收率[14]:
k=m1/m0×100%
(3)
式中:k为回收率,%;m0为磁性Fe3O4/活性炭的原始投加量,g;m1为回收磁性Fe3O4/活性炭的量,g。
于回收的磁性Fe3O4/活性炭中加入一定量的0.1 mol/L的NaOH溶液,充分浸泡一段时间后进行磁力分离,分离得到的固体继续用去离子水多次冲洗,直至中性,80 ℃下烘干,即得再生磁性Fe3O4/活性炭。
利用再生磁性Fe3O4/活性炭多次进行吸附-再生实验,分别测定各次再生磁性Fe3O4/活性炭的吸附量,比较、分析再生磁性Fe3O4/活性炭的吸附性能。
2 结果与讨论
2.1 样品表征结果
2.1.1扫描电镜分析
活性炭和Fe3O4/活性炭的扫描电镜图见图1。图1上为活性炭,活性炭为5 ~ 20 μm的块状结构,表面比较平滑,有许多的小孔。图1下为Fe3O4/活性炭,改性后活性炭表面形成了许多类似小球状的颗粒物,表明Fe3O4可能负载到活性炭表面。

图1 活性炭和Fe3O4/活性炭的扫描电镜图
2.1.2 红外光谱分析
由图2可以看出,活性炭和Fe3O4/活性炭在3423 cm-1处出现的宽的吸收峰是由-OH的伸缩振动引起的;Fe3O4/活性炭在1604 cm-1处吸收峰是由C=O的伸缩振动引起,1400 cm-1处为C=O的伸缩振动吸收峰,1121 cm-1处为C-O-C的伸缩振动吸收峰[14],在579 cm-1处出现的吸收峰应为Fe-O特征吸收峰[16],活性炭的红外光谱曲线上无Fe-O特征吸收峰。上述特征峰表明活性炭样品中存在铁氧化合物。
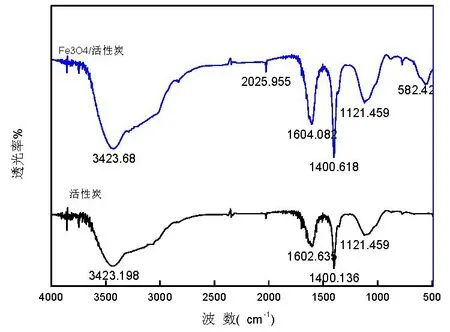
图2 活性炭的红外光谱图
2.1.3 X射线衍射分析
由图3可知,活性炭在2θ为23.80°和42.78°处出现了两个较宽较弥散峰,为非晶态的碳峰,说明此活性炭为无定形状态。磁性Fe3O4/活性炭在2θ为24.37处为无定形活性炭的特征峰,2θ为30.13°、35.51°、43.17°、53.67°、57.13°、62.72°处出现了明显的衍射峰,峰型尖锐,对称性较好,6个衍射峰分别为磁性Fe3O4(PDF卡片为19-0629)的(220)、(311)、(400)、(422)、(511)、(440)晶面[14],2θ为35.51°和62.72°处的峰较大且尖锐。通过上述XRD分析得出,本实验已成功将磁性Fe3O4负载到活性炭上,通过峰各衍射峰的峰形可知制备的Fe3O4纯度较高、结晶度较好。
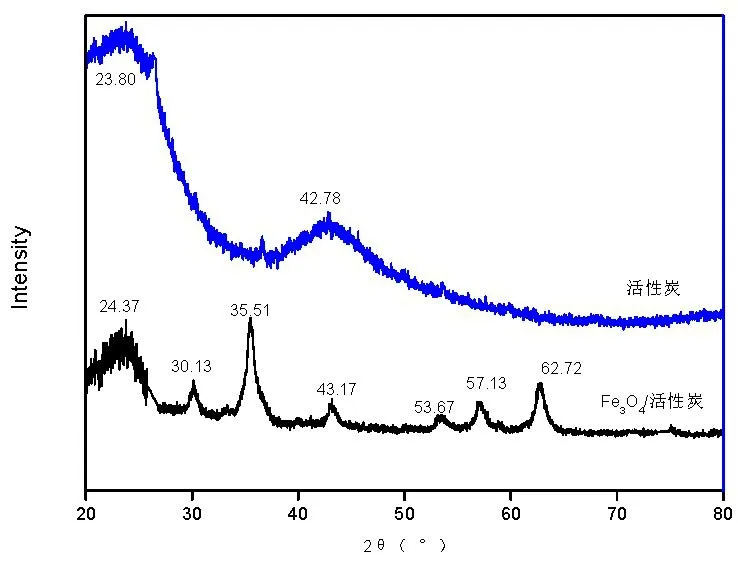
图3 活性炭的XRD图
2.2 吸附实验结果分析
在一定的条件下,配制一定浓度的Cr(VI)溶液标准溶液,加入0.5 mL硫酸和磷酸溶液后,再加入2 mL二苯碳酰二肼显色剂,摇匀。在最大吸收波长543 nm处,测定溶液的吸光度,绘制Cr(VI)溶液的标准曲线,拟合方程为y=0.1235x+0.0328。后续实验可根据拟合方程,由实验测量的吸光度可以计算出Cr(VI)的质量浓度,利用公式(1)、(2)计算Cr(VI)的吸附量和去除率。
2.2.1 Cr(VI)初始浓度对Cr(VI)吸附效果的影响
由图4可知随着模拟废水中Cr(VI)离子初始浓度的增大,磁性Fe3O4/活性炭对Cr(VI)的吸附的吸附量呈逐渐上升的趋势,而去除率则呈逐渐降低的趋势。当磁性Fe3O4/活性炭质量确定时,磁性Fe3O4/活性炭的总面积和吸附能力一定。当Cr(VI)离子初始浓度较低时,磁性Fe3O4/活性炭的吸附没有达到饱和,Cr(VI)离子能充分的占据其表面的吸附位点,此时Cr(VI)离子的量相对磁性Fe3O4/活性炭时不足的。因此Cr(VI)离子初始浓度较低时,磁性Fe3O4/活性炭对Cr(VI)离子去除率较高,但是单位质量Fe3O4/活性炭的吸附量却较低。随着Cr(VI)离子初始浓度的增加,Fe3O4/活性炭单位表面上吸附的Cr(VI)增加,吸附量增大,吸附逐渐趋于平衡,制约了吸附的进行,导致去除率逐渐降低[7,17]。综合考虑去除率和吸附量,确定最佳初始浓度为15 mg/L。
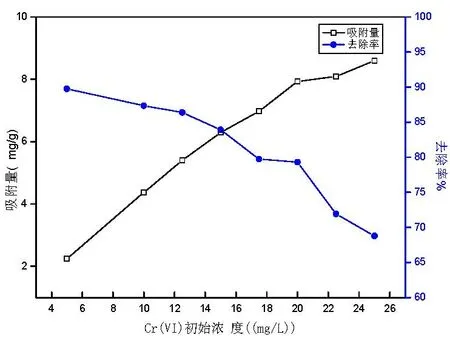
图4 Cr(VI)初始浓度对吸附效果的影响
2.2.2 溶液pH对Cr(VI)吸附效果的影响
由图5可知,溶液pH由1变化至8过程中,磁性Fe3O4/活性炭对Cr(VI)的吸附量和去除率现增加后降低。pH为3~5时吸附效果较好,pH等于3时,吸附量和去除率最高,故在吸附实验中控制溶液的pH为3。

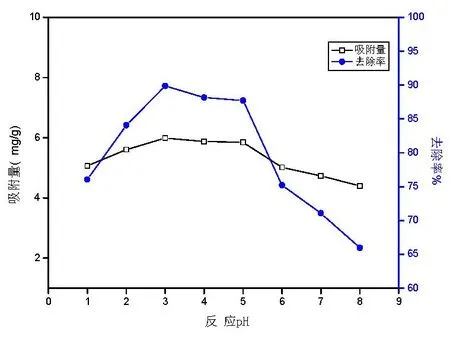
图5 pH值对吸附效果的影响
2.2.3 Fe3O4/活性炭投加量对Cr(VI)吸附效果的影响
由图6可知,随着Fe3O4/活性炭投加量的增加,吸附量呈减小趋势,而去除率呈增大趋势。当投加量从0.05 g增大至0.225 g时,吸附量从13.35 mg/g减小至4.22 mg/g,而去除率从66.75%增大至94.97%。
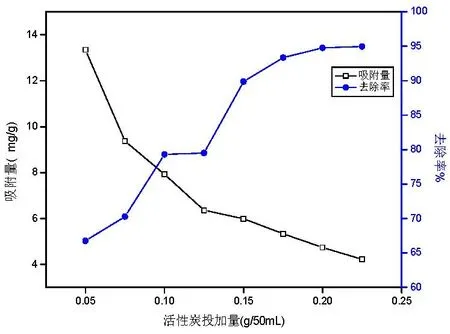
图6 Fe3O4/活性炭投加量对吸附效果的影响
形成上述结果的原因可能是,随着Fe3O4/活性炭的投加量增加,其总表面积也相应的增加,提供更多的吸附位点,溶液中Cr(VI)的浓度一定时,吸附平衡后,溶液中Cr(VI)的剩余浓度也会不断的下降,去除率逐渐升高至趋于稳定。由于Cr(VI)的浓度一定,Cr(VI)离子的数量是有限的,随着活性炭量的增加,单位活性炭的吸附量就会减少[7]。为保证去除率,可适当增加活性炭的投加量,综合考虑吸附量和去除率,最终确定Fe3O4/活性炭投加量为0.004 g/mL。
2.2.4 吸附时间对Cr(VI)吸附效果的影响
由图7可以看出,当时间小于3 h时,去除率和吸附量都是随着时间的延长,而呈较快的增长趋势。当时间超过3 h后,去除率和吸附量都随着时间的延长趋于稳定,在4 h后已基本达到吸附平衡,故在吸附实验中选定吸附时间为4 h。
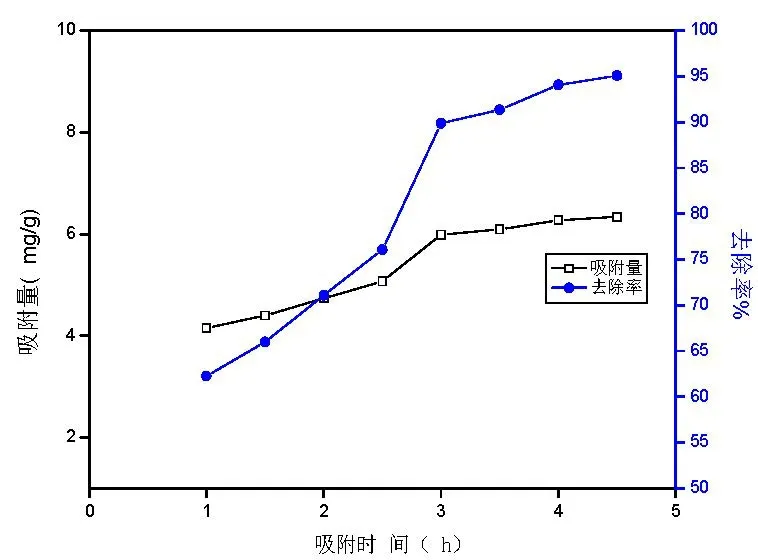
图7 吸附时间对吸附效果的影响
2.2.5 吸附温度对Cr(VI)吸附效果的影响
由图8可以看出,磁性Fe3O4/活性炭对Cr(VI)的吸附量和去除率随着实验温度的升高而逐渐增加,说明该吸附过程是吸热的,升高吸附实验的温度对Cr(VI)的吸附是有利的。当温度超过35 ℃后,吸附量的增长速度变缓,去除率基本保持不变。当温度超过50 ℃以后,去除率和吸附量变化不大,且去除率达到90%以上,故吸附实验温度选定为50 ℃。
综合考虑以上实验结果,确定吸附实验条件为:Cr(VI)初始浓度为15 mg/L、溶液pH值为3、活性炭投加量为0.004 g/mL、吸附时间为4 h,吸附温度为50 ℃,在此条件下进行吸附实验,磁性Fe3O4/活性炭对Cr(VI)的吸附去除率达到95%,吸附量为6.3 mg/g。
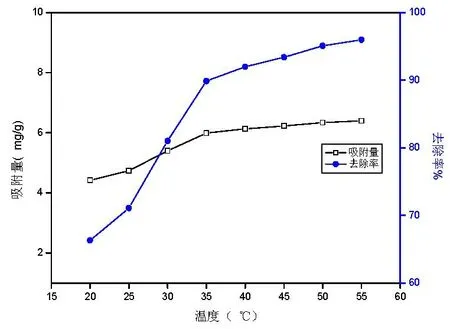
图8 吸附温度对吸附效果的影响
2.3 磁性Fe3O4/活性炭的磁力回收
初始的磁性Fe3O4/活性炭的质量为0.15 g,吸附后回收,用电子天平称量回收的磁性Fe3O4/活性炭的质量为0.1405 g。利用公式(3)计算得出回收率为93.67%,回收率高于90%。说明通过本实验中的回收方法,可以实现磁性Fe3O4/活性炭的高效率回收,且回收方法简单,可操作性强,与文献[14]结论一致。
得到的再生磁性Fe3O4/活性炭进行吸附实验,吸附-解吸实验共进行5次。由图9可以看出,再生的Fe3O4/活性炭循环使用5次过程中,吸附量逐渐减少,至第5次吸附量由5.99 mg/g减少至1.96 mg/g,第5次吸附量为初始吸附量的67%。说明回收再生的磁性Fe3O4/活性炭仍具有较好的吸附能力,磁性Fe3O4/活性炭回收和重复利用能力较强。
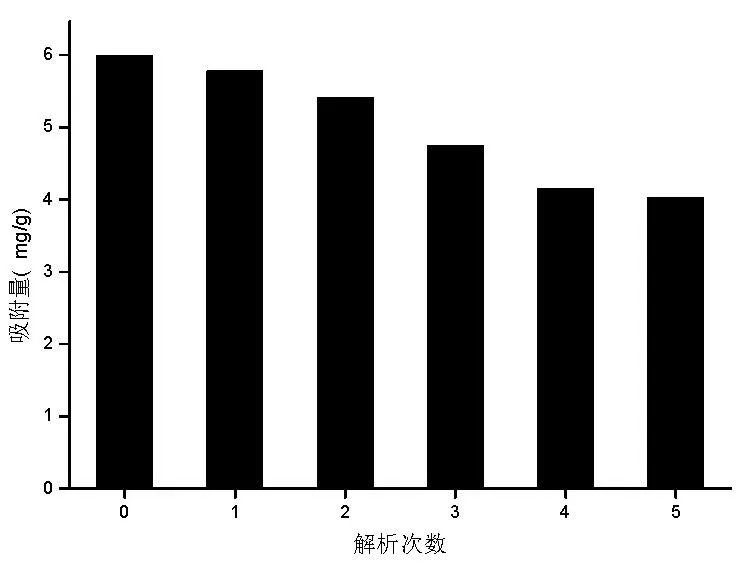
图9 改性活性炭的吸附量与解吸次数的关系
3 小结
本文运用化学共沉淀法制备磁性Fe3O4/活性炭,并对其进行了表征分析,结果显示,运用化学共沉淀法成功地制备出磁性Fe3O4/活性炭。对磁性Fe3O4/活性炭吸附Cr(VI)离子的吸附条件进行了考察,结果表明,Cr(VI)初始浓度为15 mg/L、溶液pH值为3、活性炭投加量为0.2 g/50 mL、吸附时间为4 h,吸附温度为50 ℃是磁性活性炭吸附模拟废水中Cr(VI)的最佳吸附条件,在此条件下,磁性Fe3O4/活性炭对Cr(VI)的吸附去除率达到95%。Fe3O4/活性炭进行简单的磁力分离回收,回收率超过90%,再生的Fe3O4/活性炭循环使用5次后吸附量仍较高,说明制备的磁性Fe3O4/活性炭具有很好的吸附Cr(VI)离子的能力,并且回收方法简单,回收率高,具有较好的应用前景。

