胶乳免疫比浊法在奥氮平和喹硫平药物浓度监测中的应用
金伟峰, 翁 颖, 李 萍, 陈姝子, 陈 庆, 孙佳琪, 李振华, 方 伟, 林 萍
[1.上海交通大学医学院附属精神卫生中心检验科,上海 200030;2. 复星诊断科技(上海)有限公司,上海 200444]
奥氮平和喹硫平都是第2代非典型抗精神病药物,具有疗效好、不良反应小、不会引起明显的锥体外系副反应等优点[1],近年来已广泛应用于临床。有研究结果显示,奥氮平血药个体差异较大,患者服用奥氮平治疗后药物剂量和血药浓度呈正相关,临床疗效和毒副反应与每日剂量、血药浓度等均有关[2]。段迪等[3]的研究结果显示,喹硫平血药浓度能在一定程度上反映临床疗效,且血药浓度的高低与治疗有效率和无效率明显相关。但奥氮平和喹硫平的有效治疗浓度范围(治疗窗)非常窄,不同个体之间存在非常大的疗效差异。欧洲神经精神药理学与药物精神病学协会发布的精神科治疗药物监测共识指南[4]指出,使用奥氮平、喹硫平等精神类药物治疗精神疾病时应进行药物浓度监测,并提供清晰的治疗参考区间和监测流程。目前,用于奥氮平和喹硫平药物浓度监测的常用方法有高效液相色谱、液相色谱串联质谱(liquid chromatography tandem mass spectrometry,LC-MS/MS)等。但这些方法对操作人员要求均较高,且需要昂贵的特殊仪器,难以在中小型医疗机构普及。胶乳免疫比浊法具有准确、快速、简便的优点,可实现样本的快速检测。本研究拟探讨胶乳免疫比浊法在奥氮平和喹硫平药物浓度监测中的临床应用价值。
1 材料和方法
1.1 研究对象
选取2021年7月上海交通大学医学院附属精神卫生中心住院的服用奥氮平的患者50例,其中男31例、女19例,年龄(40.98±18.92)岁;服用喹硫平的患者50例,其中男22例、女28例,年龄(44.58±21.36)岁。收集所有对象检测剩余血清样本,所有样本均无脂血、溶血。
1.2 仪器与试剂
Waters I-Class/Xevo TQD液相质谱联用仪(美国Waters公司),奥氮平、喹硫平标准品购自美国Sigma公司,流动相A为0.1%甲酸-2 mmol/L甲酸铵-水溶液、流动相B为100%甲醇,试剂均购自上海安谱科技股份有限公司,质控品购自上海市临床检验中心。奥氮平、喹硫平胶乳免疫比浊法试剂购自复星诊断科技(上海)有限公司,校准品、质控品均购自美国Saladax Biomedical公司,检测仪器为AU680全自动生化分析仪(美国贝克曼库尔特公司)。
1.3 方法
1.3.1 正确度 参照美国临床实验室标准化协会(the Clinical and Laboratory Standards Institute,CLSI)EP15-A3文件[5],以校准品(奥氮平高、低值分别为78.5、46.0 ng/mL,喹硫平高、低值分别为438、88 ng/mL)为样本,采用胶乳免疫比浊法每天重复测定2次,连续测定5 d。由于精神类药物检测无允许总误差(allowable total error,TEa)的标准,故选用《上海市医疗机构临床实验室质量管理规范》[6]中其他治疗药物的TEa(±25%)为标准,以检测结果与校准品标示值的相对偏移≤1/2TEa(±12.5%)为临床可接受。
1.3.2 精密度 参照CLSI EP15-A3文件[5],收集临床低值样本(奥氮平为39 ng/mL,喹硫平为155.65 ng/mL)和高值样本(奥氮平为84.9 ng/mL,喹硫平为520.65 ng/mL)各2份,分别测定20次,计算、s和变异系数(coefficient of variation,CV)。如CV低于厂商声明,则验证通过;如s低于厂商声明的验证值,则中间精密度验证通过。
1.3.3 线性范围 参照我国卫生行业标准WS/T 408—2012[7],收集临床高值样本(奥氮平为134.9 ng/mL,喹硫平为748 ng/mL)和低值样本(奥氮平为19.7 ng/mL,喹硫平为34 ng/mL),将高值样本(H)和低值样本(L)分别按5L、4L+1H、3L+2H、2L+3H、1L+4H、5H配制成系列浓度样本,将样本从低到高或从高到低重复测定3次,计算。将实测值(Y)与理论值(X)进行回归分析,得到回归方程Y=bX+a和r值。如厂商声明的线性范围(奥氮平为22~114 ng/mL,喹硫平为34~700 ng/mL)在实测线性范围内,则验证通过。
1.3.4 分析系统间不定期比对 参照CNASCL02-A003:2018文件[8],选取服用奥氮平和喹硫平的患者样本各50例,分为2份,一份用于LCMS/MS检测,另一份用于胶乳免疫比浊法检测。2种方法之间应有≥80%的样本的偏差<1/2 TEa。
1.3.5 分析系统间定期比对 参照CNASCL02-A003:2018文件[8],选取服用奥氮平和喹硫平的患者样本各50例,分为2份,一份用于LC-MS/MS检测,另一份用于胶乳免疫比浊法检测,根据检测结果建立回归方程,采用Passing-Baklok模型进行拟合计算,在医学决定水平处的系统误差(相对偏移)[9]应<1/2 TEa。
1.4 统计学方法
采用SPSS 23.0软件进行统计分析。采用Kolmogorov-Smirnov检验评估数据的正态性。呈非正态分布的计量资料以中位数(M)[四分位数(P25~P75)]表示,组间比较采用Wilcoxon秩和检验。采用MedCalc19.4.1软件进行偏差图分析,选择合适的回归方程进行线性拟合。
2 结果
2.1 正确度
胶乳免疫比浊法检测奥氮平高、低值校准品的结果与标示值的相对偏移分别为-6.80%、-6.98%,喹硫平高、低值校准品的相对偏移分别为6.99%、4.66%,均<1/2 TEa(±12.5%)。
2.2 精密度
2.2.1 重复性 胶乳免疫比浊法检测奥氮平低值和高值样本的CV分别为3.00%和1.26%;检测喹硫平低值和高值样本的CV分别为2.05%和0.83%,均低于厂商声明的重复性(CV<7.5%)。
2.2.2 中间精密度 胶乳免疫比浊法检测奥氮平低值和高值样本的实验室内s分别为1.680、1.786 ng/mL,检测喹硫平低值和高值样本的实验室内s分别为2.068、1.832 ng/mL,均低于厂商声明的验证值(奥氮平为4.194、9.331 ng/mL,喹硫平为16.173、52.858 ng/mL)。
2.3 线性范围
奥氮平的线性回归方程为Y=1.012 4X-1.411 9(r=0.999 4),线性范围实测值为19.7~134.9 ng/mL,理论值与实测值之间差异无统计学意义(P>0.05)。喹硫平的线性回归方程为Y=1.000 6X+5.033 6(r=0.998 0),线性范围实测值为34~748 ng/mL,理论值与实测值之间差异无统计学意义(P>0.05)。见表1。

表1 奥氮平和喹硫平线性范围验证结果及相对偏移
2.4 分析系统间不定期和定期比对结果
LC-MS/MS与胶乳免疫比浊法奥氮平和喹硫平的检测结果差异均无统计学意义(P>0.05),相对偏差<1/2 TEa的样本所占比例分别为98.00%、92.00%。不定期比对符合要求。见表2、表3。
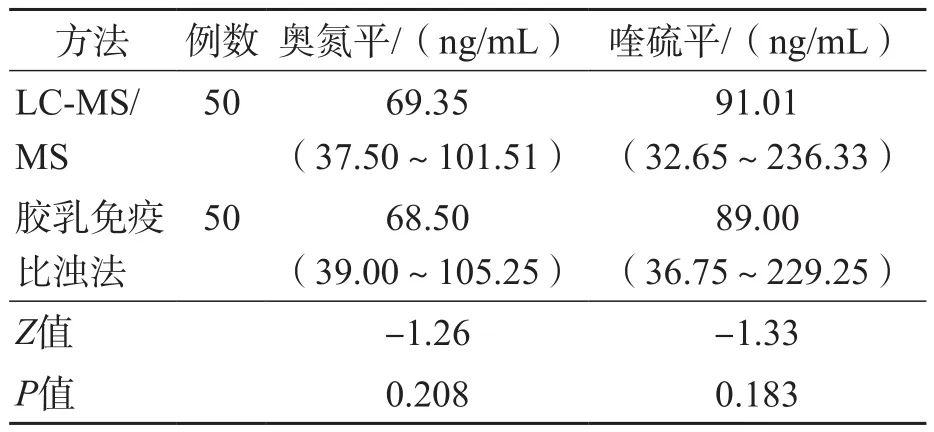
表2 LC-MS/MS与胶乳免疫比浊法奥氮平和喹硫平检测结果比较

表3 分析系统间不定期比对的相对偏差及合格率
奥氮平拟合的回归方程为Y=2.586+0.934X,在3个医学决定水平(20、80、150 ng/mL)处的相对偏移分别为6.98%、-2.50%、-4.06%。喹硫平拟合的回归方程为Y=-0.180+0.979X,在3个医学决定水平(100、500、1 000 ng/mL)处的相对偏移分别为-2.31%、-2.16%、-2.14%。见表4。
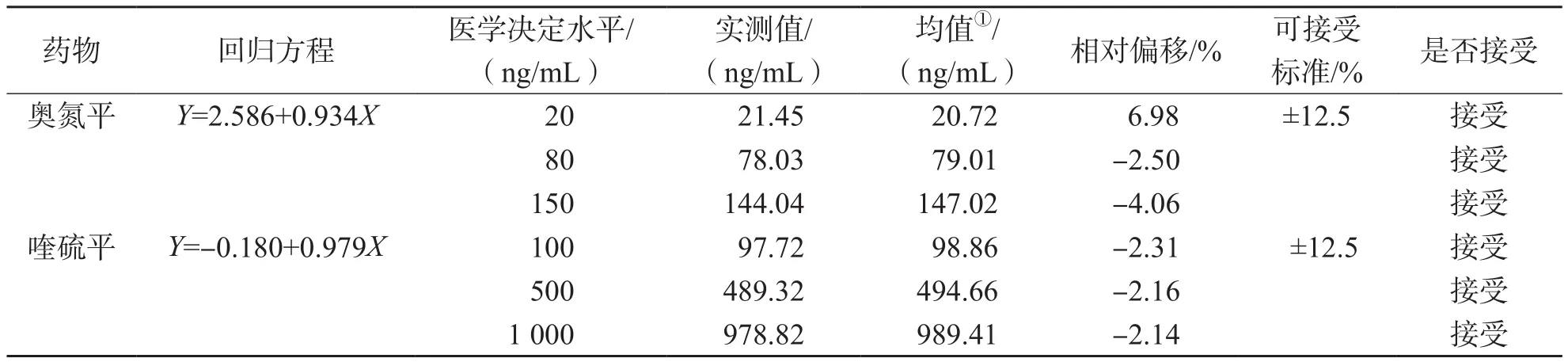
表4 分析系统间定期比对偏移
3 讨论
抗精神病药物的维持治疗可使患者明显获益,显著改善临床症状,降低患者死亡率[10-11]。在药物浓度监测的指导下制定个体化的用药方案,提升患者对治疗的依从性,维持有效治疗窗,对于精神疾病的治疗至关重要,可使治疗效果最大化,毒副作用最小化。由于抗精神病药物的治疗窗很窄,治疗剂量与中毒剂量很接近,因此需要对药物进行浓度监测,以避免出现中毒反应。目前,药物浓度监测常用的方法为LC-MS/MS,但其需要特殊仪器,对场地、检测人员的要求均较高,因此中小型医疗机构无法常规开展。胶乳免疫比浊法相对于LC-MS/MS,样本无需前处理、检测速度快、通量高;缺点是会与结构相似的非待测物结合,发生假阳性反应,导致检测结果升高[12],也会因体内高浓度免疫球蛋白的抑制作用而导致检测结果降低,出现假阴性,同时,由于方法的局限性,其定量限较质谱方法窄[13-14]。贾萌萌等[15]采用胶乳免疫比浊法检测了92例患者血浆多西他赛浓度,并与质谱法比较,结果显示,2种方法的相关性较好(r=0.998,P<0.05),检测结果差异无统计学意义(P>0.05)。ETO等[16]采用胶乳免疫比浊法和质谱法同时检测78例患者的唑尼沙胺血药浓度,并通过Bland-Altman一致性分析评估2种方法的一致性,结果显示,2种方法之间差异无统计学意义(P>0.05)。
本研究结果显示,胶乳免疫比浊法检测奥氮平和喹硫平的血药浓度具有良好的正确度(奥氮平相对偏移分别为-6.80%、-6.98%、喹硫平相对偏移分别为6.99%、4.66%)、精密度(奥氮平CV≤3%、喹硫平CV≤2.05%)及线性(奥氮平为19.7~134.9 ng/mL,喹硫平为34~748 ng/mL),其线性范围可以覆盖欧洲神经精神药理学与药物精神病学协会推荐的治疗参考区间;LC-MS/MS与胶乳免疫比浊法奥氮平和喹硫平的检测结果差异均无统计学意义(P>0.05),分析系统间定期比对和不定期比对均符合要求。
综上所述,胶乳免疫比浊法与LC-MS/MS具有良好的一致性,且更为便捷、快速,可在中小型医疗机构推广使用。

