瑞舒伐他汀和替格瑞洛在大鼠体内的药动学相互作用
田雨
(锦州医科大学附属第三医院,辽宁 锦州 121000)
瑞舒伐他汀是一种高选择性3-羟基-3-甲基戊二酰辅酶A还原酶抑制剂,通过减少肝脏胆固醇的合成,从而降低血脂水平[1]。此外,其还具有稳定斑块、抗氧化和降低炎症介质等多种作用。替格瑞洛是一种新型的抗血小板药物,能够可逆地与血小板二磷酸腺苷受体发生相互作用,影响信号传导和血小板活化,其疗效确切,出血风险小,是抗血小板治疗的一线用药[2]。两药在心脑血管疾病的治疗中均占有重要地位,并且在临床上常常联合应用。
由于替格瑞洛主要经细胞色素P450 3A4酶(cytochrome P450 3A4,CYP3A4)代谢,而瑞舒伐他汀是细胞色素P450的弱底物,仅发生有限代谢,CYP3A4参与代谢程度低,因而普遍认为二者发生药物相互作用的风险小。但近几年来,国内外报道了多例瑞舒伐他汀联用替格瑞洛后诱发横纹肌溶解症的案例[3-5],引发了二者之间是否存在某种相互作用的思考。以往的研究多集中在替格瑞洛和主要经CYP3A4代谢的他汀类药物,如辛伐他汀和阿托伐他汀等,而对瑞舒伐他汀和替格瑞洛的药动学研究较少。为此,本文建立了LC-MS/MS法同时测定大鼠血浆中瑞舒伐他汀和替格瑞洛的浓度,并研究二者之间的药动学相互作用,以期为临床合理应用提供参考。
1 仪器与材料
1.1 仪器
LC-30AD 超高速液相色谱系统(岛津公司),Qtrap 5500型三重四极杆串联质谱仪(AB Sciex公司),MS105分析天平(Mettler公司),H-101型漩涡混合器(上海康禾光电仪器公司),5810R型低温冷冻离心机(Eppendorf 公司),Tube-Heater L-119A氮吹仪(北京来亨公司),Millipore 超纯水仪(Milipore公司)。
1.2 试剂
瑞舒伐他汀钙(含量:97.6%,批号:101028-201202,中国食品药品检定研究院),替格瑞洛(含量:99.7%,批号:1489-090A1,深圳博泰尔生物技术有限公司),卡马西平(含量:99.7%,批号:100142-201105,中国食品药品检定研究院),甲醇、乙腈、甲酸(色谱纯,Merck公司),甲基叔丁基醚(分析纯,天津市凯信化学工业有限公司),超纯水,肝素钠注射液(国药集团容生制药有限公司)。
1.3 实验动物
健康SD大鼠(SPF级,雄性,体重200~220 g),购自辽宁长生生物技术股份有限公司(SCXK(辽)2015-0001)。购入后于实验室(温度20 ℃~25 ℃,湿度50%~70%)适应性饲养1 w,自由摄食饮水。
2 方法与结果
2.1 色谱条件
色谱柱为Waters XTerra MS C18(150 mm×2.1 mm,5μm),预柱为SecurityGuard Cartridges C18(4.0 mm×3.0 mm,Phenomenex),流动相为甲醇-乙腈-水(含0.1%甲酸)(80∶10∶10),等度洗脱,流速为0.2 mL/min,柱温为35 ℃,进样量为20 μL。
2.2 质谱条件
离子源为ESI源;正离子方式检测;多反应离子监测(MRM)模式;离子源喷射电压为4500 eV;离子源温度为450 ℃;离子源气体1∶40 psi;离子源气体2∶20 psi;气帘气25 psi;碰撞气压力为medium;瑞舒伐他汀、替格瑞洛和内标卡马西平碰撞能量(CE)及用于定量分析的离子对(m/z)分别为42 eV和482.2→258.2、44 eV和523.3→127.1、27 eV和237.2→201.4。
2.3 工作溶液和质控(QC)溶液的配制
分别称取适量瑞舒伐他汀钙和替格瑞洛对照品,精密称定,置于容量瓶中,用甲醇定容,获得质量浓度均为100 g/mL的储备液。取各储备液适量,用甲醇稀释,配成瑞舒伐他汀浓度分别为5、10、25、100、250、500、1000 ng/mL的标准溶液和10、100、800 ng/mL的QC溶液,替格瑞洛浓度分别为20、40、100、400、1000、2000、4000 ng/mL的标准溶液和40、400、3200 ng/mL的QC溶液。
称取适量卡马西平对照品,精密称定,置于容量瓶中,用甲醇定容,获得质量浓度为100 g/mL的内标储备液。取储备液适量,用甲醇稀释,配制浓度为100 ng/mL的内标溶液。
2.4 标准血浆样品及QC样品的制备
取瑞舒伐他汀和替格瑞洛的标准溶液各20 μL,加入空白血浆160 μL,配制含瑞舒伐他汀/替格瑞洛血浆浓度分别为0.5/2、1/4、2.5/10、10/40、25/100、50/200、100/400 ng/mL的标准血浆样品;取QC工作液,配制含瑞舒伐他汀/替格瑞洛血浆浓度分别为1/4、10/40、80/320 ng/mL的QC样品,冷冻保存备用。
2.5 血浆样品处理
取待测血浆样品100 μL,加入内标工作液10 μL,涡旋震荡30 s,加入甲基叔丁基醚3 mL,涡旋震荡3 min,4 ℃下离心10 min(1.3×104r/ min)。分取有机相,氮气吹干(40 ℃),甲醇复溶,4 ℃下离心10 min(8.5×103r/min),取上清液进样分析。
2.6 动物实验给药方案
18只健康雄性SD大鼠,随机分成3组(n=6),单剂量给药,给药方式如下:第一组单独灌胃给予替格瑞洛8.5 mg/kg;第二组单独灌胃给予瑞舒伐他汀钙1 mg/kg;第三组同时灌胃给予替格瑞洛8.5 mg/kg +瑞舒伐他汀钙1 mg/kg。
2.7 生物样品采集
采血前12 h,给予大鼠禁食不禁水处理。分别于给药前(0 h)和给药后 0.25、0.5、1、1.5、2、3、4、6、8、12、24和36 h经大鼠眼眶后静脉丛采血约0.3 mL,置于含肝素的离心管内,离心10 min(5×103r/min),分离上层血浆,于 -70 ℃保存待测。
2.8 分析方法确证
2.8.1 专属性
取大鼠空白血浆,按“2.5”项下操作(用等体积甲醇替代内标),获得空白血浆色谱图。取空白血浆加入对照品溶液(0.5 ng/mL瑞舒伐他汀和2 ng/mL替格瑞洛)和给药后1 h血浆样品,按“2.5”项下操作,获得相应的色谱图。瑞舒伐他汀、替格瑞洛和卡马西平的保留时间分别为2.1 min、2.8 min和2.3 min。结果显示,在分析物和内标相应保留时间的地方,无干扰峰出现,专属性良好,见图1。

A:空白血浆;B:空白血浆加瑞舒伐他汀/替格瑞洛(0.5 ng/mL/2 ng/mL)和内标;C:灌胃给药后1 h血浆样品;Ⅰ:瑞舒伐他汀;Ⅱ:替格瑞洛;Ⅲ:卡马西平图1 瑞舒伐他汀、替格瑞洛和卡马西平的典型色谱图
2.8.2 标准曲线及定量下限
取标准血浆样品,按“2.5”项下操作,将待测物与内标的峰面积之比同待测物浓度,通过加权最小二乘法[6]进行回归运算。经计算,替格瑞洛的线性回归方程为y=6.94×10-3x+1.61×10-2(r=0.9995),瑞舒伐他汀的线性回归方程为y=3.04×10-3x+2.08×10-2(r=0.9996)。根据标准曲线可知,瑞舒伐他汀和替格瑞洛线性范围分别为2~400 ng/mL和0.5~100 ng/mL。
2.8.3 精密度与准确度
取3个浓度的QC样品各6份,按“2.5”项下操作,连续测定3 d。根据当天标准曲线计算QC样品的浓度,考察方法的精密度和准确度。结果显示,瑞舒伐他汀和替格瑞洛每一QC浓度水平的日内、日间精密度均小于15%,准确度在96%~109%之间,满足中国药典(2020 版)9012 指导原则的要求,见表1。
2.8.4 提取回收率
取3个浓度的QC样品各6份,按“2.5”项下操作,获得相应峰面积。另取空白血浆,按“2.5”项下操作(用等体积甲醇替代内标),取全部上清液,加入相应浓度的QC溶液和内标溶液,涡旋混合后,取上清液进行LC-MS/MS分析,记录峰面积。用两种处理方法的峰面积比计算提取回收率。结果显示,本方法条件下,瑞舒伐他汀和替格瑞洛QC样品的平均提取回收率均在96.1%以上,RSD均小于15%,见表1。
2.8.5 稳定性
取低、高浓度的QC样品各3份,按“2.5”项下操作,分别在处理前室温放置2 h和处理后室温放置4 h,-70 ℃冷冻-解冻循环3次和-70 ℃放置30 d的条件下测定。结果显示,瑞舒伐他汀和替格瑞洛血浆样品浓度的RSD均小于15%,RE均在±15%之间,表明在上述条件下稳定性良好,见表2。
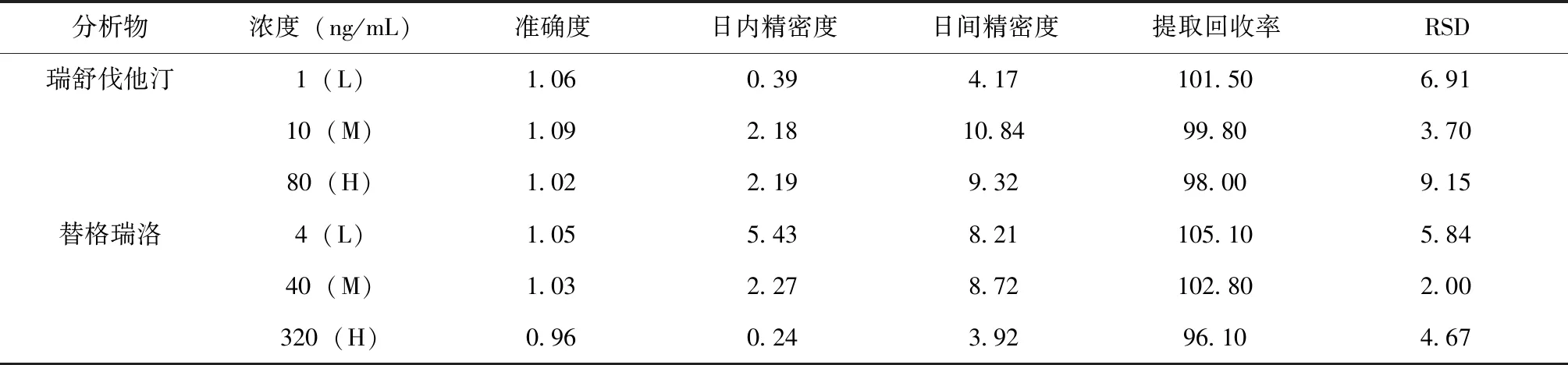
表1 血浆样品中瑞舒伐他汀和替格瑞洛的准确度、精密度和提取回收率(n=6,%)

表2 血浆样品中瑞舒伐他汀和替格瑞洛的稳定性(n=3,%)
2.8.6 基质效应
取不同来源的空白血浆6份,按“2.5”项下操作(用等体积甲醇替代内标),取全部上清液,加入相应浓度的QC溶液和内标溶液,涡旋混合后,取上清液进行LC-MS/MS分析,记录峰面积。用超纯水代替空白血浆,依同法操作,获得相应的峰面积。用峰面积比值计算基质效应。经计算,低、高浓度瑞舒伐他汀QC样品经内标校正的基质效应因子变异系数分别为3.3%和4.5%,替格瑞洛分别为4.2%和4.3%。表明可忽略基质效应的影响。
2.9 统计学方法
采用 WinNonlin 8.1软件计算主要药动学参数,并通过SPSS 24.0软件进行统计学分析,数据均以均数±标准差表示。以秩和检验法对Tmax进行非参数检验,对其他药动学参数进行独立样本t检验,以P<0.05表示差异有统计学意义。
结果显示,联合用药后,瑞舒伐他汀Cmax增加0.55倍(P<0.05),AUC0-∞和AUC0-t增加1.48倍(P<0.05),Cl降低1.8倍(P<0.05),MRT0-t和MRT0-∞延长约1h(P<0.05);替格瑞洛Tmax缩短约1 h(P<0.05),MRT0-t缩短约2.5 h(P<0.05),Cmax、AUC0-∞和AUC0-t均下降,但无统计学意义。瑞舒伐他汀和替格瑞洛的药时曲线见图2、表3。

图2 大鼠血浆中瑞舒伐他汀(I)和替格瑞洛(II)的平均血药质量浓度-时间曲线

表3 大鼠血浆中瑞舒伐他汀和替格瑞洛的主要药动学参数
3 讨 论
3.1 大鼠血浆中瑞舒伐他汀和替格瑞洛含量测定的方法学研究
目前关于同时测定体内瑞舒伐他汀和替格瑞洛血药浓度的方法未见报道,本研究建立了LC-MS/MS法同时测定大鼠血浆中二者的质量浓度,并进行方法学验证,用于两者的大鼠体内药代动力学研究。
流动相分别考察了甲醇-水,乙腈-水、甲醇-乙腈-水溶液。当流动相采用甲醇-乙腈-水时,待测物分离相对较好。而在水溶液中加入甲酸后,色谱峰型改善,保留时间缩短,仪器响应较高,最终选择甲醇-乙腈-水(含0.1%甲酸)作为流动相。
在选择样品处理方法时,考察了蛋白沉淀法和液-液萃取法。蛋白沉淀法考察了甲醇和乙腈溶液作为蛋白沉淀剂,但提取后干扰物质影响较大,待测物和内标峰形较差。考察液-液萃取法时,查阅相关文献[7],分别选择了乙酸乙酯、甲基叔丁基醚和正己烷作为萃取溶剂,结果发现正己烷提取回收率低,乙酸乙酯干扰物质的影响较大,重现性差。甲基叔丁基醚提取回收率在85%以上,响应高,重现性良好。
3.2 大鼠体内瑞舒伐他汀和替格瑞洛的药动学相互作用
本研究分别考察了单独用药和联合用药后,大鼠体内瑞舒伐他汀和替格瑞洛的药代动力学特征。结果表明两者单次口服给药后存在一定的药动学相互作用。替格瑞洛在体内主要经CYP3A4代谢,瑞舒伐他汀仅少部分经肝药酶代谢,且主要经CYP2CP代谢,少量经CYP3A4代谢,大量研究结果也证实[8-9],酶竞争作用几乎不影响两者的药动学特征。查阅文献,发现瑞舒伐他汀是有机阴离子转运体多肽OATP1B1的高亲和力底物,与之结合转运至肝脏[10]。当瑞舒伐他汀与OATP1B1抑制剂,如吉非贝奇[11]或依折麦布[12]联用后,达峰浓度和药时曲线下面积均明显升高。而Christoph等[13]研究结果表明替格瑞洛瑞对OATP1B1有明显的抑制作用。此外,P-糖蛋白(P-glycoprotein,P-gp)可能也有参与。瑞舒伐他汀是P-gp的底物,Verhulst等[14]研究发现当P-gp抑制剂长春碱和瑞舒伐他汀联用后,瑞舒伐他汀的血药浓度增加了1.6倍,而替格瑞洛是P-gp的弱效抑制剂。因此,替格瑞洛可能通过抑制OATP1B1和P-gp,降低瑞舒伐他汀的肝脏摄取和外排作用,使其Cmax、AUC0-∞和AUC0-t明显增加,MRT0-t和MRT0-∞显著延长,导致体内暴露量增加,提高了不良反应的发生风险。联合用药后,替格瑞洛的Tmax和MRT0-t显著缩短,Cmax、AUC0-∞、AUC0-t均有所降低,可能是瑞舒伐他汀加快了替格瑞洛的吸收速度和代谢速度,是否存在酶诱导作用,还有待进一步研究。
本研究尚有不足之处。因瑞舒伐他汀和替格瑞洛的代谢和分布均受基因变异影响,个体差异性较大,尚需扩大样本量,延长观察时间,以获得更丰富的数据和更准确地评价。

