超低位去大骨瓣术联合亚低温治疗重症颅脑损伤患者的效果观察
孙吉林 季 猛 张闻闻 卓健伟 王 凯 张 靖 徐亦农
江苏省泰州市第四人民医院神经外科 225300
重症颅脑损伤(Severe traumatic brain injury, STBI)死亡率高,及时有效的开颅手术治疗是降低患者的死亡率及改善预后的关键。骨瓣减压术由于安全性高、疗效确切等优势得到临床普遍认同,为治疗STBI的最常用术式。但该术法治疗STBI的效果存在一定的不足,考虑与术中骨窗暴露范围相对局限及患者颅内仍存在的高氧化应激水平有关[1]。超低位去大骨瓣术(DC)较常规骨瓣减压术暴露术野范围更大,便于术者彻底清创。亚低温治疗为物理降温联合人工冬眠合剂抑制中枢神经系统和保护脑组织,近年来,其在临床的应用逐渐得到重视,其效果已在改善癫痫持续状态得到证实[2]。亚低温治疗联合超低位DC或能有效减轻STBI患者的氧化应激反应,进一步改善预后。基于此,本文探讨超低位DC联合亚低温治疗对STBI患者的效果,具体如下。
1 资料与方法
1.1 一般资料 经伦理审核批准及患者家属同意,纳入我院在2019年6月—2021年6月收治的60例STBI患者作为观察对象。按随机数字表法分为C组和O组,各30例。其中C组男14例,女16例,年龄24~57岁,平均年龄(46.16±9.30)岁;创伤至入院时间1~5h,平均时间(3.05±0.43)h;格拉斯哥昏迷评分(GCS)5~8分,平均GCS(6.34±1.12)分;STBI类型:外伤性颅内血肿16例,弥漫性损伤5例,广泛性脑挫裂伤9例。O组男17例,女13例,年龄26~55岁,平均年龄(46.29±9.84)岁;创伤至入院时间1~4h,平均时间(3.11±0.38)h;GCS 5~8分,平均GCS(6.40±1.31)分;外伤性颅内血肿15例,弥漫性损伤4例,广泛性脑挫裂伤11例。两组一般资料对比无显著差异(P>0.05)。
1.2 选择标准 纳入标准:(1)诊断为STBI[3];(2)GCS 5~8分;(3)凝血功能正常;(4)受伤至入院时间不超过6h。排除标准:(1)合并脑血管疾病、脑肿瘤;(2)合并机体其他部位严重损伤;(3)既往颅手术史;(4)合并其他严重恶性疾病。
1.3 方法 C组:于颧弓上耳屏前做1cm切口,沿着耳郭上缘一直做切口至顶结节,在中线往前直至前发际线,沿着额颞反向翻转皮瓣,并向颞部翻转肌肉瓣,咬除部分颞鳞、蝶骨嵴,骨窗贴近前、中颅底窝,去除骨瓣,清除血肿,悬吊硬脑膜,呈放射状剪开硬脑膜,彻底清创后行止血、对硬脑膜予以减张缝合处理,在皮下放置引流管。O组:(1)超低位DC:于颧弓上耳屏前做1cm切口,沿耳郭上缘一直做切口至顶结节,在正中线往前直至前发际线,于对应头皮切口下形成骨窗,随后咬除额骨颧突至颞骨鳞部与蝶骨嵴外1/3水平处,扩大骨窗至接近横窦。悬吊硬膜后,剪开硬膜,行减压处理,并排除积血和脑脊液,清除失活组织和硬膜下血肿,然后减张缝合硬脑膜。同时松解颞肌筋膜,在皮下放置引流管。(2)亚低温治疗:开颅术后应用亚低温治疗仪(西安明克斯检测设备有限公司,HGT-200Ⅱ型治疗仪)实施局部降温治疗,给予盐酸哌替啶(东北制药,1ml∶50mg,H21023058)50mg+氯丙嗪(北京永康药业,1ml∶25mg,H11020559)25mg+异丙嗪(广东南国制药,2ml∶50mg,H44022504)25mg,均行肌内注射,8h给药1次。使患者体温维持在34~35℃,亚低温治疗共持续7d。所有患者术后接受治疗,均观察至患者出院。
1.4 观察指标 (1)氧化应激反应:于术前、术后7d,采集患者的静脉血3ml,采用化学发光分析仪测定(博科BKI2200)一氧化氮(NO)、丙二醛(MDA)、超氧化物歧化酶(SOD)水平。(2)炎症因子表达:于术前、术后7d,采集患者的静脉血3ml,采用电化学发光分析仪测定(罗氏E601)白介素-6(IL-6)、C反应蛋白(CRP)、肿瘤坏死因子(TNF-α)水平。(3)脑氧代谢情况:于术前、术后7d,通过颈内静脉置管测定颈内静脉血氧饱和度(JSO2),并采集患者的静脉血5ml,测定血乳酸(Jlac)、髓鞘碱性蛋白(MBP)、水通道蛋白质4(AQP4)、S-100蛋白水平。
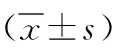
2 结果
2.1 两组氧化应激反应对比 术后7d,O组NO、MDA水平低于C组,SOD高于C组(P<0.05),见表1。

表1 两组氧化应激反应对比
2.2 两组炎症因子表达对比 术后7d,O组IL-6、CRP、TNF-α低于C组(P<0.05),见表2。

表2 两组炎症因子表达对比
2.3 两组脑氧代谢情况对比 术后7d,O组JSO2高于C组,Jlac、MBP、AQP4、S-100蛋白低于C组(P<0.05),见表3。

表3 两组脑氧代谢情况对比
3 讨论
STBI主要是受外界或间接暴力作用于头部所致的颅脑组织损伤,多伴有脑组织移位、脑脊液循环障碍、大脑后动脉受压等改变,致残率和死亡率均较高[4]。临床常规通过骨瓣减压术治疗STBI,但相关报道表明[5]其治疗效果有一定局限,是因为骨瓣减压术单纯手术治疗在降低氧化应激损伤、炎性损伤等继发性病理改变的作用有限,而上述并发改变可进一步加重脑组织损伤。超低位DC较的操作视野更大,利于受压脑组织向减压;亚低温治疗指主要将患者的温度控制在34~35℃,可降低代谢水平和继发性损伤。手术联合亚低温治疗以期减少炎症及氧化应激反应,提高治疗效果。
STBI患者颅内压升高,引起颅内缺血缺氧,继而引发高氧化应激反应和炎症反应,以及兴奋性氨基酸及单胺类物质入血增多,加剧脑组织缺氧及损伤。另外,缺血缺氧可导致无氧酵解作用增强,乳酸产生增多和自由基代谢紊乱[6]。本文结果显示:术后7d,O组NO、MDA、IL-6、CRP、TNF-α水平低于C组,SOD高于C组(P<0.05),说明超低位DC联合亚低温可有效降低STBI患者的氧化应激和炎症。超低位可拓宽颞低位、减压骨窗空间,暴露患者的中颅窝底,便于术者彻底清除顶叶、颞叶等部位颅内血肿及坏死脑组织,解除脑干受压,从而降低颅内压,改善脑脊液循环,减轻脑水肿,进而降低应激和炎症。并应用亚低温辅助治疗,通过物理降温与镇静药物将体温控制在34~35℃,可降低中枢神经系统活动,进而降低脑代谢和脑组织耗氧,抑制脑自由基的产生和减少内源性炎症因子的释放,起到脑保护的作用。与袁宝玉等[7]的研究结果一致。
MBP 在脑组织内表达丰富,血脑屏障功能损坏后的通透性增加,导致血清MBP水平升高。JSO2为反映神经组织代谢的重要指标,动脉血流经脑组织时的氧气消耗减少,静脉中耗氧量相应增加,导致JSO2下降。AQP4主要存在于中枢神经组织中,基底膜中含量较丰富,颅脑损伤后,血肿AQP4的水平增加。S-100蛋白为反映脑损伤的血清标志物。本文结果发现:O组术后7d的JSO2高于C组,Jlac、MBP、AQP4、S-100蛋白低于C组(P<0.05),说明超低位DC联合亚低温可有效改善STBI患者的脑氧代谢,减轻脑损伤。超低位DC在常规骨瓣减压术基础上增加了开窗范围,可迅速降低颅内压,改善脑循环,并有利于脊髓的血液重建,减轻脑内的灌注压力,改善脑组织的供血供氧。亚低温疗法使用人工冬眠合剂降低颅内代谢水平和机体耗氧,并提高各组织对缺氧的耐受能力,降低脑组织损伤后的耗氧量,减少乳酸沉积;也可降低血脑屏障通透性,抑制内源性有害因子及IL的生成和释放,减少神经元坏死、凋亡损伤,保护神经元,进而减轻脑组织损伤。
综上所述,超低位DC联合亚低温可有效减轻STBI患者的氧化应激反应和炎症水平,并改善患者的脑氧代谢和减轻脑组织损伤。

