不同输血次数及预防性用药对输血不良反应发生率的影响
江 飞,李燕飞,艾 红,王晓琴,高 敏
(1.合肥市骨科医院输血科;2.合肥市骨科医院脊柱外科,安徽合肥 238000)
成分输血作为临床一种特殊的治疗手段,在临床各科室已得到广泛应用,对挽救严重创伤性大出血等患者具有不可替代的作用[1-2]。但是考虑血液成分较为复杂且血型系统多样,输血风险仍不容小觑,成分输血治疗在发挥治疗效果的同时也会产生过敏、非溶血性发热等诸多输血不良反应。研究显示,我国输血不良反应发生率为1%~10%,部分多次输注患者可能会出现耐受或输注无效等情况[3]。可见,输血安全已成为临床重点关注的问题。但目前关于不同输注次数和预防性使用药物对输血相关不良反应的影响尚未完全明确,尤其是以往有过输血不良反应病史的患者输血前给予预防性使用药物能否减少不良反应的发生仍尚未有定论。因此,本研究旨在探讨不同输注次数及预防性使用药物对输血相关不良反应的影响,现报道如下。
1 资料与方法
1.1 一般资料 选取2020 年1 月至2022 年1 月合肥市骨科医院收治的300 例输血患者为研究对象进行回顾性分析,其中男性143 例,女性157 例;年龄21~85 岁,平均年龄(48.49±12.12)岁。根据不同的血液输注次数将300 例患者分为A 组(<5 次,189 例)、B 组(5~9 次,79 例)和C 组(≥10 次,32 例)。A 组患者中男性90 例,女性99 例;年龄22~85 岁,平均年龄(48.50±12.49)岁。B 组患者中男性39 例,女性40 例;年龄21~84 岁,平均年龄(48.43±12.31)岁。C 组患者中男性14 例,女性18 例;年龄22~83 岁,平均年龄(48.61±12.60)岁。3 组患者一般资料比较,差异均无统计学意义(均P>0.05),有可比性。根据是否有输血不良反应史将300 例患者分为D 组(有输血不良反应史,71 例)和E 组(无输血不良反应史,229 例)。D 组患者中男性35 例,女性36 例;年龄22~83 岁,平均年龄(48.45±12.57)岁。E 组患者中男性108 例,女性121 例;年龄23~85 岁,平均年龄(48.67±12.68)岁。两组患者一般资料比较,差异无统计学意义(P>0.05),组间具有可比性。本研究获合肥市骨科医院医学伦理委员会批准。纳入标准:①主要接受红细胞及血浆输注治疗的骨科患者;②年龄≥21 岁;③临床资料完整。排除标准:①重要器脏异常者;②对本研究药物过敏者;③其他恶性肿瘤患者。
1.2 研究方法 患者输血前给予预防性用药或不予药物处理,预防性用药主要为静脉注射地塞米松磷酸钠(石药银湖制药,国药准字H14022567,规格:1 mL ∶5 mg)5 mg 或肌内注射异丙嗪(上海禾丰制药,国药准字H31021490,规格:1 mL ∶25 mg)25 mg。患者主要采用红细胞及血浆输注治疗,根据《临床输血学》[4]要求,医护人员在输血过程中观察患者有无输血不良反应,详细记录患者输血次数、输血前预防性用药、输血前后生命体征等情况。每例患者每次血液输注视为1 例次,不同血液成分连续输注需分别计数,输血不良反应发生率=输血不良反应发生例次/总输血例次×100%。
1.3 观察指标 ①分析预防性用药情况、输注次数和输血不良反应史对患者不良反应发生率的影响;②探讨不同输注次数下预防性用药情况和不同输血不良反应史下预防性用药情况对不良反应发生率的影响。输血不良反应判断参考《血站技术手册》[5]。
1.4 统计学分析 采用SPSS 24.0 统计学软件处理数据。计数资料以[例(%)]表示,组间比较采用χ2或校正χ2检验,多个样本率的多重比较采用Bonferroniχ2检验,以P<0.01 为差异有统计学意义;计量资料以(±s)表示,组间比较采用独立样本t检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 患者输血总体情况 300 例患者共进行了1 384 例次血液输注,其中输注次数<5 次的患者有189 例,共进行了374 例次血液输注;输注次数为5~9 次的患者有79 例,共进行了537 例次血液输注;输注次数≥10 次的患者有32 例,共进行了473 例次血液输注。有输血不良反应史的患者71 例,共进行了330 例次血液输注;无输血不良反应史的患者229 例,共进行了1 054 例次血液输注。300 例患者共发生输血不良反应108 例次,不良反应总发生率为7.80%。
2.2 预防性用药对输血不良反应发生率的影响 预防性用药患者与未预防性用药患者输血不良反应发生率比较,差异无统计学意义(P>0.05),见表1。

表1 预防性用药对输血不良反应发生率的影响
2.3 不同输注次数对输血不良反应发生率的影响 A 组患者输血不良反应发生率比B 组和C 组低,B 组比C 组低,差异均有统计学意义(均P<0.05),见表2。
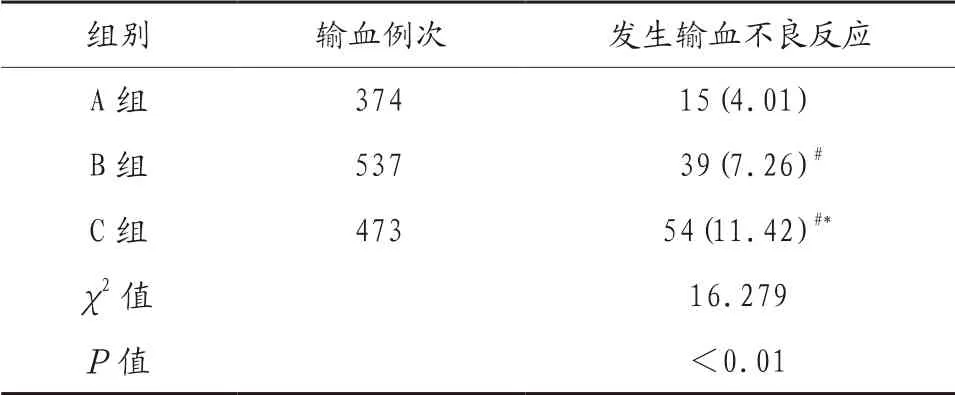
表2 不同输注次数对输血不良反应发生率的影响
2.4 不同输注次数下预防性用药情况对输血不良反应发生率的影响 A 组、B 组和C 组患者预防性用药患者与未预防性用药患者输血不良反应发生率比较,差异均无统计学意义(均P>0.05),见表3。

表3 不同输注次数下预防性用药情况对输血不良反应发生率的影响 [例(%)]
2.5 输血不良反应史对输血不良反应发生率的影响 D 组患者输血不良反应发生率比E 组高,差异有统计学意义(P<0.05),见表4。

表4 输血不良反应史对输血不良反应发生率的影响
2.6 不同输血不良反应史下预防性用药情况对输血不良反应发生率的影响 D 组和E 组预防性用药患者与未预防性用药患者输血不良反应发生率比较,差异无统计学意义(P>0.05),见表5。

表5 不同输血不良反应史下预防性用药情况对输血不良反应发生率的影响 [例(%)]
3 讨论
输血治疗虽在严重创伤性大出血等治疗中发挥着重要作用,但输血安全性仍不容小觑,以输血不良反应最为常见,而疾病种类、血液制品品类、输注次数及输血时间等均可对输血不良反应造成影响[6]。但目前关于不同输注次数及预防性用药对输血不良反应发生率的影响仍缺乏高质量的临床研究。为此,本研究针对此方面展开探究。
本研究中,输血不良反应总发生率为7.80%,这与既往报道[7]相符。但夏紫怡等[8]报道输血不良反应发生率为0.39%,与本研究结论存在偏差,原因可能与疾病类型、样本量大小、输血不良反应统计方法、医院地域及等级等因素有关。针对输血不良反应统计方法,以往临床上多由输血科等工作人员按照临床报告的输血不良反应统计结果,但实际工作中诸多因素会导致漏报事件的发生[9],而本研究中,医务人员定期随访,可降低漏报率,确保统计结果真实可靠。
本研究结果显示,A 组患者输血不良反应发生率低于B 组和C 组,B 组低于C 组,提示输注次数与患者输血不良反应发生率密切相关,输注次数与输血不良反应发生率成正比。郝欣欣等[10]也发现输注次数与输血不良反应发生率有关,输血不良反应发生率随着输注次数的增加而增加,支持本研究结论。推测原因,随着输注次数的增多,机体产生同种免疫抗体的概率越高,激活补体,导致各种输血不良反应发生率增加。
本研究结果显示,预防性用药与否对输血不良反应的影响不大,提示输血前预防性用药对输血不良反应发生率并无明显影响。有研究显示,输血前预防性用药率高达50%~80%,其中异丙嗪、地塞米松等是输血前常用药物[11]。地塞米松作为一种肾上腺皮质类合成激素,具有抗感染、抗过敏等效应,预防免疫反应发生,同时可经调节纤维蛋白原和细胞内钙离子浓度来减少不良发应的发生;而异丙嗪作为一种抗组胺药物,减少平滑肌收缩、痉挛,对血液或血浆制品的过敏反应有预防效果[12]。而郑茂[13]认为输血前进行异丙嗪、地塞米松等预防性用药对输血不良反应的发生并无明显作用,支持本研究结论。推测原因,地塞米松虽对已发生的输血反应有较好的治疗效果,但对已形成的抗体并无中和效应;而异丙嗪对抗作用多针对组胺含量升高,但发生过敏反应与组胺释放、慢反应物质释放等诸多因素有关,故其仅对已发生的部分过敏反应有治疗效果[14]。此外,本研究结果显示,A 组、B 组和C 组预防性用药患者与未预防性使用药物患者输血不良反应发生率对比,差异无统计学意义,提示预防性用药不影响不同输注次数的输血安全性。
本研究结果显示,D 组患者输血不良反应发生率高于E 组,但两组预防性用药患者与未预防性用药患者输血不良反应发生率比较,差异无统计学意义,提示输血不良反应史虽与输血不良反应发生率有关,但预防性用药对有输血不良反应史患者的输血不良反应发生率无明显影响。通常患者有输血不良反应史时可能意味着体内产生的抗体类型复杂少见,导致输血不良反应发生率增加。
综上所述,输血相关不良反应与输注次数和输血不良反应史密切相关,而预防性使用药物对不同输注次数和输血不良反应史患者的输血相关不良反应发生率的影响不大,值得临床验证。但本研究未纳入患者疾病类型、血液制品品类、预防性用药的时间进行分析,故今后仍需深入研究。

