贝伐珠单抗联合奥希替尼治疗EGFR突变晚期NSCLC的疗效及对血管生长因子水平的影响
孙虎,冯慧晶,杨晓玲,杨雪晶
(山西白求恩医院·山西医学科学院同济山西医院·山西医科大学第三医院肿瘤中心胸部肿瘤科,山西 太原 030032)
肺癌是常见的恶性肿瘤之一,非小细胞肺癌(non small cell lung cancer,NSCLC)为主要类型,约占80%,且约3/4的患者诊断时属于晚期,预后差,5年生存率为20%左右。[1]。在NSCLC患者中,表皮生长因子受体(EGFR)常会出现突变。数据[2]显示,亚洲人群中其突变率达30%~50%。在EGFR突变的NSCLC治疗中,与其他化疗药物相比,EGFR-酪氨酸激酶抑制剂(EGFR-TKI)有益于生存期延长,已成为个性化靶向治疗的一线标准药物[3]。作为第三代EGFR-TKIs,奥希替尼能同时阻断EGFR活化突变及T790M突变,较第一代EGFR-TKIs更具优势[4]。然而,随着EGFR-TKIs治疗疗程的延长,获得性耐药不可避免,如何延缓或减少耐药,提高疗效,是目前治疗面临的一大难题。为应对获得性耐药,联合治疗成为重要手段。研究[5-6]发现,贝伐珠单抗被很多联合EGFR-TKIs能够延长疾病控制时间,但联合奥希替尼的临床研究尚需进一步验证。本研究旨在探讨贝伐珠单抗联合奥希替尼治疗EGFR突变晚期NSCLC的疗效及对血管生长因子水平的影响。
1 资料与方法
1.1 一般资料
选取2016年1月至2019年12月山西白求恩医院收治的92例EGFR突变晚期NSCLC患者为研究对象,根据治疗方法不同分为单药组(n=44)和联合组(n=48)。本研究符合《赫尔辛基宣言》要求,患者知情同意。两组患者一般资料比较,差异无统计学意义(P>0.05)。见表1。纳入标准:(1)病理诊断IIIB或IV期NSCLC,属于肺腺癌;(2)基因检测显示EGFR基因突变(外显子19或21突变);(3)初治患者;(4)美国东部肿瘤协作组(ECOG)体力评分属于0~2分;(5)生存期预计不低于3个月;(6)年龄≥18岁;(7)采用EGFR-TKIs(奥希替尼)一线治疗。排除标准:(1)基因检测同时存在EGFR其他罕见突变者;(2)合并重要脏器(如心肺肾)功能不全者;(3)伴发其他癌症者;(4)严重凝血机制障碍者;(5)有活动性出血者;(6)联合放化疗等其他抗肿瘤治疗者;(7)有活动性脑转移者;(8)临床资料缺失者。

表1 两组患者一般资料比较
1.2 方法
单药组予以奥希替尼(阿斯利康制药公司)80 mg口服,1次/d。联合组在奥希替尼治疗基础上,予以贝伐珠单抗(罗氏制药公司)治疗,每次7.5 mg/kg,静脉输注,21 d定为1个周期。两组患者均持续用药到病情进展。
1.3 观察指标
(1)近期疗效:治疗3个月后按实体瘤疗效评价标准(RECIST 1.1)[7]评估。目标病灶消失为完全缓解(CR);目标病灶肿瘤最大径退缩≥30%为部分缓解(PR):目标病灶肿瘤最大径增大20%或有新病灶出现为疾病进展(PD);未达到PR,且不及PD为疾病稳定(SD)。客观缓解率(ORR)=(CR+PR)例数/总例数×100%;肿瘤控制率(DCR)=(CR+PR+SD)例数/总例数×100%。(2)肿瘤标志物水平:治疗前和治疗3个月后采集患者空腹外周静脉血5 mL,3 500 rpm离心10 min分离血清,采用电化学发光法检测细胞角蛋白19片段(Cyfra21-1)、癌胚抗原(CEA)和糖类抗原125(CA125)水平。(3)血管生长因子水平:治疗前和治疗3个月采用酶联免疫吸附法检测血清碱性成纤维细胞生长因子(bFGF)、血管内皮生长因子(VEGF)和血小板衍生生长因子(PDGF)水平。(4)生存预后:门诊或电话随访至2022年6月,以无进展生存时间(PFS)及总生存时间(OS)作为预后指标。(5)不良反应发生情况:包括消化道反应、皮疹、肝损害、肾损害、高血压等。
1.4 统计学分析

2 结果
2.1 两组患者近期疗效比较
联合组患者ORR高于单药组,差异有统计学意义(P<0.05);两组患者DCR比较,差异无统计学意义(P>0.05)。见表2。
2.2 两组患者肿瘤标志物水平比较
治疗前,两组患者血清CEA、CA125和CYFRA21-1水平比较,差异无统计学意义(P>0.05)。治疗后,两组患者CEA、CA125、CYFRA21-1水平均降低(P<0.05),且联合组低于单药组(P<0.05)。见表3。

表2 两组患者近期疗效比较[n(%)]

表3 两组患者血清肿瘤标志物水平比较
2.3 两组患者血管生长因子水平比较
治疗前,两组患者血清VEGF、PDGF、bFGF水平比较,差异无统计学意义(P>0.05)。治疗后,两组患者VEGF、PDGF、bFGF水平均降低(P<0.05),且联合组低于单药组(P<0.05)。见表4。

表4 两组患者血管生长因子水平比较
2.4 两组患者生存预后比较
随访4.6~40.4(中位数为21.2)个月。联合组、单药组的中位PFS分别为14.4、10.2个月,前者优于后者(χ2=19.892,P<0.001);联合组、单药组的中位OS分别为24.9、20.3个月,前者优于后者(χ2=9.654,P<0.001)。见图1及图2。

2.5 两组患者不良反应发生情况比较
两组患者各种不良反应发生率比较,差异无统计学意义(P>0.05),且均以1~2级为主,患者能够耐受。见表5。
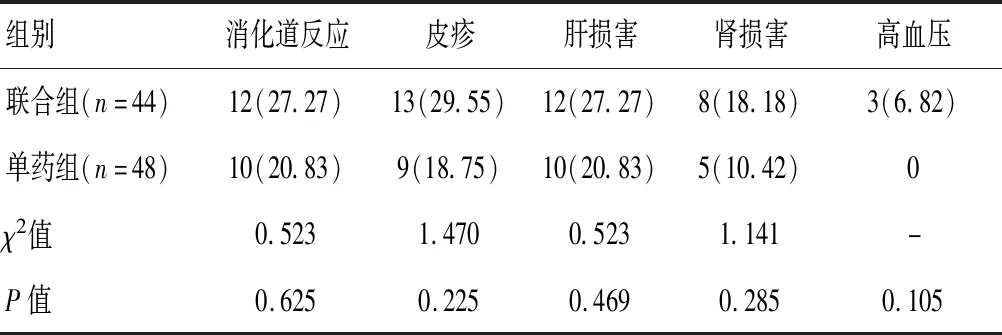
表5 两组患者不良反应情况比较[n(%)]
3 讨论
EGFR-TKI获得性耐药是制约晚期肺癌疗效的重要因素,如何延缓耐药或减少耐药发生是临床迫切需要解决的问题,联合用药是当前研究的热点。研究[8-9]表明,在肺癌血管形成中,VEGF信号通路发挥着极为关键的作用,VEGF表达上调有利于肿瘤转移,并可导致不良预后。抗VEGF药物能够抑制VEGF受体与VEGF的结合,使得血管新生受到抑制,进而产生抗肿瘤效应[10]。EGFR-TKIs、抗VEGF药物分别对肿瘤生长的不同途径产生作用,二者联用可能有助于提高晚期肺癌的疗效。Seto等[11]研究显示,第一代EGFR-TKI厄洛替尼联合贝伐珠单抗一线治疗能延长EGFR突变晚期肺腺癌患者的PFS(16.0个月vs.9.7个月)。多中心III临床试验[12]也得到类似结果,联合用药使晚期肺癌患者PFS延长(16.9个月vs.13.3个月)。抗VEGF药物不管是联合第一代EGFR-TKI或是化疗均有着更好的疗效,而奥希替尼相比第一代EGFR-TKI对于晚期肺癌的控制率更优。但目前关于奥希替尼与贝伐珠单抗组成的“强强联合”治疗方案在晚期NSCLC中的临床应用鲜有文献报道。
本研究显示,相比单药组,联合组ORR提高(P<0.05),且中位PFS、OS均延长(P<0.05),表明在EGFR突变NSCLC治疗中,贝伐珠单抗与奥希替尼联用有较好疗效,有益于患者生存期延长,可能与以下机制有关:(1)两种药物通过不同作用发挥抗肿瘤作用。奥希替尼对EGFR的磷酸化水平产生抑制作用,使肿瘤细胞生长信号通路受到阻滞,进而影响肿瘤的增殖;贝伐珠单抗对VEGF与其受体的结合过程产生阻断作用,使血管新生受到抑制,减少肿瘤生长过程中需要的血供,进而对肿瘤生长产生抑制作用[13-14]。(2)两种药物有协同抗肿瘤效果。相关研究[15-16]指出,EGFR信号通路的激活状态对VEGF的表达有诱导作用,利于血管生长,而VEGF的高表达对P13K/Akt信号通路的激活有促进作用,能代替EGFR对肿瘤生长产生促进作用,故联用抑制EGFR信号通路的EGFR-TKI和抗VEGF药物能发挥协同抗肿瘤作用。(3)延缓EGFR-TKI耐药。研究[17]发现,EGFR-TKIs在抑制EGFR磷酸化时,会引起耐药细胞的VEGF表达上调,高表达的VEGF通过对磷酸化ERK和AKT而对EGFR-TKI的获得性耐药产生诱导作用,因此予以抗VEGF药物可能有助于延缓耐药的发生。
血管新生可为肿瘤增殖、转移创造有利的血管微环境[18]。VEGF、PDGF、bFGF均是重要的血管生长因子,能够刺激肿瘤血管新生,其表达水平与肿瘤侵袭、转移紧密关联。 CEA、CA125、CYFRA21-1均是常见的肿瘤标志物,表达水平对于疗效评估和预后判断有着重要意义。本研究结果显示,治疗3个月后,联合组血管生长因子和肿瘤标志物水平低于对照组(P<0.05),从分子水平再一次验证了联合用药的疗效。两组患者各种不良反应发生率差异无统计学意义(P>0.05),且均以1~2级为主,患者能够耐受,提示本研究中联合用药方案不会增加毒副作用,安全性可接受。本研究存在不足在于纳入研究和统计分析的例数较少,难免会影响结论的外推,仍有待扩大样本量进一步验证。
综上,奥希替尼联合贝伐珠单抗治疗EGFR突变晚期NSCLC患者辅可获得较好疗效,能有效下调肿瘤生长相关因子的表达,延长患者生存期,且安全性良好。

