基于索磷布韦的直接抗病毒药物对慢性丙型肝炎细胞因子动态变化的影响
叶飞翔 李晶 刘景瑞 刘培 杜云飞
HCV感染是肝纤维化、肝硬化以及肝细胞癌发生的重要原因。CHC病情较为隐匿,目前尚无预防性疫苗问世。直接抗病毒药物(DAAs)相关研究及开发正处于迅速发展态势,多种药物相继获批问世,近年来DAAs已成为清除HCV的首选方案[1-3]。CHC患者长期炎症状态可能改变机体肝脏微环境,导致不可逆的肝细胞损伤。DAAs诱导HCV病毒载量快速下降导致免疫监视重建,伴随着II型和III型干扰素(IFN)受体及其下游刺激基因表达下调,造成体内免疫细胞水平失衡,影响抗肿瘤活性[4-5]。因此了解CHC患者DAAs抗病毒治疗后细胞因子水平具有重要临床意义,现将结果报道如下。
资料与方法
一、研究对象
选取2018年6月至2021年10月于本院首诊并接受系统治疗的初治CHC患者78例,其中男41例、女37例,年龄(52.3±10.7)岁。根据HCV感染疾病不同阶段分为慢性肝炎、肝硬化,选取同期体检者50例作为对照,其中男29例、女21例,年龄(51.2±11.5)岁。CHC诊断符合要求[6]。排除标准:合并其他类型嗜肝性病毒;并发局灶性、弥漫性慢性肝病;既往接受抗HCV、免疫抑制治疗。
二、研究方法
纳入CHC病例接受索磷布韦联合维帕他韦、利巴韦林方案进行口服治疗。搜集CHC临床资料,比较基于索磷布韦的DAAs方案治疗前后细胞因子动态变化、持续病毒学应答(SVR)率情况,SVR定义参考既往文献。
三、细胞因子检测
分别在CHC初诊时、抗HCV治疗12周时采集空腹抗凝外周血,离心回收上清液后冻存。应用多细胞因子试剂盒(BECKMAN COULTER公司,USA)检测CHC患者、健康体检者血清细胞因子,通过流式点阵仪(BECKMAN COULTER公司,USA)采用参数回顾法检测血清细胞因子浓度。
四、统计学方法
SPSS 23.0处理数据,α=0.05。计量资料用中位数(四分位间距)表示,两组间比较采用t检验;计数资料用例数(%)表示,采用卡方检验比较。
结 果
一、健康体检者、CHC基线资料比较
比较CHC、健康体检者基线资料,如表1所述,发现ALT、AST、TBil、IL-6、IL-7、单核细胞趋化蛋白-4(MCP-4)及血管内皮生长因子-A(VEGF-A)等差异具有统计学意义(P<0.05)。
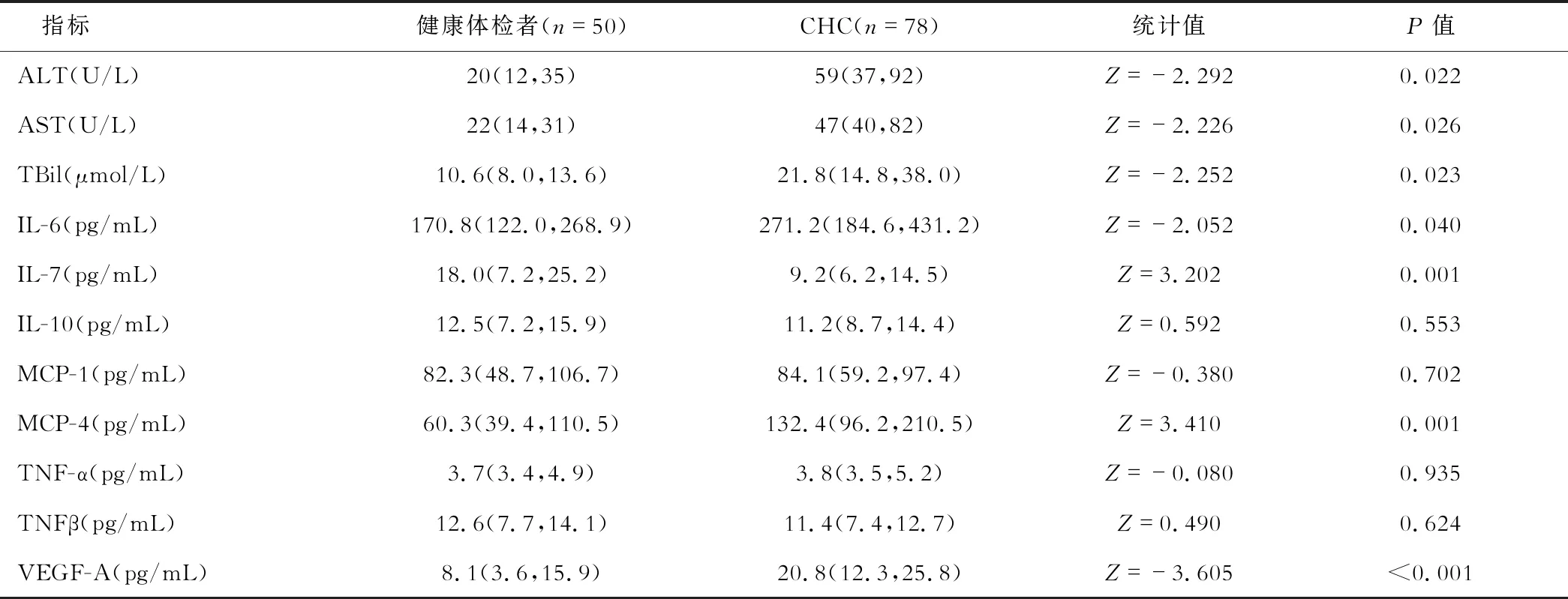
表1 CHC、健康体检者基线资料[M(P25,P75)]比较
二、CHC治疗前、治疗后12周细胞因子变化
基于索磷布韦的DAAs方案治疗12周后,CHC患者SVR率为93.6%(73/78),其中慢性肝炎病例为98.1%(52/53),肝硬化病例为84.0%(21/25),差异具有统计学意义(χ2=5.640,P<0.05)。继续解析细胞因子,如表2所述,发现治疗前CHC、治疗后慢性肝炎与肝硬化IL-6、IL-7及MCP-4差异具有统计学意义(P<0.05);治疗后慢性肝炎、肝硬化VEGF-A显著高于治疗前CHC(P<0.05),但治疗后慢性肝炎、肝硬化VEGF-A差异不具有统计学意义(P>0.05)。
讨 论
HCV感染病例慢性化机制尚待明确,通常认为是由免疫系统介导的细胞因子网络动态失衡而造成的肝细胞损伤。与健康体检者相比,我们发现治疗后CHC患者多种细胞因子发生显著变化。IL-6由各种免疫细胞、实质细胞分泌。有研究表明,基于IL-6的信号通路可以调控再生及机体免疫保护,从而发挥促炎作用机制[8]。Nawaz等[9]发现,HCV感染后IL-6异常增加引发肝脏实质损伤,促使CHC病情进展。而Naseem等[8]表示IL-6上升后可促进淋巴细胞增殖,改善衰竭细胞功能。本研究发现,感染HCV后IL-7水平呈现下降趋势,这与之前的研究是相符合的。Osburn等[10]研究显示,感染HCV后血清MCP-4浓度明显上升,我们也得出类似结果。高艺等[11]继续探讨应用DAAs治疗后血清MCP-4浓度变化,发现其表达下降,表明MCP-4参与了HCV感染后的机体炎症应答调控。另外,已有研究报道,接受DAAs治疗的HCV患者肝细胞癌发生及复发风险可能会增加[12-13]。先前研究表明,IFN在治疗HCV感染病例时具有免疫调节特性,调节各种免疫细胞从而抑制肿瘤增殖和血管生成[14]。与IFN不同,DAAs并没有抵抗肿瘤增殖和血管生成的作用,导致存在肿瘤细胞增殖的风险。研究发现,接受DAAs口服治疗后CHC病例炎症水平下降,但血清VEGF浓度显著增加[15]。这与我们的结果是相符合的,但与高艺等[11]研究结果存在差异,可能受到DAAs方案选择、CHC纳入标准的影响。
CHC治疗已进入DAAs时代,有关DAAs抗HCV感染的相关研究已陆续开展。本次研究应用以索磷布韦为基础的DAAs方案治疗12周后,CHC患者SVR率达到93.6%。不过,相较于慢性肝炎病例,并发肝硬化的CHC患者SVR率显著下降,因此后者DAAs方案选择是需要继续探究的。
综上所述,IL-6、IL-7、MCP-4及VEGF-A参与CHC患者免疫炎症反应,基于索磷布韦的DAAs治疗方案能够显著影响上述细胞因子血清浓度,改善患者炎症状态。
利益冲突声明:所有作者均声明不存在利益冲突。

