后腹腔镜下精准解剖性左侧肾上腺切除术*
张楠,马曜辉,孔素芳,郝朝辉,李香瑞,单中杰
[河南中医药大学第五临床医学院(郑州人民医院)泌尿外科,河南 郑州450003]
腹腔镜肾上腺切除术应用于临床将近30 年,已经成为肾上腺肿瘤切除的首选术式[1-2]。腹腔镜肾上腺切除术从最初的经腹腔路径,到随后的经后腹腔路径,从切除术到解剖性切除术,从三层面法到单层面法,仍在不断地探索、改进中[3-5]。不同的手术路径和手术方式各有优势,总体趋势是越来越精细化和微创化。近年来,笔者经过广泛的临床实践,结合经典的腹腔镜肾上腺切除术,提出了后腹腔镜下精准解剖性左侧肾上腺切除术,取得了较好的治疗效果。现报道如下:
1 资料与方法
1.1 一般资料
回顾性分析2016 年1 月-2019 年3 月该院202例实施左侧肾上腺切除术的患者的临床资料。选择2018年1月-2019年3月实施后腹腔镜下精准解剖性左侧肾上腺切除术的107例住院患者作为试验组。其中,男46例,女61例;年龄23~69 岁,平均(50.6±8.3)岁;皮质醇腺瘤39例,醛固酮腺瘤42例,嗜铬细胞瘤13例,肾上腺囊肿8例,副神经节瘤3例,髓样脂肪瘤2例;肿瘤直径1.2~12.0 cm,平均(4.6±2.2)cm;高血压52例,高血压合并糖尿病13例,高血压合并冠心病20例,高血压合并脑血管病16例,高血压合并2种以上疾病者6例。选择2016年1月-2018年12月实施后腹腔镜下解剖性左侧肾上腺切除术的95例住院患者作为对照组。其中,男51例,女44例;年龄25~67 岁,平均(51.0±7.6)岁;皮质醇腺瘤29例,醛固酮腺瘤32例,嗜铬细胞瘤15例,肾上腺囊肿10例,副神经节瘤5例,髓样脂肪瘤4例;肿瘤直径1.5~11.0 cm,平均(4.3±2.1)cm;高血压47例,高血压合并糖尿病11例,高血压合并冠心病17例,高血压合并脑血管病13例,高血压合并2种以上疾病者7例。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。见表1。
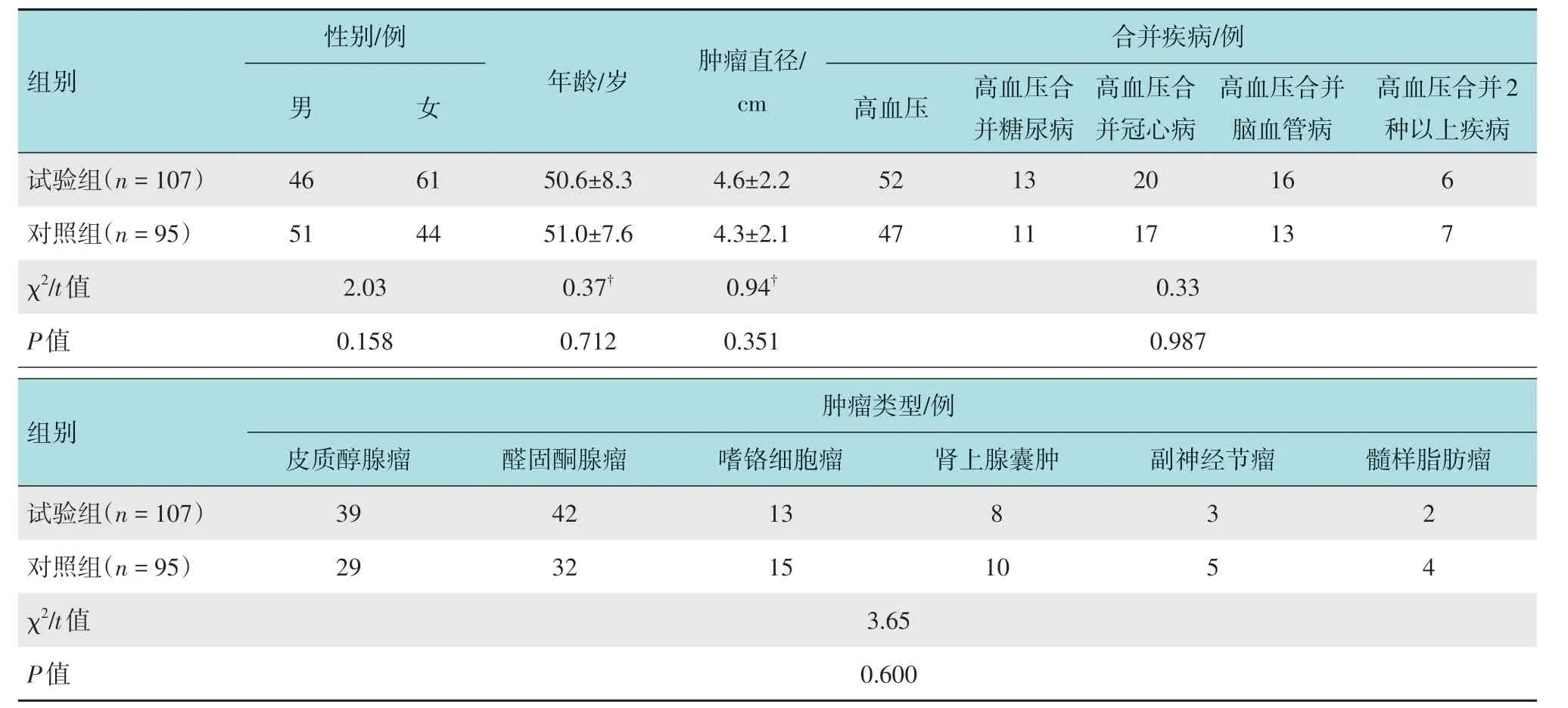
表1 两组患者一般资料比较Table 1 Comparison of general data between the two groups
1.2 术前准备
所有患者术前均完成血清皮质醇(早上8点、下午4 点和凌晨0 点)、促肾上腺皮质激素(早上8 点、下午4 点和凌晨0 点)、肾素-血管紧张素-醛固酮、血儿茶酚胺(肾素、去甲肾上腺素、多巴胺)、24 h尿17-羟皮质类固醇、24 h 尿17-酮类固醇、24 h 尿香草苦杏仁酸、24 h尿游离皮质醇、肝肾功能、血葡萄糖、血常规、尿常规、心电图、肾上腺CT平扫+增强等检查。根据病情合理控制血压及心率,扩容。
1.3 手术方法
1.3.1 手术入路 气管插管全身麻醉,患者取右侧卧位,腰部抬高,头低足低位。于十二肋下2.0 cm腰方肌外侧缘斜行切开皮肤和皮下组织,钝性分开肌层及腰背筋膜进入腹膜后间隙。置入自制扩张球囊,注入空气600~900 mL,建立后腹腔间隙,置入一次性12 mm穿刺器,连接气腹管,最高压14 mmHg,置入腹腔镜,直视下于腋中线髂嵴上2.0 cm置入10 mm穿刺器,十二肋下2.0 cm腹直肌外侧缘置入一次性5 mm穿刺器,置入操作器械,实施手术。清理腹膜外脂肪,切开侧锥筋膜进入腰肌前间隙,上至膈肌内侧弓状韧带,下至吉氏筋膜锥尖部。
1.3.2 试验组手术步骤 以膈肌内侧弓状韧带(附图A)为解剖标志寻找左肾动脉[6],在肾动脉的上缘向肾上腺方向分离,可见肾上腺中下动脉(附图B),用Hem-o-lok夹夹闭并离断,左手分离钳放置在肾动脉的上缘,将肾上极向腹侧牵引,吸引器分离即可找到肾上腺中央静脉(附图C),有时可见左侧膈下静脉,用Hem-o-lok夹夹闭并离断。松开左手分离钳,肾上极复位,在肾动脉平面后腹膜反折的外侧纵行切开肾周筋膜及脂肪囊,进入脂肪囊与肾纤维膜间隙(附图D),在此间隙向肾上腺方向分离,充分暴露肾上极,离断肾上腺底部与肾上极之间的脂肪。此时,可看到离断的肾上腺中央静脉近端。牵拉肾上腺底部脂肪,于融合筋膜和肾上腺包膜之间分离肾上腺的腹侧面(附图E),完整暴露肾上腺。如果是腺瘤和嗜铬细胞瘤等良性病变,在完整切除肿瘤的同时,应尽量保留部分正常的肾上腺组织;如果是结节性增生,对侧肾上腺正常,则给予完整切除,肾上腺残端用可吸收夹夹闭止血。检查创面有无活动性出血及周围脏器损伤,取出标本,用生物胶喷洒肾表面,脂肪囊及肾脏复位。肾脏上极背侧放置引流管1 根,从左侧髂嵴上穿刺孔引出,固定,依次缝合其余2个穿刺孔。
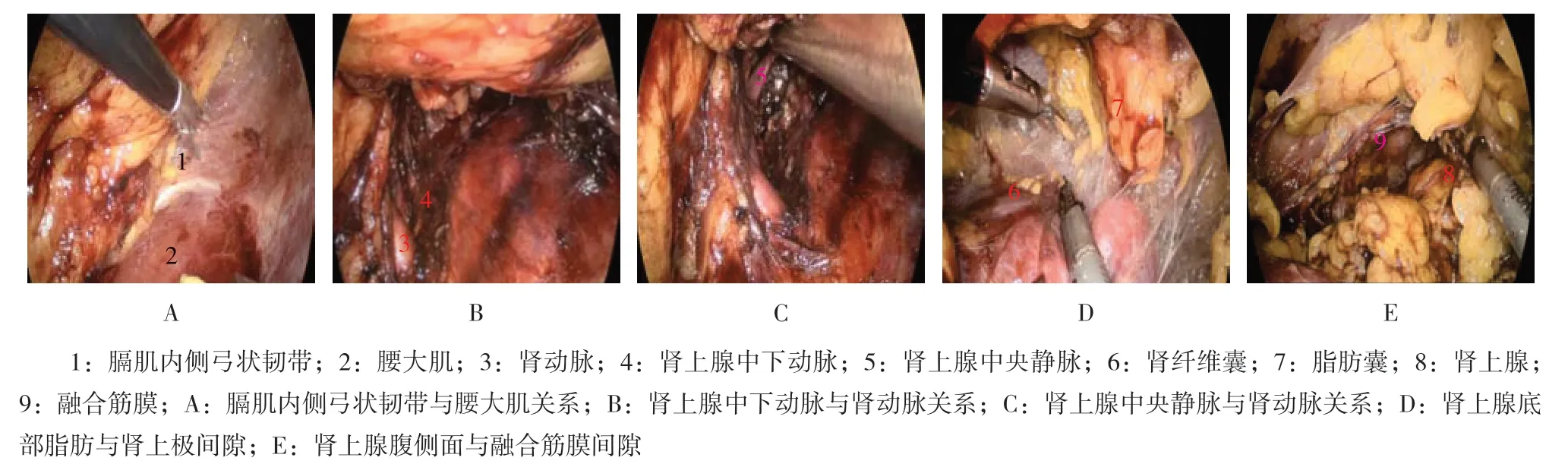
附图 精准解剖性左侧肾上腺切除术Attached fig.Accurate anatomical left adrenalectomy
1.3.3 对照组手术步骤 按文献[7]实施手术,麻醉、体位、建立后腹腔间隙以及穿刺孔位置与试验组相同。进入后腹腔间隙清理腹膜外脂肪。首先,于肾脏内上方的肾周脂肪囊与前层Gerota筋膜之间,分离肾上腺的腹侧面(第一层面);其次,于肾脏外上方的肾周脂肪囊与后层Gerota筋膜之间,分离肾上腺的背侧面(第二层面);再次,于肾上腺底部脂肪囊与肾上极实质表面之间,分离肾上腺底部(第三层面);最后,切除肾上腺及肿瘤。
1.4 评价指标
观察两组患者手术时间、术中出血量、术后引流量、术后住院时间、术后胃肠功能恢复时间、术后止痛剂用量(盐酸曲马多注射液)和术中术后并发症发生率。
1.5 统计学方法
选用SPSS 22.0 软件进行统计学处理。计量资料以均数±标准差()表示,采用t检验;计数资料用百分率(%)表示,行χ2检验。P<0.05 为差异有统计学意义。
2 结果
试验组手术时间较对照组短[(43.6±10.5)和(67.8±15.1)min],术中出血量较对照组少[(29.3±12.5)和(69.4±25.5)mL],腹膜损伤率较对照组低(4.7%和14.7%),差异均有统计学意义(P<0.05);试验组和对照组术后引流量[(79.4±22.3)和(81.9±26.9)mL]、术后住院时间[(5.9±0.7)和(5.8±0.7)d]、术后胃肠功能恢复时间[(17.7±4.4)和(16.7±3.6)d]和术后止痛剂用量[(167.3±79.8)和(174.7±77.1)mg]比较,差异均无统计学意义(P>0.05)。见表2。
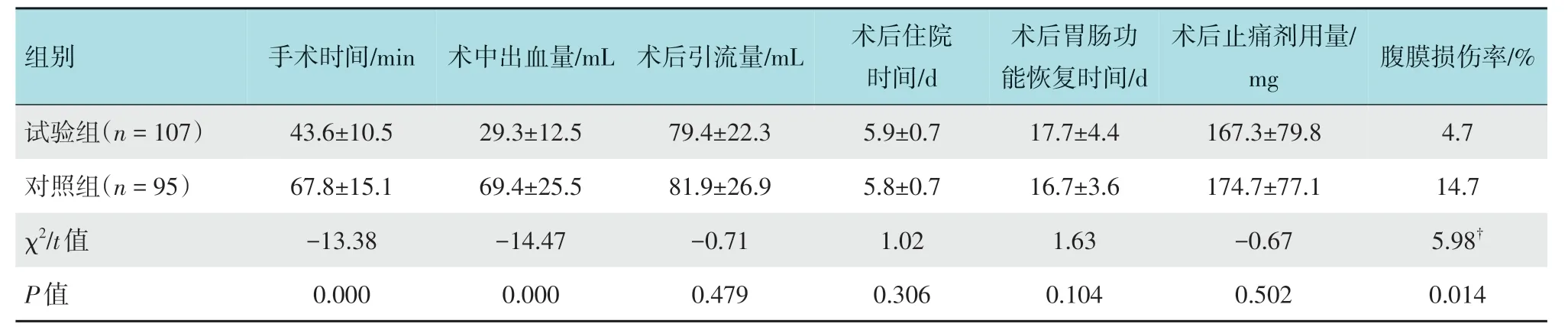
表2 两组患者手术相关情况比较Table 2 Comparison of operation related conditions between the two groups
3 讨论
1992年GAGNER等[8]报道了首例经腹腹腔镜肾上腺切除术。1995年MERCAN等[9]报道了首例经后腹腔镜肾上腺切除术。2007年张旭等[7]报道了后腹腔镜解剖性肾上腺切除术,提出了三层面法肾上腺切除术。随后,三层面法后腹腔镜肾上腺切除术的应用逐渐增多。但三层面法存在学习曲线长、腹膜破裂发生率高和肥胖患者暴露肾上腺困难等缺点[5,10]。随着后腹腔镜手术应用的增多和对后腹腔间隙解剖研究的进展,不少学者[10-12]对后腹腔镜肾上腺切除术进行了改良和优化。
2017 年以来,笔者团队逐步开展了后腹腔镜下单一解剖路径肾上腺切除术,曾在国内最大的泌尿外科专业自媒体学习联盟上推广授课,至今学习人次超过7 000。2018 年以来,经过对左侧肾上腺解剖特点的研究,笔者在单一解剖路径的基础上,进一步提出了后腹腔镜下精准解剖性左侧肾上腺切除术,这种手术方式的优点是:①处理肾上腺中下动脉及中央静脉精准迅速:在腰肌前间隙向上分离至膈肌内侧弓状韧带,以膈肌内侧弓状韧带为解剖标志,定位寻找肾动脉,再以肾动脉为解剖标志,寻找处理肾上腺中下动脉束,随后向肾上腺底部分离,即可找到肾上腺中央静脉,并给予处理;②早期控制肾上腺血管,减少术中出血:笔者在寻找肾上腺及肿瘤之前,先控制了肾上腺的中下动脉及中央静脉,大大降低了出血风险,本研究的107例患者,术中均无大出血和输血病例,试验组术中出血量明显少于对照组;③术野清晰,手术时间短;④在肾周脂肪囊与肾包膜间隙游离寻找肾上腺,降低了腹膜损伤率;⑤先控制肾上腺血管,再寻找并切除肾上腺及肿瘤,更符合脏器切除原则,无论是开放手术还是腔镜手术,无论是泌尿外科手术还是普通外科或妇科手术,在切除脏器或肿瘤时,都要求术中尽早控制血管,尤其是动脉,精准解剖性左侧肾上腺切除术完全符合这一常规原则;⑥解剖标志精准,解剖层面准确,手术步骤合理,更有利于推广学习;先寻找处理肾上腺血管,再寻找并切除肾上腺及肿瘤,每个步骤均有明确的解剖标志,术中不至于迷失方向,减少了不必要的分离,提高了手术的精准性。
综上所述,后腹腔镜下精准解剖性左侧肾上腺切除术安全、可行。与经典三层面法比较,其手术时间明显缩短,术中出血量减少,术中腹膜损伤发生率明显降低,值得临床推广应用。

