利用“设未知数求解法”计算化学反应焓变的思维模型
——以2022年高考真题化学反应焓变计算为例
江苏 董拥军
新课程标准要求学生能认识化学变化的本质特征是有新物质生成,并伴有能量转化,能从内因与外因、量变与质变等方面较全面分析物质的化学变化,关注化学变化中的能量转化,能依据物质及其变化的信息建构模型,建立解决复杂化学问题的思维框架。了解化学反应中能量转化所遵循的规律,赞赏运用化学反应原理对科学技术和人类社会文明所起的重要作用,发展化学学科核心素养。能进行反应焓变的简单计算,能定量分析化学变化的热效应,能用热化学方程式表示反应中的能量变化,能运用反应焓变合理选择和利用化学反应,能依据化学变化中能量转化的原理,提出利用化学变化实现能量储存和释放的有实用价值的建议。在素养2“变化观念与平衡思想”中要求学生能运用化学计量单位定量分析化学变化及其伴随的能量转化。
盖斯定律是由化学家盖斯于1836年从大量实验中总结出的一条规律:一个化学反应,不管是一步完成的还是分几步完成的,其反应热是相同的。盖斯定律的提出要早于能量守恒定律,是化学热力学的基础,至今仍有广泛的应用,为反应热的研究提供了极大的方便,使一些不易测准或无法测定的化学反应的反应热可以通过盖斯定律推算间接求得。
1 问题的提出
1.1 人教版教材中利用盖斯定律计算化学反应焓变的方法
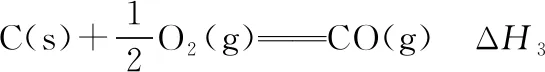
虽然该反应的反应热无法直接测定,但下列两个反应的反应热却可以直接测定:

上述三个反应具有如图1所示关系:
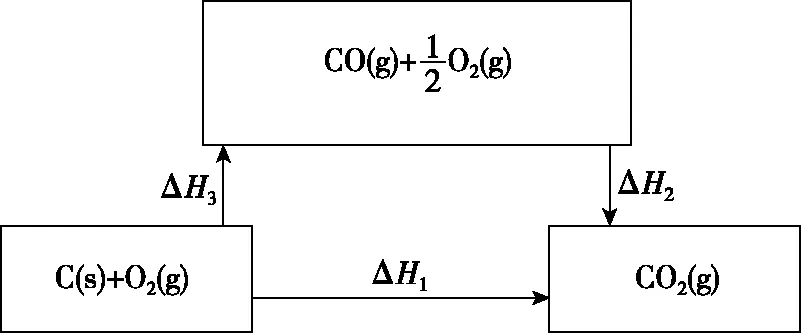
图1
根据盖斯定律,则有:
ΔH1=ΔH2+ΔH3
ΔH3=ΔH1-ΔH2=-393.5 kJ·mol-1- (-283.0 kJ·mol-1)=-110.5 kJ·mol-1
可见,根据盖斯定律,我们可以利用已知反应的反应热来计算未知反应的反应热。若某个反应的化学方程式可由另外几个反应的化学方程式相加减而得到,则该反应的反应热也可以由这几个反应的反应热相加减而得到。我们把这种方法称为“方程式加减法”,在人教版教材给出的例题中也使用了类似的方法。
【例题】焦炭与水蒸气反应、甲烷与水蒸气反应均是工业上制取氢气的重要方法。这两个反应的热化学方程式分别为:



【解析】分析各化学方程式的关系可以得出,将反应①的逆反应与反应②相加,得到反应:

即:

_____________________________________

根据盖斯定律: ΔH=ΔH3+ΔH2=ΔH2-ΔH1=+205.9 kJ·mol-1-131.5 kJ·mol-1=+74.4 kJ·mol-1
1.2 教学过程中出现的主要问题
1.2.1 使用“方程式加减法”时没有交待对方程式如何加减
在使用“方程式加减法”时,没有交待对方程式如何加减,即方程式加减的操作步骤是什么?有什么样的思维模型或流程?对于学生而言,简单的方程式之间的加减,还比较好处理。若是复杂方程式之间的转换、加减,学生就感到无从下手。
1.2.2 在处理例题时为什么要将反应①的逆反应与反应②相加?
既然我们可以对化学方程式像对待数学方程式一样进行加减,为什么还要将反应①首先转化成逆反应然后再与反应②相加?为什么不能直接用反应②减去反应①?如果转化成逆反应是为了便于将不在目标反应中出现的物质消去(即消元法),那么具体的思维模型是什么?
2 问题的讨论
方程式加减法计算化学反应焓变存在两种不同路径:一种是“消元法”,即进行方程式加减时将不在目标反应中出现的物质通过方程式的加减消去;另一种是“目标物质转化法”,即按照目标反应中出现的物质关系对原有的方程式乘以相应的系数进行加减。
【例1】(2022年全国甲卷,28题节选)金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之一是将金红石(TiO2)转化为TiCl4,再进一步还原得到钛。回答下列问题:
(1)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1 000℃ 时反应的热化学方程式及其平衡常数如下:



2.1 利用“消元法”计算化学反应焓变的思维模型



_____________________________________

ΔH=ΔH2-ΔH1=-223 kJ·mol-1

通过上述练习,总结“消元法”计算化学反应焓变的思维模型如图2所示:
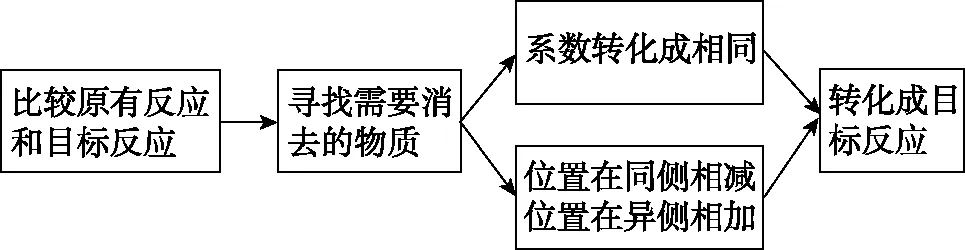
图2 “消元法”计算化学反应焓变的思维模型
2.2 利用“目标物质转化法”计算化学反应焓变的思维模型
对于例1,还可以采用“目标物质转化法”计算化学反应焓变,解析过程如下:

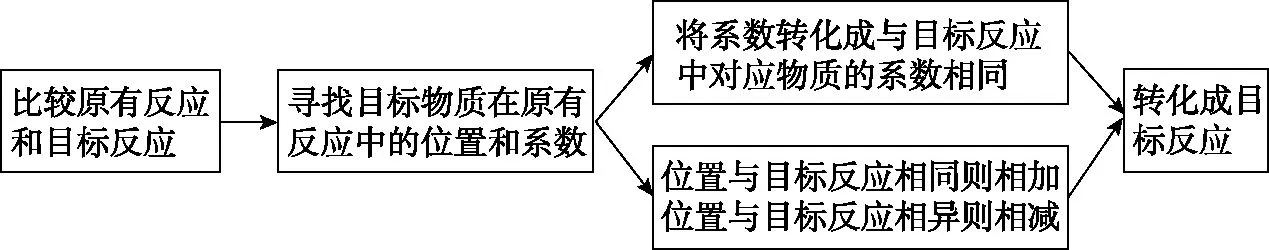
图3 “目标物质转化法”计算化学反应焓变的思维模型
2.3 “消元法”和“目标物质转化法”在计算化学反应焓变时存在的不足
不管是用“消元法”还是用“目标物质转化法”来计算化学反应的焓变,如果原有方程式和目标方程式都比较简单,关系也不复杂,使用起来问题不大。但是如果原有方程式和目标方程式都比较复杂,相互间关系也不简单,不是通过一步计算就能得到目标反应的,利用“消元法”和“目标物质转化法”来计算化学反应焓变过程复杂、思维流程不畅,容易产生错误,而“设未知数求解法”正好大显身手。
3 问题的解决——利用“设未知数求解法”,建构盖斯定律计算化学反应焓变的思维模型
3.1 利用“设未知数求解法”计算化学反应焓变的思维流程
【例2】(2022年全国乙卷,28题节选)油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加以利用。回答下列问题:
(1)已知下列反应的热化学方程式:







3.2 利用“设未知数求解法”计算化学反应焓变的思维模型
利用“设未知数求解法”计算化学反应焓变的整个过程简单,易于操作,不需要对方程式进行加减,只需要设原有的各反应参加的物质的量为一未知数xmol、ymol、zmol等,再根据目标反应中各物质的物质的量列出数学方程(物质在化学方程式的同侧符号为正,物质在化学方程式的异侧符号为负),解出方程,代入数据即可得到目标反应的化学反应焓变。思维模型如图4所示:

图4 利用“设未知数求解法”计算化学反应焓变的思维模型
3.3 利用“设未知数求解法”计算化学反应焓变思维模型的应用
【例3】(2022年湖南卷,16题节选)2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。回答下列问题:
(1)在一定温度下,向体积固定的密闭容器中加入足量的C(s)和1 mol H2O(g),起始压强为0.2 MPa时,发生下列反应生成水煤气:


反应平衡时,H2O(g)的转化率为50%,CO(g)的物质的量为0.1 mol,此时,整个体系________(填“吸收”或“放出”)热量________kJ。
【解析】根据利用“设未知数求解法”计算化学反应焓变的思维模型解题过程如下:


4.则反应热效应=0.3 mol×(+131.4 kJ·mol-1)+0.2 mol×(-41.1 kJ·mol-1)=+31.2 kJ
推出:反应平衡时,H2O(g)的转化率为50%,CO(g)的物质的量为0.1 mol,此时,整个体系吸收热量31.2 kJ。
4 教学反思
方程式加减法计算化学反应焓变,不管是“消元法”还是“目标物质转化法”,都需要对原有的化学方程式进行加减,书写复杂、繁琐,计算过程冗长,在向着目标反应转换过程中易产生错误。而利用“设未知数求解法”计算化学反应焓变的整个过程,最大的优点就在于不需要对化学方程式进行加减,只需要对未知数列方程求解,符合学生的认知过程,正确率有了大幅度的提高。

