牛/猪肺表面活性物质治疗早产儿呼吸窘迫综合征的快速卫生技术评估Δ
郭华,邵云,刘兰兰,任鹏飞,付强,孙楠,周建超,康建,任艳丽(.郑州大学第三附属医院药学部,郑州 45005;.郑州大学第一附属医院药学部,郑州 45005)
呼吸窘迫综合征(respiratory distress syndrome,RDS)是由肺表面活性物质(pulmonary surfactant,PS)缺乏所致,以胎儿出生后不久出现呼吸窘迫并进行性加重为特征的临床综合征,多见于早产儿,PS替代疗法是治疗RDS的重要手段[1]。《2019年欧洲呼吸窘迫综合征管理指南》推荐,RDS患儿应给予动物源性PS制剂(证据质量为高质量,推荐强度为强推荐)[2]。临床常用动物源性PS,分为牛PS和猪PS,两者所含的磷脂、蛋白浓度各不相同,在治疗早产儿RDS时,相关指南并无优先推荐。目前关于牛PS和猪PS治疗早产儿RDS的有效性、安全性和经济性的结论存在争议[3-4]。
卫生技术评估(health technology assessment,HTA)是指对卫生技术的特性、有效性、安全性、经济性和社会适应性进行系统评价,为各层次的决策者(卫生、医保决策者或医药卫生人员等)提供科学信息和循证依据[5]。快速HTA是一种证据合成的方法,迅速获取并分析证据,制作时间短,时效性强。基于此,本研究采用快速HTA方法,对比了牛PS和猪PS治疗早产儿RDS的有效性、安全性和经济性,旨在为临床药物选择和决策提供循证依据。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究对象 本研究纳入的患者为早产儿RDS,均符合《2019年欧洲呼吸窘迫综合征管理指南》[2]中的相关诊断标准。
1.1.2 干预措施 试验组患儿给予牛PS;对照组患儿给予猪PS;两组患儿的用药品种、给药剂量和疗程均不限。
1.1.3 结局指标 结局指标为:(1)有效性指标,包括死亡率、支气管肺发育不良(broncho-pulmonary dysplasia,BPD)发生率、PS再治疗率、新生儿重症监护病房(neo‐natal intensive care unit,NICU)住院时间、血气指标[pH值、血氧分压(partial pressure of oxygen,PO2)、血二氧化碳分压(partial pressure of carbon dioxide,PCO2)]、总有效率。(2)安全性指标,包括漏气综合征(air leak syn‐drome,ALS)发生率、肺出血发生率、动脉导管未闭(patent ductus arteriosus,PDA)发生率、肺外指标[脑室内出血、坏死性小肠结肠炎、早产儿视网膜病变、细菌性败血症、脑室周围白质软化]发生率。(3)经济性指标,包括平均住院费用、平均药品费用、每剂给药成本、平均每剂浪费成本和治疗24 h平均费用。
1.1.4 研究类型 本研究的文献类型包括 HTA报告、系统评价/Meta分析和药物经济学研究。
1.1.5 排除标准 本研究的排除标准为:重复发表的文献,会议摘要,无法获取全文的文献,非中英文文献,个案报道。
1.2 文献检索策略
计算机检索PubMed、Embase、Cochrane Library、中国知网、SinoMed和万方数据,同时检索国内外HTA机构官方网站及相关数据库。英文检索词为“pulmonary surfactant”“respiratory distress syndrome”“systematic review”“meta-analysis”“cost”“economic”“pharmacoeco‐nomics”;中文检索词为“肺表面活性物质”“呼吸窘迫综合征”“系统评价”“荟萃分析”“Meta 分析”“成本”“经济”“费用”。检索时限均为各数据库建库起至2022年2月。采用主题词结合自由词进行检索,同时手工检索纳入研究的参考文献。
1.3 文献筛选和数据提取
由2位研究者独立筛选文献,如遇分歧则通过讨论或咨询第3位研究者解决。提取资料包括纳入研究人群、样本量、干预措施、对照措施、结局指标和结论等。
1.4 文献质量评价
采用国际卫生技术评估组织协会制定的HTA Checklist评价纳入的HTA报告质量[6];采用系统性评价方法学质量评估表(A measurement Tool to Assess Sys‐tematic Reviews,AMSTAR 2)评价纳入的系统评价/Meta分析的质量[7]。由于新生儿的特殊性,无法进行常规的成本效益、成本效果、成本效用分析,故不适合采用卫生经济评估报告标准量表(Consolidated Health Eco‐nomic Evaluation Reporting Standards,CHEERS)评价纳入的经济学研究质量,仅描述各研究的结果。
1.5 数据分析
对纳入研究的结果进行描述性分析。纳入的指标以比值比(odds ratio,OR)、相对危险度(relative risk,RR)、均方差(mean deviation,MD)、95%置信区间(con‐fidence interval,CI)表示。
2 结果
2.1 文献筛选结果
初筛共获得文献396篇,经阅读摘要、标题及全文后,最终纳入13篇文献[8-20],包括1篇HTA报告[8],6篇系统评价/Meta分析[9-14],6 篇药物经济学研究[15-20]。文献筛选流程见图1。
2.2 纳入文献的基本特征和质量评价结果
2.2.1 HTA报告 HTA报告的质量良好。纳入HTA报告的基本特征见表1,质量评价结果见表2。

表1 纳入HTA报告的基本特征

表2 纳入HTA报告的质量评价结果
2.2.2 系统评价/Meta分析 3篇文献的计划书进行提前注册,检索策略全面,且提供了排除文献的清单及理由[10―12];1篇文献没有详细描述发表偏倚情况[9]。3篇文献质量为中等[10-12],2 篇文献质量为低级[13-14],1 篇文献质量为极低级[9]。纳入系统评价/Meta分析的基本特征见表3,质量评价结果见表4。

表3 纳入系统评价/Meta分析的基本特征

表4 纳入系统评价/Meta分析的质量评价结果
2.2.3 药物经济学研究 纳入药物经济学研究的基本特征见表5。
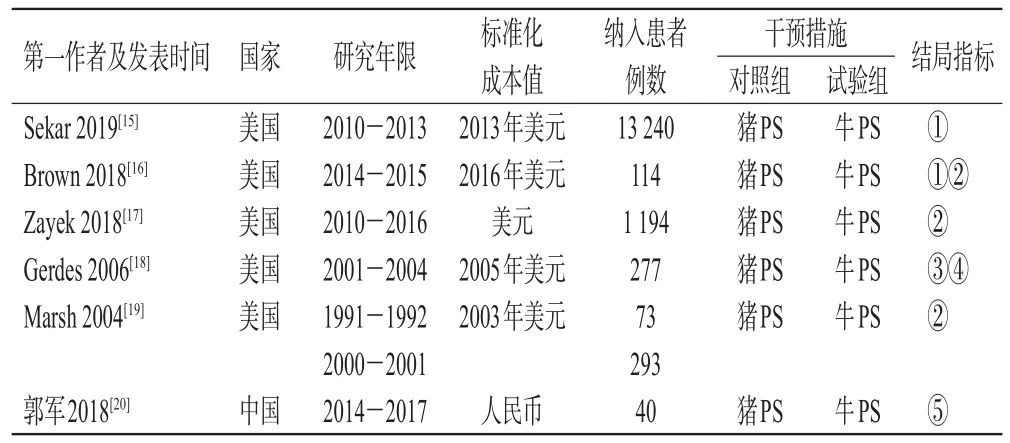
表5 纳入药物经济学研究的基本特征
2.3 有效性与安全性结果评价
2.3.1 死亡率 4项研究报道了死亡率[9,11―13]。3项研究的结果显示,两组患儿的死亡率比较,差异无统计学意义(P>0.05)[9,11,13]。根据死亡时间进行亚组分析的结果显示,两组患儿<28 d的死亡率比较,差异无统计学意义[RR=1.48,95%CI(0.72,3.07),P=0.29];与对照组比较,试验组患儿的出院前死亡率更高[RR=1.44,95%CI(1.04,2.00),P=0.03][12]。
2.3.2 BPD发生率 4项研究报道了BPD发生率[9,11―12,14]。3项研究的结果显示,两组患儿的BPD发生率比较,差异无统计学意义(P>0.05)[9,12,14]。有1项研究认为,对照组患儿的BPD发生率更低[OR=0.717,95%CI(0.542,0.949),P=0.019],该研究中对照组患儿的猪PS初始剂量多为200 mg/kg[11]。
2.3.3 PS再治疗率 2项研究报道了PS再治疗率,结果显示,对照组患儿的PS再治疗率显著低于试验组(P<0.05)[11―12]。
2.3.4 NICU住院时间 1项研究报道了NICU住院时间,结果显示,两组患儿的NICU住院时间比较,差异无统计学意义[MD=-2.977,95%CI(-6.659,0.705),P=0.113][10]。
2.3.5 血气指标 1项研究报道了血气指标,结果显示,与试验组比较,对照组患儿的PCO2显著降低[MD=-1.67,95%CI(-2.92,-0.43),P=0.009],PO2显著升高[MD=3.15,95%CI(1.02,5.28),P=0.004];但两组患儿的pH值比较,差异无统计学意义[MD=0.01,95%CI(-0.01,0.03),P=0.31][14]。
2.3.6 总有效率 1项研究报道了总有效率,结果显示,对照组患儿的总有效率显著高于试验组[OR=2.40,95%CI(1.33,4.32),P=0.004][14]。
2.3.7 ALS发生率 4项研究报道了ALS发生率[9,11-12,14]。3 项研究的结果显示,两组患儿的 ALS 发生率比较,差异无统计学意义(P>0.05)[9,12,14]。1项研究认为,与试验组比较,对照组患儿的ALS发生率更低[OR=0.566,95%CI(0.366,0.876),P=0.01][11]。
2.3.8 肺出血发生率 3项研究报道了肺出血发生率[11―12,14]。2项研究的结果显示,两组患儿的肺出血发生率比较,差异无统计学意义(P>0.05)[12,14]。1项研究认为,试验组患儿的肺出血发生率显著高于对照组[OR=0.369,95%CI(0.143,0.949),P=0.038][11]。
2.3.9 PDA发生率 2项研究报道了PDA发生率,结果显示,对照组患儿的PDA发生率显著低于试验组(P<0.05)[10,12]。
2.3.10 肺外指标发生率 2项研究报道了肺外指标发生率,结果显示,两组患儿肺外指标发生率比较,差异无统计学意义(P>0.05)[10,12]。
2.4 经济学结果评价
2.4.1 平均住院费用 2项研究报道了平均住院费用,结果显示,两组患儿的平均住院费用比较,差异无统计学意义(P>0.05)[15―16]。
2.4.2 平均药品费用 3项研究报道了平均药品费用[16―17,19]。1项研究认为,与试验组比较,对照组患儿能显著节省药品费用[19]。2项研究则认为,与试验组比较,对照组患儿的平均药品费用更高(P<0.05)[16―17]。
2.4.3 每剂给药成本 1项研究报道了每剂给药成本,结果显示,两组患儿的给药时间存在差异,每剂给药成本与给药时间呈正相关,试验组患儿的每剂给药成本高于对照组,但差异无统计学意义(P>0.05)[18]。
2.4.4 平均每剂浪费成本 1项研究报道了平均每剂浪费成本,结果显示,试验组患儿的平均每剂浪费成本为337.34美元,显著高于对照组(141.21美元)(P<0.001)[18]。
2.4.5 治疗24 h平均费用 1项研究报道了治疗24 h平均费用,包括药品费用和治疗费用,结果显示,与对照组比较,试验组患儿的费用更低(P<0.05)[20]。
3 讨论
PS是以磷脂和特异性蛋白质为主要成分的混合物质,具有降低肺表面张力,维持肺泡稳定,改善肺气体交换的功能。PS替代疗法已成为全世界早产儿RDS的常规治疗方法,尤其是动物源性PS制剂,可减少气胸发生率,提高生存率[2]。动物源性PS主要来源于牛和猪的肺灌洗液或绞碎的肺组织,不同来源的PS制剂成分、制备工艺均不同,因此临床疗效的差异尚不确定。Singh等[12]研究结果显示,使用牛PS患儿的死亡率以及PDA发生率、PS再治疗率均高于使用猪PS的患儿,这种差异可能与猪PS中磷脂成分较高相关。
本研究结果显示,牛PS与猪PS在治疗早产儿RDS时的死亡率、BPD发生率、ALS发生率、肺出血发生率方面的结论存在争议,可能与纳入研究的时间跨度较大有关。2003年希腊的研究发现,约30%早产儿(胎龄<32周)的母亲在产前使用过激素[21];2017年加拿大的研究发现,超过95%早产儿(胎龄24+0~31+6周)的母亲产前使用过激素[22]。《2019年欧洲呼吸窘迫综合征管理指南》推荐,孕周<32周有早产可能的妊娠期妇女,建议在产前给予1个疗程的糖皮质激素以促进胎肺成熟,降低RDS发生率[2]。由于在不同时期、不同地区,产前糖皮质激素使用的情况差异较大,这可能会造成结局的不同。另外,本研究中,在PS再治疗率、血气指标、总有效率、PDA发生率方面,猪PS较牛PS更有优势,可能与两者的初始剂量不同有关。纳入的原始研究中,猪PS的初始剂量以200 mg/kg居多,而牛PS组的初始剂量均为100 mg/kg。高剂量猪PS可以更长时间地抵抗极早产儿分泌的磷脂酶A2和其他炎症因子造成的水解和损伤[23];且药代动力学数据提示,200 mg/kg的猪PS半衰期更长,可以在较长时间保持活性,降低PS的再治疗率[24]。
综上所述,牛PS治疗早产儿RDS的有效性、安全性和经济性与猪PS相当或劣于猪PS,但其劣势尚不确定是否具有显著的临床意义。本研究的局限性为:(1)影响临床结局的混杂因素较多,如纳入研究的原始文献时间跨度大、患儿胎龄、出生体质量、PS初始用药剂量、给药方式以及结局指标的定义和标准等不同,可能会引入潜在的偏倚。(2)药物经济学研究主要来自美国,研究年限跨度大(1991-2017年),国内市场价格有较大不同,因此结果的参考价值有限。(3)本研究仅纳入中文和英文文献,可能存在文献选择偏倚。故本研究所得结论有待大样本的真实世界研究进一步验证。

