不同种植地糙米萌芽过程中可培养内生真菌菌群的变化研究
严婷婷, 王天圻, 赵 艳
(浙江工商大学食品与生物工程学院,杭州 310018)
发芽糙米,是指脱壳水稻种子即糙米经过消毒后,在水分足量、温度适宜、氧气充足条件下,吸水膨胀发芽到一定程度的制品[1]。萌芽处理不仅可以有效改善糙米食用风味,而且可以提高总酚、谷维素、类黄酮、抗氧化活性、维生素E、大多数氨基酸等功能性成分的含量[2,3]。因此,富含营养物质的发芽糙米越来越受到消费者的欢迎。
水稻种子是发芽糙米的直接原料,也是内生菌的携带者和传播者[4]。内生真菌(endophyfic fungi)是指其生活史的一定阶段或全部阶段定殖在宿主植物体内,而不引起植物发生明显病变的一类真菌总称[5],可提高宿主植物抗旱、抗寒、抗病虫害的能力,并促进宿主生长,也可能产生有毒的代谢产物[6]。Arundhati等[7]从水稻种子中分离到内生真菌Dendryphiella和Cochliobolusmiyabeanusspp。田新莉等[8]从不同种植地的水稻样本中分离出多种内生真菌,主要属于镰刀菌属(Fusarium)、梨孢霉属(Piricularia)、 酵母(Yeast)、青霉属(Penicillium)、曲霉属(Aspergillus)等。Alexander等[9]利用Illumina MiSeq测序技术从水稻种子中检测链格孢属(Alternaria)、Hannaella、Pleosporales等真菌。由于种子中的内生真菌无法采用常规消毒方法去除,理论上在发芽糙米制备的浸泡和萌发阶段可能发生产毒真菌的爆发。因此,研究糙米萌芽过程中内生真菌群落的变化对保障发芽糙米的食用安全具有重要意义。
目前对于糙米产制的工艺改进和营养增效方面的研究报道较多[10-12],关于发芽糙米产制过程中的内生真菌变化的研究鲜见报道。本实验通过分析糙米萌芽过程中内生真菌类群的变化,比较研究了种植地域和萌发加工过程对糙米中内生真菌群落分布的影响,以期为糙米的加工处理、合理利用与风险规避提供新思路。
1 材料和方法
1.1 实验材料
实验所用材料来源于2018年从海南省和浙江省富阳市种植地收获的粳稻品种日本晴,收获种子自然晾干后,4 ℃保存备用。
1.2 实验仪器
PRX-80C型和PRX-600B型智能人工气候箱,PCR仪T100TM Thermal Cyeler,电泳仪DYCZ-21,凝胶成像系统,漩涡混合器GL-88B。
1.3 糙米萌发、消毒
根据糙米萌芽产制的几个阶段将实验材料分成原糙米组、浸泡组、萌发组、干燥组、消毒组,分别进行内生真菌的分离,每组各选取150粒种子作为样品。
原糙米组:选取相对饱满无明显病变的稻米研磨脱壳并表面消毒后进行内生真菌的分离。
浸泡组:将表面消毒后的种子置于无菌水中,30 ℃培养箱浸泡24 h。
萌发组:将浸泡过的糙米均摊在经消毒处理的铺有2层滤纸的平皿上,加5 mL的无菌水,于30 ℃的黑暗培养箱中持续发芽24 h。每24 h补充1 mL无菌水,保持滤纸湿润。
干燥组:按照上述方法萌发后,用无菌水清洗3遍后放入烘箱,50 ℃干燥6 h。
消毒组:按照上述方法干燥后进行再次表面消毒进行内生真菌的分离。
样品表面消毒:按照参考文献[13]对样品进行表面消毒。用无菌水冲洗种子5次,接着分别用70%乙醇浸泡3 min、5%次氯酸钠浸泡5 min、70%乙醇清洗30 s,最后用无菌水冲洗6次。取最后1次清洗液100 μL涂布在PDA培养基上,28 ℃培养7 d,作为检验种子表面彻底消毒的对照。如果对照培养基没有菌长出,说明表面消毒彻底。
1.4 内生真菌分离方法
根据文献[14],将表面消毒的样品均摊到经消毒处理的含有滤纸的平板上,然后用无菌的镊子掰成2段,切面朝下半埋于PDA培养基中,在28 ℃的恒温培养箱中培养6~10 d,待组织块周围长出的菌丝体后,在无菌条件下挑取菌丝接到新的PDA培养基上纯化、编号、保藏。
1.5 内生真菌的分子鉴定
将纯化后的真菌续接到新的PDA固体培养基上,在28 ℃培养7 d。在无菌条件下,刮取足量的平板上的菌丝体到研钵中,用液氮充分研磨,然后采用CTAB法提取菌体DNA[15],采用ITS1(5’-TCCGTAGGTGAACCTGCGG-3’)和ITS4(5’-TCCTCCGCTTATTGATATGC-3’)引物进行PCR扩增[16],扩增片段约550 bp。PCR反应体系采用50 μL反应体系:10×PCR buffer (含Mg2+) 5 μL,5 μmol/L上、下游引物各1 μL,DNA模板3 μL,2.5 mmol/L dNTP 4 μL;rTaq酶 1 μL;补ddH2O至50 μL。PCR扩增条件:94 ℃保持5 min;32个循环(94 ℃ 45 s;54 ℃ 30 s;72 ℃ 90 s);72 ℃保持10 min。PCR产物用1.0%琼脂糖凝胶电泳检测合格后,送由生工生物工程(上海)股份有限公司进行测序。测序结果与GenBank中已知菌株的ITS rDNA序列进行用Blast比对,相似度大于97%的为同属,大于99%的为同种。最后根据形态学鉴定结果和分子生物学鉴定结果确定分离菌株的分类地位。
1.6 数据处理与分析
参考文献[17,18],将糙米内生真菌的分离率( isolation rate,IR)、分离频率(isolation frequency,IF)、margalef丰富度指数、Shannon-Wiener指数、均匀度指数及Sorenson相似性指数(Cs)进行统计,分析内生真菌的多样性及分布特征。分离率用于衡量样品中内生真菌的定植丰度和每个组织块受侵染的发生频率[5]。分离频率指某一特定类型真菌的菌株数量占分离培养的内生真菌菌株数量的百分率,可用于判断优势菌群;Shannon-Wiener指数和 Margalef指数被用于分析内生真菌的菌群多样性;均匀度指数用于分析菌群在样品中分布的均匀程度;Sorenson相似性指数用于比较不同样品内生真菌菌群组成的相似程度[18]。
2 结果与分析
2.1 糙米萌芽过程中内生真菌的分离鉴定
根据菌落形态特征将海南和富阳两地的供试糙米样品中分离到内生真菌归为63种(部分菌落形态见图1),经序列鉴定后归为3个纲,6个目,7个科,20个属。其中海南组分离到30株,归为3个纲,5个目,5个科,10个属,包括弯孢菌属(Curvularia)、镰刀菌属(Fusarium)、链格孢属(Alternaria)、枝孢属菌(Cladosporium)、Pleosporales、球黑孢霉属(Nigrospora)、球腔菌属(Phaeosphaeria)、Letendraeahelminthicola、Setophoma、 拟层孔属(Fomitopsis)。富阳组分离到48株内生真菌,归为2个纲,4个目,7个科,16个属,包括弯孢菌属(Curvularia)、球腔菌属(Phaeosphaeria)、Ophiosphaerella、Setophoma、Dendryphiella、双极霉属(Bipolaris)、皮司霉属(Pithomyces)、Edenia、附球菌属(Epicoccum)、小球腔菌属(Leptosphaeria)、黑孢属(Nigrospora)、枝孢属(Cladosporium)、链格孢属(Alternaria)、镰刀菌属(Fusarium)、帚枝霉属(Sarocladium)、葡柄霉(Stemphylium)。分离到的真菌大多是水稻种子中常见的真菌[19-22],但未分离到稻谷储藏过程中经常导致稻谷结块、出糙率低的真菌[23],如黑曲霉(Aspergillusniger)、黄曲霉(Aspergillusflavus)以及产黄青霉(Penicilliumchrysogenum)[24,25]。这表明本次实验选取的稻谷保藏较好。
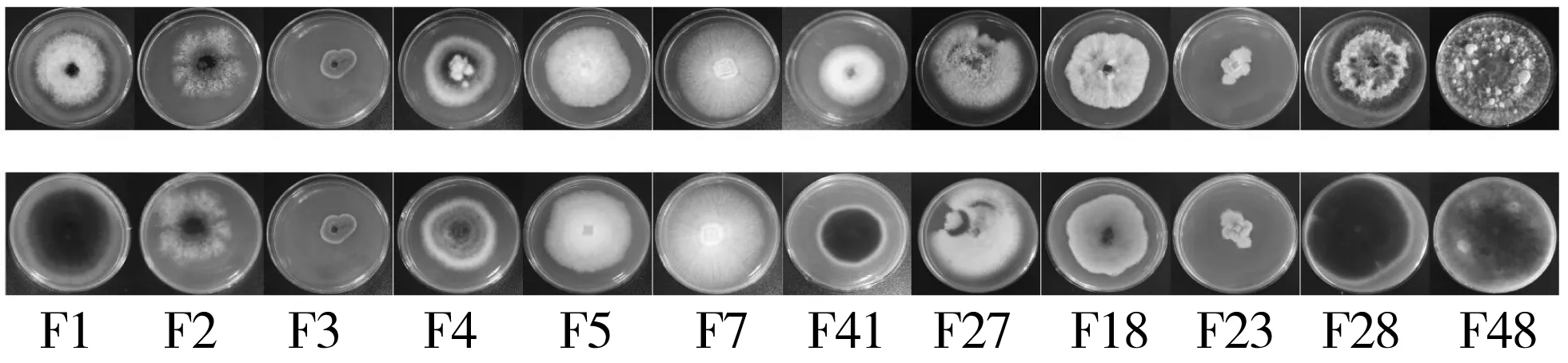
注:上排为菌落正面图,下排为菌落被面图。图1 部分分离的霉菌单菌落图片
2.2 种植地域对糙米内生真菌群落分布的影响
许多研究者发现地域对植物内生菌的群落分布会产生影响[26-28]。因此,本研究对海南省和浙江省富阳市两地的糙米内生真菌群落多样性进行了比较分析。
采用margalef指数、Shannon-Wiener指数和均匀度指数评价糙米萌芽过程中内生真菌的多样性和分布特征。由表1可以看出,富阳组原糙米中分离的内生真菌的margalef指数、Shannon-Wiener指数和均匀指数较海南组更高。说明富阳组的内生真菌多样性组成更为丰富。从分离率上看,富阳种植地的原糙米中内生真菌的分离率(8.42%)要远远高于海南种植地的分离率(1.88%)(表2)。因此,富阳种植地的糙米中内生真菌的丰度更高。

表1 不同种植地的糙米在萌芽过程中的内生真菌多样性指标
按照IF>10%的内生真菌为优势菌[29]。由表2和图2可知:海南组糙米中获得的内生真菌归为10个属,优势菌属为Curvularia、Cladosporium、Alternaria、Fusarium,分离频率分别为26.67%、16.67%、13.33%、16.67%。富阳糙米中获得的内生真菌归为12个属(表2和图2),Fusarium、Epicoccum、Dendryphiella为其优势菌株,分离频率分别为13.86%、14.85%、44.55%。Fusarium为两地的共同优势真菌,Alternaria为海南组特有优势菌株,Dendryphiella和Epicoccum为富阳组特有的优势菌株。因此,不同种植地的内生真菌群落结构不同。
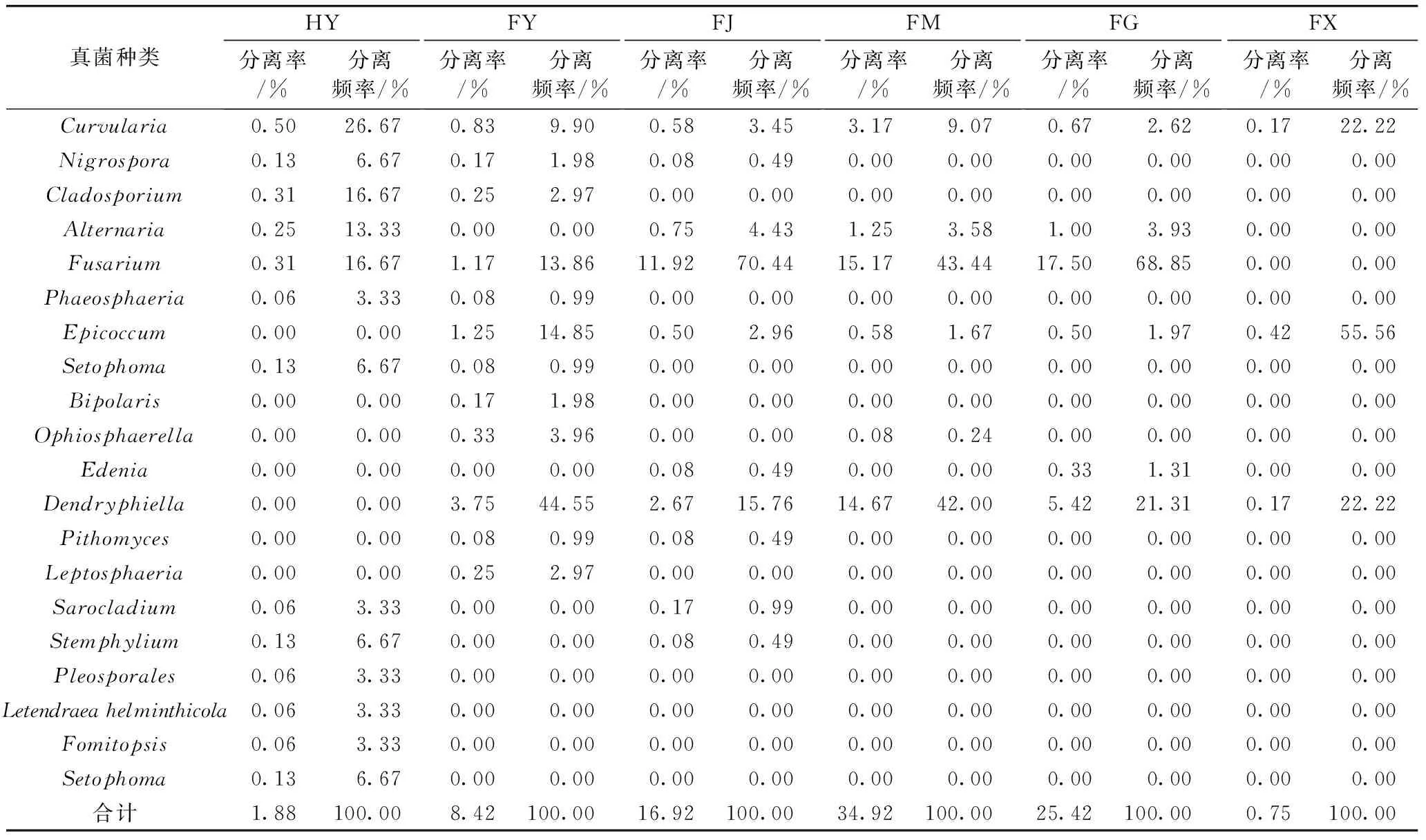
表2 糙米萌芽过程中内生真菌的分离率、分离频率

图2 不同地域不同处理的水稻种子内生真菌菌群属水平组成及相对丰度
2.3 处理方式对糙米萌芽过程中内生真菌群落分布的影响
Adams等[30]发现棉花在种子萌发和幼苗发育过程中,遗传学、形态学和生理学特性的差异会导致定殖的内生菌群结构的差异。已有研究表明,水稻种子含水量的增加,有利于稻谷霉菌的生长[31],当湿度大于 95% 时镰刀菌分生孢子的萌发率较高[32]。因此,以内生菌多样性和丰度更高的富阳产地的糙米为例,研究浸泡、萌发、干燥、消毒等处理方式对糙米萌芽过程中内生真菌群落分布的影响。
从表1可以看出,富阳产地的糙米试样在浸泡处理后内生真菌多样性指标margalef指数、Shannon-Wiener指数和均匀指数均下降,差异显著,而萌发后的差异极为显著。干燥、消毒处理后发现,其内生真菌的margalef指数、Shannon-Wiener指数和均匀指数也较原糙米显著性降低,但较萌发组差异不明显。
由表2 可知,富阳产地糙米经过浸泡、萌发处理,内生真菌总分离率逐渐增加;干燥后虽有所下降但较原糙米仍增加17%;消毒处理可显著降低内生真菌总分离率(较萌发后降低34.17%)。Fusarium、Epicoccum、Dendryphiella为其原糙米中的优势内生真菌(分离频率分别为13.86%、14.85%、44.55%),且在浸泡、萌发、干燥后仍保持优势菌属地位(图2)。浸泡后,未分离到某些相对弱势的内生真菌如Nigrospora、Letendraeahelminthicola、Cladosporium、Setophoma。浸泡、萌发、干燥后,Fusarium的分离率相比原糙米组分别增加10.75%、14.00%、16.33%,但Dendryphiella和Epicoccum的分离率变化不显著。消毒处理后,糙米中Fusarium及Dendryphiella的分离率都显著降低,但Epicoccum的分离率变化不明显。不同的处理方式对内生真菌的影响不同。究其原因可能有:不同的处理方式导致环境不能满足某些菌群的定殖需求;宿主体内处于相对优势的菌群Fusarium、Dendryphiella在合适的环境条件下可能产生具有生物活性的次生代谢产物[9,33,34]逐渐占据竞争的绝对优势;宿主与某些菌株建立了互利共生关系。而以上推测尚需更多试验证明。另外,Fusarium可产生脱氧雪腐镰刀菌烯醇、玉米赤霉烯酮等毒素。因此,糙米浸泡、萌发、干燥处理存在固有优势内生真菌甚至是有毒真菌爆发的可能性,消毒处理能有效减少内生真菌的分离率。
由表3可知,富阳组浸泡与原糙米及萌发组的内生真菌之间相似性为中等相似;干燥组与原糙米组的内生真菌的相似性为中等不相似,与萌发组的内生真菌的相似性为极相似;消毒组与与原糙米的内生真菌的相似性为中等不相似,与干燥组内生真菌之间相似性为中等相似。这进一步表明,不同的处理方式会影响糙米内生真菌菌群的组成。

表3 富阳组糙米萌芽过程中的内生真菌相似性系数
3 结论
本实验从海南省和浙江省富阳市两地的糙米萌芽过程中共获得63株内生真菌,经ITS序列鉴定后归为3个纲,6个目,7个科,20个属,其中Fusarium为两地共有的优势菌属,Alternaria为海南组特有优势菌株,Dendryphiella和Epicoccum为富阳组特有的优势菌株,不同种植地糙米内生真菌菌群多样性和群落结构不同。浸泡、萌发、干燥后处理后内生真菌群落多样性降低,但内生真菌的分离率尤其是固有优势内生真菌Fusarium的分离率增加显著,存在内生真菌甚至是病原菌爆发的可能性,消毒处理可有效减少样品中内生真菌的积累。本研究为糙米的加工处理、合理利用与风险规避提供新思路。

