超声心动图对房间隔缺损合并肺动脉高压术后的早期评价
岳超 厦门大学附属第一医院超声影像科 (福建 厦门 361001)
内容提要: 目的:应用超声心动图观察房间隔缺损(ASD)合并肺动脉高压(PH)患者行房间隔修补术后的早期疗效,分析超声心动图指标对其评估的应用价值。方法:选择ASD合并PH患者32例,所有患者均行房间隔修补手术。应用超声心动图测量患者术前(术前组)、术后1周内(术后组)的左右室舒张末期内径(LVEDD、RVEDD)、左右室舒张末期左右径(LVEDT、RVEDT),并计算其比值(LVEDT/RVEDT)。测量左房内径(LAD)、左室舒张末期容积(LVEDV)、左室射血分数(LVEF)、肺动脉主干内径(MPAD)、呼气末下腔静脉最大内径(IVCmax)。应用频谱多普勒测量三尖瓣反流峰值压差(PTr),并计算肺动脉收缩压(PASP)。比较两组间各指标变化,分析手术前后心脏结构、肺动脉压力及血流动力学变化特点。结果:术后组右室结构相关指标:RVEDD、RVEDT较术前组明显减小,LVEDT/RVEDT大于术前组(P<0.01)。两组间左心结构相关指标:LAD、LVEDD、LVEDT、LVEDV差异无统计学意义(P>0.05)。两组间LVEF、MPAD、IVCmax差异无统计学意义(P>0.05)。术后组肺动脉压相关指标:PTr、PASP较术前组明显减低(P<0.01)。结论:超声心动图能评估ASD合并PH患者行房间隔修补术后心脏结构及肺动脉压力的早期变化,为临床提供可靠的诊疗依据。
先天性心脏病(CHD)是先天异常最常见的原因,每1000名活产中大约有8名患有CHD,其中ASD是CHD最常见的病因之一[1,2]。由于医疗条件受限、ASD患者临床症状不明显,部分患者往往在体检或其他诊疗活动中发现,确诊时已经过较长的病程,此时经常合并PH。本研究应用超声心动图对ASD合并PH患者房间隔修补术前、术后心脏结构及肺动脉压力变化进行分析,探讨其在手术决策及观察手术早期效果中的应用价值。
1.资料与方法
1.1 临床资料
选择2016年11月~2021年5月在本院诊断ASD合并PH,PASP≥40mmHg,并行房间隔修补术的患者32例,分为术前组及术后组,其中男性10例,女性22例,年龄18~71岁,平均(45.25±15.17)岁。上述患者房间隔缺损最大直径为(34.83±8.28)mm,包含13例中央型房缺、13例下腔型房缺、4例上腔型房缺、1例原发孔型房缺、1例冠状静脉窦型房缺,其中3例合并右上肺静脉异位引流。31例患者心房水平左向右分流,1例患者心房水平双向分流。2例患者术前剧烈活动后口唇轻微发绀,余患者无明显症状或偶感胸闷。所有患者均不合并高血压、糖尿病、肾病、肺部其他疾病等。
1.2 方法
采用PHILIPS EPIQ 7C、iE Elite彩色多普勒超声诊断仪,S5-1探头,频率1~5MHz。术前多切面观察测量患者ASD最大直径并应用彩色多普勒观察心房水平分流方向。患者取左侧卧位,于胸骨旁左室长轴切面,应用M型超声测量患者术前及术后左室舒张末期内径(Left ventricular end-diastolic diameter,LVEDD)、右室舒张末期内径(Right ventricular end-diastolic diameter,RVEDD)、左房内径(Left atrial diameter,LAD)、左室舒张末期容积(Left ventricular enddiastolic volume,LVEDV)、左室射血分数(Left ventricular ejection fraction,LVEF);于心尖四腔心切面测量患者术前及术后左室舒张末期左右径(Left ventricular end-diastolic transverse diameters,LVEDT)、右室舒张末期左右径(Right ventricular end-diastolic transverse diameters,RVEDT),并计算其比值(LVEDT/RVEDT);于胸骨旁大动脉短轴切面测量舒张末期肺动脉主干内径(Main pulmonary artery diameter,MPAD);于剑突下腔静脉长轴切面测量呼气末下腔静脉距右房入口2cm处最大内径(Maximum inferior vena cava diameter,IVCmax)。应用连续多普勒测量合并三尖瓣反流者的三尖瓣反流峰值压差(Tricuspid regurgitation pressure gradient,PTr)。根据下腔静脉内径及深吸气时塌陷率估测右房压[3],正常情况下,IVCmax≤21mm、深吸气时塌陷率>50%,右房压估算为3mmHg,当出现一项异常或两项均异常时,右房压分别估算为8mmHg、15mmHg。计算肺动脉收缩压(Pulmonary systolic pressure,PASP),计算方法为:PASP=PTr+右房压。
1.3 统计学分析
使用SPSS 20.0统计分析软件进行统计学处理,各项计量资料均经正态性检验,用±s表示,两组间采用t检验进行比较,P<0.05认为差异有统计学意义,P<0.01时认为有显著性差异。
2.结果
2.1 两组间心脏结构相关指标测量值比较
术后组右室结构相关指标:RVEDD、RVEDT较术前组明显减小,差异显著(P<0.01),LVEDT/RVEDT大于术前组,差异显著(P<0.01)。两组间左心结构相关指标:LAD、LVEDD、LVEDT、LVEDV差异无统计学意义(P>0.05)。两组间LVEF、MPAD、IVCmax差异无统计学意义(P>0.05),见表1、图1、图2。

图1. 术前,四腔心切面显示右室增大

图2. 术后,四腔心切面显示右室回缩
表1. 两组间心脏结构相关指标测量值比较(±s)

表1. 两组间心脏结构相关指标测量值比较(±s)
注:与术前组比较,*P<0.01
组别 术前组 术后组n 32 32 LAD(mm) 36.54±7.45 33.47±7.05 LVEDD(mm) 39.96±5.33 41.30±4.15 RVEDD(mm) 38.27±5.90 26.05±6.25*LVEDT(mm) 34.59±6.36 35.18±4.36 RVEDT(mm) 47.49±6.31 35.52±5.89*LVEDT/RVEDT 0.75±0.23 1.00±0.13*LVEDV(mL) 72.64±23.49 76.03±20.29 LVEF(%) 63.58±4.70 62.05±5.86 MPAD(mm) 35.26±8.78 32.24±8.15 IVCmax(mm) 17.77±2.78 17.26±2.46
2.2 两组间肺动脉压相关指标测量值比较
32例患者术前均合并三尖瓣反流,27例患者术后合并三尖瓣反流,5例患者术后三尖瓣反流消失。术后组PTr、PASP较术前组明显减低,差异显著(P<0.01),见表2。
表2. 两组多普勒超声相关指标测量值比较(±s)
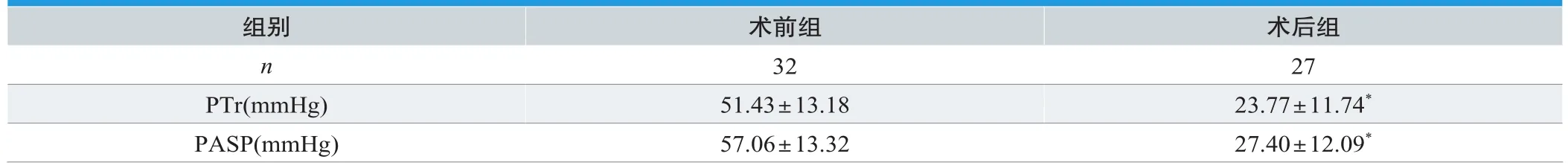
表2. 两组多普勒超声相关指标测量值比较(±s)
注:与术前组比较,*P<0.01
组别术前组 术后组n 32 27 PTr(mmHg) 51.43±13.18 23.77±11.74*PASP(mmHg) 57.06±13.32 27.40±12.09*
本研究结果表明,所有患者术前右室均明显增大,术后30例患者右室明显回缩,接近正常值。约1/3患者术前左室存在不同程度的减小,术后各相关指标略增加,但无统计学意义。2例患者术前左室收缩功能正常低限,LVEF分别为51%、54.4%,术后LVEF分别为54.9%、61%,余患者左室收缩功能均正常。超过半数患者肺动脉有不同程度的增宽,其术后内径无明显变化。除2例患者房间隔修补后肺动脉压下降不明显(下降幅度<20%),仍合并PH,余患者肺动脉压显著减低,接近正常值。
3.讨论
肺动脉高压是先天性心脏病的常见并发症[4],在体-肺分流的CHD中,过多的血流进入肺循环,引起肺血管不同程度的病理改变,导致继发性PH。为避免发生重度PH,影响患者生活质量及寿命预期,国内外专家一致认为这类患者在儿童期就应尽早手术治疗闭合分流。过去有研究[5]认为先天性心脏病相关肺动脉高压(CHD-PAH)发生的预测因素是年龄、缺损大小、非闭合状态和女性性别。由于心房压力较小,ASD患者心房水平的分流为以舒张期为主的双期低速分流,其对肺血管产生的影响小于室间隔缺损、动脉导管未闭等高速度、高压力分流的CHD,所以ASD发生严重肺血管病变的危险性小于后者。对于未能早期手术并且已经发生PH的ASD患者,评估是否具有手术指征,预测手术效果及预后,为临床提供诊断依据和制定治疗方案显得尤为重要。
肺动脉压力主要取决于肺循环血容量和肺血管阻力。ASD患者心房水平左向右分流导致右心前负荷增加,右房右室增大、进入肺循环血容量增加,当肺血管未发生严重病变时,肺动脉压力升高主要为动力型。随着病情进一步发展,肺血管受到高血流量的影响,将发生一系列的病理变化,主要是远端肺小动脉内膜增殖、中膜增厚、外膜纤维化,并可伴发血管及血管周围炎性浸润,进一步导致血管壁增厚、管腔狭窄、甚至闭塞。同时,滋养血管迂曲增生、肺静脉血管重塑,也参与到PH的形成。此时肺血管将发生不可逆转的病变,肺循环阻力进行性增加,出现阻力型PH,甚至出现艾森门格综合征而失去手术的机会[6,7]。
本研究中30例患者术后早期RVEDD及RVEDT均较术前明显减小,增大的右室明显回缩,LVDT/RVDT较术前增高,双侧心室左右径大致相等,心脏形态结构接近正常水平。其中5例患者三尖瓣反流消失,余病例PTr及PASP均较术前明显减低(下降>50%),肺动脉压指标降至正常水平。表明这些患者肺血管在术前尚未发生严重的病理改变,肺阻力不高,其肺动脉压力升高主要是容量负荷过重所致,即动力型PH。与ASD容量负荷相关的右室在术后早期即可明显回缩、PASP明显降低,房间隔修补手术有效地逆转了ASD患者心脏结构及血流动力学改变,恢复至接近正常水平。本研究中2例患者右室回缩不明显、PTr及PASP下降不明显(<20%),表明患者肺血管病变严重,术前即存在阻力型PH的情况。这2例患者术前均有剧烈活动后发绀的症状,其中一例患者年龄为18岁,ASD较小,心房水平双向分流。PH指南[7]中指出年轻、缺损小而合并严重PH的患者除了CHD本身的影响外,还可能存在与特发性PH相关的病因。这也表明ASD肺血管病变机制是复杂的,不能单纯依靠缺损大小、肺动脉压力升高程度进行肺血管病变程度的预判,对于有发绀症状、年轻、缺损小、双向分流的ASD合并PH患者应全面评估肺阻力情况,结合更多反映肺阻力的超声心动图[8]及其他影像学指标,并行右心导管检查,进一步评估肺血管病变情况,这与专家共识[6]中提出的CHD-PAH治疗原则是一致的。本研究中这类患者样本量较小,可以收集更多病例进一步研究。
ASD患者心房水平分流以舒张期为主,其分流方向主要取决于左右心房舒张压力差。当ASD合并阻力型PH而右心房舒张压不高时,心房水平分流方向仍为左向右,右房、右室进一步增大,而进入肺循环的血流量却减少,此时经肺静脉回流入左房、左室的血流量亦减少,左房、左室减小。本研究中约1/3患者左室不同程度减小,但术后右室明显回缩、肺动脉压明显下降,说明其术前仍为动力型PH。由此表明不能单纯根据左心房室的大小来判断PH性质,左室减小可能为容量及压力增高的右室压迫室间隔所致。本研究中ASD患者术后早期LAD、LVEDD、LVEDT、LVEDV与术前相比略增加,但无统计学意义,表明ASD患者左心房室结构在心房水平分流闭合后早期不会发生明显变化。MPAD手术前后无明显变化,表明由于肺循环血流量增多引起的肺动脉增宽,术后早期不能恢复至正常水平。
右心导管检查是诊断及判断肺动脉高压性质的金标准,因其有创、价格高等局限性不能作为常规检查应用于临床。超声心动图具有无创、低价、简便易行的优点,广泛应用于临床中,它可以对心脏结构、功能、血流动力学进行整体、综合判断,较准确地评估患者手术前及手术后情况。
本研究结果表明:成年ASD合并PH患者中,大部分为动力型PH,术后早期心脏结构形态及肺动脉压力均可恢复至接近正常水平,此时闭合分流是有益的,应积极手术治疗。超声心动图可以综合判断ASD患者手术前病变情况和手术后恢复情况,为临床诊疗决策提供可靠依据。

