黄芪真武汤对心衰患者神经-体液指标的影响
李亚洲,马瑞,卢东磊
安徽省亳州市蒙城中医院 安徽亳州 233500
慢性心衰(CHF)是多种因素引起对的心脏泵血功能下降引起周围组织缺血缺氧的一组临床综合征。新中国成立以来,特别改革开放后,经济发展迅速,医疗水平明显提高,心血管病存活患者的增加。加之物质水平提高,高脂肪高盐饮食习惯,人口老龄化加剧,促使作为心脏疾病终末期的心衰成为心血管领域常见、棘手的问题。我国约有 1500 万心衰患者,根据中国高血压调查(CHS)研究显示,2012至2015 年,在≥35岁的中国人群中,心衰患病率为1.3%,男性和女性之间患病率相似[1]。
心衰早期治疗理念以“强心、扩管、利尿”为主要模式,包括洋地黄类药物、β受体阻滞剂、利尿剂的使用,主要针对血流动力学改善。随着对心衰认识的深入,心衰的发作与RAAS系统、交感神经系统、脑钠肽系统有密切关系,其治疗方式从改善短期血流动力学状态转变为长期修复性策略,开始重视神经-体液因子分泌的作用,更加侧重于防止和延缓心肌重构,改善心衰患者的中、长期预后[2]。在2018年《中国心衰诊断与治疗指南》强调心衰早筛查、早诊断、早治疗的管理策略,降低心衰住院率和病死率[3]。
中医是中华民族之瑰宝,黄芪真武汤具有补气温阳,活血利水的功能,前期研究显示能减轻CHF临床症状,减轻炎症反应,改善 CHF 患者心脏舒缩功能。本研究进一步的探讨了黄芪真武汤对神经-体液因子的调节作用,为临床使用提供科学的依据。
资料与方法
1 诊断标准
1.1 西医诊断标准 参照2018年《中国心衰诊断与治疗指南》[4]制定:符合心衰症状、体征,如劳力性或夜间阵发性呼吸困难、端坐呼吸、胸腔积液、颈静脉怒张、肝脾肿大、下肢水肿等;高血压、冠心病等心脏病史;左室舒张末期内径增大,LVEF≤50%;心功能分级参照 NYHA 标准。
1.2 中医诊断标准 参照《中药新药临床研究指导原则》[5]主症:心慌、惊悸、咯喘(痰呈泡沫样)、四肢浮肿,怕冷肢寒。次症:烦躁不安、易汗出、面色青灰或白,面唇紫绀,尿少或无伴纳差腹胀,或胸腹水。舌脉:舌淡或胖或边有齿痕,苔白或滑,脉弦或滑或滑数。2项主证+2项次证即可诊断阳虚水泛型心衰。
2 纳入及排除标准
2.1 纳入标准 符合慢性心力衰竭诊断标准;心功能分级Ⅱ~Ⅲ级;符合阳虚水泛证者;年龄40~80岁;无其他脏器系统病变者;取得患者或家属知情同意。
2.2 排除标准 顽固性心力衰竭或心功能I级者;合并严重肺、肝、肾功能不全的患者; 严重精神障碍者;过敏体质或有过敏史者;严重感染或其他疾病急性发作;服用其他药物期间。
3 一般资料
选择2022年1-12月蒙城中医院心血管门诊或住院患者70例。随机按诊病前后分为研究组和对照组各35例。研究组男17例,女18例;年龄45~76岁,平均(58.2±7.8 )岁;病程2~10年,平均(3.4±1.2)年;心功能分级:Ⅱ级16例,Ⅲ级19例。对照组男18例,女17例;年龄44~75岁,平均(59.4±6.9)岁;病程2~12年,平均(3.5±0.9)年;心功能分级:Ⅱ级27例,Ⅲ级18例。2组患者性别、年龄等一般资料比较差异无统计学意义,具有可比性。
4 治疗方法
4.1 对照组 予常规西医治疗:包括诱因祛除、控制原发病、钠水摄入限制、休息为主,严重者吸氧治疗,药物予以沙库巴曲缬沙坦(北京诺华制药有限公司,国药准字J20190001)100mg早晚1片、美托洛尔缓释片(阿斯利康制药有限公司,国药准字J20150044)47.5mg 晨起1片、螺内酯(上海上药信谊药厂有限公司,国药准字H31021273)20mg 晨起1片,期间药物根据血压、心率调整。
4.2 研究组 在对照组基础上加服黄芪真武汤200mL(由本院制剂中心提供,组成:黄芪20g,熟附片6g,白术12g,白芍12g,茯苓12g,生姜6g),早晚1次,8周1疗程。
5 疗效观察
5.1 中医证候学评分 统计治疗前后症状体征积分(气喘、乏力、心悸、气短、浮肿、咳嗽、咯痰、舌苔脉象),主症轻中重分别赋分3、6、9分,次症轻中重赋予1、2、3分,舌苔、脉象分别有则计分3分,无则不计分。
5.2 心脏彩超测定 治疗前后检测2组患者超声心动图并记录左室舒张末期内径(LVED)、左室射血分数(EF值)。
5.3 6min步行实验(6 MWT)。
5.4 神经-体液指标 治疗前后抽取2组患者肘静脉血,采用放射免疫法测定精氨酸加压素(AVP)、脑利钠肽(BNP)、血管紧张素II(AngII)和醛固酮(ALD)。
6 统计学方法
统计学软件统计数据使用SPSS 22.0,计量资料表示为(±s),组间对比采用独立样本t检验,组内对比则采用配对样本t检验。以P<0.05为差异有统计学意义。
结果
1 中医证候积分比较
2组治疗前对比,P=0.607,具有可比性;2组治疗后研究组积分优于对照组,差异有统计学意义(P= 0.019),见表1。
表1 2组患者中医证候积分比较 (±s)

表1 2组患者中医证候积分比较 (±s)
组别 例数 治疗前积分 治疗后积分研究组 35 48.36±4.58 13.52±1.32对照组 35 46.54±4.36 20.36±2.34
2 心脏彩超比较
2组治疗前LVED对比,P=0.342,具有可比性,研究组LVED减小优于对照组,差异有统计学意义(P=0.031);2组治疗前EF值对比,P=0.446,具有可比性,治疗组 EF 提升优于对照组,差异有统计学意义(P=0.007),见表2。
表2 2组患者LVED、EF值比较 (±s)
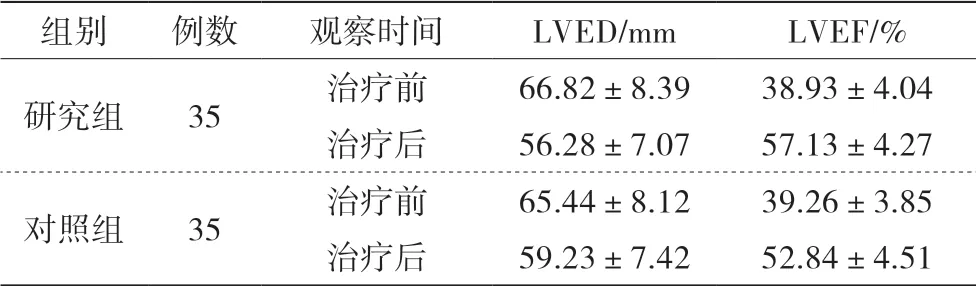
表2 2组患者LVED、EF值比较 (±s)
组别 例数 观察时间 LVED/mm LVEF/%研究组 35 治疗前 66.82±8.39 38.93±4.04治疗后 56.28±7.07 57.13±4.27对照组 35 治疗前 65.44±8.12 39.26±3.85治疗后 59.23±7.42 52.84±4.51
3 6min步行实验比较
2组治疗前6min步行距离对比,P=0.483,具有可比性,研究组步行距离增加优于对照组,差异有统计学意义(P=0.004),见表3。
表3 2组患者6MWT比较(±s)

表3 2组患者6MWT比较(±s)
组别 例数 治疗前距离/m 治疗后积分/m研究组 35 204.5 ± 58.2 404.7 ± 69.5对照组 35 212.5 ± 60.7 361.6 ± 66.3
4 神经-体液指标比较
2组治疗后精氨酸加压素(AVP)、脑利钠肽(BNP)、血管紧张素II(AngII)和醛固酮(ALD)水平均比治疗前下降(P<0.01),治疗后研究组精氨酸加压素(AVP)、脑利钠肽(BNP)、血管紧张素II(AngII)和醛固酮(ALD)水平均低于对照组(P<0.01)。见表4。
表4 2组患者神经-体液指标比较(±s)

表4 2组患者神经-体液指标比较(±s)
组别 例数 观察时间 AVP/ug·L-1 BNP/pg·ml-1 AngII/ng·L-1 ALD/ng·dl-1研究组 35 治疗前 498.4 ± 51.5 281.4±18.8 144.2±12.8 42.5±6.2治疗后 109.7 ± 32.9 97.2±10.8 92.8±10.7 18.6±4.2对照组 35 治疗前 467.3 ± 50.8 269.8±20.6 137.7±11.2 38.3±5.8治疗后 202.3 ± 38.6 110.8±11.4 110.4±11.6 22.4±3.9
讨论
肾素-血管紧张素-醛固酮系统(RAAS)是人体神经内分泌系统的重要组成部分,能够维持水电解质平衡及保证血流动力学稳定[6]。当心衰发作,周围循环血量减少,肾脏供血减少,肾内压力下降,RAAS就会激活,由于a-肾上腺能神经的刺激和AngⅡ增加近曲小管Na+的转运,这样肾脏远曲小管和集合管转运Na+减少,早期这样钠水排出减少,增加灌注。同时AngⅡ收缩肾脏出球小动脉强于入球小动脉,能够维持肾脏压力,保证肾小球滤过率[7]。但是长期心衰,失代偿期RAAS系统被激活以后,AngII大量生产,钠水潴留加之肾脏微血管阻力增加,并醛固酮分泌释放,保钠保水排钾,进一步引起钠水潴留、心脏容量负荷增加,加重心衰,同时ALD与AngII协同增加心脏纤维化、心脏结构性重塑,使心衰患者预后差[8]。总之RAAS激活后一系列物质的产生导致心脏结构、血管内皮、心肌细胞发生异常改变的,称为细胞和组织重构[9]。由此可见,早期RAAS可以起到代偿作用,后期反而加重心衰患者症状,因此抑制RAAS系统过度激活,能够明显改善心衰患者症状及预后[10]。
精氨酸加压素(AVP)在人体下丘脑垂体分泌,主要作用肾脏集合管,促进水的重吸收,减少水和电解质的排出,起到维持血容量的作用[11]。心房牵张受体的调控对于AVP的释放有重要的价值,心脏牵张受体敏感性会在心衰过程中下降,使得血浆中AVP水平升高。心衰早期,AVP起到代偿作用,维持血浆渗透压,但心衰日久,长期的增加会引起游离水的过度吸收,导致血管内容量的增加,将导致心内压力升高和肺淤血以及水肿,进一步加重心衰。因此CHF 患者AVP水平显著升高,是心衰发生的重要因素[12]。
脑钠肽(BNP)合成和分泌的部位主要在左心室,由于心衰病人心脏收缩功能较差,加之外周血管收缩等,左心室内积聚大量血液,左心室舒张末期压力急剧升高,刺激BNP的大量分泌,心衰早期由于各种代偿作用,心室壁压力升高不明显,而后期代偿作用不明显,则BNP血浆含量增高更加明显,由此可以看出 BNP在血浆浓度直接反应出心衰的严重程度[13]。心衰时肾脏利钠肽受体敏感性下降,近曲小管中有一种降解利钠肽的酶(性钠肽酶)降解作用变强,两个方面促使BNP原本具有的利尿作用变得微乎其微[14]。BNP具有抑制交感神经激活,拮抗RAAS,控制精氨酸加压素和内皮素的活性,扩张周围血管,利尿排钠,增加心脏排出量等一系列作用[15]。而对于血压和肾脏功能影响较小。因此BNP在早期能够起到代偿作用,后期对于心衰患者的病情判断和治疗指导、预后预判等具有重要的意义[16]。
心衰属中医学喘证、胸痹、短气、水肿、心悸等病证的范畴。中医认为心气不足是根本,推动无力,气属阳,气虚日久,则心阳虚,心阳不能温煦脾肾之阳,则脾肾阳损。心气虚,血运无力则血瘀,脾肾阳虚,水运失常,则痰饮、水肿内生,这是其主要病理环节[17]。黄芪真武汤中黄芪补肺脾肾之气,同时益卫固表、升阳举陷、利水消肿,既可防外邪侵袭又可补内虚[18];附子归心、脾、肾经,味辛,性大热,补火助阳、回阳救逆,温阳之首药,两药合用为君,补气温阳同用治其本[19]。白术健脾益胃、燥湿利水,加之茯苓健脾渗湿、安神,两药共为臣药,一燥一渗,使水有去处。白芍为佐,养血柔肝、缓急止痛,缓附子燥热、生姜升散;生姜温散水湿,为佐使之用,既可助附子温阳,亦协茯苓、白术祛除水湿。诸药合用,共奏益气温阳、利水消肿之 效[20]。本组资料显示,在西医常规治疗的基础上加用黄芪真武汤治疗CHF后,LVED比西药组减小,LVEF比西药组增加,中医证候学积分比西药组降低,6MWT较西药组增加,均提示了黄芪真武汤能改善患者心功能。进一步的研究显示,研究组治疗后AVP和BNP水平低于西药组,提示了黄芪真武汤具有抗心力衰竭功能;治疗后研究组 AngⅡ和ALD水平低于西药组,证明了黄芪真武汤能对CHF患者RAAS有一定的抑制作用,从而逆转心室重塑,有利于心功能的改善。

