HRCT肺小叶结构改变与原发性肺癌相关性分析初步研究
罗龙贵,曾秀英(抚州市广昌县人民医院,江西 广昌 344900)
研究肺癌的X线表现,不应仅注意肿块本身的形态,还必须观察肿块周围肺野内的一系列改变,邻近肺野的改变和肿块的病变性质有一定的联系,有助于从侧面观察和判断肿块的病理性质[1]。因此,开展在HRCT下对原发性肺癌周围结构的研究,觉得有一定的必要性。
1 资料与方法
1.1 一般资料 选取我院2017至2021年原发性肺癌确诊病例46例作为研究组,其中男30例、女16例;年龄43~85(平均63.6)岁。选取同期肺结核病例46作对照组,其中男35例、女11例;年龄32~75(平均48.3)岁。两组患者在性别、年龄等一般资料比较,差异无显著性(P>0.05),具有可比性。
1.2 纳入与排除标准 纳入标准:(1)符合原发性肺癌(《WHO胸部肿瘤分类(第5版)》)标准;(2)年龄>10岁;(3)资料完整。排除标准:(1)肿瘤合并肺结核;(2)其他肿瘤合并肺转移;(3)心脏、肺部及气管先天畸形并发慢性疾病。
1.3 检查方式 (1)GE otpe680 64层128排螺旋CT机,取仰卧位,屏气状态下自肺尖至膈顶扫描,参数设置如下:准直0.625×128、管电压120 kV、管电流250 mAs,SFOV 400 mm,层厚5 mm,重建间隔5 mm,矩阵512×512,图像重建方式为标准算法及肺算法,扫描时长l~3 s,SFOV l80 mm。(2)影像分析:将所得影像学资料上传至后处理工作站进行MRP重建,重建层厚0.78 mm、重建间隔0.625 mm,并由两位副主任医师及以上级别对图像进行分析及评分,若有意见不统一则由上一级医师评价后达成统一意见。
1.4 临床观察指标 分析两组肺小叶间隔(光滑、粗糙),小叶中心(增大、结节),小叶实质密度的增高或降低(磨玻璃、簇状),小叶结构扭曲的改变,分析肺小叶结构改变与原发性肺癌的相关性。
1.5 统计学处理 本研究中所有数据均使用SPSS 26.0软件进行处理,技术数据如各指标水平以(±s)表示,使用t检验比较组间差异,采用Pearson相关性分析及单因素方差ANOVA分析,P<0.05表示差异有统计学意义。
2 结果
在92例病例中,小叶间隔增厚光滑32例,小叶间隔增厚粗糙22例;小叶中心增大35例,小叶中心结节15例,小叶间隔扭曲19例,小叶实质密度增高35例;在46例肺结核病例中小叶间隔增厚光滑24例,小叶中心结节大33例,小叶间隔扭曲6例,小叶实质簇密度增高影28例。见表1。

表1 肺肿瘤与肺结核数据统计比较
T检验,t=-4.006,肺肿瘤与肺结核两组数据间存在显著性差异(P=0.000,P<0.05)。Pearson相关性系数为0.389**,Sig.(双尾)(P=0.000,P<0.05)。见表2。
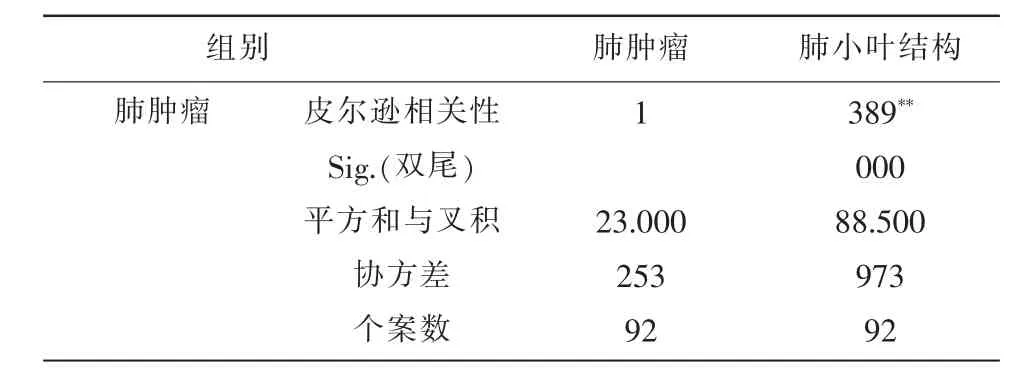
表2 肺肿瘤与肺小叶结构改变相关性
一元线性回归ANOVAaF=16.0,系数aB=0.039,t=4.0,肺肿瘤及肺结核在肺小叶结构上存在显著性(P=0.000,P<0.05)。见表3。肿瘤的大小与小叶中心增大及小叶实质密度增高有明显相关性;小叶间隔增厚与小叶中心结节增大,小叶实质密度增高之间有明显相关(P<0.05)。
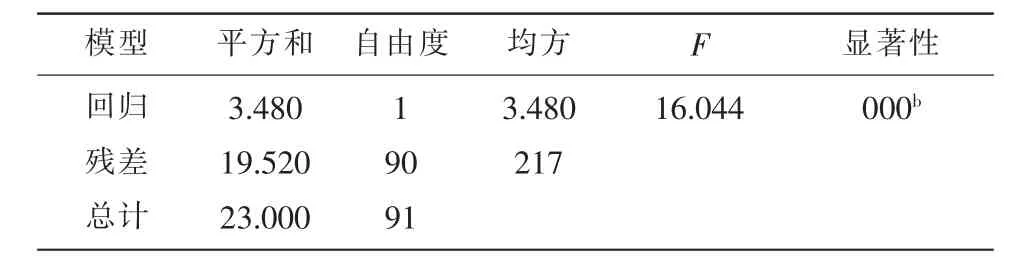
表3 肺肿瘤及肺结核在肺小叶结构的相关性ANOVAa
3 讨论
肺小叶作为肺组织的最小的单位,它的结构改变就意味着肺部存在着早期的疾病。由于肿瘤周围环境非常复杂,目前国内大多数学者的研究都集中于肺结节的分析,而对肿瘤周围环境及结构研究分析相对比较少[2-9]。细胞的病理变化,必然会引起组织的结构变化,而组织的结构变化是影像诊断的基础[10];那么不管肿瘤是发生在小叶中心还是小叶周围间质,必然会引起小叶结构的改变。
HRCT采用薄层扫描,高分辨的算法及重建,大大降低了扫描层面内的部分容积效应,明显提高了空间分辨率,能在肺小叶水平上显示肺部的微细结构,达到几乎能显示与人体标本相似的形态学改变,在显示肺小叶间隔增厚有很大优势,对不同程度的小叶间隔增厚均显示清晰[11]。肺部HRCT的异常表现经常看见下面几个方面:(1)线状影和网状致密影。表现为小叶间隔增厚,蜂窝、小叶内间质增厚。(2)多发结节或结节样致密影,可表现为间质性结节、气腔结节。(3)实质致密影,可比性为实变和磨玻璃影。(4)含气囊性病变。(5)肺衰减减低[12];分析肿瘤周围的小叶结构的改变,可以从另一个方面了解肿瘤的早期病理改变与肺小叶结构改变之间的相互关系,从而更好地提高影像对肿瘤的早期认识。本研究发现,肺结核小叶结构改变较肺肿瘤明显,国内学者研究发现[13-14]肺间质改变为主的肺结核CT征象有明显的特点,当中心介质出现异常时,支气管血管会出现增粗、模糊,伴有细支气管壁增厚;当周围间质出现异常时,会构成小叶间隔,主要表现为小叶中心结节、小叶间隔线、胸膜下线或许与肺结核的炎性浸润及感染方式有关,肿瘤周围小叶间隔增厚与肿瘤的大小及年龄无关,磨玻璃结节密度腺癌也可以看到小叶间隔的增厚。小叶间隔增厚可以表现为不均匀性光滑增厚,也可以表现为结节状增厚,小叶中心可见增大,邻近肺小叶实质可见纯磨玻璃密度影;肺小叶间隔增厚的病理基础是肿瘤纤维化及浸润,肿瘤细胞,这种纤维化并非既往的陈旧性改变,而是肿瘤造成的纤维增生;周围肺小叶实质看见密度的增高呈磨玻璃影改变,可能与肿瘤在肺泡内的浸润、分泌有关;肿瘤周围的磨玻璃影,病理基础是肺出血,肿瘤匍匐浸润或炎症,无特异性[15]。
通过研究发现肿瘤表现为磨玻璃结节时,结节邻近的小叶间隔增厚,肺实质无明显异常,这种现象或许与肿瘤早期伏壁性生长则是以肺结构作为支架,并且经由淋巴道及小气道采取直接浸润形式,自一个肺小叶逐渐扩展至另一肺小叶,而支气管则可仍旧保持在畅通的状态[16]。可能当肿瘤早期仅限于一个肺小叶,邻近肺小叶结构的小叶间隔与其形成间质框架,与其相邻一侧小叶间隔浸润,间隔内的肺静脉及淋巴管渗出,增厚。国内研究发现恶性肿瘤中存在丰富的新生血管生成[17],国外最新研究证实肿瘤周围同样存在肿瘤新生血管形成,肿瘤侵入与其相邻的肺实质前沿[18]。研究中发现早期肺结核的小叶间隔增厚,多表现为光滑均匀性增粗,多个小叶中心可见气腔结节,肺小叶实质呈簇状改变,考虑病灶多为气道播散。国内学者研究发现急住血行播散性肺结核和肺血行转移癌小叶间隔异常主要表现为呈结节状和串珠状改变,支气管播散性肺结核主要表现为小叶核心结节和分支状影(即树芽征)[19]。
随着HRCT及MRP对肺小叶结构改变的影像与病理性相关性进一步的研究,国内U-HRCT(超高分辨CT)研究发现,U-HRCT在诊断COVID-19较C-HRCT有优势,特别是在显示病灶关键细节方面,以帮助放射科医师精准评估磨玻璃病灶的内部结构[20];国外最近研究发现HSR CT(高空间分CT,HSRCT扫描仪具有0.25 mm的探测器元件,最大平面内空间分辨率为0.15 mm)有可能缩小传统CT与组织学检查之间的差距,更好地显示继发性肺小叶和各种病理的体内变化,增加的空间分辨率,允许更准确地观察更精细的解剖结构,并更好地评估终末气道和结节磨玻璃不透明度与实性成分[21]能够对结节末端或远端细支气管的精细形态特征的准确评估[22]。
本研究通过HRCT特征性初步探讨包括肺小叶实质以及腺泡在内的肺小叶结构的影像改变发现肺小叶结构改变与原发性肺癌存在着一定的正相关性,初步认为肺小叶间隔,小叶中心,小叶实质可以作为小叶结构改变的参考指标,对肿瘤的发生方式(中心性,周围性)和肿瘤的早期侵犯方式(血液,淋巴)进行分析,或许能够提供一些参考。本研究目前还存在着很许多不足,有不够详尽与完美,相信随着螺旋CT的长足发展,影像超微结构改变与病理之间的相关分析研究将更加明白。

