氯钌酸铵一步法制备钌粉研究
龚斯宇,刘秉国,2,3,刘 鹏,张 婷,宇文超,董希志,董恩华
(1.昆明理工大学 冶金与能源工程学院,云南 昆明 650093; 2.非常规冶金省部共建教育部重点实验室,云南 昆明 650093; 3.复杂有色金属清洁利用国家重点实验室,云南 昆明 650093)
0 引 言
钌(Ru)是稀贵金属中的一种,Ru粉是制备钌靶材、高纯钌化合物等材料的关键原材料之一[1],钌靶是计算机硬盘记忆材料和超大规模半导体集成电路晶圆制造中薄膜材料的关键原料,其质量主要受Ru粉的纯度和性质影响[2-4],行业标准《制备钌靶用钌粉》规定硬盘和集成电路行业用Ru粉纯度须满足大于等于3N5[5-6].随着电子元器件的发展,对金属靶材的需求量猛增,对Ru粉的需求量也急剧增大[1],但受原材料限制,国内高端钌系靶材仍严重依赖进口,要想保持技术竞争力,就必须通过技术创新改善Ru粉品质,提升钌系靶材性能[7-8].
目前国内外制备高纯Ru粉以化学法为主,其原理是将含Ru物料中的Ru氧化为具有较高蒸气压的RuO4,经蒸馏处理将Ru与杂质阳离子分离,再采用铵盐沉淀、煅烧和还原处理上一步得到的Ru,分离Ru与杂质阴离子,并制得高纯Ru粉.值得一提的是,煅烧分解、氢气还原是制备高纯Ru粉不可或缺的重要工序.永井燈文等[9-10]将NP进行煅烧、氢还原处理,得到4N级高纯Ru粉,但Ru粉大多呈不规则形状.YOON等[11]采用市售普通Ru粉(杂质金属含量较多)为原料制备得到RuOCl3晶体,经煅烧、热还原处理后得到5N级Ru粉,可用于制备溅射靶材.目前,我国Ru粉的制备相对较少,金川公司将制得的RuCl3经煅烧、氢还原得到Ru粉,该Ru粉的纯度在99.0%~99.95%之间,未达到高纯Ru粉的标准[12].贵研铂业将NP进行三温度段煅烧、氢气还原、球磨,得到高纯度(4N)Ru粉[13-14],然而,多温度段煅烧和球磨工序均会导致增加生产周期和成本.李红梅等[15]将NP经800 ℃煅烧6 h,得到钌氧化物并在750 ℃通氢还原 30 min,制得纯度为99.95%的近球形Ru粉.综上可知,我国常规煅烧制备得到的高纯Ru粉在纯度上满足Ru系靶材要求,但因多温度段煅烧、氢还原和球磨等工序,存在工艺复杂冗长等问题.针对上述问题,探索一种加热NP制备Ru粉新工艺迫在眉睫,有学者提出一种微波一步法制备高纯Ru粉的方法[16],该方法是在保护性环境中,将NP微波加热到分解温度后保温一段时间,在该温度下,NP实现了热分解自还原为金属Ru粉.为了推进NP热分解自还原一步法的工业化应用进程,深刻揭示NP的受热分解机理,并优化NP受热分解制备Ru粉的工艺条件具有重要意义.
TG-MS[17]是一种联用分析技术,在同一次测量中,通过TG-DTA技术检测样品的重量变化与热效应,同时利用MS鉴别和定量分析体系受热逸出的挥发性气体组分.有助于更精确地研究反应进程,推断反应机理.
本研究采用TG-MS技术研究NP在保护气氛中的热分解机理,并利用GSL-1600X型管式炉进行煅烧NP试验,以NP的分解率为重要指标,分析煅烧温度、煅烧时间和物料量对分解率的影响,最后在单因素研究的基础上,进行正交优化分解工艺条件,以期为NP热分解一步法制备Ru粉工艺的条件优化及后续研究提供指导.
1 试验部分
1.1 试验原料
NP购买自贵研资源易门有限公司,经ICP测得其Ru≥30.34%,检测结果见表1.对其进行SEM和EDS表征,得到NP的低倍SEM和EDS图谱(见图1).根据图1可知,NP的微观形貌主要呈现不规则的片块状,粒径约在0.1~10 μm之间.由EDS图谱可知,NR主要由Ru、Cl和N三种元素组成,伴随少量的O元素,这可能是由于NP在空气中被氧化.

表1 NR化学成分(质量分数)
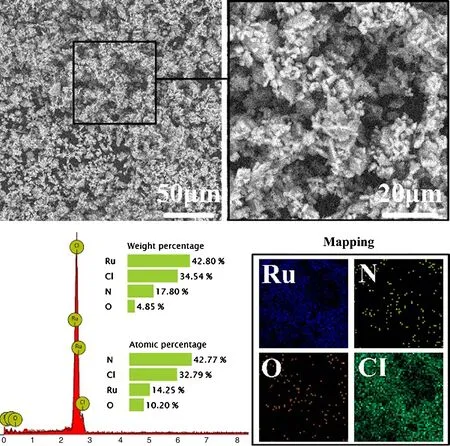
图1 NP的SEM和EDS图谱Fig.1 SEM & EDS patterns of NP
1.2 试验仪器及设备
1.2.1 试验仪器
TG-MS分析采用日本理学Thermo plus EV2型热重-质谱联用分析仪.样品质量为9.4 mg,温度范围为30~500 ℃,升温速率为10 ℃/min,气氛(Ar)流速为300 mL/min.
XRD分析采用UltimalV型转靶X射线衍射仪(XRD),辐射源为Cu-Ka 靶(λ=0.154 06 nm),管电压40 kV,管电流40 mA,扫描速度10(°)/min,扫描区间10°~90°.
SEM分析采用Phenom-World 型扫描电镜,加速电压为15 kV.
1.2.2 试验设备
加热试验采用合肥科晶材料技术有限公司生产的GSL-1600X型管式炉,样品质量范围为20~50 g,温度范围为30~500 ℃,升温速率为 10 ℃/min,通入Ar,且流速为300 mL/min.
1.3 NP分解率的计算
NP的分解率计算公式如(1):
(1)
式中:γ-物料的分解率,%;M0-物料的初始质量,g;M-物料的最终质量,g;Wt-物料理论失重率,%.
2 结果与讨论
2.1 TG-MS实验
2.1.1 TG实验
如图2所示为保护气氛(Ar)中,NP以10 ℃/min的升温速率升温至500℃的TG、DTG和DTA曲线.由TG曲线和DTA曲线可知,NP的热分解分两步进行:第一阶段发生在300~363 ℃之间,对应DTA曲线上的吸热峰,表明该分解反应是一个吸热反应;第二阶段发生在363~420 ℃左右,对应DTA曲线上的吸热峰也说明第二阶段分解反应是一个吸热反应.根据DTG曲线可知,第二阶段的分解反应速率更快,且在372 ℃左右有最大分解速率.根据TG曲线可知,NP热分解结束后物料的剩余质量约为33% (理论值为31%),两者基本吻合.
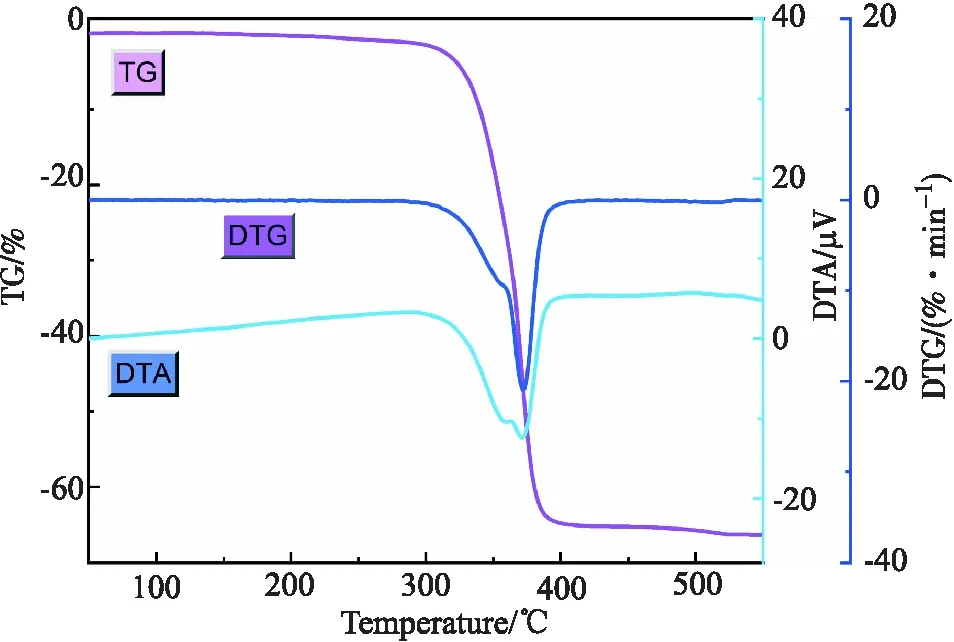
图2 NP在10 ℃/min下的热重曲线Fig.2 TG curves of NP at 10 ℃/min
2.1.2 MS实验
根据以上热重分析可知,NP热分解过程可分两步进行.分解反应的起始温度点为300 ℃,温度分段点为363 ℃,终止温度点为420 ℃.为确定NP不同阶段释放的气体种类,开展质谱定性分析实验[17].图3为NP以10 ℃/min的升温速率在Ar气氛中的MS图谱.由该图谱可知,NP第一步热分解主要发生在300~363 ℃之间,并释放NH3和HCl气体;NP第二步热分解主要在363~420 ℃之间进行,该过程中释放的气体主要为N2和HCl气体.
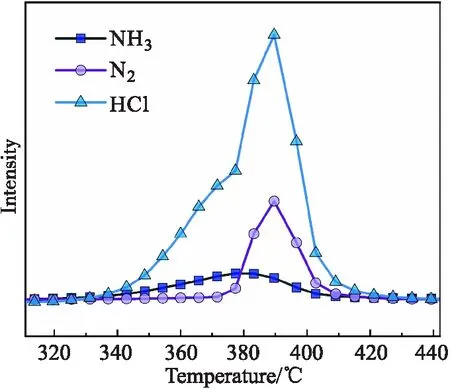
图3 NP热分解质谱图谱 (10℃/min)Fig.3 Mass spectrometry pattern of thermal decomposition of NP at 10℃/min
2.1.3 363℃和 420℃下的产物XRD表征
为了进一步确定NR不同热分解阶段的固体产物为何种物质,本研究用方舟坩埚盛装50 g NR物料后置于管式炉中,并往管式炉中通入一定流速的Ar气以排尽空气,分别在363 ℃和420 ℃下保温90 min后随炉冷却,然后取出冷却物料进行XRD表征分析.其XRD图谱见图4.图4(a)为室温下NP的XRD图谱,该XRD图谱为NP原始XRD图谱.图4(b)和图4(c)是NP在363 ℃和 420 ℃ 下保温 90 min后所得固体产物的XRD图谱.
图4(b)为NP升温至363 ℃、保温90 min所得第一段热分解产物的XRD图谱,图4(b)与标准图谱对比未确定该物质.由于NP第一段热分解释放出 NH3和HCl气体,第二段热分解生成N2和HCl气体,故推断第一段分解的产物为一种新的含Ru化合物[18-19],将其化学简式命为(NH3)xRuyClz,通过分析NP的TG-MS,可知其第一阶段质量的损失量和释放气体的成分,再利用质量守恒定律理论计算,得到第一阶段热分解产物的化学简式为(NH3)4Ru3Cl12.当温度升至 420 ℃时,产物XRD图谱如图5(c)所示,此时Ru的图谱与Ru的标准XRD图谱吻合,表明NP在该温度下已经完全分解.
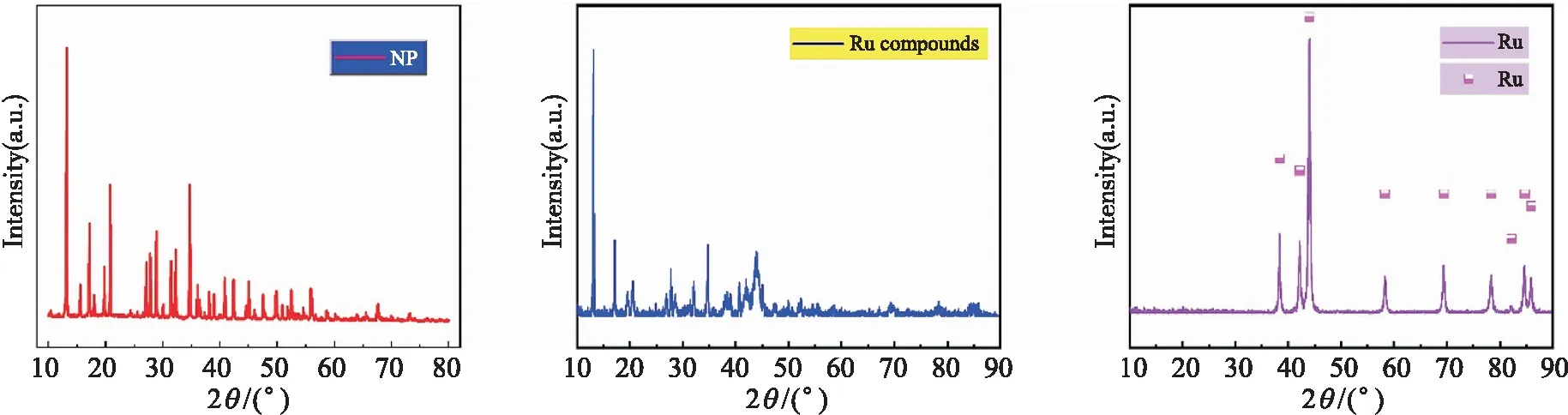
(a) 25 ℃ (b) 363 ℃ (c) 420 ℃
2.2 NP的热分解机理
结合上述TG-MS分析,确定了NP在300~363 ℃之间的热分解产物为含Ru的新化合物,同时释放出NH3和HCl气体;NP在363~420 ℃之间的热分解反应产物为单质Ru、N2和HCl气体[20].这是因为随着温度升高到300 ℃,NP受热分解,在高温环境中,NH4+转化为NH3和H+[21],其中NH3一部分随分解释放,另一部分则和分解固体产物结合形成含Ru中间产物,H+则和Cl-结合生成HCl气体,经计算得到含Ru中间产物的化学简式为(NH3)4Ru3Cl12,因此将第一阶段的反应方程式写为:
3(NH4)2RuCl6→(NH3)4Ru3Cl12+6HCl↑+2NH3↑
(2)
当反应温度到达363 ℃后,释放的NH3凭借自身的还原性将Ru中间产物还原为单质Ru,而NH3则与Ru(Ⅳ)发生氧化反应生成N2,解离的H+和Cl-结合生成HCl气体,故将第二阶段的反应方程式写为:
(NH3)4Ru3Cl12→3Ru+2N2↑+12HCl↑
(3)
2.3 热分解产物表征
收集TG实验剩余物质用XRD和SEM分析表征其物相和微观组织及成分,得到NP热分解产物XRD图谱(图5)与SEM和EDS图谱(图6).如图5所示,NP热分解产物的物相组成为单质Ru,说明NP完全转化为单质Ru.图6表明NP在保护气(Ar)中完成了热分解自还原过程,即NP受热分解过程中产生的NH3作为还原剂将Ru(Ⅳ)的化合物还原为零价Ru,证实了一步法工艺的可行性.同时还可看出,NP在受热分解过程中由于在高温下煅烧并释放出气体,导致产物的片块状特征削弱,出现了团絮状结构,同时粒径更加均匀、细化.
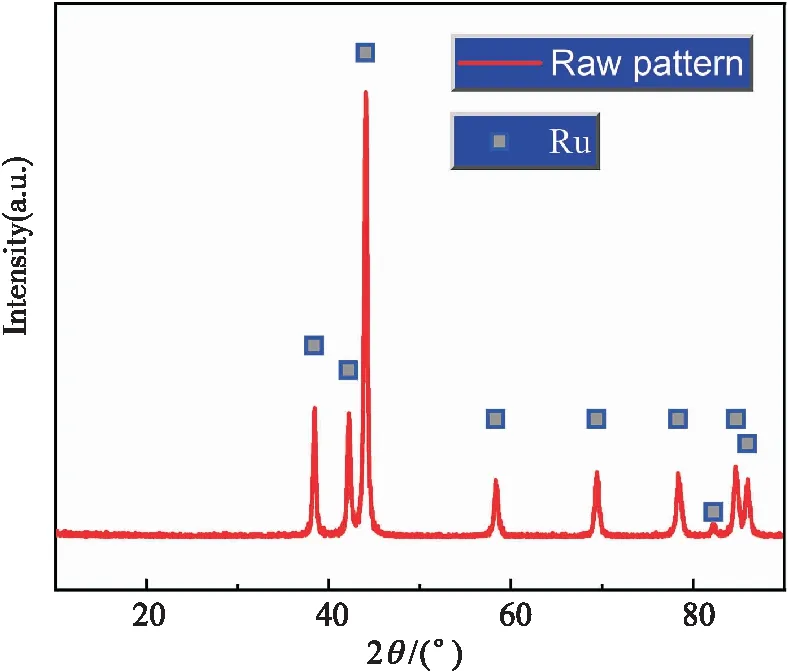
图5 热分解产物的XRD图谱 Fig.5 XRD pattern of decomposition residues
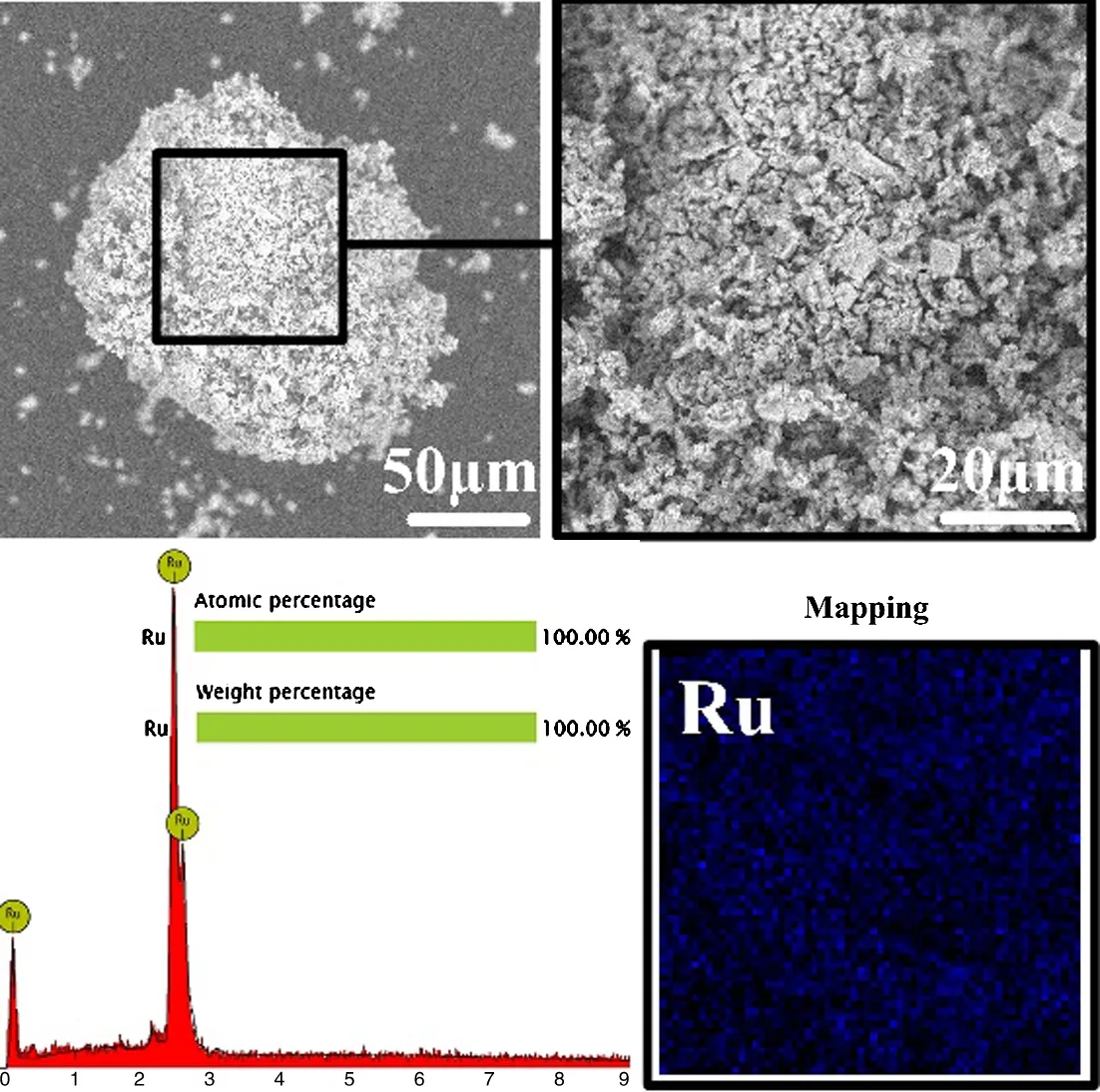
图6 热分解产物的SEM和EDS图谱Fig.6 SEM & EDS patterns of decomposition residues
2.4 单因素实验
根据NP热分解TG/DTG曲线分析,进行初步的条件探索试验,选定对NP热分解影响较大的煅烧温度、煅烧时间和物料量作为实验的三个影响因素开展单因素实验,考察这三个因素对NP分解率的影响[22].称取一定质量的物料平铺在方舟刚玉坩埚中,置于密闭的管式炉中,启动加热程序之前先以一定的流速通入Ar以排净炉腔内的空气,确保管内为无氧环境后,点击开关按钮启动加热程序,并持续通入Ar,直到煅烧阶段结束、物料冷却至室温时停止通气.
2.4.1 煅烧温度的影响
煅烧温度对NP的分解率有显著影响.为了探究煅烧温度对热分解还原阶段NP分解率的作用规律,在350~500 ℃范围内以50 ℃的温度梯度设置了四个保温温度,物料分别在不同保温温度下保温 90 min,以保证热分解反应充分进行.为了单独研究煅烧温度对NP分解率的影响,采用了单因素方法进行条件试验,如物料量50 g,保温时间90 min.用刚玉坩埚盛装50 g NP物料在保护性气氛中以10 ℃/min的升温速率升温到不同温度点(350 ℃、400 ℃、450 ℃和500 ℃)并保温90 min,随后关掉电源结束加热,待热分解产物随炉冷却后取出,称量剩余质量,计算分解率,考察煅烧温度对分解率的影响,图7表示了煅烧温度与NP分解率的关系.
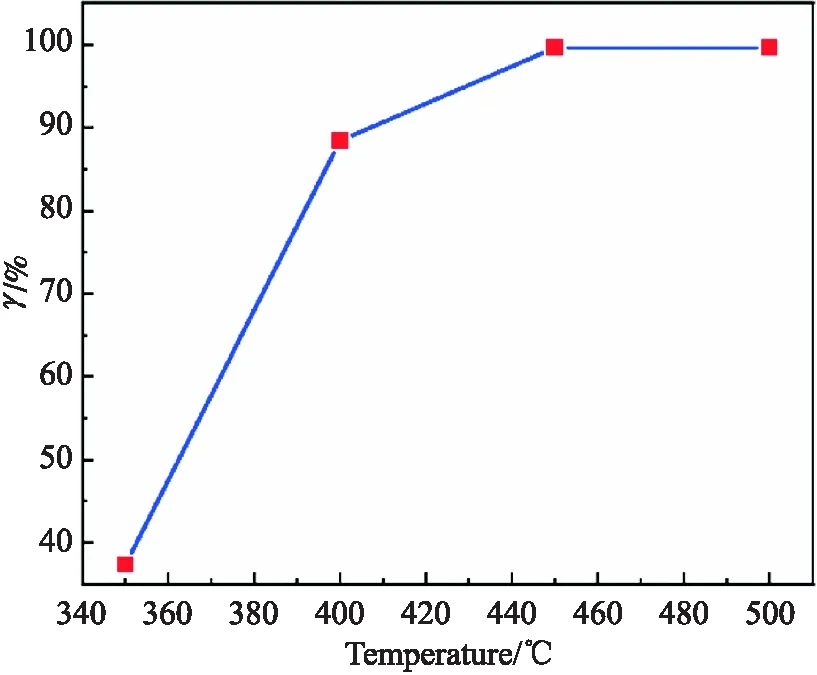
图7 煅烧温度对分解率的影响Fig.7 Influence of calcination temperature on decomposition rate
NP是一种无机化合物,由分子和离子组成,相互之间的作用力主要依靠共价键、离子键和氢键及分子间作用力,如N—H键、H—Cl键和Ru—Cl键.当温度较低时,物质的动能较小,物质间的相互碰撞频率低.所以,从图7中可以看出,当温度升高到300 ℃左右时,NP的分解率仍然处于较低水平,这时NP才开始转化成含Ru中间产物并释放出NH3和HCl气体,在该过程中伴随着N—H键的断裂和H—Cl键的形成.并且在450 ℃之前,NP的分解率随温度升高显著提高,450 ℃之后,分解率基本保持在100%左右,此时NP完全分解还原为Ru单质,这一变化趋势可以解释为:当温度持续升高到363 ℃时,含Ru中间产物开始被NH3还原为单质Ru,并释放出N2和HCl气体,在这个过程中涉及到Ru—Cl键、N—H键的断裂以及N—N键和H—Cl键的形成.随着温度升高到450 ℃,含Ru中间产物完全分解为Ru单质,由于继续升温至500 ℃会造成更高的能耗,因此,选择450 ℃为NP的最佳煅烧温度.
2.4.2 煅烧时间的影响
影响NP分解率最重要的一个阶段就是受热分解阶段,在这一阶段,物料内部发生了复杂的化学变化,单质Ru就是在这一阶段产生的.在热分解还原阶段,有两个主要因素值得探究,一个是煅烧温度,另一个就是煅烧时间.NP在热分解过程中有两个损失的主要途径,一个是随温度升高释放出挥发性气体,一个是发生氧化还原反应后生成单质Ru.本试验将物料(50 g NP)置于管式炉中,在惰性气氛中以10 ℃/min的升温速率升温到 450 ℃ 并保温不同时长(60 min,70 min,80 min和90 min),结束加热后待热分解产物随炉冷却后取出,称量剩余质量,计算分解率,以探究煅烧时间对分解率的影响,如图8所示,结果表明,最佳时间为90 min.
图8表示了热分解煅烧时间对NP分解率的影响,从图8中可以看出,NP的分解率与煅烧时间呈正相关关系,当煅烧时间低于70 min时,NP的分解率随煅烧时间延长增涨幅度更大,而在物料煅烧70 min后,物料分解率增涨幅度的走向开始趋于平缓,说明NP在保温到70 min前发生的热分解反应较为激烈,而在 70 min 后分解反应的激烈程度较之前有所缓和,最终在90 min时已经彻底完成热分解反应,NP分解完全.如果继续增加反应时间不仅增加了能耗,还增加了单质Ru被氧化的风险,所以,最佳的煅烧时间应该为90 min.
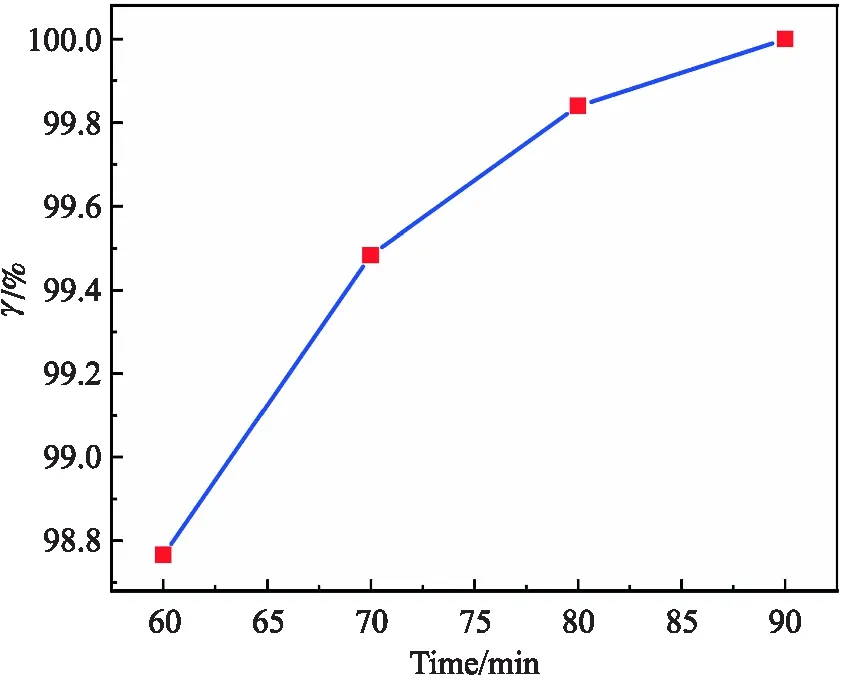
图8 煅烧时间对分解率的影响Fig.8 Influence of calcination time on decomposition rate
2.4.3 物料量的影响
影响NP分解率的另一个重要影响因素是物料量.为了探究物料量对热分解还原阶段NP分解率的影响,在20~50 g范围内按照10 g的质量梯度取20 g、30 g、40 g和 50 g NP分别置于管式炉中,让不同量的物料在450 ℃下保温 90 min,以保证充分发生热分解反应.为了单独研究物料量对NP分解率的影响,采用了单因素方法进行条件试验,如保温温度450 ℃,保温时间90 min.用相同的刚玉坩埚盛装不同物料量(20 g、30 g、40 g 和 50 g)NP,在保护性气氛中以 10 ℃/min 的升温速率升温到 450 ℃,并保温90 min,随后关掉电源结束加热,结束加热后待热分解产物随炉冷却后取出,称量剩余质量,计算分解率,考察煅烧时间对分解率的影响,实验结果如图9所示.
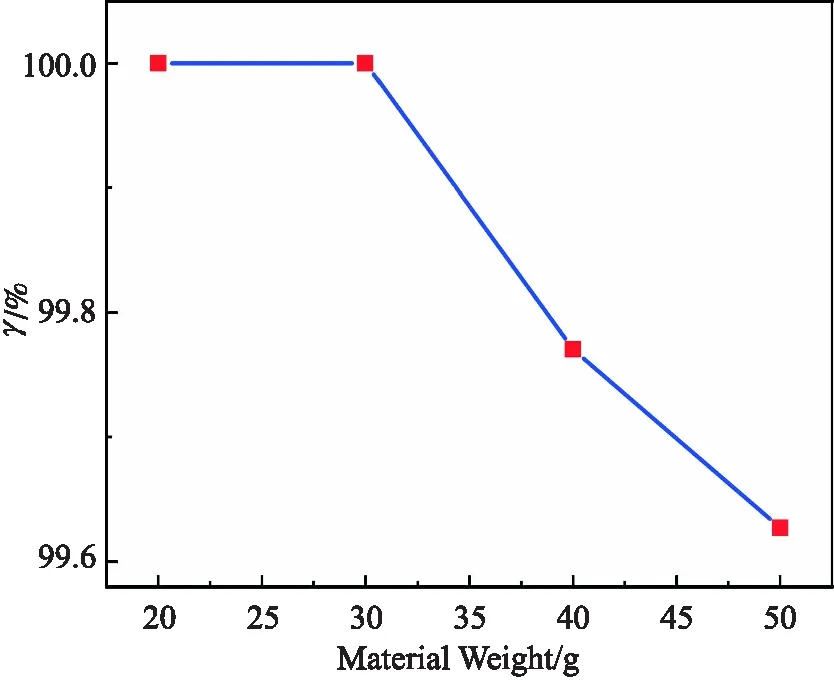
图9 物料量对分解率的影响 Fig.9 Influence of material weighton decomposition rate
图9表示物料量对NP分解率的作用规律,从图9可以看出,NP的分解率随物料量的增加呈现降低的趋势,并且当物料量在30 g左右时NP的分解率达到100%,表明 30 g 物料在 450 ℃ 下保温90 min后,NP基本分解完全.这说明了热源提供的热量满足该条件下NP对热量的需求.当物料量大于30 g时,NP的分解率开始降低,当物料量增大到50 g时,NP的分解率降低到99.6%,表明随着物料量增多,热源提供的能量不足以供NP完全分解,为了保证NP能够完全分解还原,选择最佳物料量为30 g.
2.5 NP热分解正交实验
为探究煅烧温度、煅烧时间和物料量对分解率的非线性影响,基于单因素实验的基础上对上述三个因素进行三因素三水平的正交试验,以期优化NP热分解制备钌粉一步法工艺[23].实验因素水平见表2,NP热分解L9(33)正交试验方案和结果见表3.

表2 正交因素和水平表
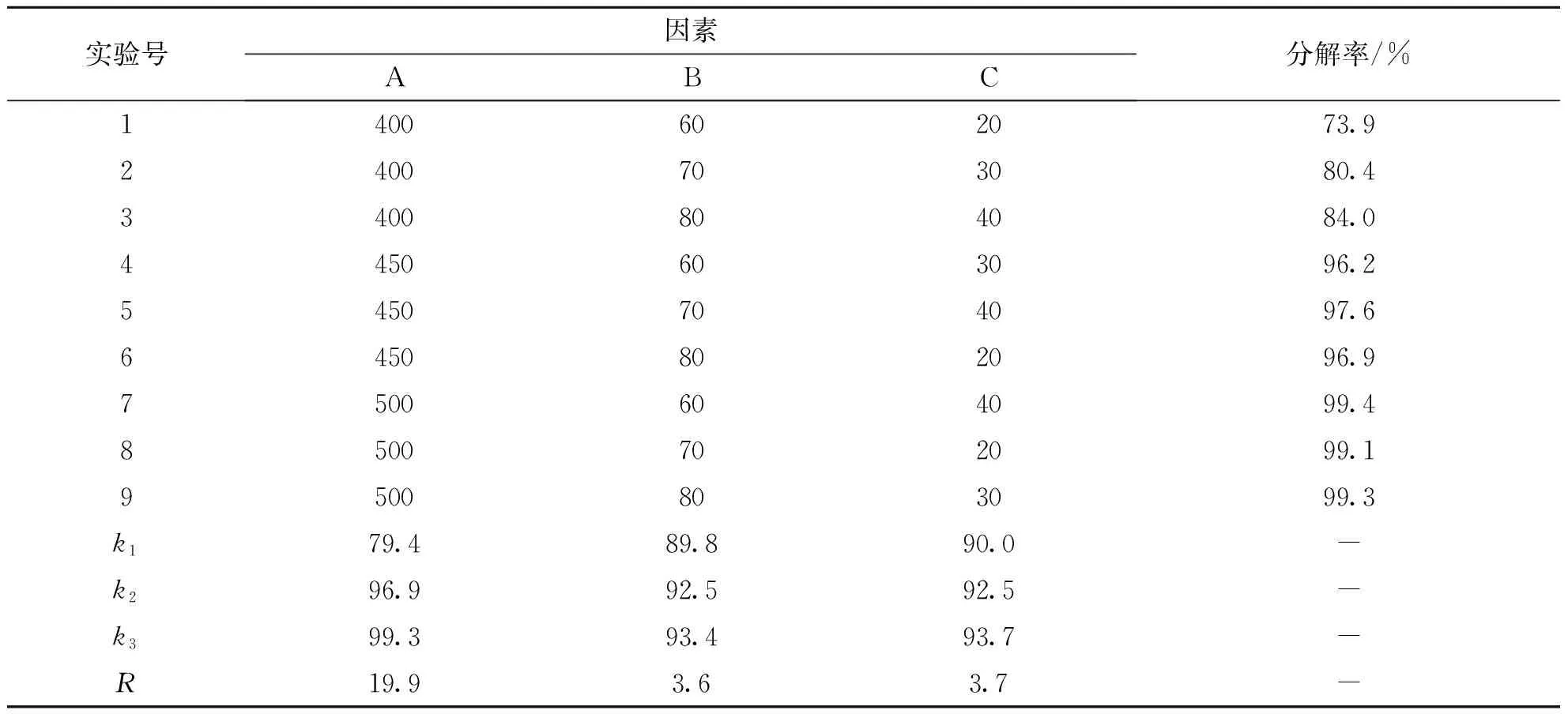
表3 NP热分解工艺优化正交试验结果
从表3中的极差分析可知,A、B和C三个因素对NP分解率影响顺序为A>C>B,优化组合为A3C3B3.说明为了提高NP的分解效率和节约成本,可以适当提高煅烧温度,减少物料量和缩短煅烧时间.取A3C3B3进行验证试验,即煅烧温度500 ℃,煅烧时间80 min,物料量40 g.在优化条件下,进行三次重复试验,测得其分解率分别为99.4%、99.8%和99.7%,其平均分解率为99.6%,NP基本完全分解.
3 结 论
本文利用TG-MS技术探究NP一歩法制备钌粉的机理,并利用单因素法分析了煅烧时间、煅烧温度和物料量对NP分解率的影响,最后使用正交法优化工艺参数,得到如下结论:
1) 对NP进行热重质谱分析,发现其热分解过程分两步进行,对应热分解机理为:第一步热分解的主反应温度区间在300~363 ℃ 之间,主要发生NP受热转化成含Ru中间产物并生成NH3和HCl气体的反应;第二步热分解的主反应温度区间则在363~420 ℃,反应则以含Ru中间产物的自还原为主,即NH3将Ru(Ⅳ)还原为单质钌,释放出N2和HCl气体.
2) 采用XRD与SEM和EDS对NP的热分解产物进行物相分析和微观形貌分析,结果表明NP在保护气氛中实现了热分解自还原生成钌粉一步法.
3) 根据单因素实验和正交试验得出NP的最佳分解工艺为:煅烧温度500 ℃,煅烧时间 80 min,物料量 40 g,此时分解率高达99.6%,NP基本分解完全.

