氟比洛芬酯脂微球注射液的制备及不同蛋黄卵磷脂对其影响
单腾腾,潘海群,禹玉洪*
(1山西医科大学药学院药剂教研室,晋中 030600;2北京鑫开元医药科技有限公司;*通讯作者,E-mail:3024546064@qq.com)
乳剂是两种不相混溶的液体在表面活性剂的作用下,经超声、均质、高速剪切等方法形成的多分散体系[1]。由脂质、卵磷脂等制备得到的纳米级粒子称作脂质微球,也被称作为脂微乳,最早主要用于为不能在正常饮食中获得足够营养物质的患者提供能量,通常脂质微球包括内部油相和油相与水相的界层,疏水性药物可被包裹在内部的油相或油水分界层中。纳米乳具有粒径小,分散均匀度高,药物分散度高,能提高药物生物利用度,或改变药物的组织分布的靶向性;同时对药物透皮吸收也有促进作用[2]。
氟比洛芬酯属于非甾体抗炎药物的一种,有止痛、抗炎以及解热作用,临床应用广泛,其氟比洛芬酯注射液主要用于术后及癌症的镇痛[3]。氟比洛芬酯脂微球注射液则是由脂微球和其所包裹的氟比洛芬酯组成的注射液,脂微球使药物易于跨越细胞膜,加快药物进入细胞内,缩短起效时间[4],且药物进入体内能靶向分布于创伤及肿瘤部位[5],氟比洛芬酯从脂微球中释放出来在羧基酸酶的作用下,迅速水解成氟比洛芬,通过氟比洛芬抑制前列腺素的合成而发挥镇痛作用[6]。
在治疗术后疼痛或因癌症引起的疼痛时,与口服制剂相比,氟比洛芬酯脂微球注射液可避免服用不方便和口服引起的不良反应,并且起效更快。本文对氟比洛芬酯脂微球注射液的处方与生产工艺进行研究,为氟比洛芬酯脂微球注射液的深入研究与临床应用奠定基础,并且能够适应工业化生产。
1 仪器与试药
1.1 仪器与设备
十万分之一电子天平(BSA3202S,赛多利斯公司);百万分之一分析天平(BSA223S,赛多利斯公司);pH计(FE28,梅特勒-托利多公司);磁力搅拌器(RCT basic,IKA);高剪切分散乳化机型号(T25,IKA);纳米均质机(AH-1500,安拓思纳米技术(苏州)有限公司);小型台式低温冷却水循环泵(XHDL-20,广州市予华仪器有限公司);医用离心机(TGA-16A,湖南平凡科技有限公司);紫外可见分光光度计(UV-2600,岛津);纳米粒度电位仪(Zetasizer Nano-ZS90,英国Malvern公司);立式压力蒸汽灭菌器(BXM-3OR,上海博讯实业有限公司医疗设备厂);高效液相色谱仪(S02-HPLC-33,岛津);色谱柱(NX-C18,phenomenex);循环水真空泵(S02-ZSB-10,巩义市予华仪器有限责任公司)。
1.2 试剂与试药
注射用氟比洛芬酯(20210619,南京康满林化工实业有限公司);含量测定用氟比洛芬酯对照品(100696-202003,中国食品药品检定研究院);注射用大豆油(20210901,浙江田雨山药用油有限公司);蛋黄卵磷脂E80 ST(512320-2190001-01,Lipoid);9种蛋黄卵磷脂磷脂酰胆碱含量70%,80%,98%各3种(含量数据由厂家的质量检验报告提供);注射用泊洛沙姆-188(GNE32721B,Basf);注射用甘油(20210306,浙江遂昌惠康药业有限公司);水合磷酸氢二钠(210201,四川金山制药有限公司);枸橼酸(210101,四川金山制药有限公司);注射用油酸(20210801K,南京威尔药业集团股份有限公司);乙腈(色谱纯,上海星可高纯溶剂有限公司);冰乙酸(分析纯,天津市大茂试剂厂);无水乙醇(色谱纯,赛默飞世尔科技(中国)有限公司);水为超纯水。
2 方法与结果
2.1 氟比洛芬酯脂微球注射液的制剂工艺
2.1.1 氟比洛芬酯脂微球注射液的处方筛选 氟比洛芬酯脂微球注射液的油相处方包括氟比洛芬酯、大豆油和油酸。水相处方包括甘油、蛋黄卵磷脂、泊洛沙姆188(F68)、水合磷酸氢二钠和水。油相配制温度以60~70 ℃为宜。蛋黄卵磷脂呈颗粒、黏稠状,磷脂的加入方式通常有两种:分散于水相中或溶解于油相中。本试验采用将蛋黄卵磷脂加于水中制备乳剂。
氟比洛芬酯脂微球注射液的处方优化:采用正交试验法,以卵磷脂用量(1.0,1.2,1.4 g)、初乳pH值(7.0,8.0,9.0)、大豆油加入量(8.0,10.0,12.0 g),泊洛沙姆188用量(0,0.3,0.6 g)为考察因素,每个因素取3个水平,选用L9(34)正交设计试验,以离心稳定常数Ke为评价指标,并对结果进行方差分析。
稳定性常数(Ke)的测定:采用离心-光谱法测定Ke,以评价脂微球的稳定性[7],Ke越小,乳剂越稳定[8]。取乳剂3 ml,4 000 r/min,离心15 min,取下层液50 μl,用水稀释至10 ml,以水为空白,在500 nm处测定吸光度值A,取未离心乳剂50 μl,同法稀释后测定吸光度A0,按Ke=(A0-A)/A0×100%,计算Ke。处方筛选的正交试验结果见表1,方差分析见表2。结果分析:4个因素的主次关系为:C>D>B>A,以极差最小的因素A作为误差来源,进行方差分析,结果因素C、D差异有统计学意义(P<0.05),而因素B不具有统计学意义(P>0.05)。处方筛选的最佳组合为A1B3C2D3,即蛋黄卵磷脂1.0 g,初乳pH=9,大豆油10.0 g,F68加入量0.6 g;次佳组合为A1B3C1D3,即蛋黄卵磷脂1.0 g,初乳pH=9,大豆油8.0 g,F68加入量0.6 g。大豆油加入量C1、C2的Ke均值分别为0.116和0.113,二者的Ke均值仅相差2.586%,考虑到制剂处方尽可能减少辅料用量的原则,故选择A1B3C1D3。
优选确定的制剂处方为氟比洛芬酯1.0%,大豆油8.0%,蛋黄卵磷脂1.0%,泊洛沙姆188 0.6%,浓甘油2.2%,水合磷酸氢二钠0.068%,氢氧化钠调节pH=9,油酸0.4%,加超纯水适量。
2.1.2 氟比洛芬酯脂微球注射液制备工艺研究 采用正交试验法。以剪切时间(6,7,8 min)、均质压力(700,800,900 bar)、均质次数(4,6,8次)为考察因素,每个因素取3个水平,对制备工艺进行研究,选用L9(34)正交设计试验,以粒径(size)、粒度分布、ζ电位(zeta)、离心稳定常数Ke为评价指标,采用综合评分法对脂微球进行评价。总分L=L1+L2+L3+L4,其中,L1为平均粒径,L2=多分散系数(PDI)×100,L3=100+ζ电位值,L4=Ke×100,总分越小,脂微球的稳定性越好。
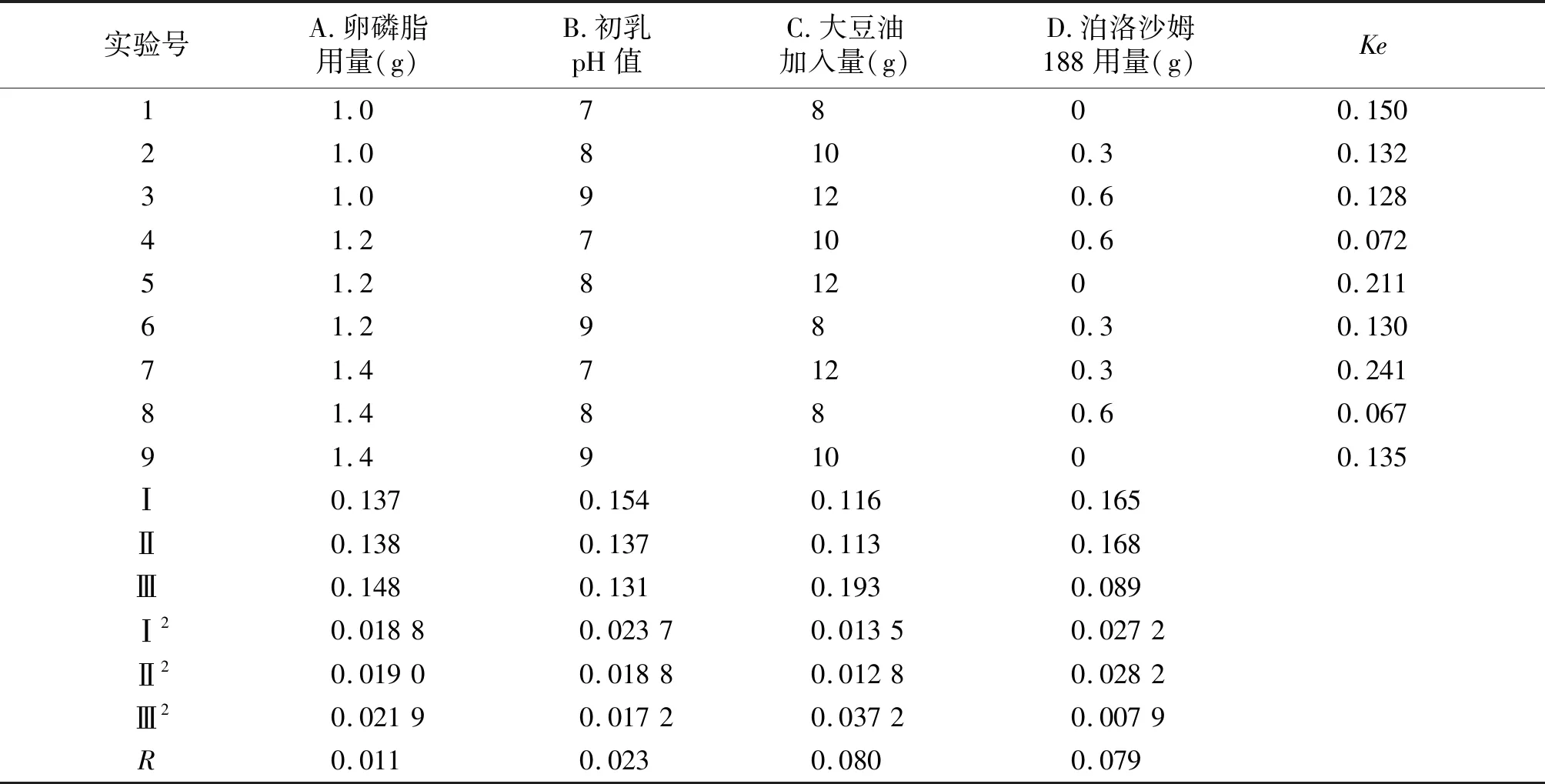
表1 处方筛选的正交试验结果Table 1 Orthogonal test results of prescription screening
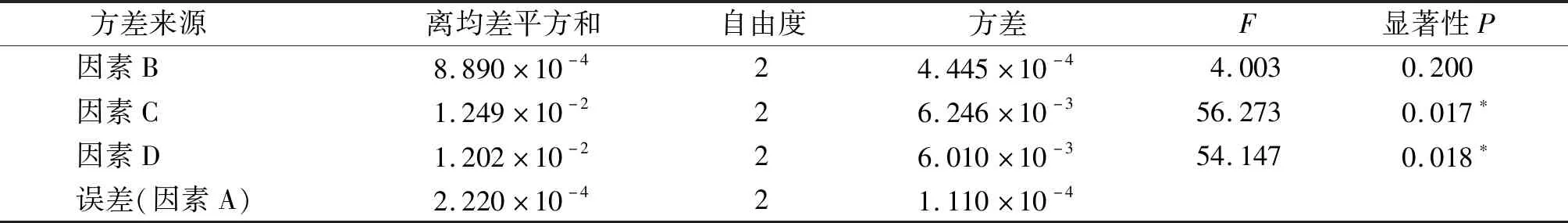
表2 处方筛选的正交试验结果方差分析表Table 2 Analysis of variance of orthogonal test results for prescription screening
使用纳米粒度仪测定粒径(size)、PDI和ζ电位(zeta),测试温度设定为25 ℃,每个样品测量3次。稳定性常数(Ke)的测定:采用离心-光谱法测定Ke,以评价脂微球的稳定性。取乳剂3 ml,4 000 r/min,离心15 min,取下层液50 μl,用水稀释至10 ml,以水为空白,在500 nm处测定吸光度值A,取未离心乳剂50 μl,同法稀释后测定吸光度A0,按Ke=(A0-A)/A0×100%,计算Ke。并对结果进行方差分析。制备工艺正交试验设计与结果见表3,方差分析见表4。结果分析:三个因素的主次关系为:B>A>C,以空白项D作为误差来源,进行方差分析,结果因素B差异有统计学意义(P<0.05),而因素A、C不具有统计学意义(P>0.05)。制备工艺筛选的最佳组合为A3B3C2,即剪切时间8 min,均质压力1 000 bar,均质次数6次。
最终优选的处方及制备工艺为:称取大豆油8 g,加热至65 ℃,称取氟比洛芬酯1 g,油酸0.4 g,置上述大豆油中搅拌使溶解,为油相;取水50 ml加热至65 ℃,加入水合磷酸氢二钠0.068 g,浓甘油2.20 g,泊洛沙姆188 0.6 g,蛋黄卵磷脂1.0 g置上述水中,搅拌使溶解,为水相;将油相与水相混合,13 000 r/min剪切8 min制得初乳,以0.1 mol/L氢氧化钠溶液调节pH值至9,以水定容至100 ml,以高压均质机1 000 bar循环6次将所得初乳进行精制得微乳;以0.65 μm微孔滤膜过滤;分装,充氮,封口,121 ℃湿热灭菌15 min,即得氟比洛芬酯脂微球注射液。

表3 制备工艺正交试验设计与结果Table 3 Design and results of orthogonal test for preparation process

表4 制备工艺筛选的正交试验结果方差分析表Table 4 Analysis of variance of orthogonal test results for preparation process screening
2.1.3 考察高温灭菌对氟比洛芬酯脂微球注射液的影响 将制得的氟比洛芬酯脂微球注射液灌装熔封于5 ml安瓿瓶中,选用热压灭菌的方式进行灭菌,分别采用:①115 ℃灭菌15 min,②115 ℃灭菌30 min,③121 ℃灭菌8 min,④121 ℃灭菌15 min,共4个条件进行灭菌,考察灭菌前后乳剂的外观,测定粒径、电位以及pH变化,结果见表5。结果发现:115 ℃条件下灭菌30 min会有轻微破乳现象,其余灭菌条件所得注射液的差异不大,为保证灭菌效果,灭菌条件选用121 ℃,15 min。
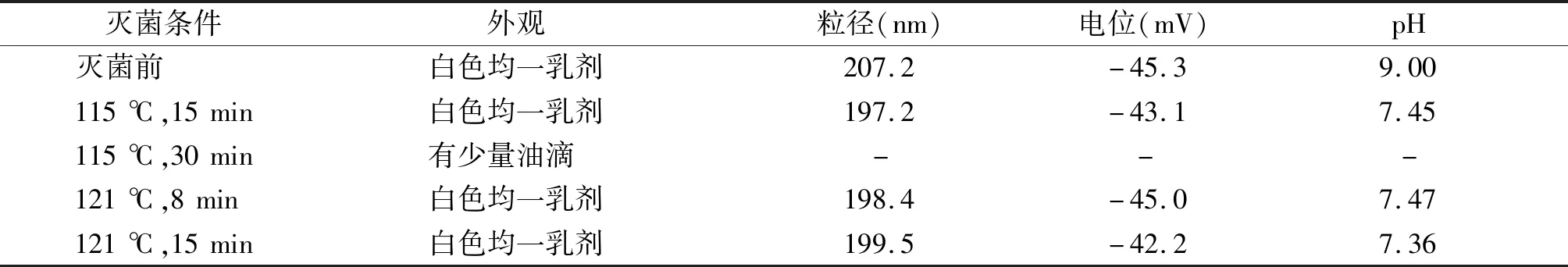
表5 灭菌条件对乳剂的影响Table 5 Effect of sterilization conditions on emulsion
2.2 不同磷脂酰胆碱(PC)含量的蛋黄卵磷脂对氟比洛芬酯脂微球注射液质量性能的影响
采用不同型号及不同来源的9种蛋黄卵磷脂制备氟比洛芬酯脂微球注射液,称取大豆油8 g,加热至65 ℃,称取氟比洛芬酯1 g,油酸0.4 g,置上述大豆油中搅拌使溶解,为油相;取水50 ml加热至65 ℃,加入水合磷酸氢二钠0.068 g,浓甘油2.20 g,泊洛沙姆188为0.6 g,蛋黄卵磷脂1.0 g置上述水中,搅拌使溶解,为水相;将油相与水相混合,13 000 r/min剪切8 min制得初乳,以0.1 mol/L氢氧化钠溶液调节pH值至9,以水定容至100 ml,以高压均质机1 000 bar循环6次将所得初乳进行精制得微乳;以0.65 μm微孔滤膜过滤;分装,充氮,封口,121 ℃湿热灭菌15 min,即得氟比洛芬酯脂微球注射液。测定结果见表6,结果分析见表7。
根据表6及表7可以得出不同PC含量卵磷脂做出的脂微球注射液性能指标pH值差异不大;以粒径、电位、离心稳定常数及多分散系数为指标,PC含量为70%和80%的蛋黄卵磷脂制备的脂微球注射液质量性能差异不大,而PC含量为98%的蛋黄卵磷脂制备的氟比洛芬酯注射液质量性能劣于以上两种。因此,制备氟比洛芬酯脂微球注射液,可选择PC含量为70%~80%的蛋黄卵磷脂。
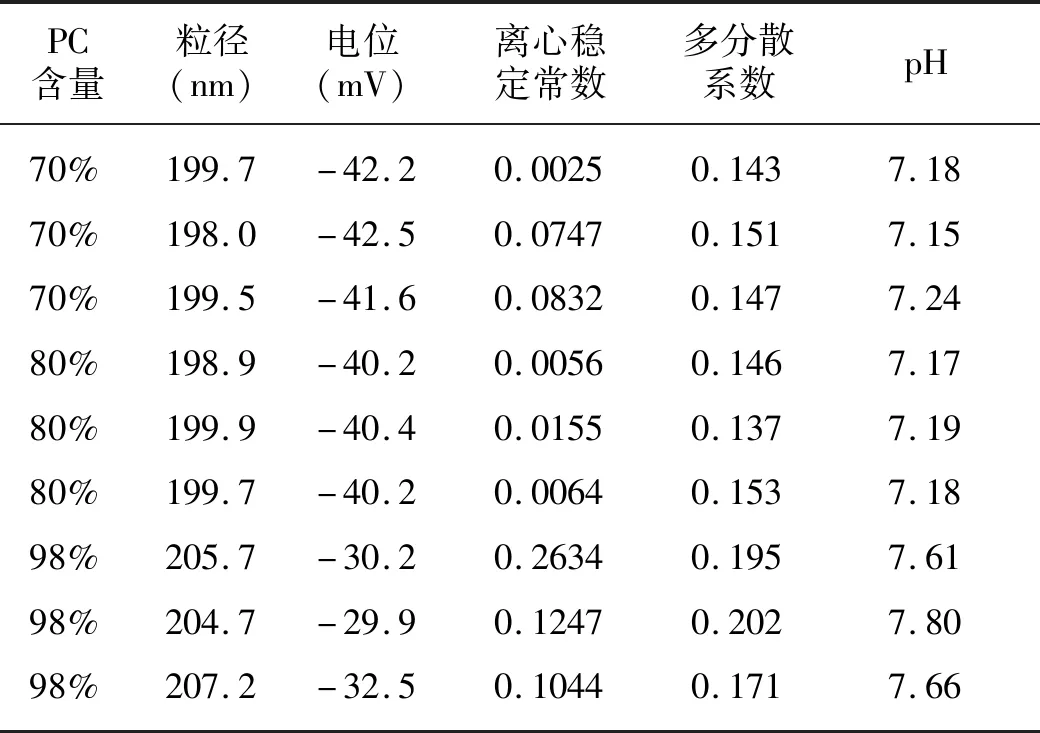
表6 不同蛋黄卵磷脂做出的脂微球注射液性能对比Table 6 Comparison of performance of lipid microsphere injection made from different egg yolk lecithin
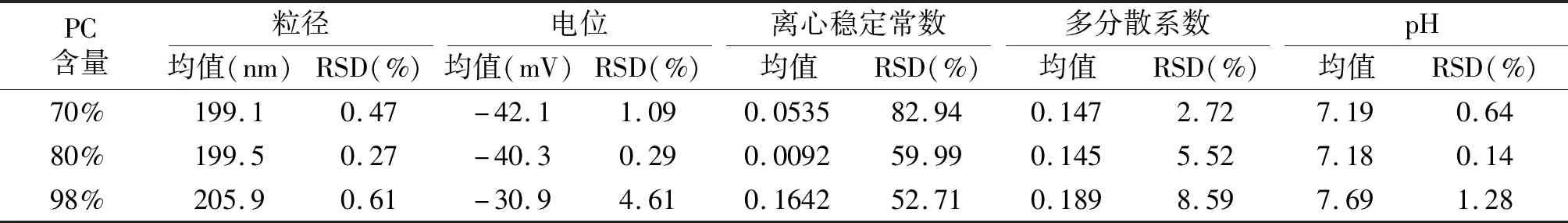
表7 不同蛋黄卵磷脂制备的脂微球注射液性能指标比较Table 7 Comparison of performance indexes of lipid microsphere injection made from different egg yolk lecithin
2.3 氟比洛芬酯脂微球注射液制备工艺重现性考察
称取大豆油8.0%,加热至65 ℃,称取氟比洛芬酯1.0%,油酸0.4%,置上述大豆油中搅拌使溶解为油相;取水适量加热至65 ℃,加入水合磷酸氢二钠0.068%,浓甘油2.2%,泊洛沙姆188 0.6%,蛋黄卵磷脂E80 ST 1.0%置上述水中,搅拌使溶解为水相;将油相与水相混合,13 000 r/min剪切8 min,以0.1 mol/L氢氧化钠溶液调节pH值至9,用水定容得初乳。以高压均质机1 000 bar循环6次将所得初乳进行精制得微乳。以0.65 μm微孔滤膜过滤,分装,充氮,封口,121 ℃湿热灭菌15 min,即得氟比洛芬酯脂微球注射液。分别以外观、pH值、含量、电位、平均粒径以及粒径分布为指标,制备3批氟比洛芬酯脂微球注射液进行重现性评价。结果发现:以上各指标均RSD≤2%(见表8),表明此处方及制备工艺的生产重现性良好。
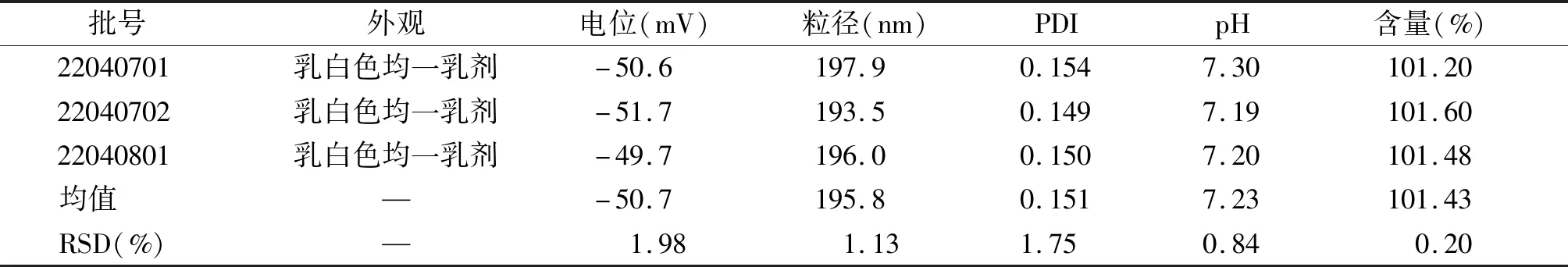
表8 三批氟比洛芬酯脂微球注射液处方及制备工艺重现性考察Table 8 Reproducibility of prescription and its preparation process of three batches of flurbiprofen axetil lipid microsphere injection
2.4 制得的氟比洛芬酯脂微球注射液稳定性考察
稳定性实验温度设定在4~8 ℃(25%相对湿度,25%RH),(25±2)℃(60%RH),(40±2)℃(75%RH),将乳剂分装于安瓿瓶内,灭菌,避光保存。测定氟比洛芬酯脂微球注射液在不同条件下贮存30 d的稳定性,结果见表9;计算各指标在0 d测定值与30 d测定值之间变化的绝对值均值和相对值均值,结果见表10及表11。结果表明:氟比洛芬酯脂微球注射液在不同温度条件下贮存30 d,温度越高,所测各项指标的相对值变化越大,总体上在25 ℃以下的条件下贮存30 d,其稳定性良好。
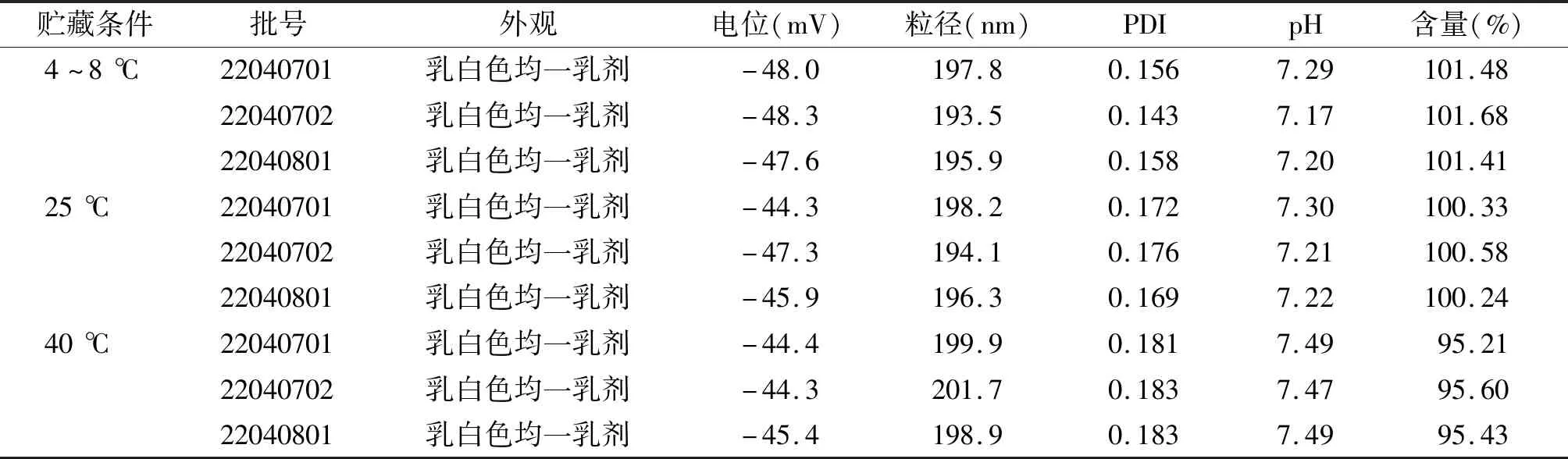
表9 氟比洛芬酯脂微球注射液在不同贮存条件下的稳定性考察结果Table 9 Stability of flurbiprofen axetil lipid microsphere injection under different storage conditions
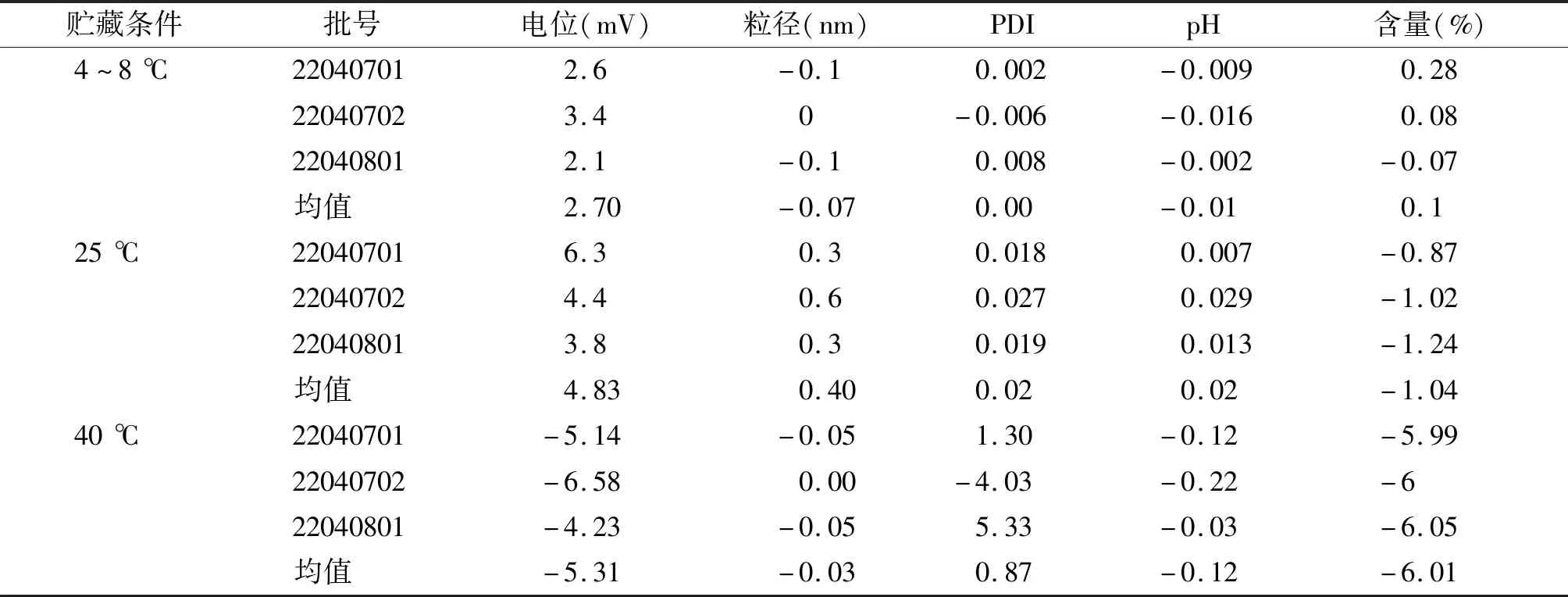
表10 各指标在0 d与30 d测定值之间变化的绝对值均值Table 10 Mean value of absolute value of difference of each index between the measured values at 0 d and 30 d

表11 各指标在0 d与30 d测定值之间变化的相对值均值 (%)Table 11 Mean value of relative value of difference of each index between the measured values at 0 d and 30 d (%)
3 讨论
磷脂和泊洛沙姆188以及油酸三者合用可提高乳剂稳定性。因为磷脂可产生表面电荷,使得乳滴由于静电斥力而不易聚集,泊洛沙姆188是高分子聚合物,其亲水性的聚氧乙烯链吸附在乳滴表面。这种空间位阻作用进一步抑制了乳滴聚集,另外,加入的少量油酸可增强泊洛沙姆l88和磷脂的相互作用,提高复合凝聚膜的稳定性,同时可使电位绝对值增高[9]。
蛋黄卵磷脂加入大豆油中,加热状态下搅拌很长时间仍不能完全溶解,乳化效果明显降低,且由于卵磷脂易氧化,在加热过程中不稳定;而溶于水相中加热搅拌便可很快形成均匀的胶体分散溶液,因此,将蛋黄卵磷脂加于水中制备乳剂。
高压均质过程中粒子的碰撞加剧,产生热量,容易使乳剂粒径增大,均质过程中采用低温冷却液循环泵,使均质温度保持在10 ℃左右。
PC含量为98%的蛋黄卵磷脂中几乎没有酸性脂质,乳化后乳粒的表面电荷减少,乳滴间的静电斥力较小乳滴易聚集,粒径容易增大,电位绝对值减小,Ke增大,不利于氟比洛芬酯脂肪乳的形成和稳定性,因此并不是理想的乳化剂。
氟比洛芬酯脂微球注射液在4~8 ℃条件下贮存30 d其稳定性良好,表明其不适宜在高温下贮存;还需在25 ℃以下继续放置60,90 d后测定其各项指标,进一步观察其稳定性,为后续加速或长期稳定性考察积累数据,以便确定适宜的贮存条件。

